数字化实验探究题归类分析
陈云龙
数字化实验探究是近几年中考比较热点的探究试题。试题将实验中得到的数据以图表、曲线的形式呈现出来,综合考查同学们信息获取与分析能力以及实验设计与探究能力。
一、数字化实验在实验探究中的作用
数字化实验通常由“传感器+数字采集器+计算机配套的系统支持软件”三部分构成,通过传感器对压强、浓度、pH、温度、电导率等物理量进行识别,再将这些物理量转换为电信号,通过数据采集器及软件将电信号转化为数字,并以数字和图形相结合的形式呈现在计算机的屏幕上。同学们可以非常直观地对图形进行观察,然后做出判断或预测,发现隐藏在数据背后的化学规律和原理。
二、数字化实验探究题的解题基本思路
解数字化实验探究题时要从图表、曲线中获取相关实验数据,并对实验数据进行分析,将数据转化为与探究方法相关的实验结论。解答此类试题的关键是基于“曲线—宏观—微观—符号”四重表征思想分析曲线,运用证据推理分析化学变化本质与规律。解题基本思路如下:
(1)曲线分析:直接读出曲线坐标中的两个变量(横、纵坐标)之间的变化关系,关注起点、终点以及变化的趋势;
(2)宏观辨识:分析纵坐标中相关物理量(如压强、浓度、pH等)变化的原因;
(3)微观探析:分析化学反应的微观过程,形成对变化规律的认识;
(4)符号表征:用相关的化学用语(如化学方程式等)进行表征。
三、数字化实验探究题的常考题型归纳
1. 气体压强传感器
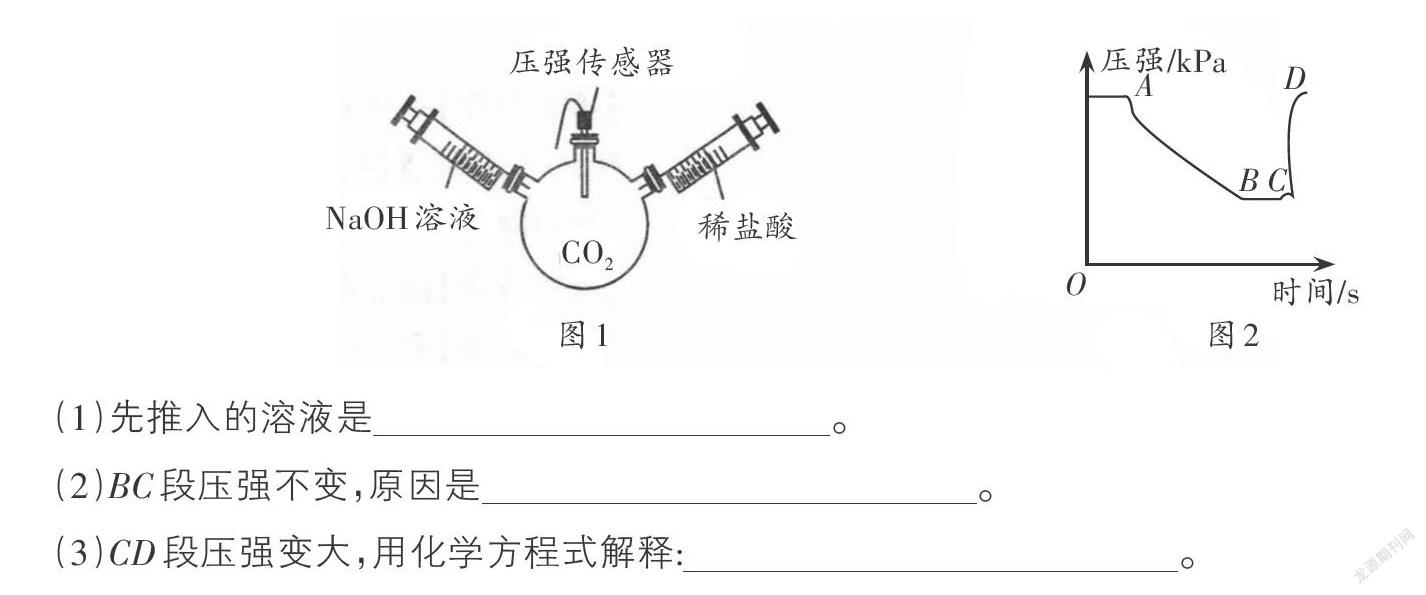
例1(2019·北京)用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。
(1)先推入的溶液是___________。
(2)BC段压强不变,原因是______。
(3)CD段压强变大,用化学方程式解释:______。
解析:(1)AB段压强先减小,是因为CO2与先推入的NaOH溶液反应,装置内气体减少;(2)BC段压强基本不变,是因为CO2与NaOH溶液完全反应,反应停止。(3)CD段压强变大,是因为新生成的Na2CO3与稀盐酸反应生成CO2,装置内气体增加。
答案:NaOH溶液 NaOH溶液与CO2充分反应,反应停止 Na2CO3 + 2HCl [ ] 2NaCl + H2O + CO2↑
[小结][以气体压强传感器为情境的数字化实验题解题四部曲:
首先,分析“压强-时间”曲线中,压强随时间的变化规律。如本题中,AB段压强减少——BC段压强不变——CD段压强变大。
其次,分析压强变化的原因。如本题中,气体体积变化引起压强变化,气体体积的变化过程为:减少——不变——变大。
再次,分析气体体积变化的原因。如本题中,反应经历三个主要阶段: NaOH与CO2反应——NaOH与CO2反应停止——Na2CO3与稀盐酸反应。
最后,用相关的化学方程式进行表征。如本题中,相关反应如下:2NaOH +CO2 [ ] Na2CO3 + H2O,Na2CO3 + 2HCl [ ] 2NaCl + H2O + CO2↑。]
2.气体体积分数传感器
例2(2019·福建节选)某兴趣小组开展“测定空气中氧气的体积分数”的探究实验。
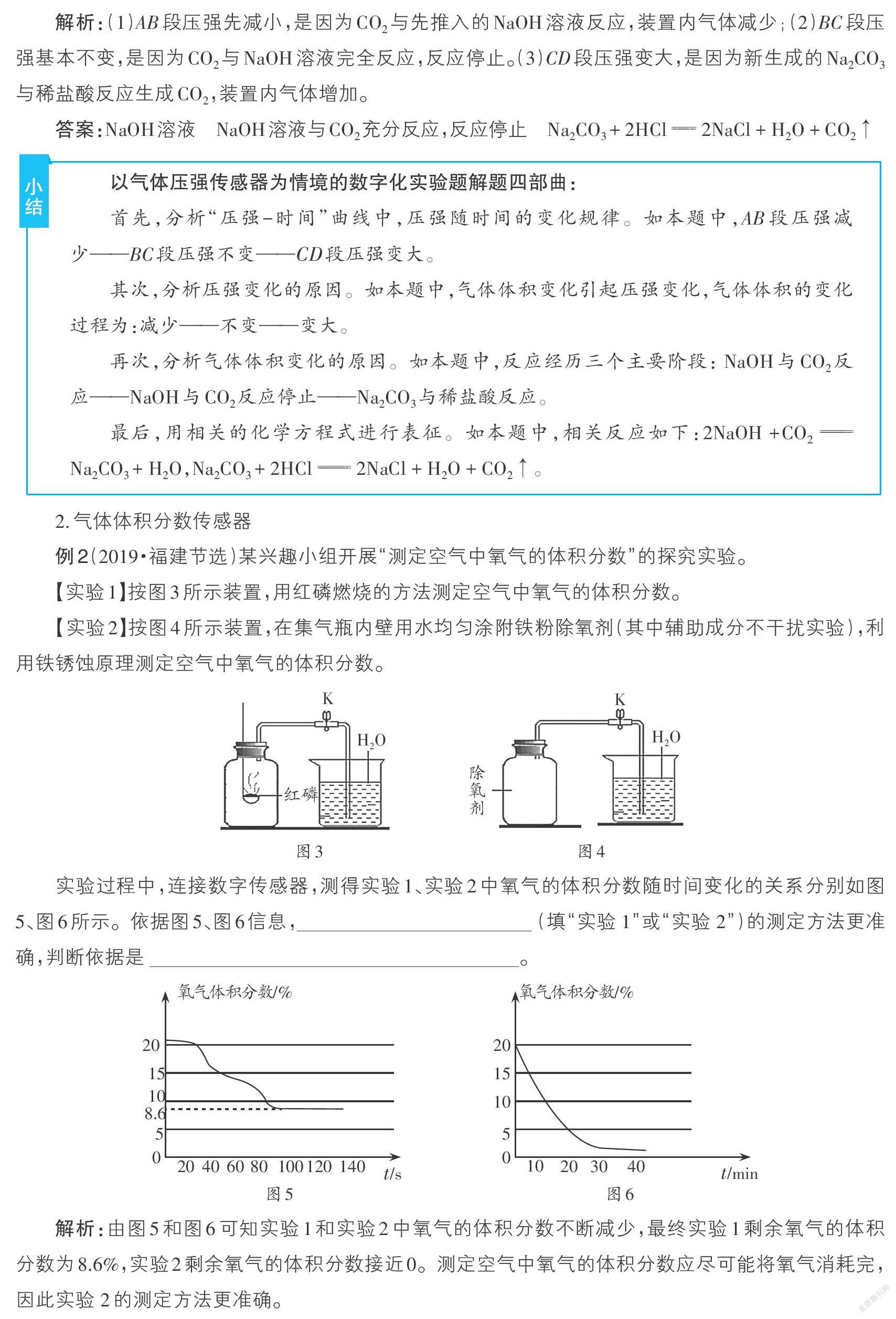
【实验1】按图3所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。
【实验2】按图4所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。
解析:由圖5和图6可知实验1和实验2中氧气的体积分数不断减少,最终实验1剩余氧气的体积分数为8.6%,实验2剩余氧气的体积分数接近0。测定空气中氧气的体积分数应尽可能将氧气消耗完,因此实验 2的测定方法更准确。
答案:实验2 反应后,实验1集气瓶中剩余氧气的体积分数为8.6%,而实验2集气瓶中氧气几乎耗尽
[小结][以气体体积分数传感器为情境的数字化实验题解题四部曲:
首先,分析“体积分数-时间”曲线中,浓度随时间的变化规律。如本题中,氧气的浓度(体积分数)不断减少。
其次,分析浓度变化的原因。如本题中,氧气的不断消耗引起氧气的体积分数不断减少。
再次,分析气体变化的原因。如本题中,红磷燃烧、铁锈蚀均不断消耗氧气。
最后,用相关的化学方程式进行表征。如本题中,相关反应为:4P + 5O2 [ 点燃 ] 2P2O5等。]
3. 溶液pH传感器
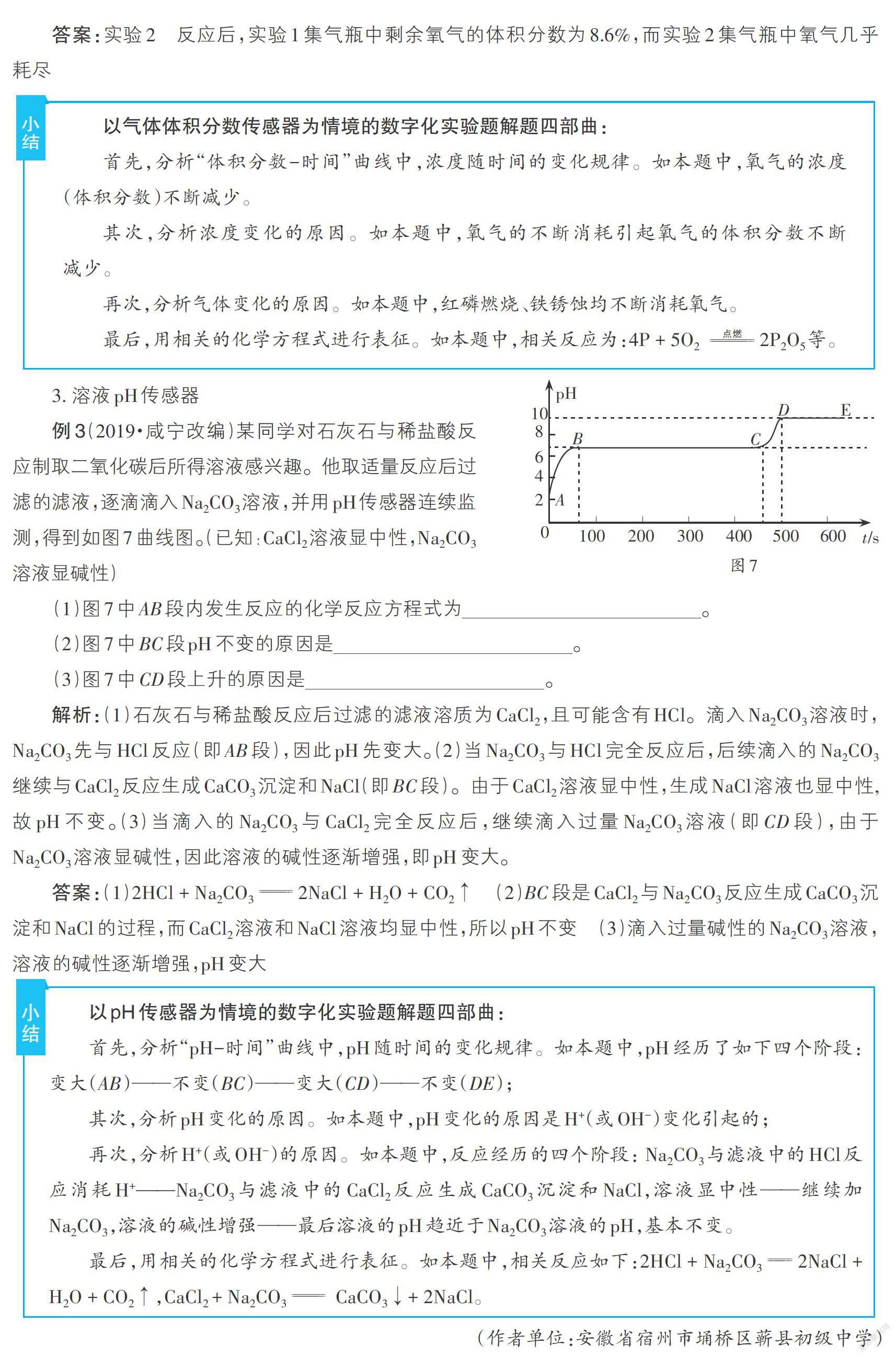
例3(2019·咸宁改编)某同学对石灰石与稀盐酸反应制取二氧化碳后所得溶液感兴趣。他取适量反应后过滤的滤液,逐滴滴入Na2CO3溶液,并用pH传感器连续监测,得到如图7曲线图。(已知:CaCl2溶液显中性,Na2CO3溶液显碱性)
(1)图7中AB段内发生反应的化学反应方程式为______。
(2)图7中BC段pH不变的原因是______。
(3)图7中CD段上升的原因是______。
解析:(1)石灰石与稀盐酸反应后过滤的滤液溶质为CaCl2,且可能含有HCl。滴入Na2CO3溶液时,Na2CO3先与HCl反应(即AB段),因此pH先变大。(2)当Na2CO3与HCl完全反应后,后续滴入的Na2CO3继续与CaCl2反应生成CaCO3沉淀和NaCl(即BC段)。由于CaCl2溶液显中性,生成NaCl溶液也显中性,故pH不变。(3)当滴入的Na2CO3与CaCl2完全反应后,继续滴入过量Na2CO3溶液(即CD段),由于Na2CO3溶液显碱性,因此溶液的碱性逐渐增强,即pH变大。
答案:(1)2HCl + Na2CO3 [ ] 2NaCl + H2O + CO2↑ (2)BC段是CaCl2与Na2CO3反应生成CaCO3沉淀和NaCl的过程,而CaCl2溶液和NaCl溶液均显中性,所以pH不变 (3)滴入过量碱性的Na2CO3溶液,溶液的碱性逐渐增强,pH变大
小结
以pH传感器为情境的数字化实验题解题四部曲:
首先,分析“pH-时间”曲线中,pH随时间的变化规律。如本题中,pH经历了如下四个阶段:变大(AB)——不变(BC)——变大(CD)——不变(DE);
其次,分析pH变化的原因。如本题中,pH变化的原因是H+(或OH-)变化引起的;
再次,分析H+(或OH-)的原因。如本题中,反应经历的四个阶段: Na2CO3与滤液中的HCl反应消耗H+——Na2CO3与滤液中的CaCl2反应生成CaCO3沉淀和NaCl,溶液显中性——继续加Na2CO3,溶液的碱性增强——最后溶液的pH趋近于Na2CO3溶液的pH,基本不变。
最后,用相关的化学方程式进行表征。如本题中,相关反应如下:2HCl + Na2CO3 [ ] 2NaCl +H2O + CO2↑,CaCl2 + Na2CO3 [ ] CaCO3↓+ 2NaCl。

