视神经管减压联合自体干细胞动员治疗视神经损伤的疗效观察
魏振宇 李志营 王帮庆 胡 森 步亚鸽 闫兆月 周志龙 步星耀△
1)新乡医学院第二附属医院,河南 新乡 453000 2)郑州市第七人民医院,河南 郑州 450000 3)河南省人民医院/郑州大学人民医院/河南大学人民医院,河南 郑州 450003
外伤性视神经损伤(traumatic optic nerve injury,TONI)多由交通事故导致的头部外伤引起,为颅脑损伤的常见并发症之一[1]。因外力作用常造成视神经管发生骨折、变形,致使视神经受到挤压、挫伤、水肿,甚至断裂(图1)[2]。其发病机制主要包括两个方面:一方面,外力通过骨骼变形及传导作用于视神经,使其受到牵拉及剪切[3];另一方面,作用于面部骨骼的力量瞬间减速引起蝶骨弹性变形,这一改变直接把力量传向视神经管[4]。由于管内段视神经同骨膜紧密相连,所以可以直接损伤视神经轴突或(和)影响视神经的血液循环而造成视神经挫伤性坏死[5]。颅脑损伤患者常伴明显的视力损害,如视力下降、色觉障碍、相对性传入性瞳孔阻滞(RAPD)和眼底改变等,如不采取及时有效的治疗方法,将对视力产生严重影响,进而大大降低患者生活质量[6]。因此,视神经管减压术得到临床认可。但术后除激素、营养神经、脱水及高压氧等综合治疗外,如何更快使受损视神经通过修复再生,恢复视神经功能,成为临床研究的一个难点和热点[7]。本研究回顾性分析河南省人民医院神经外科2014—2018年收治的TONI患者,与传统综合治疗相比,在视神经减压及综合治疗基础上采用联合自体骨髓干细胞(BMSCs)动员移植治疗[8]的疗效更佳。
1 资料和方法
1.1研究对象选取2014-01—2015-12河南省人民医院治疗的TONI患者29例为对照组,观察组为2016-01—2018-12治疗的TONI患者31例。所有患者为同一术者完成视神经减压术,且资料完整。所有方案实施前均已向河南省人民医院伦理委员会提交伦理审查方案并获得患者或家属知情同意书签名。排除颅脑损伤导致意识障碍者,眼部疾病所致视力障碍者。2组患者性别、年龄、受伤原因、受伤到手术时间等基础资料比较无显著差异(P>0.05)。见表1。
1.2临床表现所有入选患者术前均意识清楚,无眼部本身疾病。2组中各有8例患者当地医院出现嗜睡,在转入省医院后意识转清,能配合指令活动,伤后患侧视力均呈现进行性下降(表2)。患眼均表现为Marcus-Gunn瞳孔,即直接对光反射消失,间接对光反射灵敏[9]。所有患者术前均行头颅及视神经管薄层扫描,明确颅内及视神经管骨折情况(图2)。其中伴少量硬膜外血肿6例,蛛网膜下腔出血11例,额颞叶小片挫伤9例,2组CT检查结果差异无统计学意义(P>0.05),且格拉斯哥昏迷量表(GCS)评分均为15分。

表1 2组患者临床资料比较Table 1 Comparison of basic clinical data of two groups
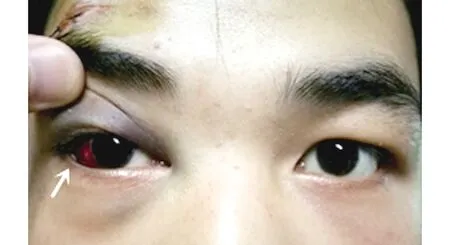
图1 如箭头所示,术前患者外伤可见右额部缝合伤口,巩膜充血及扩大的瞳孔Figure 1 Preoperative image,as shown by the arrow,the patient's trauma can be seen on the right frontal suture wound,scleral congestion and dilated pupil

图2 术前CT骨窗像,黑色箭头可见视神经管狭窄,白色箭头可见右眼眶外侧壁粉碎性骨折Figure 2 CT bone window image of the patient before operation.The black arrow shows the stenosis of the optic canal,and the white arrow shows the comminuted fracture of the lateral wall of the right orbit
1.3手术方法手术采用额颞瓣切口入路,蝶骨嵴磨平至额底平面,沿蝶骨嵴上缘至视神经管上壁剥离眶顶部硬膜,暴露出视神经管上壁[10]。如有碎骨片或血肿则予以清除(图3),除去视神经管上壁及外侧壁,开窗横径4~6 mm,纵行剪开背侧视神经鞘膜与前端的总腱环,使视神经管充分减压(图4)。
1.4治疗方案2组患者术后均给予脱水、大量激素冲击、扩血管及抗感染等治疗,对照组给予鼠神经生长因子(苏肽生,舒泰神北京药业有限公司)30 μL溶解于2 mL生理盐水肌内注射,1次/d,持续28 d[11]。观察组在对照组治疗基础上采用联合自体骨髓干细胞动员治疗,即神经管减压术后1周后皮下注射重组人粒细胞集落刺激因子(recombinant human granulocyte-colony stimulatingfactory,rhG-CSF)(厦门特宝生物工程股份有限公司)或重组人巨噬细胞集落刺激因子(recombinant humangranulocyte macrophage-colony stimulating factory,rhGM-CSF)(辽宁卫星生物制品研究所)5~10 μg/(kg·d),3 d一次,2种交替[12]。出院后2组患者继续行神经生长因子治疗3个月。

表2 2组患者临床表现Table 2 Clinical manifestations of 2 groups

图3 黑色箭头为破碎的骨折片,黑色星状图标为视神经,白色箭头为颈内动脉,可见破碎的骨折片刺入视神经Figure 3 The black arrow is a broken fracture,the black star icon is the optic nerve,and the white arrow is the internal carotid artery.It can be seen that the broken fracture penetrates the optic nerve

图4 黑色箭头所示为磨除视神经管上壁,白色箭头所示为纵行剪开背侧视神经鞘膜与前端的总腱环以及黑色星状图标所示的视神经,已达到充分减压的目的Figure 4 The black arrow shows the abrasion of the upper wall of the optic canal.The white arrow shows the longitudinal cut of the dorsal optic nerve sheath and the anterior tendon ring and the optic nerve shown by the black star icon
1.5疗效评价视力Ⅴ级:无光感;Ⅳ级:光感≤视力<0.02;Ⅲ级:0.022≤视力<0.05;Ⅱ级:0.055≤视力<0.1;Ⅰ级:0.11≤视力<0.3。若视力无改变则为无效;视力提高1个级别即为有效;视力提高2个级别为显效;视力提高3个级别或以上为特效。有效率=(特效+显效+有效)/总例数×100%。
2 结果
随访6~12个月,2组均无明显不良反应。末次随访显示,观察组视力恢复有效率80.65%,明显高于对照组的55.17%(Z=2.1054,P<0.05)。其中观察组7例失明患者中4例患眼视力达0.07以上,2例达0.05,1例效果不明显,可能原因为视神经断裂。而对照组6例失明患者中仅2例患眼视力达0.04,一例达0.02,1例存在光感,2例无改善。2组视力恢复对比见表3。
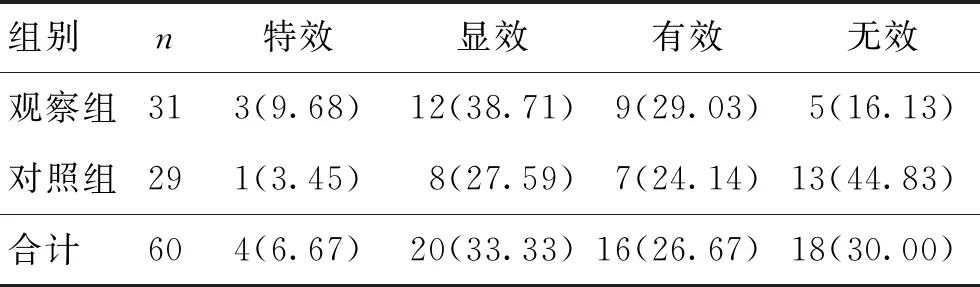
表3 2组末次随访视力恢复情况 [n(%)]Table 3 Vision recovery at the last follow-up oftwo groups [n(%)]
3 讨论
创伤性视神经损伤是颅脑创伤常见的并发症,占颅脑创伤的0.5%~5%[13],通常发生于车祸伤、重物打击和高处坠落伤等,是继发于颅脑创伤的视神经急性损伤。当额颞部受到较大的外力打击后,冲击力作用传到眶上缘、眶顶、视神经管,视神经受到挫伤或牵拉,由于管内段中视神经被硬膜固定,其对外来压力缺乏足够缓冲空间,管内段中视神经极易受到严重的压迫,甚至造成视神经断裂,即使没有视神经管骨折所致的压迫损伤,其他形式的损伤以及冲击也可能导致视神经轴突直接或间接受损,也会造成视力部分丧失,甚至完全损失[14]。造成视神经直接损伤一般是由于其附近的解剖学部位被损毁所致,如视神经管内的骨碎片切割伤[15]。视神经的间接损伤往往由头部钝性创伤导致的冲击传导至视神经管引起[16]。视神经一旦损伤,其周围的神经胶质细胞以及下游靶器官通常会出现一系列对损伤的中枢神经修复与再生不利的电生理变化、形态学改变以及生物化学等方面的改变[17]。原因包括:(1)高度分化的视网膜节细胞自身在损伤后缺乏再生的能力[18];(2)神经生长因子生成不足,包括靶源性神经生长因子的传送因轴突的断裂而中断,受损的神经细胞失去营养而渐渐坏死[19];(3)损伤细胞的细胞外基质不适宜,损伤后的神经胶质细胞分泌了神经生长抑制因子,这些抑制因子可抑制神经细胞的再生[20];(4)视神经损伤后星形胶质细胞形成的瘢痕组织可阻碍神经再生[21],视神经损伤后局部发生的炎症、水肿及释放的细胞因子可阻碍轴突的再生[22]。以上不利因素不同程度影响视神经的再生,进而影响患者的预后。
如果缺乏及时有效治疗,视神经将会萎缩、变性,导致视力下降,甚至永久性失明[23]。因此,视神经管减压得到临床共识,通过减压可清除碎骨片的直接压迫,去除神经鞘膜,营造宽松缓解,缓解视神经水肿,改善局部血液循环,避免视神经继发损害[24]。根据术前影像学资料,不同术者依照各自经验可采用不同手术方式,如经颅视神经减压术、经蝶窦视神经减压术、筛窦视神经减压术、经鼻内镜下视神经减压术等完成视神经管减压[25]。
在解除视神经受压因素后,如何进行神经修复成为临床研究热门课题。鼠神经生长因子作为脑保护剂,是神经系统中最重要的神经营养因子[26]。可能作用机制如下:(1)鼠神经生长因子能够拮抗兴奋性氨基酸毒性,减少神经元凋亡,保护受损神经元存活;(2)改善血供促进受损部位血管形成;(3)增进神经递质的活性及合成代谢,促进神经髓鞘生成等[27],故鼠神经生长因子一直作为临床神经修复常规用药。近年来干细胞移植对中枢神经系统损伤的作用在不同疾病模型的研究中得到证实[28],而自体骨髓干细胞(BMSCs)以其多项分化潜能,极强的自我更新能力,且具有无创、不存在组织配型及免疫排斥问题等优点,得到神经学科研究者的青睐[29]。本研究通过皮下注射重组人粒细胞集落刺激因子或重组人巨噬细胞集落刺激因子作为激活因子,动员骨髓中的干细胞到达外周血液,然后通过血液循环流入受损组织,在适合内环境的作用下能够分泌多种参与修复损伤和功能重建的神经营养因子,促进受体自身的神经干细胞分化为神经细胞,完成BMSCs动员[30]。研究还发现鼠神经生长因子不仅能够促进损伤中枢神经细胞的再生和修复,而且还可以营造利于BMSCs动员移植后存活、生长、分化和成熟的内环境,有助于BMSCs移植后神经元的存活和再生以及轴突再生,形成功能性连接从而促进神经功能的修复,协同提高BMSCs动员治疗视神经损伤的临床疗效。
外伤性视神经损伤病理机制复杂,单纯依靠视神经管减压术改善视力下降治疗作用有限[31-32],而mNGF联合自体BMSCs动员可达到协同治疗、修复视神经损伤作用。本研究观察组患者视力改善程度均明显优于对照组(P<0.05),且观察组7例失明患者中4例患眼视力达0.07以上,进一步说明NGF联合自体骨髓干细胞动员移植对TONI具有很好的修复作用,具有广阔的临床应用前景,值得进一步研究。

