格列齐特片(Ⅱ)溶出曲线的一致性评价研究
孔 彬,刘晓霞,赵 昕
0 引言
格列齐特片(Ⅱ)是磺酰脲类降糖药,临床用于治疗非胰岛素依赖型糖尿病,该药物的药理作用是选择性作用胰岛B细胞,促进胰岛素分泌,进食后产生葡萄糖时,快速提高胰岛素的释放,抑制肝糖生成以及输出;能降低血小板的聚集和黏附力,有助于防治糖尿病微血管病变。其药物分子结构中有氮杂环结构,具有独特的药物特点[1]。本品具有缓释作用,可以显著增加餐后胰岛素和C-肽分泌水平,疗效持久。本实验参照药典方法[2-4],采用光纤药物溶出度过程分析仪(简称:FODT-601)对格列齐特片(Ⅱ)开展溶出度实验[5-8]:参照药典通则,用磷酸盐缓冲液(pH 8.6) 1 000 ml作为溶媒,选取测定波长226 nm,实验转速150 r/min,分别在60、180 min时按缓释制剂溶出度进行判定。180 min后,观察溶出曲线,并获得对应时间的相对溶出百分率,比较溶出曲线的一致性。
1 仪器与试剂
光纤药物溶出度过程分析仪(FODT-601,上海富科思生物技术发展有限公司)、分析天平(梅特勒-托利多 AB135-S)、脱气仪(天大天发),纯水仪(艾柯)。
格列齐特对照品(中国食品药品检定研究院,批号100269-201004);格列齐特(Ⅱ)片(A厂,法国某公司,规格:80 mg×60片,批号:4C747T;B厂,贵州某公司,规格80 mg×60片,批号:20140901;C厂,石家庄某公司,规格:80 mg×60片,批号:G0130513)。磷酸二氢钾(分析纯);氢氧化钠(分析纯);冰醋酸(分析纯);醋酸钠(分析纯);浓盐酸(分析纯)。
2 方法与结果
2.1 配制溶媒 磷酸盐缓冲液(pH 8.6):氢氧化钠42.0 g加入脱气水至5 000 ml,摇匀得溶液1。称得磷酸二氢钾136.0 g,加入脱气水至5 000 ml,摇匀得溶液2。取溶液1与溶液2,加3 150 ml乙醇,加脱气水至10 000 ml,摇匀,测得pH值(8.6±0.05),用于溶出度实验。
2.2 配制对照品溶液 精密称取对照品16.39 mg置于100 ml容量瓶中,用磷酸盐缓冲液(pH 8.6)溶解并稀释至刻度,摇匀,制成浓度为163.0 μg/ml的对照品溶液。
2.3 配制供试品溶液 格列齐特片(Ⅱ)10片,研磨成细粉,精密称得格列齐特片(Ⅱ) 16.07 mg置于100 ml容量瓶中,加入磷酸盐缓冲液(pH 8.6)溶解后,稀释至100 ml,制成供试品溶液。
2.4 检测方法的建立 将浓度81.35 μg/ml的片粉溶液,浓度为81.95 μg/ml的格列齐特标准溶液,在220~600 nm光谱范围内扫描。见图1。
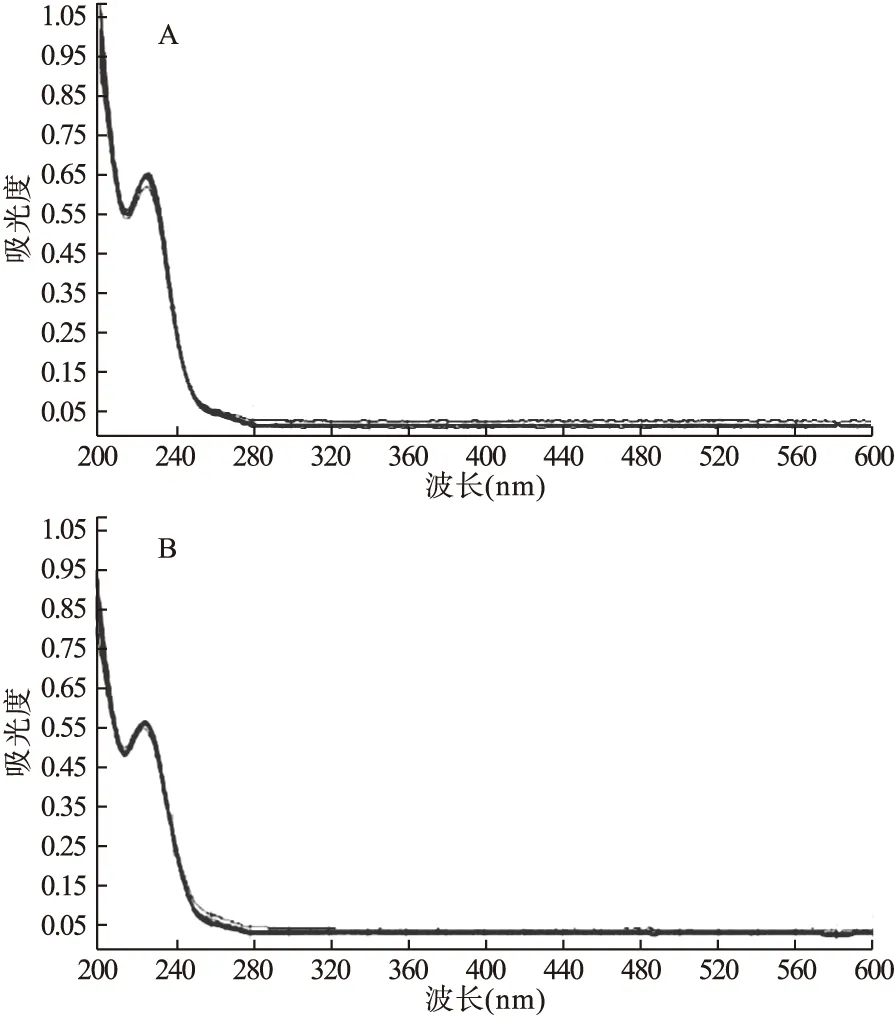
图1 仪器扫描格列齐特片(Ⅱ)吸收光谱图注:A.片粉,B.对照品
通过在分析仪上扫描对照品光谱显示:在波长226 nm处有明显吸收峰,且吸收度大小符合测定要求,采用550 nm为参比波长,仪器软件用双波长法扣除辅料。
2.5 线性与范围 分别精密量取4.0、6.0、12.0、18.0、25.0 ml浓度为163.9 μg/ml的格列齐特对照品溶液,分别置于50 ml容量瓶中,用pH 8.6磷酸盐缓冲液稀释后配制成梯度溶液。分别在分析仪上进行测定,将相对浓度C%作为纵坐标,以吸收度A作为横坐标,作每个通道的线性回归方程。在FODT-601的6个通道上测定后得到标准方程。见表1。
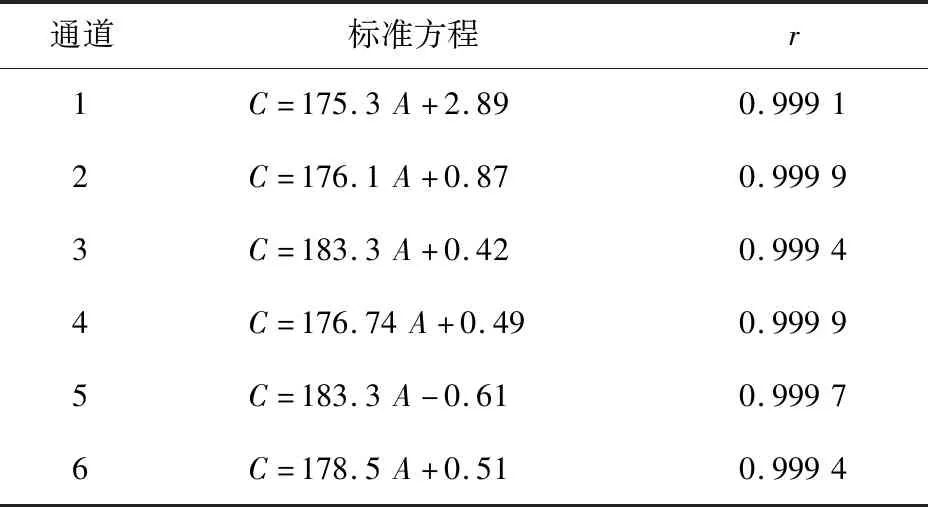
表1 溶出介质为pH 8.6磷酸盐缓冲液的标准方程
2.6 精密度与回收率
2.6.1 日内及日间精密度 取“2.5.1”项下溶液,24 h内在仪器上连续测定6次,获得吸收度RSD=1.94%;并连续测定6 d,吸收度的RSD为2.08%,证明该方法日内及日间精密度良好。
2.6.2 准确度 精密称取相当于20 mg格列齐特的药粉适量,用溶媒溶解并稀释至250 ml 量瓶中,摇匀。分别称得约7.0、9.0、10.0 mg的格列齐特对照品加入上述片粉溶液中,分别配制成各3份高、中、低浓度的供试品溶液,在FODT-601上测定吸收度,后带入标准方程计算回收率。结果显示,高、中、低浓度溶液的平均回收率在90.2%~105.7%范围内(RSD=2.56%~3.78%,n=6),表明本方法的准确度较好,符合要求。
2.7 溶出度试验 转篮法在光纤药物溶出度过程分析仪(FODT-601)测定,使用探头为1 mm,溶媒为磷酸盐缓冲液(pH 8.6) 1 000 ml,转速为150 r/min,温度设定(37±0.5) ℃,将各通道上的线性方程带入监测软件,设定226 nm作为测定波长,550 nm作为参比波长,扫描空白溶液,并把6片药片投入经脱气处理的溶媒中,同时按下“开始”按键,设定溶出时间180 min,进行监测溶出曲线。
2.8 三个厂家的溶出曲线比较结果 见图2。
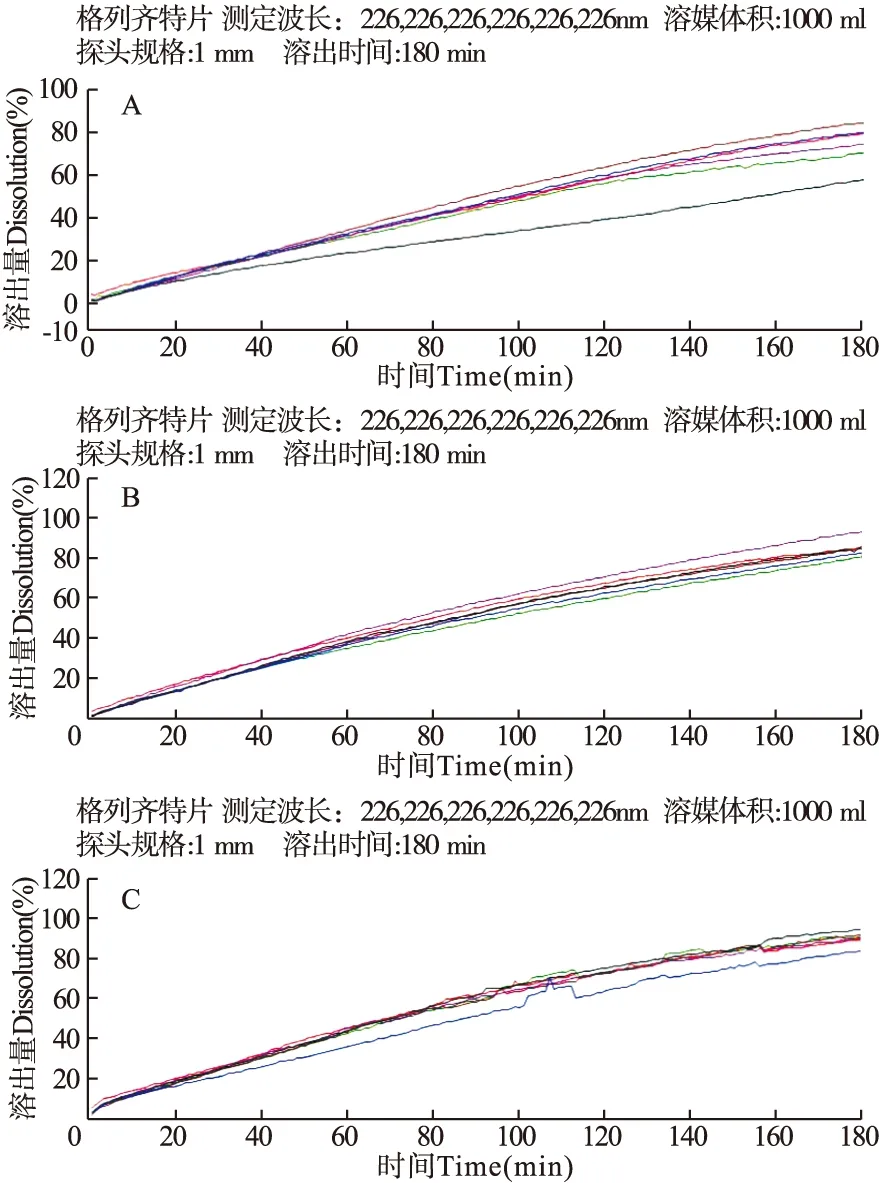
图2 三个厂家实时溶出曲线
2.9 溶出度曲线相似性评价 FODT-601软件结果显示,仿制药与原研药在药典规定的溶出介质中的f2分别为65.6、50.4。结果显示,样品2厂家的仿制药与原研药在药典规定的溶出介质中的溶出行为相似。
3 讨论
3.1 依据国家公布的“仿制药质量一致性评价意见”的质量标准以及《普通口服固体制剂溶出度试验技术指导原则》,采用相似因子f2法,遵照取点原则,本实验参比制剂180 min内平均溶出率达85%以上,为严格试验结果,本实验增加了60、120 min两个点进行采样,采用相似因子法比较溶出曲线,参比制剂与受试制剂累积溶出量差的平方和最小,当f2在50~100之间时表明二者溶出曲线相似[3-4]。由结果f2分别为65.6、50.4可知,仿制药与原研药在药典规定的溶出介质中的溶出行为相似[6-7]。并实时得到180 min内的真实溶出曲线。
3.2 目前,格列齐特片(Ⅱ)的释放度测定方法 主要采用2015年版中国药典的方法[2],需要人手动抽溶出液、补充取出液、膜过滤后稀释等步骤,操作费时繁琐,针对缓释制剂溶出度试验周期较长,耗时耗力,容易产生疲劳后带来操作误差。光纤药物溶出度过程分析仪可全程记录药物溶出曲线过程,节省实验人员的时间精力和物力;简化缓释制剂释放度测定的繁琐过程,并获得真实完整的大量监测过程数据[7-8];有利于药品工艺的研究,为仿制药一致性评价中的制剂溶出度试验提供现代化的测定方法[4]。

