光(电)催化氮气还原合成氨研究进展
任晓玲,严孝清,龚湘姣,吴志强,杨伯伦,魏进家,杨贵东
(西安交通大学化学工程与技术学院工业催化研究所,陕西省能源化工过程强化重点实验室,陕西西安710049)
氨作为世界上最大的工业合成化学品之一,因其具有能量密度高(4.3kW·h/kg),易液化便于运输(沸点-33℃)等优势,在农业、化工、医药、储能等领域被广泛应用[1-2]。目前,工业上所采用的合成氨技术为Haber-Bosch 工艺,其是在铁基催化剂下,以氮气和氢气为原料,在高温(300~600℃)、高压(150~250atm,1atm=101325Pa)的严苛条件下进行的反应过程[3]。其中氢气通常由甲烷蒸气重整的耗能反应提供。在当今世界上氮肥的产能已经超过5 亿吨的情况下,Haber-Bosch 工艺每年耗能约占世界总能源的2%[4]。与此同时,此工艺每年排放3 亿吨CO2温室气体,约占全球总排放量的1.6%。因此,在日益严峻的能源危机以及全球变暖给人类带来严峻挑战的背景下,为了缓解现有工业合成氨能耗高的难题,降低全球环境污染,在较温和条件下,通过利用可再生资源(例如太阳能)驱动氮气还原合成氨反应,一直是世界范围内工业界和学术界关注的热点和不懈追求的目标之一[5]。
近年来,光(电)催化氮气还原(NRR)合成氨技术,被认为是一种具有潜力替代工业Haber-Bosch工艺生成NH3的方法,引起社会的热切关注。与传统的工业Haber-Bosch 工艺相比,该技术在常温常压条件下,以氮气和水为原料,经太阳能驱动发生氧化还原反应而合成氨,实现了太阳能向化学能的转化。作为新一代的合成氨工艺,具有特殊的技术优势:使用的能源为取之不尽的太阳能,具有绿色可持续的优点;可在常温常压下进行,反应条件温和,能耗低,成本低;以水作为氢源,取代了Haber-Bosch 工艺所需的不可再生的化石燃料,减少CO2气体排放,对环境较为友好,并且地球的大部分被海洋所覆盖,水资源丰富[6]。自1977 年,Schrauzer 等[7]首次发现半导体二氧化钛基光催化剂在紫外光照射下具有氮气还原合成氨性能以来,光(电)催化氮气还原合成氨技术一直是各国学者的研究热点。
一个高效的催化反应需要具备性能优良的催化剂以及合适的催化反应体系。光催化氮气还原合成氨反应亦是如此。该催化反应的基本原理为:以光能作为驱动力,照射半导体催化剂,催化剂吸收特定波长的光子,激发产生具有氧化还原能力的光生电子-空穴对。具有还原能力的光生电子,从催化剂体相迁移至催化剂表面,再与催化剂表面被吸附的氮气进行还原反应;具有氧化能力的空穴则氧化水溶剂产生质子,用于氮气加氢质子化过程。从整个反应过程来看,光(电)催化氮气还原合成氨反应历程可分为以下多个步骤:氮气在水溶剂中的溶解扩散,氮气在催化剂表面的吸附和活化,光生电子还原氮气,以及氮气逐步加氢质子化生成氨。基于上述光催化氮气还原过程分多步进行以及包含多电子复杂反应,光催化氮气还原合成氨整体效率与上述各步骤都相关,不仅受限于催化剂将光能转化为光生电子-空穴的氧化还原能力,催化剂理化特性和催化反应体系也对电子-空穴的利用效率产生显著的影响。
目前基于光(电)催化氮气还原合成氨技术的研究重点主要集中在如何促进氮气的吸附和活化,缺少关于具体氮气反应物传质步骤和反应过程强化的综述报道。因此,本文在介绍光(电)催化氮气还原合成氨反应过程以及机理的基础上,重点综述近期关于强化氮气扩散传质、吸附活化以及光生载流子分离等反应过程的最新研究现状,并对其未来发展趋势进行分析与展望。
1 光(电)催化氮气还原合成氨反应过程
基于半导体材料的光催化氮气还原基本的过程[图1(a)]包含以下几个步骤。
(1)光激发过程 以光能作为驱动力,照射半导体催化剂,催化剂吸收特定波长的光子,被激发产生具有氧化还原能力的光生电子-空穴对,产生的光生电子(e-)快速从价带跃迁至导带,同时在价带上留下光生空穴(h+)。
(2)光生载流子分离、迁移过程 光生电子和空穴通过扩散作用,分别从催化剂体相向催化剂表面迁移。部分光生电子和空穴在迁移过程中会发生复合。
(3)表面氧化还原反应 迁移至催化剂表面的具有还原能力的光生电子,与催化剂表面被吸附的氮气进行还原反应;具有氧化能力的空穴氧化水溶剂产生质子,用于氮气加氢质子化过程。
对于光电催化氮气还原体系[图1(b)],与上述光催化体系相似,不同的是其通常采用三电极系统(工作电极、对电极和参比电极)。催化剂位于用作工作电极的光电阴极上,用于氮气的还原;太阳能水分解则发生在阳极的反电极上。在此光电协同催化氮气还原体系中,电发挥的作用是通过外加偏压电场来抑制光生载流子复合。

图1 光(电)催化氮气还原反应基本原理
通过了解整个光(电)催化氮气还原合成氨反应历程,发现其实质就是光生电子-空穴对载流子从催化剂的内部向表面扩散和转移,伴随着氮气溶解扩散吸附至催化剂表面,经过活化、分解解离、解吸脱附的反应过程。由于光(电)催化体系为多相体系,其反应物扩散传质过程的优化、反应物的活化、光生电子的迁移效率、载流子的复合程度以及催化剂和催化反应体系的设计都对整个体系的催化转化效率起着重要作用。本综述将重点介绍在整个光催化氮气还原合成氨过程中,促进氮气溶解扩散、氮气吸附和活化,以及有效促进载流子分离和传输的策略。综述重点关注内容如图2所示。
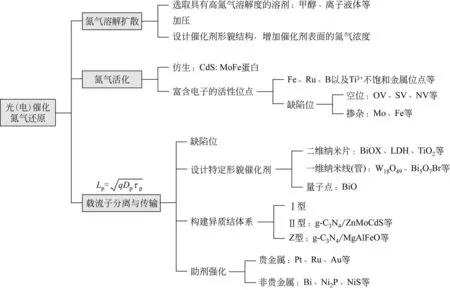
图2 综述内容框架
2 氮气溶解扩散
在光(电)催化氮气还原合成氨技术中,以液相水作为质子源时,氮气还原反应系统是一个气液固三相反应体系。在催化剂作用下,氮气发生还原反应需要分多步进行。氮气首先需要在水中溶解,其次扩散至催化剂材料外层的液膜,再转移至催化剂表面活性位点后才能进一步参与光催化氮气还原反应。氮气为非极性物质,在水相反应体系中溶解度极低(约1mmol/L,25℃,1atm),扩散系数小(约10-5cm2/s),导致光(电)催化氮气还原合成氨性能受制于水相反应体系中氮气溶解和扩散过程。除此之外,氮气在水中较低的溶解度和扩散系数也导致反应步骤更为简单的产氢竞争反应更易于发生,致使整体产氨选择性低,不利于达到理想的光(电)催化氮气还原合成氨效果[6]。因此,强化氮气在水相反应体系中的扩散和传质过程,是提升光催化合成氨整体反应速率的重要手段,也是该技术从基础研究到实际应用的关键之举。
通过选取合适的溶剂,例如具有高氮气溶解度的溶剂(甲醇、离子液体等),促进氮气在水中的溶解扩散,增加氮气浓度,可以间接提高催化体系的氮气还原合成氨性能。甲醇溶剂的氮气溶解性是纯水的10 倍,其作为溶剂有望提高氮气在水中的溶解扩散传质速率。王文中课题组[8]首次利用纯甲醇作为质子源和溶剂,使K掺杂氮化碳催化剂的光催化氮气还原合成氨活性大幅提高,进一步表明通过增加甲醇在水相中的比例可增加氮气溶解性,提高氮气还原性能[图3(a)]。离子液体是由一种阴阳离子组成的液体盐,作为一种绿色溶剂,具有结构可设计性、电导率高等优势[9]。一些功能化离子液体中的阴离子可与氮气发生较强的吸附作用,进而使得离子液体对氮气的溶解能力大幅提升。Jacquemin 等[10]和Stevanovic 等[11]通过测试,发现氮气在[P6,6,6,14][eFAP]离子液体中的溶解度是水的20倍。Zhou等[12]发现用上述离子液体为电解质(含有微量水<20~250μg/g),显著提高了金属Fe 催化剂的电催化氮气还原性能,并进一步基于理论计算证实了离子液体和氮气之间有较强的作用力,有利于合成氨过程中氮气还原过程的发生。Kang等[13]后续又探索出多种具有较高氮气溶解度的含氟离子液体,为未来促进氮气溶解扩散速率的研究提供了实验参考和理论依据。需要注意的是:以上具有高氮气溶解性的离子液体普遍呈现疏水性,因此在水作质子源的情况下,调控离子液体和水的比例对催化剂的氮气还原性能尤其重要。此外,若将离子液体具有高氮气溶解性这一特性引入合成氨光催化剂的表面或者孔道中,在催化剂和水相界面间形成特殊的离子液体传输介质层,通过增强氮气的溶解和扩散速率,强化氮气在反应体系中的传质及向活性位点的转移过程,有望实现水相反应体系中整体光催化氮气还原效率显著提高。

图3 甲醇作溶剂,氮气压力以及不同催化反应体系对氨产率的影响[8,14-15]
除了选取合适的溶剂增强氮气的溶解扩散速率外,通过增加一定的压力,也可以提高氮气在水中的溶解性。从亨利定律中也可以看出,在水中氮气的溶解度与压力有关。MacFarlane 团队[14]通过实验证明了氨产率与氮气压力成近似线性关系,结果表明通过增加压力,可以提高氮气还原性能[图3(b)]。
鉴于氮气在气相中的扩散系数(约0.1cm2/s)高出在水相中的扩散系数4个数量级,使得研究者尝试利用气态氮气作为氮来源,增强氮气传质扩散。张铁锐团队[15]和张礼知团队[16]等利用水蒸气作为质子源,通过增加氮气的扩散系数,显著提高了整体的产氨活性。此外,通过构建新型的光催化剂反应体系[图3(d)],使光催化剂位于气液界面,增强氮气在光催化剂表面的浓度,进而增加催化剂吸附氮气的概率,从而提高整个反应体系的产氨性能。氮气在光催化剂表面的浓度取决于催化剂在气-水界面的浸润程度,为此调控光催化剂的表面亲疏水性十分重要。研究人员发现金属氧化物光催化剂上的表面氧缺陷和无定形表面结构可调控催化剂的润湿程度[17-18]。此外,有学者也发现介孔结构的存在,在促进氮气和水的扩散同时,也可以改变材料表面的亲疏水性。综上所述,通过构建具有介孔结构的光催化剂,结合新型的光催化剂反应体系,充分利用气态氮气作反应物,有望提高整体的氮气还原效率[19]。
综上可知,通过选取合适的溶剂,适当增加氮气分压,以及设计具有特殊结构的新型催化剂和反应体系,均可强化氮气的溶解、扩散传质过程,从而提高氮气还原性能。目前,虽然离子液体具有高氮气溶解性的这一特点在光催化氮气还原合成氨方面还没有相关报道,但是将其合理应用于未来研究具有一定的潜力;同时设计调控光催化剂的结构,构建新型的催化反应体系,以及发展其他增强氮气溶解扩散速率的手段也是未来的一个研究方向。
3 氮气活化
氮气作为合成氨中的氮源,同时也是构成自然氮循环的主要成分之一。其在大气中的含量高达78%,来源广泛。从热力学角度出发,氮气还原合成氨过程为热力学可发生的过程。由于氮气第一解离能大(942kJ/mol),使得氮气体现出稳定的化学特性,不易活化,成为氮气还原反应合成氨的限速步骤。因此,催化剂对于氮气的吸附活化能力是影响整体光催化氮气还原效率的关键因素。强化氮气的吸附活化,实现氮气的解离,是有效提高氮气还原合成氨性能的手段之一。
3.1 仿生活化
氮的循环在自然界元素的循环中具有重要意义,其中,生物固氮是最早的一种将氮气转化为氨的手段。生物固氮是通过固氮微生物(根瘤菌、鱼腥藻、固氮螺菌等)中的固氮酶利用三磷酸腺苷(ATP)水解产生的化学能实现氮气的固定。深入认知固氮酶的固氮机理可为后续一系列仿生固氮催化剂的研究提供理论基础,相关学者通过研究固氮酶的结构和功能发现其固氮原理是在温和的条件下利用固氮酶中含有的钼铁(MoFe)蛋白,通过核心的MoFe 辅因子的催化作用活化氮气。值得注意的是生物固氮过程需要消耗大量由ATP 水解提供的能量。
基于上述固氮酶的固氮机制,可发现若利用太阳能取代ATP 水解产生的化学能作为驱动力,模仿固氮酶中MoFe 蛋白的催化作用,对实现常温常压下的氮气还原反应将会非常有利[20]。Banerjee等[21]通过合成含FeMoS无机团簇的Mo2Fe6S8-Sn2S6硫凝胶,并在光照条件下模仿固氮酶进行氮气还原反应,研究结果证实了MoFe 硫化物在光驱动作用下将氮气转化为氨是一个可行的过程。Kanatzidis等[22]利用Mo2Fe6S8(SPh)3和Fe4S4仿生簇分别模仿固氮酶中FeMo辅因子和Fe蛋白,并将其分别或同时封装在聚合物网络中,从结构和功能上模拟生物固氮酶,并探究其光催化氮气还原性能,结果表明具有还原活性的含铁硫化物团簇的物质在可见光激发下能够激活氮气。另外,Brown 等[23]借鉴固氮酶固氮原理[图4(a)],将MoFe 蛋白吸附到CdS 纳米晶体上构筑了生物杂化复合物催化剂体系,利用CdS纳米晶体光敏化MoFe 蛋白,通过光能取代ATP 水解的化学能驱动氮气还原成NH3;结果表明CdS:MoFe蛋白生物杂化复合物中的MoFe蛋白发挥氮气还原作用的速率,可与生理学转换频率(TOF)的速率相当,量子效率达3.3%。

图4 固氮酶、过渡金属和硼的氮气还原机理[24-25]
3.2 设计富含电子的活性位点
相关学者通过研究固氮酶固氮机理以及深入探究工业上合成氨的Haber-Bosch 工艺所用的铁基催化剂对氮气的活化机理发现,富含电子的过渡金属(Fe、Mo、Ni、Co等)可以活化氮气且具有较高的氮气还原活性。究其原因是过渡金属不仅能够提供高能量的d 轨道电子填充至氮气的π*反键轨道,而且可以接受氮气σ 轨道的电子进而激活氮气[图4(b)]。
富含电子的过渡金属Fe 是氮气还原领域研究最为广泛的催化剂活性组分之一。Rees等[26]通过构建与氮气具有等电位的CO分子连接的FeMo蛋白体系,发现氮气的激活是源于FeMo 辅因子的双铁组分,充分证明了Fe 原子是氮气还原的活性中心。Smith 等[27-28]同样指出Fe 具有氮气活化能力归因于其高能的d 轨道电子填入氮气的π*反键轨道,削弱了N N键。基于Fe与氮气之间可通过电子的相互转移形成化学吸附,促进氮气的活化,Hu 等[29]合成了Fe 掺杂蜂窝状氮化碳,通过表征手段检测到Fe 与氮化碳之间形成了Fe-N 键,并进一步指出Fe3+的存在不仅能够以化学吸附的形式活化氮气,也可以促进氮化碳光激发产生的光生电子的转移,进而提高光生载流子利用率。结合密度泛函理论(DFT)计算出的电荷密度差数据也证实了电子从Fe3+活性位点向氮气的转移。基于以上研究,Azofra等[30]通过DFT计算探究Fe掺杂MoS2的合成氨性能,计算结果显示Fe 活性组分的有效掺杂使得本身不具备活性的MoS2产生了氮气还原合成氨活性。究其原因是当Fe 通过3 个Fe-S 键被引入到MoS2表面时,产生了一个四面体的晶体分裂场,计算结果显示来自氮气的电子可以填满Fe 中心未占据的t2轨道,充分证明氮气能被有效地捕获和激活。Sun 等[31]通过考察磷酸基团修饰LaFeO3的光催化氮气还原合成氨性能,发现磷酸基团修饰LaFeO3具有最高的合成氨活性和选择性,产氨活性达250μmol/(g·h),而N2H4产量仅为1.45μmol/(g·h)。N2-TPD 显示经磷酸基团修饰后LaFeO3的化学吸附信号增强,并且峰值向高温方向偏移。结合酸碱理论,可以将其解释为带有孤对电子的氮气为Lewis碱,更容易和Lewis 酸或催化剂表面修饰的氢键种类发生化学吸附。
除富含电子的过渡金属基光催化剂之外,非金属B因同时具有空轨道和已占据轨道,也被证实具有氮气活化性能[32]。Ling 等[25]通过密度泛函理论模拟B 单原子修饰具有旋光性的石墨氮化碳(B/g-C3N4)光催化剂的合成氨性能[图4(b)],g-C3N4上N 原子与B 原子结合生成两个N—B 键,使B原子稳定在g-C3N4上,同时留下一个已占据和一个空的sp3轨道,进而B 原子能与氮气发生较强作用。结果表示通过B/g-C3N4上的酶解机制可有效地将氮气还原为NH3,其还原起始电位为0.20V,为目前报道的最低电位。B的存在可增强g-C3N4的光转换效率,生成更多光生电子,提高光催化性能。
此外,缺陷工程作为一种可调节半导体光催化剂中金属中心局部配位环境的手段,可提供具有低价金属中心的配位不饱和位点以及多余电子,使局域在缺陷处的电子转移至被吸附氮气的反键π 轨道,从而有效实现N N键的弱化作用,其所构筑的缺陷是一种新型的光(电)催化氮气还原合成氨活性中心。催化剂有无缺陷,以及缺陷的种类、浓度等都会对半导体催化剂的性质产生影响。目前,研究较多的是氧空位(OV)、氮空位(NV)、碳空位(CV)以及硫空位(SV)[33]。
氧空位对氮气活化影响的研究是氮气还原领域的研究热点之一,其中具有氧空位的催化剂如卤氧化物、层状双氢氧化物(LDH)及TiO2等得到了较多关注。张礼知团队[16]设计合成具有氧空位的暴露001 优势晶面的BiOBr 纳米片催化剂,通过原位漫反射傅里叶变换红外(FTIR)光谱检测催化剂表面官能团随时间的变化,证实了在可见光下催化剂中氧空位的存在有利于激活氮气,显著提高氮气还原性能。研究发现表面OVs具有典型的缺陷态,可以捕获电子并抑制光生载流子的复合,从而促进捕获的载流子向催化剂表面吸附的氮气吸附质转移(图5)。该团队[34]后续合成具有氧空位的BiOCl 材料,考察了不同暴露晶面(001 和010)以及不同缺陷浓度对催化氮气还原活性和反应机制的影响。通过利用电子顺磁共振(EPR)技术对缺陷浓度进行定量分析,发现在BiOCl-001上,将OVs浓度从0 增加到0.052%,氧空位周围的Bi-Bi 距离从0.392nm缩短到0.378nm,并且附近的两个Bi2+原子上的过量电子逐渐向附近的氧空位离域。在此基础上,结合DFT计算和原位红外傅里叶变换(FTIR)谱表征技术,发现OVs催化氮气转化合成氨经历了几个连续的质子耦合电子转移的低能反应步骤,阐明了氧空位活化氮气的机理。Bai 等[35]通过原位方法制备了具有氧空位的BiOI 光电极,同样证明空位的存在对氮气的吸附和活化起着重要作用。Shiraishi 等[36]近期合成具有界面氧空位的BiOCl 光催化剂,通过在反应溶液中加入Cl-,使得氮气在通过溶液时实现还原,并进一步指出氧空位附近的Bi2+提供多余电子给氮氮三键(Bi2+上孤对电子信号随着氮气的注入而减弱),促进氮气的活化。通过氧化材料夹层中的Cl-实现水氧化反应,结合光生电子的还原能力,最终将氮气转化为氨。
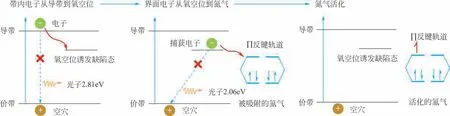
图5 在固氮过程中氧空位相关界面电子转移的示意图[16]
层状双氢氧化物(LDH)光催化剂,由于其易于控制的金属阳离子组成和厚度,易于进行缺陷工程和带隙调控,是一种有效的氮气还原光催化剂。张铁锐团队[15]以NaOH 为沉淀剂,合成一系列不同金属离子的具有可见光催化氮气还原性能LDH 材料MⅡMⅢ-LDH (MⅡ=Mg,Zn,Ni,Cu;MⅢ=Al,Cr),探究其光催化氮气还原性能。研究发现当LDH纳米片的尺寸控制在几纳米时,易于产生OVs和不饱和位点。通过高分辨率透射电镜(HRTEM)表征,在其纳米薄片上可以看到轻微的晶格无序和位错,证实了缺陷的存在。OV 的存在,增强金属离子与氮气相互作用力,使氮气更容易被活化。相比于块状CuCr-LDH 和ZnAl-LDH 材料,具有缺陷位的LDH 纳米片的光催化性能大幅提高。后续该团队[37]通过低价Cuδ+改性具有氧空位的ZnAl-LDH纳米片(图6),进一步提高其催化性能和稳定性[图7(b)]。在紫外光照射下,改性后的ZnAl-LDH的产氨活性达110μmol/(g·h)。氧空位和富电子Cuδ+既促进氮气的吸附活化,又促进电子和空穴的分离和转移,协同提高催化剂光催化活性。

图6 富含电子Cuδ+和氧空位的ZnAl-LDH纳米片合成示意图[37]
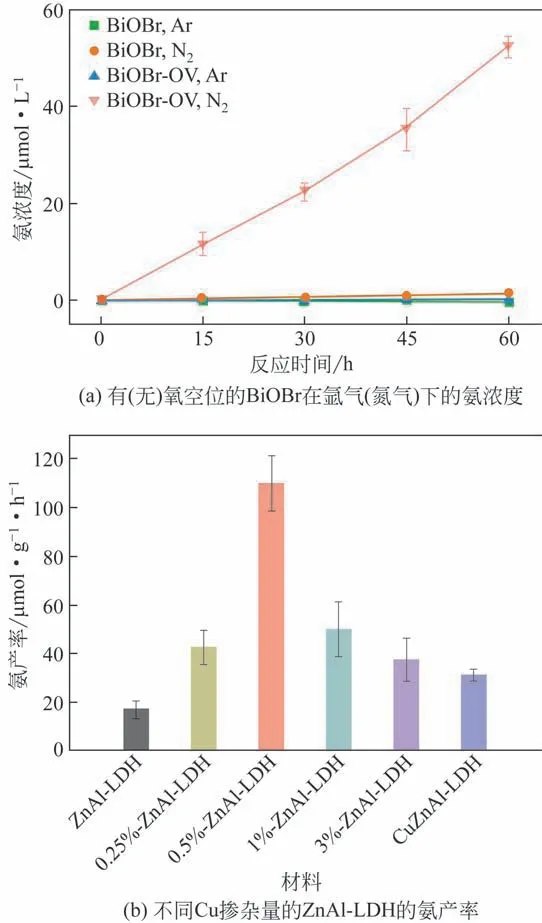
图7 氧空位以及Cu掺杂对不同催化剂的产氨活性的影响[16,37]
自从Schrauzer 等[7]首次发现二氧化钛基光催化剂具有氮气还原合成氨活性以来,基于二氧化钛的缺陷工程调控用于光催化氮气活化领域的研究得到广泛关注。Hirakawa 等[38]研究发现TiO2表面的Ti3+通过给电子至氮气,可形成化学吸附,成为氮气活化位点。在紫外光激发下,光生电子被表面氧空位捕获,利于Ti3+活化位点的再生(图8、图9)。Zhao 等[39]后续通过合成Cu 掺杂具有氧空位的TiO2,发现氧空位可在拓阔TiO2的光吸收范围的同时实现氮气的活化,在入射光源拓展到700nm波长条件下其仍具有氮气还原活性。Li 等[40]利用原子层沉积(ALD)技术合成表面氧空位修饰的等离子体增强Au-TiO2纳米棒光电极,所得非晶态的TiO2富含缺陷可提供更高的载流子浓度和更多的活性位点从而促进氮气的吸附和活化。同时,他们通过系列对比实验发现表面OVs与等离子体金纳米颗粒的存在可协同增强TiO2/Au/a-TiO2光电极的光催化氮气还原性能。此外,具有氧空位的其他氧化物也被应用于光催化氮气还原领域。董晓丽等[41]合成H-Bi2MoO6的光催化剂,发现加氢反应使Bi2MoO6产生氧空位可促进氮气的活化, 其产氨活性高达1300μmol/(g·h)。

图8 金红石TiO2(110)表面的氮气固定机理图[38]
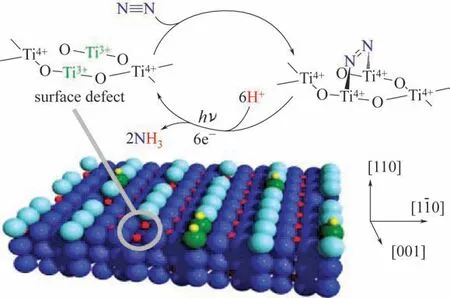
图9 含Ti3+复合物的催化氮气固定循环图[38]
除了氧空位外,硫空位也具有与氧空位相类似的作用,其中金属硫化物是一种易于构建硫空位的有效光催化剂[42]。相对于单一金属硫化物,三元金属硫化物(MoNiCdS、ZnSnCdS、ZnMoCdS)上的硫空位更容易产生。Hu等[43]利用水热法制备g-C3N4/ZnSnCdS异质结催化剂,系统探究了硫空位和异质结结构对催化剂的光催化氮气还原性能的影响。研究结果显示硫空位是吸附和活化氮气的活性位点,也促进催化剂界面电荷向氮气的转移,显著提高光催化氮气还原能力,最高的活性达419μmol/(g·h)。王文中团队[44]利用水热-超声处理方法制备具有硫空位的超薄MoS2纳米片材料。电感耦合等离子体发射光谱仪(ICP)分析结果显示超声处理的超薄MoS2中Mo∶S的化学计量比为1∶1.75,表明超薄结构中可能存在大量的硫空位。氮气分子被这些硫空位捕获,氮气在提供成键轨道电子的同时,接受电子填充到3个反键轨道,从而被激活。He等[45]以MIL-68(In)金属有机骨架材料作为In 源,硫脲为硫源,采用水热自组装技术制备In2S3中空纳米管,后续通过在不同温度(200℃、300℃)的氮气气氛中退火形成硫空位。利用电子自旋共振光谱(ESR)检测硫空位及其浓度,发现随温度升高,空位浓度增加。硫空位的存在可作为活性位点,促进氮气的吸附和活化,提高氮气还原性能。
相比于氧空位和硫空位,氮空位因其形状和大小与氮气中的氮原子相同,可以高选择性地吸附和活化氮气。为此,相关研究者尝试构建具有氮空位的催化剂并探索其光催化氮气还原性能。g-C3N4作为一类二维非金属半导体光催化剂,具有成本低、物理化学性质稳定、易于合成等优点,可通过不同的制备方法制备具有氮空位的氮化碳材料。Dong等[46]通过氮气热处理方法合成了具有氮空位的g-C3N4,系统研究NVs与g-C3N4的氮气光催化还原能力的关系(图10)。研究证实了NVs不仅可选择性地吸附和活化氮气,而且能有效提高光生载流子的分离效率,产生更多的光电子。同时,NVs提高了g-C3N4的导带位置,增强催化剂的还原能力。Wu 等[47]通过一种无模板的方法合成具有较大比表面积和氮空位的海绵状g-C3N4,同样发现氮空位可以激活氮气,促进催化剂界面电子传递。他们进一步研究发现通过改变g-C3N4合成过程中溶剂种类,可调整g-C3N4比表面积和氮气还原性能大小。相比于未处理的g-C3N4,经甲醇处理合成的g-C3N4的比表面积和氮气还原性能分别提高15.2 倍和27.2 倍。Li 等[48]则通过红外线微波辅助制备具有氮空位的g-C3N4,结合DFT计算,证实了氮空位可以活化氮气。在氮空位的作用下,N N 三键的键长从0.1107nm 增长至0.1242nm。此催化剂可以大量制备,对促进光催化氮气还原合成氨的实际应用具有重要意义。另外,王文中团队[8,49]利用KOH 对g-C3N4进行表面修饰,通过暴露氮空位以及钾的掺杂协同促进产氨活性的增加, 活性高达3632μmol/(g·h)。为了便于分析和比较,表1 列出了上述研究的产氨活性,并对温度、光源、牺牲剂的选择等条件进行了适当的总结。
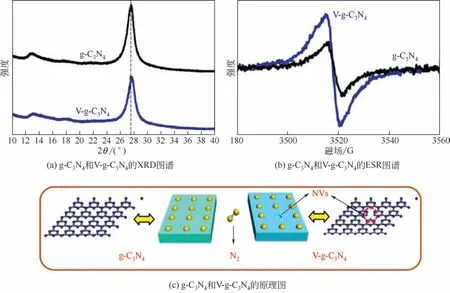
图10 g-C3N4和V-g-C3N4的结构表征以及原理图[46]

表1 光(电)催化剂总结
4 载流子分离与传输
光催化氮气还原过程需要光生电子和空穴均要有效发挥作用,而光生载流子运动过程是影响光催化剂氮气还原性能的关键因素之一[50]。相关学者经过系列研究发现载流子在催化剂中的迁移不仅和催化剂本身性质有关,而且与催化剂结构、形貌、缺陷等众多因素有关。在光催化氮气还原过程中,通过强化电子传递动力学过程,增强载流子的分离,可实现电子和空穴的有效利用,提高催化剂整体合成氨活性。其中,光激发产生的电子-空穴载流子的迁移是通过内部浓度梯度扩散来实现。扩散距离为非平衡载流子从注入浓度到平衡浓度走过的距离,可以表示为Lp=(qDpτp)1/2。其中,Dp为载流子扩散系数,与半导体催化剂的特性有关,比如,缺陷和杂质的量、载流子有效质量以及载流子的流动性;τp为非平衡载流子的寿命;q为维度因子(当维度为1D、2D、3D 时,q 分别为2、4、6)[51]。从式中可看出,通过设计具有特定形貌的催化剂,合理构建缺陷位(包含空位、金属/非金属掺杂)以及添加助剂或构建异质结结构等,可以调控载流子的扩散距离和寿命,进而影响催化剂的光催化活性。
4.1 设计具有特定形貌的光(电)催化剂
光催化剂的形貌对催化性能有着至关重要的影响。从Lp=(qDpτp)1/2可以看出,光激发产生的载流子的迁移率和寿命与光催化剂的形貌结构相关。多相催化反应在催化剂表面进行,通过控制催化剂的形貌,使反应物和载流子更易于扩散到催化活性位点,缩短电子传输距离,对催化剂的催化活性有着显著影响。此外,与传统的块状材料相比,具有特定形貌的光催化氮气还原纳米催化剂除了具有更高的比表面积,有助于氮气等分子在催化剂表面的吸附,提高光催化氮气还原反应速率之外,通常具有更多的缺陷和活性位点也更容易激活氮气。
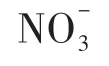
TiO2作为研究最为广泛的光催化剂之一,被成功应用于在光催化氮气还原合成氨领域,尤其是具有纳米片结构的TiO2。Liu 等[53]设计合成TiO2纳米片,通过在纳米片结构的基础上添加单原子Ru 活性位点,可以进一步强化载流子的分离提高催化活性。Yang等[54]合成了金纳米晶锚定具有氧空位的超薄TiO2纳米薄片(4.3nm±0.3nm)催化剂,其以“串联工作”的方式完成光催化氮气还原反应。具有氧空位TiO2纳米薄片吸附并激活氮气,金纳米晶体等离子体激发产生的热电子将氮气还原为NH3。
其他二维光催化剂也被报道具有氮气还原合成氨性能。王文中团队[44]首次合成带电激子修饰超薄MoS2纳米片材料(图11),发现带电激子修饰超薄MoS2纳米片相比于不具备光催化合成氨性能的块状MoS2具有较高的产氨活性和选择性。在没有任何牺牲剂和助剂的条件下, 产氨活性达325μmol/(g·h),选择性为100%。他们通过分析光电化学测量中还原峰电位(Ep)的变化以及扫描速率(v)的变化,发现超薄MoS2纳米片光催化氮气还原反应过程是六电子还原过程。
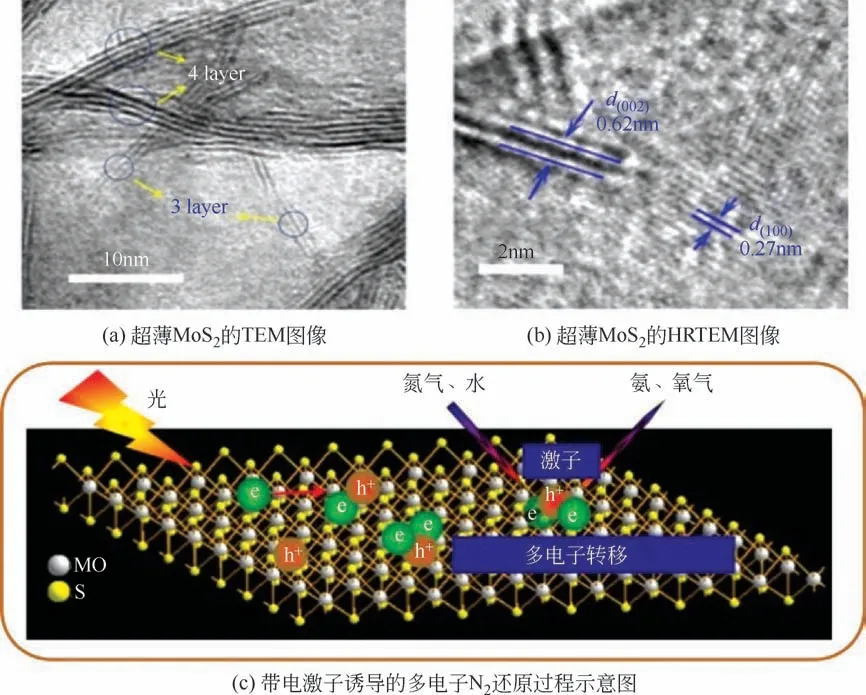
图11 超薄MoS2的结构表征以及带电激子诱导的多电子氮气还原过程[44]
一维材料的载流子扩散距离更短,其也被应用于氮气还原合成氨领域,强化载流子的分离,提高氮气还原活性。熊宇杰团队[55]通过Mo 掺杂超细W18O49纳米线载体,证明一维纳米线结构的存在,使得光激发产生的光生电子更易于迁移至表面的不饱和位点,并传输至表面被吸附的氮气上,减少载流子的复合,同时促进质子耦合过程的发生。Wang 等[56]通过水辅助自组装的低温新方法合成了直径为5nm 的Bi5O7Br 纳米管,缩短了光生电子的传输距离,减少了电子-空穴的复合。在无牺牲剂且水做质子源的条件下,产氨活性达1380μmol/(g·h)。
具有量子点结构的光催化材料近期在光催化领域成为研究热点。量子点材料的特点是催化剂在三个维度上的尺寸都不大于所对应的半导体材料的激子玻尔半径的两倍,直径常在2~20nm之间。已有研究证明量子点特殊结构的存在有利于光生载流子的分离。吴凯丰团队[57]采用电荷掺杂CdS量子点构建模型体系,结合飞秒瞬态吸收光谱动力学测试,揭示了纳米晶在多电子光催化和光电转换应用中的一系列重要动力学过程,证明量子点结构的存在对催化剂的电荷分离速率和效率具有重要影响。在光催化氮气还原领域,王文中团队[58]报道了平均尺寸为2~5nm的BiO量子点在模拟太阳光下,具有高效的光催化氮气还原合成氨活性(图12)。其活性是传统的Fe-TiO2的1000倍。需要指出的是,BiO量子点结构的存在,使得所有晶格铋都是潜在的氮气活化中心。为了便于分析和比较,表2列出了具有特定形貌结构的光(电)催化剂的产氨活性表,并对温度、光源、牺牲剂的选择等条件进行了适当的总结。

图12 BiO量子点的合成示意图及结构表征[58]
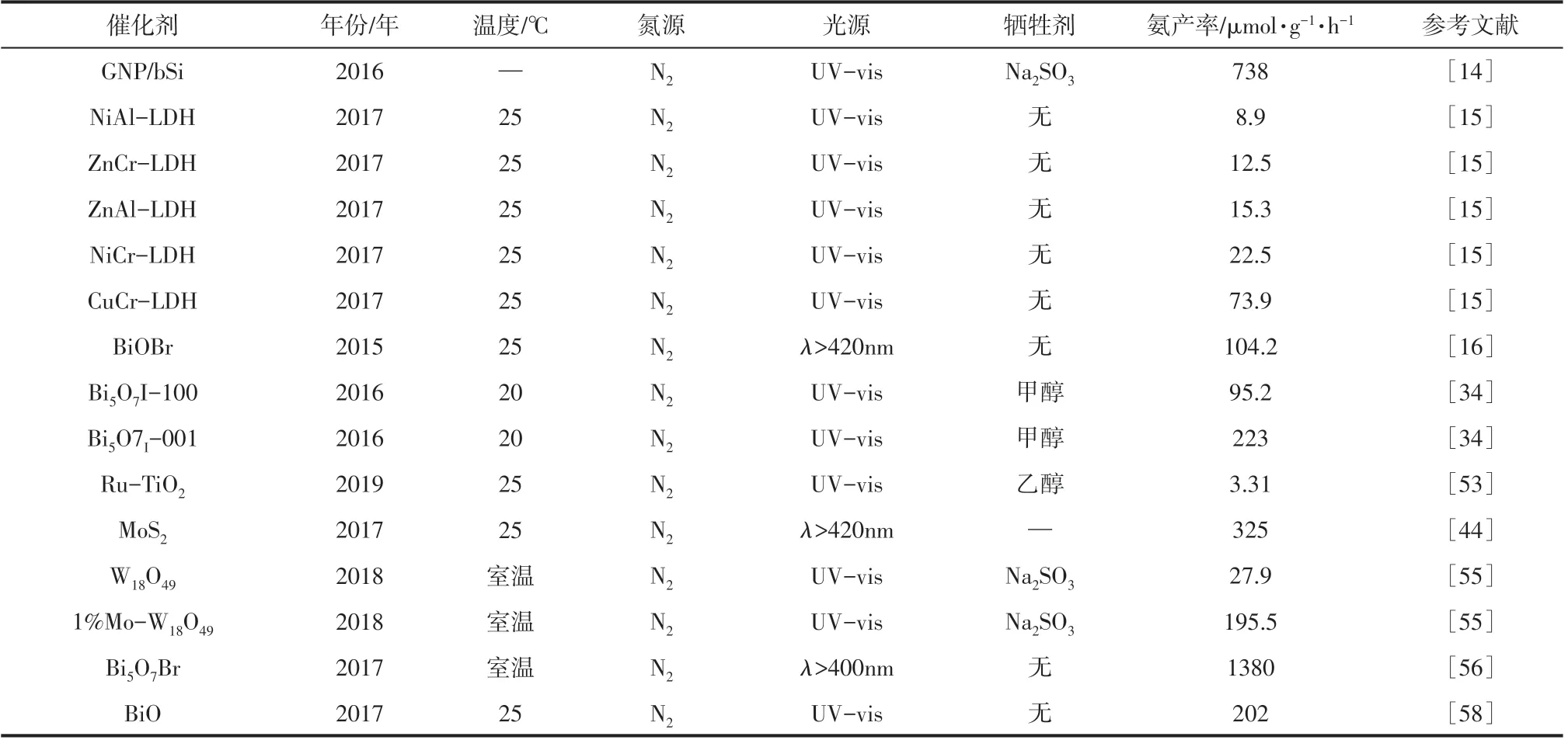
表2 具有特定形貌结构的光(电)催化剂总结
4.2 构建缺陷位
半导体的缺陷也对光生载流子的分离具有显著影响。已有研究发现催化剂中由于杂质、空位、隙间原子或位错会在禁带中产生一些能级,这些能级或者起陷阱的作用,或者起复合中心的作用。缺陷的引入,必然会影响半导体能带特征,通常会实现禁带宽度变窄,增强对可见光的吸收能力,形成更多的光生载流子,同时也利于载流子的分离[59-60]。缺陷的存在对载流子动力学和表面反应动力学有显著影响。与不含缺陷态的初始材料相比,缺陷丰富的半导体材料通常具有显著的光催化氮气还原合成氨性能。目前,最为熟知和易于实现的是通过元素掺杂或引入结构空位,形成一定的半导体晶体结构缺陷。在光催化氮气还原合成氨领域,通过构建缺陷位,不仅能促进氮气的吸附活化,而且能强化载流子的分离和迁移[19,33,50]。
张礼知团队[16,61]设计合成具有氧空位的一系列卤氧化物(BiOBr、BiOCl)光催化氮气还原催化剂,结合稳态和瞬态光致发光光谱证实了缺陷能级可以捕获电子或空穴,抑制载流子的复合,也可以促进这些捕获的载流子向催化剂表面吸附的氮气吸附质转移。张铁锐团队[15]设计合成的一系列具有氧空位的LDH 材料,也证明了因氧空位的存在,使得带隙产生显著的缺陷能级,促进载流子的分离。He等[45]利用MIL-68(In)棱柱作为前体,采用自组装技术成功制备In2S3中空纳米管并通过在不同温度的氮气气氛中退火形成硫空位,结果也证实硫空位在催化剂CB和VB之间引入了杂质能级,促进了载流子的分离。Dong等[46]和Li等[48]分别通过氮气热处理方法和红外线辅助微波辅助合成了NVs-g-C3N4,也证明了氮空位可以促进催化剂界面电荷向氮气转移,减少载流子的复合,从而提高氮化碳的光催化氮气还原性能。
掺杂是一种有效改变催化剂本身电子结构的一种手段,也是一种易于形成缺陷位的手段,在光催化材料的设计中被广泛研究。近年来,国内外已有大量的关于掺杂离子影响光催化性能的研究。吴凯丰团队研究了结构简单的铜掺杂以及未掺杂CdSe量子点的热电子驰豫动力学。研究结果显示亚铜离子可在飞秒时间尺度(≪390fs)快速捕获价带中的光生空穴,减少电子-空穴复合,使量子点中1Pe热电子寿命从约0.25ps 延长到约8.6ps (>30倍)[62]。Schrauzer等[7]首次发现0.2%Fe掺杂TiO2相比于纯TiO2具有更高的氮气还原性能,引起了后续的一系列金属掺杂TiO2的研究(掺杂Co、Mo、Ni、Pd、Pt、Ag、Au、V、Cr、Pb和Cu等)[63-65]。熊宇杰团队[55]通过Mo掺杂超细W18O49载体实现缺陷态的精细调控,结果表明Mo 取代W 原子后,形成了Mo-W中心,实现对氮气的化学吸附及活化;同时利于光生电子从不饱和位点传输至吸附的氮气上,减少载流子的复合(图13)。
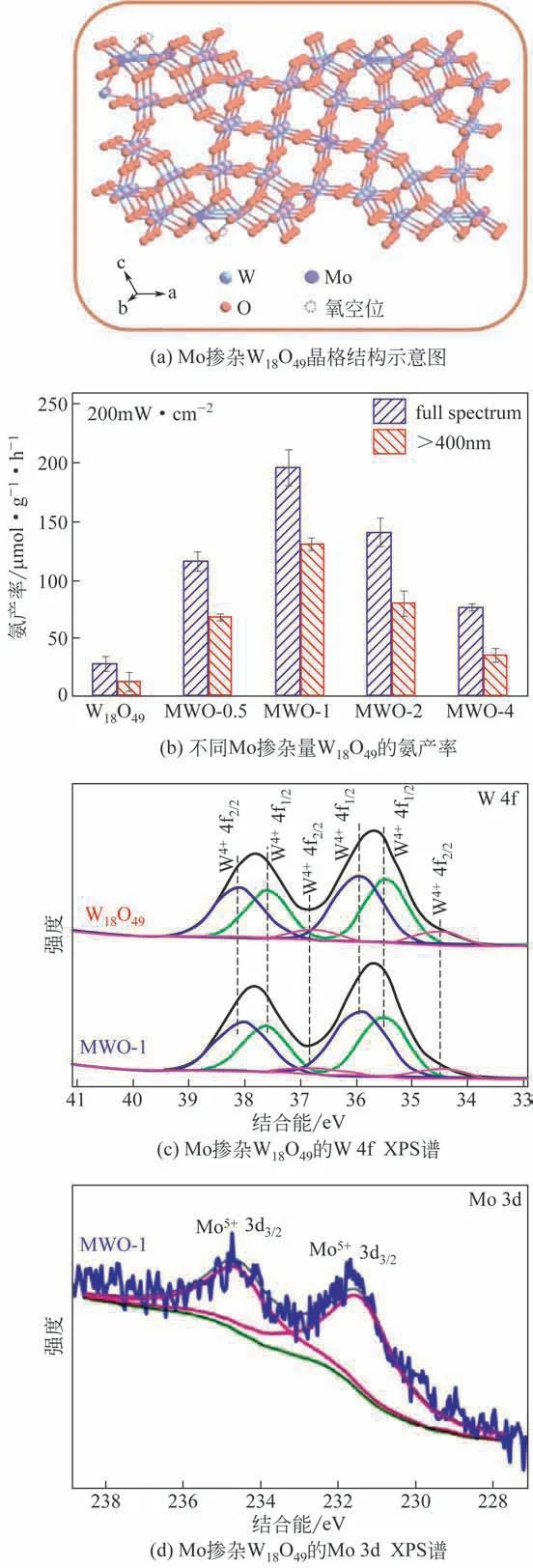
图13 Mo掺杂W18O49晶格结构、产氨活性以及结构表征[55]
通过对半导体进行非金属掺杂,也可以有效实现载流子的分离。Feng等[66]采用一锅水热法合成了氧-硫共掺杂的石墨相氮化碳(HGCNOS),考察其可见光催化氮气还原合成氨性能。数据显示相比于未掺杂的氮化碳,氧硫共掺杂后的石墨相氮化碳表现出更高的光催化活性,达2180μmol/(g·h)。Li等[67]报道了一种碳掺杂钨酸(WO3·H2O)复合物的光催化氮气还原性能,其中C的存在促进了光生电子的分离和传输。在模拟光照条件下,该复合物的氮气还原活性达205μmol/(g·h)。通过系列对比,他们发现C掺杂方法具有普适性,C掺杂光催化剂对比未掺杂的光催化剂具有更高的氮气还原活性。为了便于分析和比较,表3列出了构建缺陷位强化载流子分离的光(电)催化剂的产氨活性,并对温度、光源、牺牲剂的选择等条件进行了适当的总结。
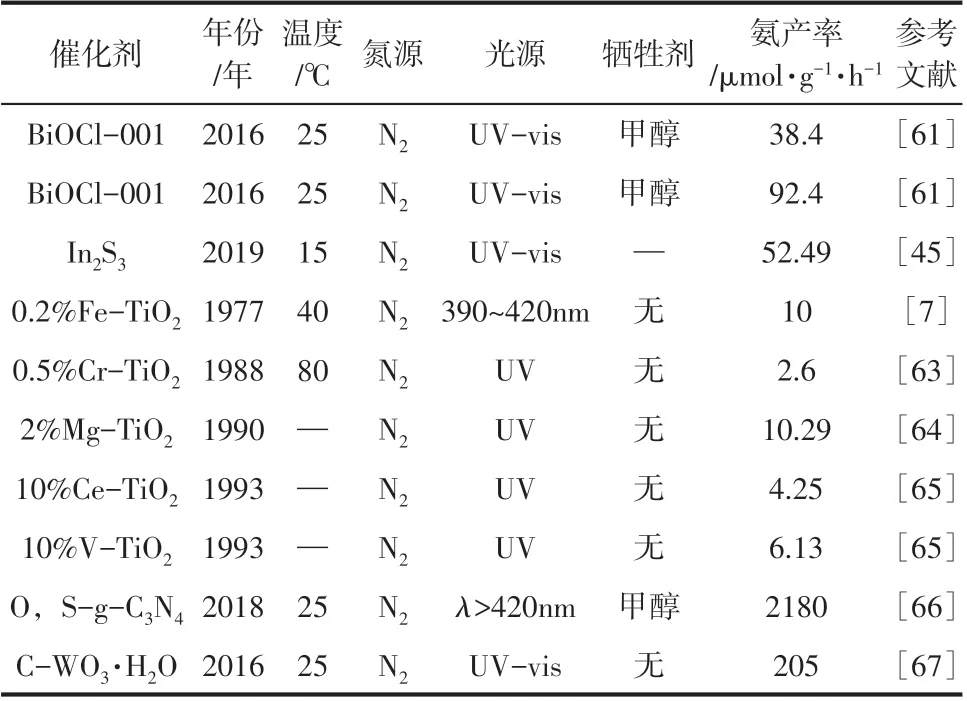
表3 构建缺陷位强化载流子分离的光(电)催化剂总结
4.3 构建异质结结构
单一的半导体氮气还原光催化剂虽然本身具有较强的还原能力,但是通常面临着光生载流子分离效率低的挑战,导致载流子易于复合,氮气还原性能低。鉴于此,相关学者通过构建异质结调控光生电子和空穴的传输方向,强化载流子的分离和传输。通过构建匹配良好的异质结光催化剂体系还可以充分发挥各组分之间的优势,比如增加光吸收范围,增强光稳定性,提高电子和空穴的有效利用率。
Hu 等[68]以rGO 为导电基质,通过静电自组装技术构建2D/2D g-C3N4/rGO复合异质结体系增加了g-C3N4/rGO之间的接触面积,促进电子的转移和传输并减少空穴-电子的复合,使得催化性能提高5倍。Zhang 等[69]选取导带和价带能级与g-C3N4匹配良好的金属硫化物,构建g-C3N4/ZnMoCdS Ⅱ型异质结光催化氮气还原体系[图14(a)],证实g-C3N4与ZnMoCdS 之间具有良好的能级匹配关系,使得光生电子-空穴对的分离更有效,界面电荷转移更快,提高了光催化剂的活性。Xue 等[70]通过简单的水热法制备Bi2MoO6纳米棒锚定具有氧空位的BiOBr纳米片的p-n异质结光催化剂,此异质结体系具有匹配的带隙结构,在无贵金属助催化剂和牺牲试剂的条件下,仍具备较高的光利用效率和光生电子-空穴对分离特性。Shi等[71]采用阳极氧化、电子束蒸发和化学气相沉积(CVD)相结合的简便方法制备了WS2@TiO2纳米多孔膜。由于WS2与TiO2的能级匹配良好,在WS2@TiO2中可以形成Ⅱ型异质结,增强了电荷-载流子的分离和转移。经过WS2与TiO2之间比例优化,20WS2@TiO2(20 为W 层厚度)复合体系具有最高活性,达1390μmol/(g·h)。

图14 g-C3N4/ZnMoCdS体系Ⅱ型异质结机制和MgAlFeO(2)-CN体系Z型异质结机制[69,72]
传统的异质结结构能带关系多是type Ⅱ型,这种类型的能带匹配容易实现载流子的有效分离,但是同时会造成复合半导体整体的氧化还原能力下降。在此情况下,可以保持本身氧化还原能力的Z型异质结结构引起研究者的关注。Wang 等[72]原位制备了Z 型g-C3N4/Mg1.1Al0.3Fe0.2O1.7纳米棒复合异质结材料证实了g-C3N4和Mg1.1Al0.3Fe0.2O1.7两组分之间存在着较强的电子耦合,促进了光生电子-空穴对的有效分离和界面电荷转移[图14(b)],具有较高的氮气还原产氨活性和稳定性,经过优化后的复合催化剂的催化活性是纯g-C3N4的3.5 倍。Liang 等[73]将具有合适的禁带宽度和大量氧空位的W18O49与氮化碳复合构建Z型异质结催化剂,同样证实了构建异质结体系可以提高太阳能的利用,特别是在近红外区域,而且可减少光生电子-空穴对的组合。经过比例优化的W18O49(0.6)/g-C3N4具有最高的光生电子-空穴对分离效率和氮气还原活性,活性达144.5μmol/(g·h),是纯g-C3N4的7.2倍。由于g-C3N4和CsxWO3分别具有优异的导电性和质子导电性。Shi等[74]选择g-C3N4/CsxWO3(CW)纳米复合材料作为光催化剂,结合TEM 表征技术发现CsxWO3纳米棒分散在单层g-C3N4纳米薄片表面,证明了单层厚度的g-C3N4可以改善电子空穴对的分离。在无贵金属助催化剂的情况下,g-C3N4/CsxWO3复合材料在全光谱下可以有效地将氮气还原为NH3。
4.4 助剂强化
除了构建异质结体系之外,通过添加助催化剂,半导体和助催化剂之间的界面接触会产生电场,也可以有效地分离光激发的电子和空穴,使光生电子-空穴对的再复合概率降低,提高半导体光催化剂的催化效率。为了便于分析和比较,表4列出了构建异质结结构/助剂强化载流子分离的光(电)催化剂的产氨活性,并对温度、光源、牺牲剂的选择等条件进行了适当的总结。贵金属(Pt、Au、Ru 等)作为有效的助剂,实现其负载是强化催化剂载流子分离的一种有效手段。Janet等[75]通过湿法刻蚀和化学沉淀两种湿化学方法合成超晶格型ZnO,利用Pt助催化剂提供适当的费米能级来捕获光生电子,并探究降低光催化分解水产氢和氮气还原过程中电子-空穴对复合的可能性(图15)。Liu等[53]通过设计合成单原子Ru 修饰TiO2纳米片,进一步强化载流子的分离,提高催化活性。含1%Ru的复合催化剂的氨产率最高,达到3.31μmol/(g·h),是纯TiO2纳米片的2倍以上。
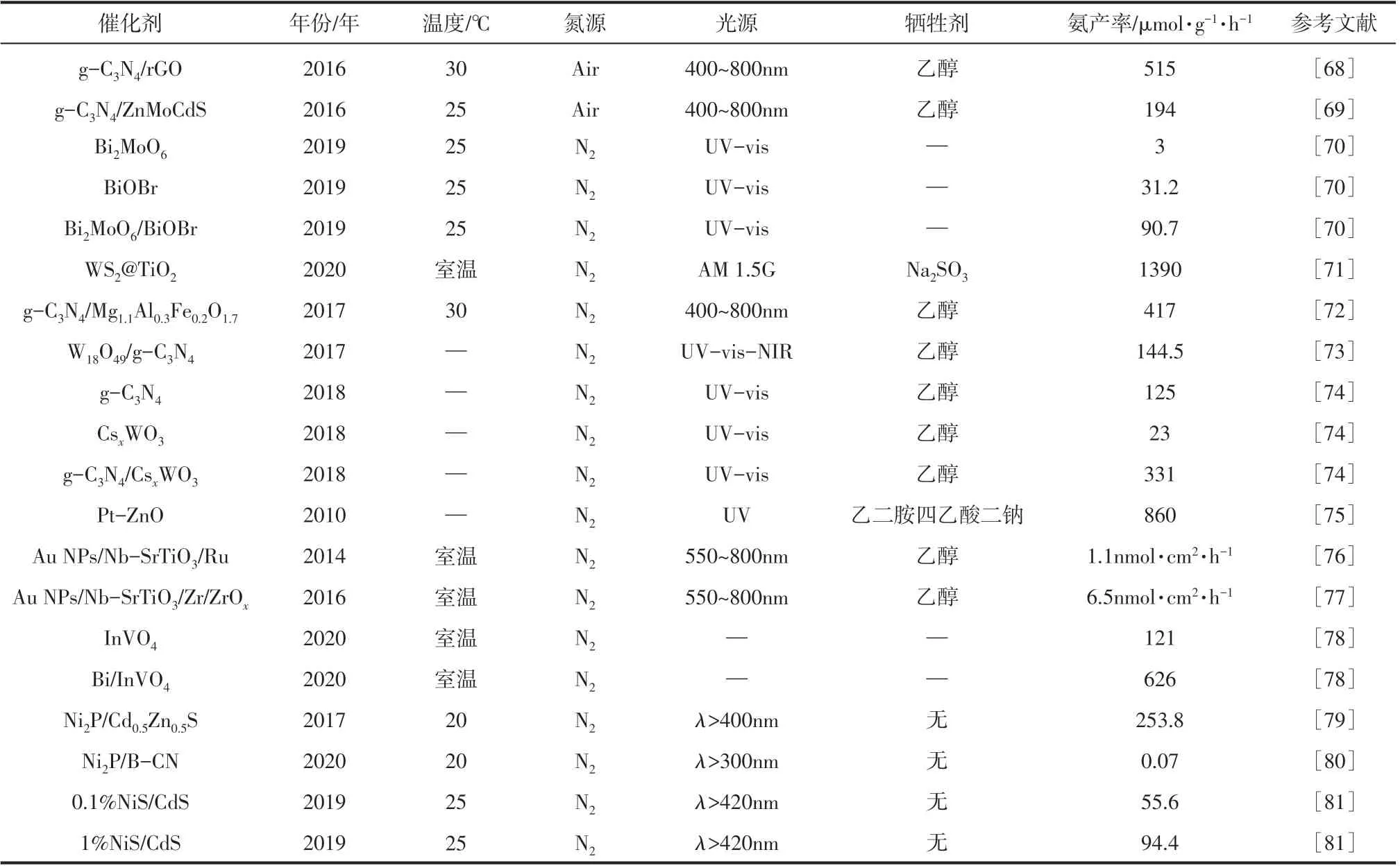
表4 构建异质结结构/助剂强化载流子分离的光(电)催化剂总结
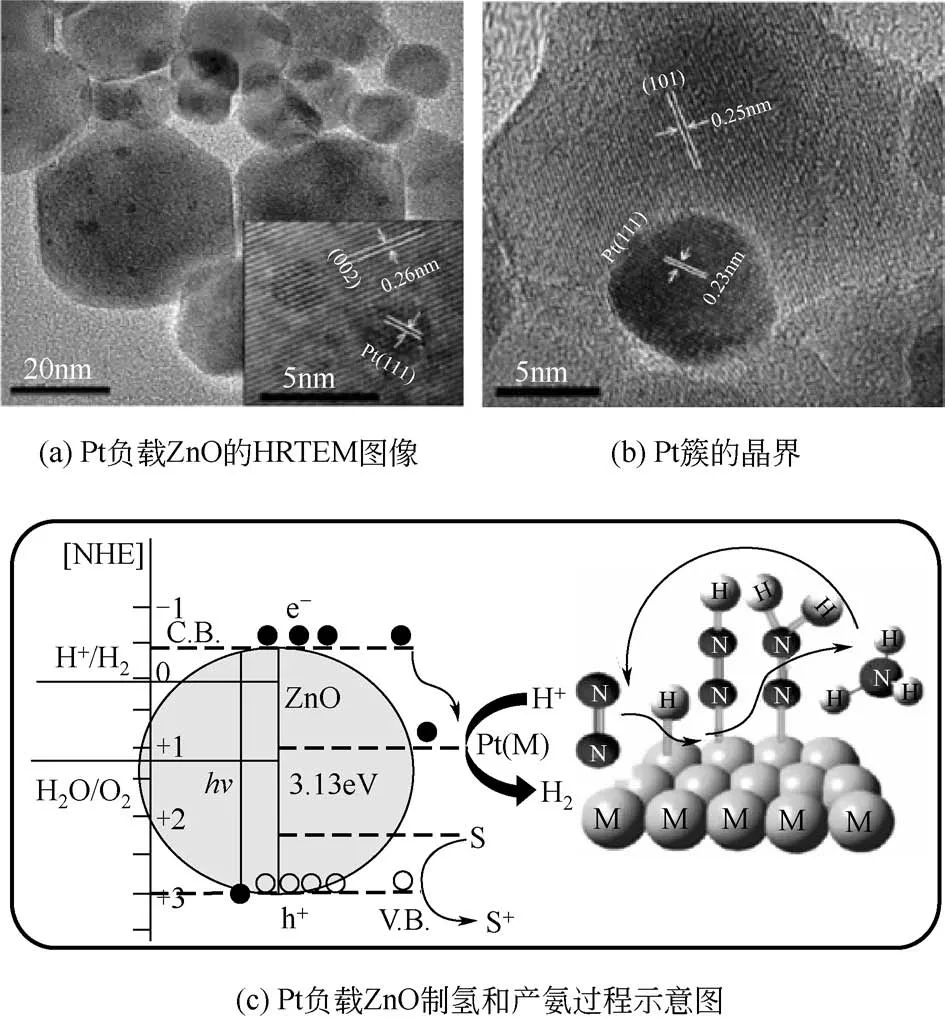
图15 Pt负载ZnO的催化剂性能[75]
Oshikiri 等[76]开发了一种可见光下等离子体诱导的光电协同催化氮气还原合成氨技术,通过在铌(Nb)掺杂钛酸锶(Nb-SrTiO3)半导体光电极的两侧分别负载金纳米颗粒(Au-NPs)和Ru助剂,构建Au-NPs/Nb-SrTiO3/Ru 体系[图16(a)]。研究发现在Au-NPs/SrTiO3界面,等离子体诱导的电荷分离促进阳极氧化以及阴极氮气的还原。后续他们[77]利用Zr/ZrOx薄膜替代Ru 助剂,构建Au-NPs/Nb-SrTiO3/Zr/ZrOx体系。通过对比Zr/ZrOx体系和Ru 体系的氮气还原反应活性[图16(b)],发现Zr/ZrOx具有更高的合成氨活性以及选择性,究其原因是Zr/ZrOx与N原子作用力大于H原子,更偏向于和N原子结合,抑制产氢竞争反应的进行。
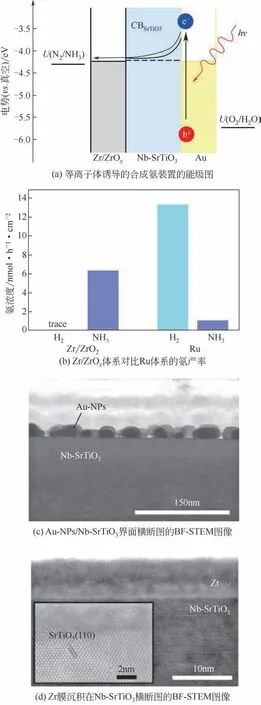
图16 光电协同催化氮气还原NH3技术[76-77]

5 电子-质子转移
在光催化氧化还原反应中,往往伴随着化学计量的光生电子和质子的转移。目前,大部分研究仅仅关注光生电子的转移,研究质子具体转移路径的较少。因为在多相催化体系中,相界面复杂,电子是催化剂与反应物之间发生的离域态/定域态相互转移,质子转移则需考虑相界面以及溶剂化学环境等的影响,历程复杂且难以定义[82]。但相关研究表明,质子转移对光催化反应动力学、反应路径具有重要影响。通常情况下,电子和质子同时发生得失有利于氧化还原反应,将这两个粒子聚集在一起可避免由于局部电荷积聚而产生的高能化学中间体[83]。
由于氮气还原合成氨过程中,涉及多步电子-质子转移过程,通过了解氮气还原过程中具体的电子-质子转移机制,对整体催化效率的提高具有指导作用。目前,在光催化氮气还原合成氨领域中,基于电子-质子转移的研究相对较少。研究者大部分从实验和密度泛函理论计算的角度对各种合成氨光催化剂上氮气的还原机制进行研究,具体的光催化氮气还原机制可分为2种,即解离机制和缔合机制(含交替缔合机制,末端缔合机制)。具体的机制如图17所示。

图17 氮气还原机制
张礼知团队[61]结合理论模拟和原位傅里叶变换红外光谱手段,发现具有氧空位的BiOCl催化剂催化氮气转化为氨的反应经历了几个连续的质子耦合电子转移的低能反应步骤,具体的反应途径取决于氧空位的表面结构。BiOCl-001晶面材料偏向于末端缔合机制,BiOCl-010偏向于交替缔合机制。通过与不具有氧空位的P25对比,结果显示在光催化合成氨过程中,质子辅助电子转移过程与氮气在OVs上的活化水平呈正相关。原因是活化的氮气积聚更了多的负电荷,表现出更强的Lewis 碱度,促使质子靠近,进而促进了氮气固定的后续电子转移,避免了局部电荷积聚。Xie 等[84]在前期研究中发现,由于质子与水分子的相互作用,产生的质子可以很容易地在表面氧原子之间转移。后续他们[85]采用可靠的密度泛函理论的方法,探究了氮气在二氧化钛表面光催化还原的微观机理。计算结果显示二氧化钛经光解水之后形成羟基,此羟基化二氧化钛表面以及激发产生的光生电子促进氮气在氧空位的化学吸附,活化难解离的N N 三键。此外,计算结果显示质子耦合的电子转移过程大大降低了反应的能垒,促使反应易于在温和条件下发生。
鉴于光催化氮气还原合成氨反应过程为六电子反应过程,包含多步加氢质子化过程,整体历程复杂。目前,许多催化剂的氮气还原微观机理仍不清晰。通过研究氮气还原过程中质子/电子转移路径,对提高整体催化反应效率及合理设计氮气还原光催化剂有着重要意义。
6 结语
光(电)催化氮气还原合成氨技术具有清洁可持续、反应条件温和等优点,有望解决工业合成氨所带来的高能耗、环境污染等问题,引起工业界和学术界的热切关注。催化剂作为催化反应的核心,对催化性能起着决定性作用。但目前光(电)催化氮气还原合成氨活性普遍低,需要研究者进一步去合理设计具有高活性、高选择性及高稳定性的催化剂。针对目前基于光(电)催化氮气还原合成氨材料设计的研究仍存在一些不足的情况下,研究者采用先进的表征技术来精确研究氮气还原反应过程中的活性位点和中间体结构,对催化剂设计和选取具有指导意义,如球差校正透射电镜(ACTEM)以及众多原位表征技术[原位同步辐射(SR)技术、原位X 射线光电子能谱(XPS)、原位漫反射傅里叶变换红外光谱(DRFTIRS)、原位电子顺磁共振波谱(EPR)等]。此外,原位FTIR可用于监测催化剂表面官能团随时间产生的变化,有助于确定氨的形成过程,阐明氮气还原机制。利用密度泛函理论,通过对催化剂进行结构优化以及能带结构计算等,可以深入研究缺陷工程调控、能带工程调控等手段对光催化剂的还原电势,以及氮气还原性能的影响,进而辅助氮气还原光催化剂的设计,同时推测氮气还原反应中可能形成的能级,探究氮气还原机理,预测具有氮气还原前途的催化剂,为进一步的实验和应用提供了理论指导。
由于实验耗材以及空气中会携带微量的氨易于造成催化剂氮气还原性能的误测,为了排除实验操作以及大气中的氨污染[86],需要严格规范操作氮气还原反应过程,以及利用同位素标记技术直接有效地检测反应产物来源和途径[87]。此外,产物氨的检测也需要精确的技术手段。目前氨的定量分析常用手段有分光光度法,离子色谱法和核磁共振波谱法。其中离子色谱和核磁共振波谱法是比较精确的检测手段。综合操作方便性、灵敏度、经济性等考虑,利用离子色谱检测氨是一种值得推广的检测手段。需要指出的是目前的光(电)催化氮气还原合成氨技术的实验操作条件并没有统一标准,使不同催化剂之间的氮气还原性能难以深层次比较。在此背景下,研究者通过制定出统一的光催化氮气还原合成氨实验操作标准,可以更为准确地判定催化材料的优劣,利于设计出具有高效氮气还原合成氨催化剂,促进光催化技术的发展。
本文综述了在光(电)催化氮气还原合成氨技术中,基于强化氮气溶解扩散、吸附和活化以及载流子分离和迁移等反应过程的最新研究进展,充分展示了在氮气还原反应中,每一个反应步骤对整体的光催化效率的影响。综合上述,构建具有缺陷位,尤其是具有高选择性的氮空位的催化剂是有效促进氮气的吸附和活化以及载流子分离、提高氮气还原活性的手段。另外,通过进一步设计催化剂体系,使得上述催化剂处于气液界面,增加氮气浓度,有望进一步增强催化活性。尽管目前光(电)催化氮气还原技术仍面临着巨大的挑战,但是通过合理设计光催化材料和优化催化反应体系,强化速控步骤,有望通过可再生能源太阳能实现氨的工业化生产。若能实现此目标,将对自然环境和人类社会发展具有深远意义。

