三种长链烷氧基苯甲酰基硫脲衍生物的合成及其凝胶行为
籍向东, 赵爱娟, 刘 欢, 岳国仁, 曹 成
(河西学院 甘肃省河西走廊特色资源利用重点实验室,甘肃 张掖 734000)
N-取代苯甲酰基硫脲衍生物由于具有可与金属键合的强给电子基团(羰基和硫羰基)在配位化学中得到了广泛的关注[1]。经研究证实,这类衍生物在生物活性[2]、金属离子溶剂萃取[3]、液晶材料[4]等领域有很重要的应用价值。由于化合物中含有电负性较大的硫、氧原子及N—H键,可将其应用于催化剂的制备[5]、阴离子识别[6]及离子传输[7]等研究方向。此外,研究人员发现含有烷氧基团的N-取代苯甲酰基硫脲衍生物在液晶材料制备领域具有潜在的应用价值[8]。其中,含有长链结构的此类化合物由于分子间长链的疏水作用具有良好的凝胶性能,且所含长链结构的位置与个数均对凝胶的形成有一定的影响[9-11]。并且可以通过改变芳环上取代基的位置和个数来调控化合物的凝胶能力,利用小分子的自组装性质制备具有不同凝胶性质的小分子凝胶剂[12-13]。通过长链烷氧基团的引入,可以利用分子中长链的分子间作用力或空间填充的性质形成凝胶,而不是由化合物中氢键所引起[14]。因此,发展新型具有凝胶性质的N-取代苯甲酰基硫脲衍生物仍然是一个具有挑战的课题。
低分子量凝胶在过去的几十年里备受关注,不仅是因为他们多种多样潜在的应用价值,而且对凝胶形成机理的研究一直也有所欠缺[15]。在凝胶形成的过程中,凝胶分子主要通过非共价键自组装的方式结合,其中的非共价键作用主要包括:氢键、π-π相互作用、范德华力作用和偶极作用等[16]。以氢键为例,糖类化合物[17]、核酸[18]、氨基酸[19]及硫脲类凝胶剂[20]在形成凝胶的过程中绝大多数都是以氢键作为主要结合方式。基于部分低分子量凝胶具有温度、pH、阳离子、光、电磁响应等感应性能,可在光电子设备、药物传递及控释、分子监测等领域作为新型功能材料[20-21]。此外,利用小分子凝胶自组装的特殊性质,可以利用纤维状聚集体作为模板将溶剂、甚至化合物分子从凝胶中通过冻干蒸出去,可以得到金属纳米级微粒[22]。为了扩充凝胶分子的种类,长链凝胶分子逐步被研究人员发现,特有的疏水作用赋予凝胶特有的性质[23]。
本文以没食子酸和溴代十四烷为原料,经过烷基化、醇化、酸化及卤代得到中间产物1,化合物1与硫氰酸铵的混合物分别与对硝基苯胺、对硝基苯肼和2,4-二硝基苯肼作用得到3种长链烷氧基苯甲酰基硫脲衍生物2、3和4(Scheme 1),其结构经1H NMR,13C NMR,IR和MS确证,并考察了3种化合物的凝胶行为。
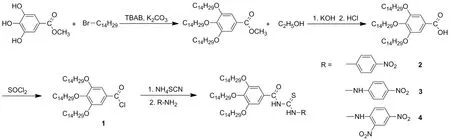
Scheme 1
1 实验部分
1.1 仪器与试剂
Bruker-NMR 400 MHz型核磁共振仪(氘代CDCl3为溶剂,TMS为内标);Nicolet iS50型红外光谱仪;Bruker-micro TOF-Q Ⅲ型电喷雾质谱仪;Quanta450FEG型扫描电子显微镜。
化合物1参照文献[22]合成;其余所用试剂均为分析纯或化学纯。
1.2 合成
(1)化合物2~4的合成(以2为例)
称取11.50 g(2 mmol)和硫氰酸铵0.31 g(4 mmol),搅拌下加入丙酮20 mL,加入0.5 mL PEG-400,升温回流,反应2 h(TLC检测)。完成后不经分离,直接加入对硝基苯胺0.28 g(2 mmol),继续回流2 h,冷却至室温,将反应液倒入冰水混合物中搅拌至出现絮状沉淀,过滤,滤饼用冷丙酮(3×10 mL)洗涤,干燥后得化合物2,化合物3和4的合成方法与化合物2类似。
化合物2:淡黄色固体1.45 g,收率77%,m.p.69~71 ℃;1H NMRδ: 11.04(s, 2H), 9.14(d,J=4.0 Hz, 2H), 8.31(dd,J=4.0 Hz, 1H), 8.29(dd,J=4.0 Hz, 1H), 7.97(d,J=8.0 Hz, 2H), 4.05(m, 6H), 1.79(m, 6H), 1.47(m, 6H), 1.26(m, 60H), 0.88(t,J=8.0 Hz, 9H);13C NMRδ: 178.26, 167.05, 153.58, 145.18, 143.75, 143.33, 126.31, 125.46, 124.61, 123.09, 113.56, 106.29, 73.77, 69.68, 31.92, 29.73, 29.70, 29.66, 29.37, 29.36, 29.30, 26.05, 22.68, 14.09; IRν: 3360, 2954, 2850, 2920, 1710, 1570, 1470, 1340, 1227, 1111 cm-1; MS(ESI)m/z: Calcd for C56H95N3O6S{[M+K+H2O+2H]+}996.684, found 996.604。
化合物3:黄色固体1.49 g,收率78%,m.p.44~46 ℃;1H NMRδ: 13.16(s, 1H), 9.01(s, 1H), 8.30(d,J=8.0 Hz, 1H), 8.08(m, 3H), 7.04(s, 1H), 6.63(d,J=8.0 Hz, 2H), 4.03(m, 6H), 1.84(m, 6H), 1.56(m, 3H), 1.47(m, 6H), 1.26(m, 57H), 0.88(t,J=8.0 Hz, 9H);13C NMRδ: 182.49, 169.21, 166.34, 153.47, 153.09, 150.40, 147.94, 139.90, 126.13, 111.58, 106.23, 31.93, 30.32, 29.74, 29.70, 29.66, 29.64, 29.36, 29.29, 26.07, 25.33, 22.68, 15.76, 14.10; IRν: 3299, 2954, 2850, 2920, 1720, 1617, 1430, 1330, 1220, 1120 cm-1; MS(ESI)m/z: Calcd for C56H96N4O6S{[M+K+H2O-H]+}1008.671, found 1008.830。
化合物4:深黄色固体1.64 g,收率82%,m.p.62~64 ℃;1H NMRδ: 8.36(d,J=12.0 Hz, 1H), 8.25(d,J=8.0 Hz, 1H), 8.14(s, 1H), 8.12(d,J=8.0 Hz, 1H), 7.90(d,J=8.0 Hz, 1H), 7.56(d,J=8.0 Hz, 1H), 7.05(d,J=8.0 Hz, 2H), 4.02(m, 6H), 1.82(m, 6H), 1.47(m, 6H), 1.26(m, 60H), 0.88(t,J=8.0 Hz, 9H);13C NMRδ: 169.25, 155.16, 153.46, 153.09, 152.05, 145.15, 137.68, 129.98, 128.99, 123.54, 116.36, 106.26, 73.53, 69.43, 31.92, 30.32, 29.73, 29.70, 29.66, 29.63, 29.36, 26.07, 25.48, 22.68, 16.99, 14.09; IRν: 3320, 2954, 2850, 2920, 1730, 1610, 1470, 1331, 1295, 1110 cm-1; MS(ESI)m/z: Calcd for C56H95N5O8S{[4M+H]+}3993.775, found 3993.776。
1.3 凝胶实验
将0.05 g化合物加入一个密闭的玻璃瓶中,然后再加入0.5 mL待测纯溶剂,通过加热使化合物全部溶解,冷却至室温,观察冷却后的结果并记录实验现象。上述实验中所使用的纯溶剂均为分析纯,且未纯化直接使用。
2 结果与讨论
2.1 化合物2、3 和4 的凝胶行为
详细研究测试了在20种常见纯溶剂中3种化合物2、3和4的凝胶行为,凝胶实验溶液的浓度为5.5 mg/mL,如表1所示。
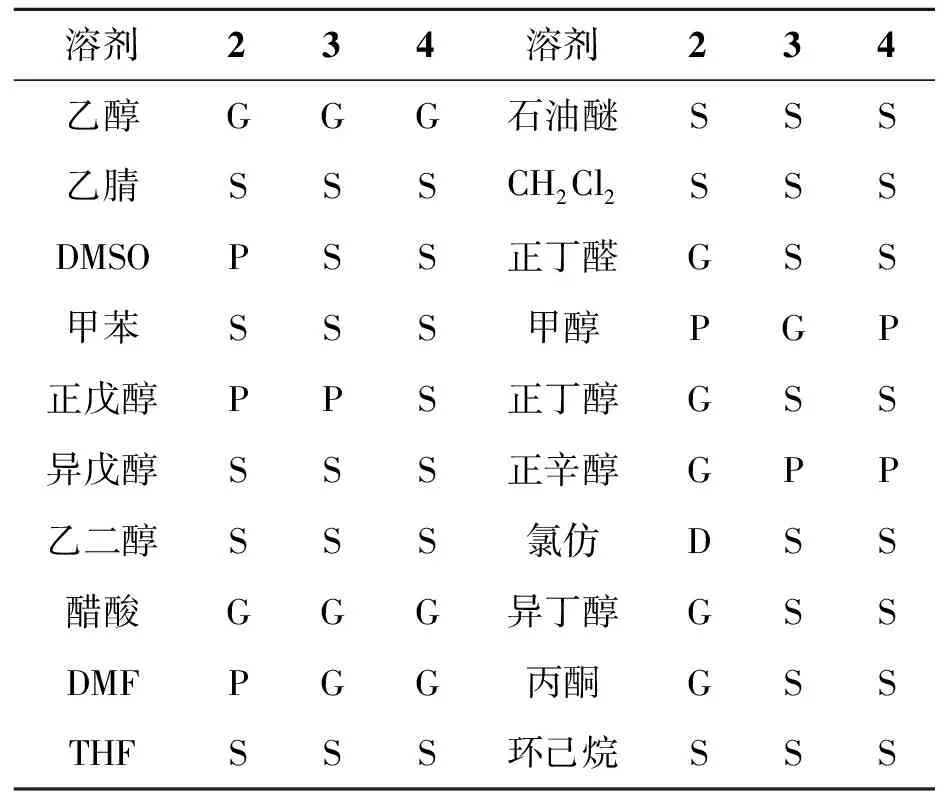
表1 化合物2、3 和4 在不同溶剂中的凝胶行为#

图1 化合物在乙醇中凝胶示意图
化合物2在测试的20种纯溶剂中可以形成7种凝胶,形成的凝胶包括醇类(乙醇、正丁醇、异丁醇、正辛醇)、羧酸类(醋酸)、醛酮类(正丁醛、丙酮),并且均为不透明凝胶,而在DMSO、正戊醇、DMF和甲醇中形成沉淀。从极性角度分析,能够形成凝胶的纯溶剂均为极性溶剂,主要是由于溶剂极性的升高促进了长链烃基的疏水聚集能力,从而更容易形成凝胶。在这20种纯溶剂中,化合物3在乙醇、醋酸、DMF、甲醇中形成凝胶,且在正戊醇和正辛醇这两种醇类试剂中有沉淀。而在化合物2形成凝胶的正丁醇、异丁醇、正辛醇、正丁醛和丙酮中,化合物3则为溶液。这可能是由于化合物3比化合物2多了一个N—H键,形成更多的氢键,从而使化合物3的极性增强。
化合物在乙醇中均为黄色不透明凝胶。2中酰基硫脲单元可与DMF分子形成分子间氢键而使得分子刚性增加,不能形成凝胶。与化合物2和3相比,化合物4仅在极性较大的乙醇、醋酸和DMF中形成凝胶,而在甲醇和正辛醇中形成沉淀。考虑到化合物4的结构中含有2个强吸电子的硝基基团,增加了化合物的极性,且邻位硝基的引入在一定程度上增强了其形成分子内氢键的能力,从而降低了分子间的聚集能力,最终导致化合物4形成凝胶的能力有所减弱。通过以上分析可知,活泼氢的个数及分子的极性对化合物的凝胶行为有一定影响。因此,可以通过替换芳香环取代基及胺,肼等含可形成氢键单元,实现对化合物凝胶能力的有效调控。
2.2 凝胶的微观形貌
通过SEM技术对3种凝胶剂在不同溶剂中所形成凝胶进行微观结构分析,测试样品是将刚制备的凝胶经冷冻干燥所得到的干凝胶,同时利用导电胶固定于样品台,并进行喷金处理。
如图2所示,通过对3种典型不同溶剂干凝胶的SEM图分析可知,化合物中活泼氢和硝基个数对凝胶的微观结构具有一定的影响。化合物2在乙醇中形成了条带状网格结构(图2a),条带宽度约为1 μm。多了一个N—H键的化合物3在醋酸中形成的凝胶与化合物2差别较大,形成了不规则的叶片形状(图2b)。多了一个N—H键和硝基的化合物4在DMF中同样形成了不规则的叶片结构,且叶片致密,凹凸不平(图2c)。正是由于在整个凝胶体系中充满了这些条带或叶片的堆积,使得溶剂被固定而形成凝胶。

图2 化合物2、3和4在不同溶剂中形成的干凝胶SEM图(a.乙醇; b.醋酸; c.DMF)
以没食子酸和溴代十四烷为最初原料,合成了3种长链烷氧基苯甲酰基硫脲衍生物2、3和4,并考察研究了这3种化合物的凝胶行为。结果表明:3个化合物N—H键和硝基个数的差异,导致分子极性及聚集能力不同,形成凝胶的能力化合物2>3>4。不同化合物及溶剂形成凝胶的微观结构具有一定的差异。该类长链烷氧基苯甲酰基硫脲衍生物的开发对长链有机化合物的发展及凝胶制备领域均有参考及应用价值。
——以高中化学“氢键”的教学为例

