坎地沙坦酯聚乙烯吡咯烷酮K30共沉淀物分散片的制备与质量评价
徐丽清,张丽妍(大连市第三人民医院药剂科,大连 116033)
坎地沙坦酯属于血管紧张素Ⅱ(Ang Ⅱ)受体亚型高选择性竞争拮抗剂[1-2],在临床主治高血压、动脉粥样硬化、充血性心力衰竭以及代谢综合征[3]。坎地沙坦酯属于生物药剂学分类系统(BCS)Ⅱ类药物,在水中溶解度较差[4-5],口服生物利用度仅为15%。文献报道[6-9],将难溶性药物与聚乙烯吡咯烷酮K30 (PVP-K30)制备成共沉淀物,不仅能有效增加药物的溶解度,加快药物释放,提高药物口服生物利用度,而且共沉淀物物理化学性质稳定,可作为中间体制备成片剂或胶囊,便于患者服用与携带。本研究通过共沉淀技术将坎地沙坦酯与PVP-K30制备成共沉淀物,并进一步制备成分散片[10-11],以期增加药物的口服生物利用度和治疗效果,为坎地沙坦酯的临床应用提供更多选择。
1 仪器与试药
1.1仪器 YND-A1型差热分析仪(上海盈诺精密仪器有限公司);Aeris型台式X射线衍射仪(马尔文帕纳科公司);FTIR-8300型岛津红外光谱仪(日本岛津公司);YD-1型片剂硬度仪(天津市光学仪器厂);LB-2D型崩解时限仪(天津创兴电子设备制造厂);ZP-8型压片机(天祥健台制药机械厂);ZRS-8G型智能溶出试验仪(天大天发科技有限公司);KH3200B型超声波清洗器(予华仪器有限责任公司)。
1.2试药 坎地沙坦酯原料药(珠海润都股份有限公司,批号56713040205);坎地沙坦酯片(日本武田药品工业株式会社,规格:4 mg,批号1207A);微粉硅胶(Aerosil 200,赢创德固赛中国投资有限公司);聚乙烯吡咯烷酮K30(PVP-K30,上海源叶生物科技有限公司);乙醇(国药集团化学试剂有限公司);羧甲基淀粉钠、羟丙基纤维素、微晶纤维素、乳糖和交联聚维酮,均购于安徽山河药用辅料股份有限公司;预胶化淀粉(山东聊城阿华制药有限公司);低取代羟丙基纤维素、硬脂酸镁和甘露醇,均购于湖州展望药业有限公司;溴化钾(百灵威科技有限公司)。
2 方法与结果
2.1坎地沙坦酯PVP-K30共沉淀物的制备 将一定比例的坎地沙坦酯与PVP-K30溶解于少量乙醇中,加入Aerosil 200,超声30 min,使其完全分散于溶液中;再将溶液置于恒温水浴锅内,在50 ℃条件下不断搅拌溶液,挥干乙醇;回收残留的共沉淀物,将其置于真空干燥箱内过夜,以确保乙醇溶剂完全挥发;将共沉淀物经机械粉碎后过40目筛网,即得到坎地沙坦酯PVP-K30共沉淀物粉末。经测定坎地沙坦酯PVP-K30共沉淀物中药物含量为0.2 g·g-1[12-13]。
2.2坎地沙坦酯PVP-K30共沉淀物表征
2.2.1差热分析(DTA) 使用差热分析仪对坎地沙坦酯、Aerosil 200、PVP-K30和坎地沙坦酯PVP-K30共沉淀物进行差热分析。每份样品称取5 mg,置于铝盘中,在氮气保护下(流速为30 mL·min-1),以每分钟升10 ℃的扫描速率加热,扫描温度范围为25~300 ℃。经差热分析仪测定坎地沙坦酯原料药有2个吸热峰,第1个吸热峰Tm(吸热峰对应的温度)值为171.3 ℃,为药物熔点,可以说明坎地沙坦酯是以某种结晶状态存在;第2个吸热峰Tm值为283.2 ℃,表示药物在该温度条件下碳化分解;PVP-K30具有1个较宽的吸收峰,吸热峰Tm值为54.6 ℃,经分析该吸热峰是由于PVP-K30中水分蒸发吸热所致;Aerosil 200为无机盐,无吸收峰;坎地沙坦酯PVP-K30共沉淀物中药物的吸热特征峰消失,且无其他显著吸热峰,说明坎地沙坦酯在共沉淀物中以无定形存在。
2.2.2X射线粉末衍射分析(XRD) 取坎地沙坦酯原料药、Aerosil 200、PVP-K30和2.1项下制备的地沙坦酯PVP-K30共沉淀物样品,分别进行XRD分析,工作参数为:Cu K辐射源,辐射波长为1.542 Å,高压40 kV,电流40 mA,扫描2θ角度范围为3°~60°,扫描速率为0.02°·s-1。XRD分析结果显示,Aerosil 200和PVP-K30的衍射图完全无任何特定的衍射峰,显示为漫射图,这说明Aerosil 200与PVP-K30是非晶体;坎地沙坦酯的衍射图谱中2θ角有5.8°,10.1°,11.9°,17.46°,18.84°,19.44°,20.46°,22.38°,23.43°,25.29°等多个独特衍射峰,说明坎地沙坦酯原料药是高度结晶态;而在共沉淀物的衍射图中,不存在坎地沙坦酯原料药的任何吸收特征峰,这表明坎地沙坦酯的结晶度显著降低,在共沉淀物中以非晶体形态存在。
2.2.3傅里叶变换红外光谱分析(FTIR) 取坎地沙坦酯原料药、Aerosil 200、PVP-K30和2.1项下制备的坎地沙坦酯PVP-K30共沉淀物样品,分别与溴化钾粉末研磨后压片,经傅里叶变换红外光谱扫描分析,扫描范围为400~5 000 cm-1,分辨率为2 cm-1。经FTIR检测,坎地沙坦酯原料药在3 385 cm-1处为四唑环N-H键的伸缩振动吸收峰,2 924 cm-1处为芳香环上C-H键的伸缩振动吸收峰,2 846 cm-1处为脂肪链上(-CH2,-CH3)的C-H键的伸缩振动吸收峰;1 710,1 745 cm-1处为2个羰基(C=O)的特征峰,1 603 cm-1处为四唑环N-H键的弯曲振动吸收峰;1 238 cm-1处为芳香环上C-N键的伸缩振动吸收峰,740 cm-1为脂肪链上C-H键的弯曲振动吸收峰;1 036 cm-1处为C-O-C的伸缩振动吸收峰。PVP-K30的FTIR谱图显示,1 658 cm-1为羰基特征峰,3 450 cm-1处非常宽的谱带表明了水分的存在,说明PVP-K30具有吸湿性,与DTA的结果相符合。Aerosil 200的光谱图在3 426,3 105 cm-1处的宽峰是羟基(O-H)的伸缩振动吸收峰;1 089 cm-1处为Si-O键的对称伸缩振动吸收峰,1 640 cm-1处为结晶水分子H-O-H的弯曲振动吸收峰,820,470 cm-1处分别为Si-O键的反对称伸缩振动吸收峰和弯曲振动吸收峰。坎地沙坦酯PVP-K30共沉淀物的FTIR光谱图与坎地沙坦酯原料药相比,药物的主要特征吸收峰无明显变化,表明坎地沙坦酯和其他辅料之间未产生化学反应和相互作用。
2.3坎地沙坦酯PVP-K30共沉淀物分散片的制备 坎地沙坦酯PVP-K30共沉淀物粉碎后过80目筛,其他辅料过30目筛,按处方量将共沉淀物与辅料混合均匀,采用粉末直压法进行压片[14]。制剂规格为4 mg。采用单因素考察方法,以分散片的外观、硬度、脆碎度、崩解时限以及10 min溶出度作为评价指标,对分散片的填充剂、崩解剂和润滑剂的用量进行筛选。
2.3.1填充剂种类的筛选 以硬脂酸镁作为润滑剂,以交联聚维酮作为崩解剂,按处方F1~F5进行压片,对填充剂种类进行筛选,见表1。实验结果见表2。

表1 填充剂种类筛选实验
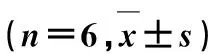
表2 填充剂筛选实验结果
按照处方F1~F5制备分散片,硬度、脆碎度及崩解时限均符合要求,其中按处方F5制备的分散片在10 min时溶出度最高,因此本研究选用微晶纤维素与乳糖(1∶1)作为分散片的填充剂。

表3 崩解剂种类筛选实验
2.3.2崩解剂种类的筛选 以硬脂酸镁为润滑剂,微晶纤维素与乳糖(1∶1)为填充剂,按处方F6~F9进行实验,对崩解剂种类进行考察,见表3。实验结果见表4。
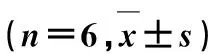
表4 崩解剂筛选实验结果
按照处方F6~F9制备的分散片,硬度、脆碎度及崩解时限均符合要求,其中处方F6的崩解时限最短,且在10 min时溶出度最高,因此本研究选择交联聚维酮作为坎地沙坦酯PVP-K30共沉淀物分散片的崩解剂。
2.3.4润滑剂用量的筛选 以微晶纤维素与乳糖(1∶1)作为填充剂、交联聚维酮作为崩解剂,按处方F10~F14进行实验,对润滑剂硬脂酸镁用量进行考察,见表5。实验结果见表6。

表5 润滑剂用量筛选实验
F10、F11和F12的处方制备过程中出现黏冲现象,无法正常压片。这是由于润滑剂硬脂酸镁加入量不足导致;而按照F14处方制备的分散片,在10 min时的溶出度明显降低,这是由于硬脂酸镁具有疏水性,加入量过多,减慢了药物的溶出速度。因此本研究确定坎地沙坦酯PVP-K30共沉淀物分散片中硬脂酸镁的加入量为4 mg。
2.4体外溶出度比较 通过溶出度Ⅱ法(桨法)比较自制坎地沙坦酯PVP-K30共沉淀物分散片与市售坎地沙坦酯分散片的体外药物溶出速率[15]。随机选取用F13处方制备的坎地沙坦酯PVP-K30共沉淀物分散片与市售坎地沙坦酯分散片,各6片。溶出度测定条件:转速为 50 r·min-1,溶出介质为pH 6.8磷酸盐缓冲液(含有3.5 g·L-1十二烷基硫酸钠),介质体积为900 mL,取样时间点分别为5,10,15,20,30,45,60 min,测定各时间点的累积溶出度,结果见表7。
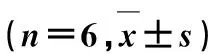
表6 润滑剂用量筛选实验结果
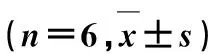
表7 坎地沙坦酯PVP-K30共沉淀物分散片与市售坎地沙坦酯分散片体外溶出度
由表7可知,坎地沙坦酯PVP-K30共沉淀物分散片在10 min时溶出度为79.3%±0.3%,而市售坎地沙坦酯片在10 min时溶出度为22.5%±0.5%,坎地沙坦酯PVP-K30共沉淀物分散片的最终溶出度为96.7%±0.6%,市售坎地沙坦酯分散片的最终溶出度为86.2%±0.4%,说明本研究制备的坎地沙坦酯PVP-K30共沉淀物分散片的体外溶出速率明显高于市售坎地沙坦酯分散片。
2.5稳定性考察 考察坎地沙坦酯PVP-K30共沉淀物分散片在加速(40 ℃、相对湿度为75%)条件下的稳定性,定时取样测定坎地沙坦酯PVP-K30共沉淀物分散片的晶型、崩解时限和10 min时的溶出度,实验结果见表8。
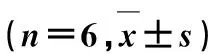
表8 加速条件下稳定性实验结果
由表8可知,在加速6个月时间内,坎地沙坦酯PVP-K30共沉淀物分散片药物始终以无定形存在,未发生转晶或生成新的晶型;崩解时限基本无变化,10 min溶出度为80.2%±5.9%,未发生明显改变。由此可见,坎地沙坦酯PVP-K30共沉淀物分散片稳定性良好。
3 讨论
溶解度低、溶出困难是导致坎地沙坦酯口服生物利用度低的主要原因。目前国内外研究人员通过制剂技术来提高坎地沙坦酯的溶解度,主要包括β-环糊精包合物[16]、自乳化释药系统[17]和纳米粒[18]等。这些技术虽然能提高坎地沙坦酯的溶解度,但不够显著,且稳定性不佳,无法从根本上解决坎地沙坦酯生物利用度低的难题。本研究以Aerosil 200作为载体,以PVP-K30作为亲水型聚合物,通过共沉淀方法将坎地沙坦酯原料药制备成坎地沙坦酯PVP-K30共沉淀物,以提高坎地沙坦酯的溶出速率和溶解度。应用DTA、FTIR及XRD对坎地沙坦酯PVP-K30共沉淀物进行表征,结果显示,制备的共沉淀物中药物与辅料之间未发生化学作用,同时证明药物以无定形存在,这种变化有利于坎地沙坦酯的溶出。
由于口服分散片具有比普通片剂崩解更快的特点,为了进一步提高坎地沙坦酯的溶出速率和溶出度,本研究将坎地沙坦酯PVP-K30共沉淀物制备成口服分散片。通过对口服分散片处方中填充剂、崩解剂以及润滑剂用量的考察,筛选出了最佳制备处方,成功制备了符合要求的坎地沙坦酯PVP-K30共沉淀物分散片。
本研究对制备的坎地沙坦酯PVP-K30共沉淀物分散片以及市售坎地沙坦酯片进行溶出实验,坎地沙坦酯PVP-K30共沉淀物分散片的溶出速率以及溶出度均明显高于市售坎地沙坦酯片,这说明本研究达到了提高坎地沙坦酯溶出速率和溶出度的目的。

