Toric IOL植入与角膜缘松解切开术矫正白内障低中度角膜散光的效果及安全性观察
黄燕治,欧婷婷,吴瑜瑜
随着医学水平发展和患者对术后视功能要求的提升,白内障手术已逐渐演变为屈光性手术,摘除混浊晶状体同时矫正角膜散光并控制手术源性散光(surgically induced astigmatism, SIA)对改善患者术后视力具有重要意义[1]。角膜切开术和散光矫正型人工晶状体(toric intraocular lens, Toric IOL)植入均为现阶段矫正角膜散光常用方法,对提升白内障术后视功能具有重要意义,其中角膜缘松解切开术(limbal relaxingincision, LRI)是角膜切开常用术式,操作简单且经济实用,尤其对低中度角膜散光(1.0~2.0 D)效果良好[2-4]。既往研究表明,Toric IOL植入可对1.0~4.5 D的散光进行矫正,LRI最高可以矫正约3 D的散光[5],但关于二者对低中度角膜散光治疗效果的报道尚少。本研究主要分析Toric IOL植入和LRI对白内障患者低中度角膜散光的矫正效果和安全性,为临床选择合理手术方案提供更多循证医学证据。
1 资料与方法
1.1一般资料 选取2016年1月—2020年1月我院行白内障超声乳化及散光矫正治疗患者90例(90眼)。纳入标准:①完成白内障超声乳化及散光矫正治疗;②角膜规则散光1.0~2.0 D;③年龄18~80岁;④单眼患病;⑤Emery-Little分级Ⅰ~Ⅳ级;⑥术后完成6个月随访且临床资料完整;⑦患者及家属知晓本研究并签署同意书。排除标准:①有其他眼部器质性疾病或病史;②伴眼内手术或外伤史;③角膜不规则散光或伴高度近视。90例根据手术方案不同分为两组,其中观察组38例(38眼),男17例,女21例;年龄43~79(61.85±9.27)岁;左眼17例,右眼21例;Emery-Little分级包括Ⅰ级8例、Ⅱ级13例、Ⅲ级15例及Ⅳ级2例。对照组52例(52眼),男28例,女24例;年龄41~78(62.14± 9.56)岁;左眼27例,右眼25例;Emery-Little分级包括Ⅰ级11例、Ⅱ级19例、Ⅲ级17例及Ⅳ级5例。两组临床资料比较差异无统计学意义(P>0.05),具有可比性。本研究经福建医科大学附属第二医院医学伦理委员会批准。
1.2研究方法 两组入院后完善相关检查并择期手术。观察组将术眼角膜曲率K1、K2及其轴位和眼轴长度等信息导入SRK/T公式计算人工晶状体球镜度数,然后综合SIA等数据采用爱尔康公司在线计算器选择Toric IOL型号和预设轴位。术前3 d给予妥布霉素滴眼液预防感染,每日3次,术前30 min予复方托吡卡胺滴眼液散瞳,每5 min 1次,至瞳孔直径约8 mm后向结膜囊滴加聚维酮碘消毒30 s并以0.9%氯化钠注射液冲洗,术前15 min采用0.5%丁卡因表面麻醉,在裂隙灯显微镜下根据术前标记的0°和180°轴位做手术切口和Toric IOL轴位标记,3 mm角膜缘内三阶梯透明切口,5~6 mm连续环形撕囊,水分离后采用超声乳化术粉碎并吸除晶状体核,I/A系统吸除晶状体皮质并抛光后囊膜,囊袋内填充黏弹剂,植入Toric IOL并顺时针方向旋转至距目标轴位10°~20°后彻底清除Toric IOL前后方黏弹剂,继续调整Toric IOL轴位使其与术前预设轴位一致,轻压光学部以确保Toric IOL贴附后囊,完成后重建前房并水密切口,术后第1日起采用妥布霉素滴眼液,每日4次,每5 d减量1次,至0次后停药,同时每日睡前给予复方托吡卡胺滴眼液3~4次散瞳,每次间隔5 min,术后1个月复查无异常后停药。
对照组术前在裂隙灯下采用Pentacam测量散光轴位并标记陡峭轴位置,根据每90° LRI矫正1.5 D角膜散光,将K值、SIA和隧道位置导入公式计算角膜缘松解切口,术前常规消毒铺巾并以0.5%丁卡因表面麻醉,采用角膜散光定位环在角膜周边血管拱内标记LRI切口弧长,设置角膜钻石刀深度为周边角膜厚度的90%,于角膜缘作2.8 mm切口,向前房内注入黏弹剂,5~6 mm连续环形撕囊,水分离和水分层后以超声乳化术吸除晶状体核,I/A系统吸除晶状体皮质,后囊膜抛光后将人工晶状体植入囊袋,清除黏弹剂,调整人工晶状体并将其贴附后囊后水密切口,术后处理同观察组。
1.3观察指标 ①患眼视力:采用标准化最小分辨角对数(LogMAR)视力表检查两组术前和术后3个月时裸眼视力(UCVA)和最佳矫正视力(BCVA)。②角膜散光相关指标和SIA:采用Thibos矢量分析法[6]计算两组术前和术后3个月时角膜散光相关指标,根据切口位置和K1、K2及其轴位采用在线计算机计算术后实际SIA。③眼前节参数:记录两组术前和术后3个月时散瞳前后眼压(采用日本TOPCON公司生产的CT-800型非接触式眼压计测量)、前房容积(采用德国Oculus公司生产的Pentacam三维前房分析仪测量)以及中央区和切口区角膜厚度(采用德国Heidelberg公司生产的Spec-KT-06426型光学相干断层扫描仪测量)变化情况。④角膜高阶像差:采用Humphrey角膜地形图仪测量并计算两组术前及术后3个月时瞳孔6 mm范围内彗差(Coma)、三叶草像差(Trefoil)及总高阶像差(HOA)。⑤并发症:记录两组术中及术后3个月并发症发生率。

2 结果
2.1两组手术前后UCVA和BCVA比较 术后3个月,两组UCVA和BCVA较术前均明显降低,且观察组UCVA低于对照组,差异有统计学意义(P<0.01);但术后3个月两组BCVA比较差异无统计学意义(P>0.05)。见表1。
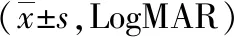
表1 不同方法治疗的白内障低中度角膜散光两组手术前后UCVA和BCVA比较
2.2两组手术前后角膜散光比较 术后3个月,两组角膜散光、CJ0和CJ45均较术前明显降低,且观察组角膜散光、CJ0和CJ45低于对照组,差异均有统计学意义(P<0.05或P<0.01)。见表2。
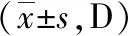
表2 不同方法治疗的白内障低中度角膜散光两组手术前后角膜散光比较
2.3两组SIA比较 两组术前预设SIA均为0.5 D,术后3个月时,两组SIA分别为(0.56±0.14)D和(0.58±0.19)D,两组比较差异无统计学意义(P>0.05)。
2.4两组散瞳前眼前节参数比较 术后3个月,对照组散瞳前切口区角膜厚度较术前明显增加(P<0.01),眼压、前房容积及中央区角膜厚度较术前无明显改变(P>0.05);观察组手术前后上述指标比较差异均无统计学意义(P>0.05)。术后3个月对照组仅散瞳前切口区角膜厚度高于观察组(P<0.01),余指标两组间比较差异均无统计学意义(P>0.05)。见表3。
2.5两组散瞳后眼前节参数比较 术后3个月,对照组散瞳后切口区角膜厚度较术前明显增加(P<0.01),眼压、前房容积及中央区角膜厚度较术前无明显改变(P>0.05);观察组手术前后上述指标比较差异均无统计学意义(P>0.05)。术后3个月对照组仅散瞳后切口区角膜厚度高于观察组(P<0.01),余指标两组间比较差异均无统计学意义(P>0.05)。见表4。
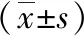
表3 不同方法治疗的白内障低中度角膜散光两组散瞳前眼前节参数比较
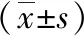
表4 不同方法治疗的白内障低中度角膜散光两组散瞳后眼前节参数比较
2.6两组手术前后角膜高阶像差比较 术后3个月,对照组Coma、Trefoil和HOA较术前明显增加(P<0.01),观察组Coma、Trefoil和HOA较术前未见明显变化(P>0.05);且术后3个月时观察组Coma、Trefoil和HOA均低于对照组,差异有统计学意义(P<0.05或P<0.01)。见表5。
表5 不同方法治疗的白内障低中度角膜散光两组手术前后角膜高阶像差比较
2.7两组并发症比较 两组术中均未发生严重并发症。观察组术后3个月发生黄斑囊样水肿1例(2.63%),给予抗炎治疗1周后逐渐恢复。对照组术后3个月发生角膜上皮脱落1例,采用绷带镜治疗2周后恢复正常,发生干眼症2例,随访3个月时自行缓解,并发症发生率为5.77%。两组并发症发生率比较差异无统计学意义(χ2=0.509,P=0.476)。
3 讨论
白内障是临床常见致盲性眼病,常见病因包括年龄相关退行性病变以及中毒或辐射等[7]。文献报道全世界约2.85亿人存在视力受损,其中盲人3900万,且由白内障导致者占比为51%[8-9]。约95.2%的白内障患者术前合并角膜散光,27.5%散光度数≥1.25 D,有研究认为散光超过0.75 D即可引起视物模糊、重影或炫光等不适症状,对白内障患者术后视力恢复造成不利影响,因此角膜散光矫正逐渐成为白内障手术治疗的重要组成部分[10-11]。
角膜切开术即在角膜缘不同位置作1个或多个切口来松解角膜,利用眼压作用降低弹性应力方向角膜屈光度,同时提升垂直方向屈光度,从而减少角膜散光,随着飞秒激光技术的快速发展和应用,术后矫正效果明显提升且角膜相关并发症也大幅度减少[12]。LRI矫正效果与切口数量、位置以及弧长等因素紧密相关[13]。Toric IOL取代普通人工晶状体治疗白内障合并角膜散光,在理论上较角膜切开术更为快捷和高效,一次手术即可同时解决两种问题,且可根据散光程度选择不同型号柱镜,手术效果可预测性好,故有利于降低术后残余散光,改善UCVA并提升脱镜率[14]。本研究回顾性分析LRI和Toric IOL植入对白内障低中度角膜散光的矫正效果,结果显示两组术后3个月时UCVA和BCVA较术前均明显降低,且观察组UCVA低于对照组,表明LRI对UCVA的改善效果不及Toric IOL植入,但通过眼镜等进行矫正可以达到弥补效果。同时本研究分析了两组术后角膜散光情况,结果显示术后3个月时两组角膜散光、CJ0和CJ45较术前明显降低,且观察组角膜散光、CJ0和CJ45均明显低于对照组,表明Toric IOL植入对白内障中低度角膜散光的改善效果具有明显优势。CJ0和CJ45为散光矢量分解结果,分别代表顺逆方向散光和斜向散光[15]。SIA是影响散光矫正效果的重要原因,角膜切开与手术切口、是否缝线及超声乳化等因素有关,而Toric IOL植入则主要受植入后散光轴位置与角膜最陡峭经线偏差影响[16-17]。本研究中对照组采用3 mm角膜缘内三阶梯透明切口,而IOL组Toric IOL由疏水性丙烯酸酯材料制成,可与囊袋紧密贴附并防止Toric IOL旋转,结果显示两组术前预计SIA为0.5 D,术后3个月两组SIA比较未见明显差异,产生此种结果的原因与SIA无关,因Toric IOL植入较LRI本身就有一定优势,与既往文献[18]报道结果一致。
Toric IOL植入和LRI两种手术方案均需植入Toric IOL替代病变晶状体,区别为Toric IOL植入兼有矫正散光的作用,无需再行角膜切口,术前即可根据患眼角膜曲率和轴位等数据选择合适Toric IOL型号,植入后调整散光轴位与角膜最陡峭经线保持重合即可完全矫正角膜散光,因而效果更为稳定可靠,具有可预测性,且对眼压、角膜厚度和眼房容积等参数影响较小[19]。本研究结果显示,观察组对散瞳前后眼压、前房容积及中央区角膜厚度均无明显影响,但对照组术后3个月时散瞳前后切口区角膜厚度明显增加,其原因可能与角膜切口造成的炎性反应和增生有关,并可能对角膜散光矫正效果造成不利影响。另外本研究分析了两组手术前后角膜高阶像差变化情况,结果显示对照组术后3个月时Coma、Trefoil和HOA较术前明显增加,观察组Coma、Trefoil和HOA较术前未见明显变化。文献报道角膜前表面像差较后表面像差高约3倍,LRI主要通过调节角膜前表面屈光度来矫正散光,因此切口数量、大小和位置均与Coma、Trefoil和HOA等参数紧密相关并对角膜散光矫正效果造成影响,进一步减少切口数量和大小有利于控制Coma、Trefoil和HOA增加,对提升手术效果具有积极作用[20]。本研究比较两组术后并发症显示,观察组术后3个月发生黄斑囊样水肿1例,对照组术后发生角膜上皮脱落1例、干眼症2例,均在随访期间恢复正常且未对手术效果造成不利影响,可见两种手术方案已较为成熟,均具有良好安全性,可根据患者病情和医疗条件进行合理选择。
综上所述,Toric IOL植入和LRI两种手术方案治疗白内障低中度角膜散光均具有良好效果和安全性,但Toric IOL植入有利于减少切口对角膜厚度和高阶像差的影响,UCVA和角膜散光改善效果较LRI更具优势。

