低温等离子体协同生物质热解-催化制备烃类燃料*
侯光喜,樊永胜,2**,卢东升,朱越峰,李子豪
(1. 盐城工学院汽车工程学院, 江苏盐城 224051;2. 京都大学能源科学研究科,日本京都 6068501)
近年来,生物质因其多样性和丰富性而成为世界第三大能源。生物质热解液化技术可以将低能量密度的生物质转化为高能量密度的生物油,从而成为能源领域的研究热点[1]。生物质直接热解制取的生物油缺陷明显,如含氧量高、热值低、腐蚀性强、稳定性较差等[2]。采用酸性择形分子筛催化,可以使生物质热解气中的氧主要以CO、CO2和H2O的形式脱去,显著改善生物油的燃料品位[3]。目前,HZSM-5分子筛因其独特的酸性分布和孔道结构,被广泛应用于生物油催化提质制备芳香烃[4-7]。采用HZSM-5进行生物质催化热解的方式主要分为2种:一是将生物质和催化剂直接混合进行原位催化热解;二是可将生物质热解段和催化段分开,进行异位热解催化。前者大量热解焦炭和无机物易覆盖催化剂表面,致使其失活,且在催化接触面积上有明显的缺陷;后者在一定程度上改善了催化剂循环使用性能和催化接触面积缺陷,但热解和催化需分段控制,增加了反应器匹配设计和控制的难度[8]。所以,将生物质和催化剂分区进行一段式热解催化,既可以减少初级产物二次裂解,提高催化剂循环使用性能,又能降低反应控制的难度。
低温等离子体(non-thermal plasma, NTP)技术是利用放电产生高能活性物质,进而活化解离反应物分子,促进或加速反应的进行,通过放电直接向反应物分子化学键输入能量,以降低常规反应所需的能量。此外,高能活性物质的冲击,可以在催化剂表面形成等离子体鞘,抑制或减少催化剂结焦,促进反应物/产物在催化剂上的吸脱附。因此,引入NTP技术协同生物质热解催化,有利于降低反应温度,提高催化剂的循环使用性能和反应转化率。目前,采用NTP协同生物质一段式热解-催化方面的研究鲜见报道。
笔者以HZSM-5分子筛为催化剂,采用NTP协同生物质真空热解-HZSM-5催化制备精制生物油的试验,考察生物质质量与催化剂高度(质高比)、反应温度和体系压力对精制生物油收率的影响,并对最优工艺条件下制备的精制生物油元素组成、高位热值(high heating value, HHV)、官能团构成和分子组分进行分析,以期为生物质能源高效转化利用提供试验基础据和理论依据。
1 试验系统与方法
1.1 生物质原料和催化剂
以自然风干的油菜籽壳为生物质原料,收集于江苏省盐城市某农场。试验前,将原料粉碎至粒径为0.1~1.0 mm的细小颗粒,并将其置于恒温干燥箱中于105 ℃下干燥4 h后备用。对原料的元素分析结果表明,原料含有质量分数46.17%的碳、6.08%的氢和47.52%的氧(差减法);工业分析结果表明,原料中含有质量分数75.77%的挥发分、5.68%的水分、2.45%的灰分和16.10%的固定碳。
催化剂HZSM-5购自天津南化催化剂厂,硅铝摩尔比50。采用北京彼奥德公司SSA4300型分析仪进行液氮吸附-脱附测定催化剂比表面和孔隙性质。采用美国赛默飞世尔公司Frontier型红外光谱配合真空吡啶吸附-脱附系统测定催化剂的B酸和L酸分布。催化剂理化性质的测定结果如表1所示。

表1 催化剂的理化性质
1.2 试验装置和过程
NTP协同生物质热解-催化一段式反应系统如图1所示。
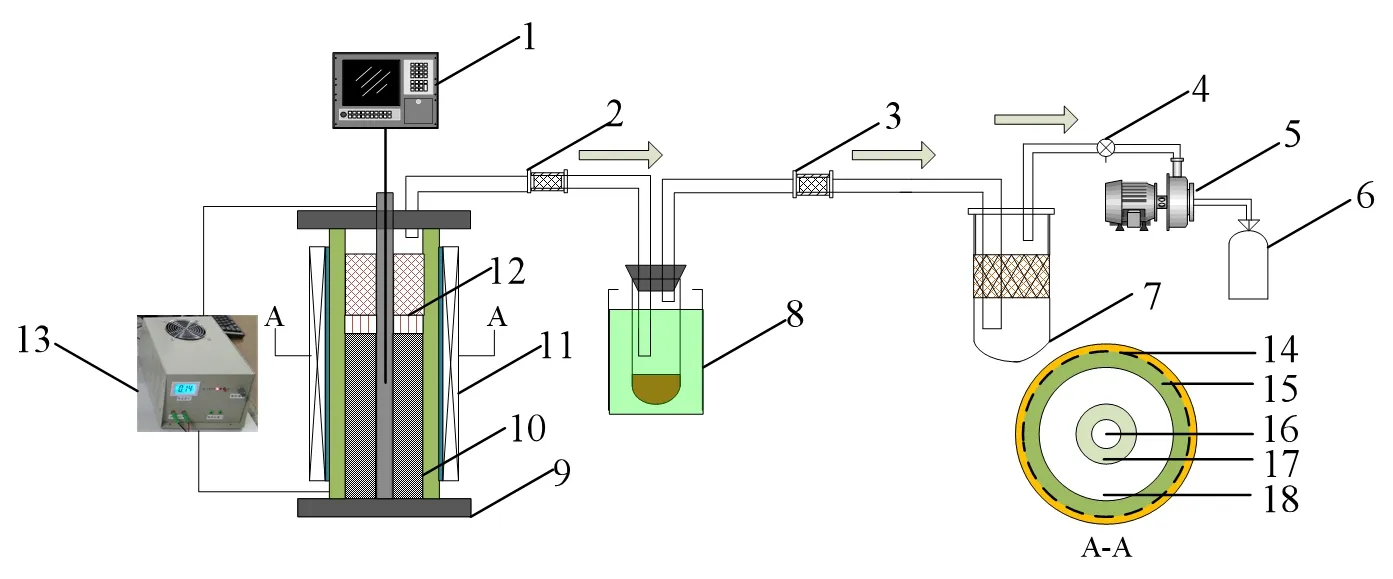
图1 NTP协同生物质热解-催化一段式反应系统示意
NTP协同生物质热解-催化一段式反应系统由一段式反应器、温控器、电加热套、等离子电源、冷阱、真空泵等部分组成。基于介质阻挡放电原理,一段式反应器由经过特殊处理的石英制成,中心为一端封闭的不锈钢中空管作高压电极,反应器外表面包裹0.075 0 mm(200目)的铜网作低压电极,以形成介质阻挡放电,产生低温等离子。中心高压电极的内孔用于测量反应温度。反应器轴向长度为100 mm,放电区长度80 mm,放电间隙为10 mm。试验时,等离子电源使用的输入电源为220 V交流电。生物质热解区和HZSM-5催化区置于放电区。填装生物质和催化剂,完成系统连接,经密封测试后,开启真空泵抽真空至指定压力条件;然后,接通电加热套,加热至预定温度,加热过程中同时开启等离子电源,设定放电功率为500 W和放电电流为30 mA,进行NTP协同生物质热解-催化试验。在真空泵抽吸作用下,生物质热解产生的热解气经过催化剂层后,进入冷阱冷凝液化,不可冷凝气体经真空泵抽出,被集气袋收集。试验完成后,停止加热,并持续抽真空,至系统冷却至室温后,关闭真空泵,待压力恢复至常压后,收集液化产物。利用二氯甲烷(CH2Cl2)作为萃取剂对液化产物中有机相进行萃取分离,得到CH2Cl2萃取相;同时,利用CH2Cl2对反应器和部分管路进行清洗,清洗液亦加入萃取相中;最后,在40 ℃水浴条件下蒸馏去除CH2Cl2,所得有机相即为精制生物油,进行称量。
1.3 试验方法
1.3.1 精制生物油收率计算
精制生物油收率(Y)的计算公式如下:

式中:m为收集的精制生物油质量,g;M为生物质质量,g。
1.3.2 Box-Behnken响应面试验设计
响应面法中Box-Behnke设计是利用二次方程表征响应值和因素之间的关系,可以减少试验次数,科学高效地优化参数[9]。选取质高比A、反应温度B和体系压力C为主要影响因素,精制生物油收率(Y)为响应值。采用Box-Behnken响应面法安排试验,因素水平分布如表2所示。

表2 因素水平分布
1.3.3 精制生物油分析
采用赛默飞世尔的FLASH EA-1112A型元素分析仪检测精制生物油的元素组成。并根据元素组成,计算理论高位热值QHHV,计算公式如下[10]:
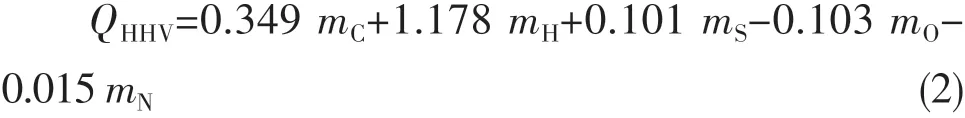
式中:mC,mH,mS,mO,mN为对应元素C,H,S,O,N的质量分数。
采用赛默飞世尔的Nicolet iS5型傅里叶变换红外光谱仪(Fourier transform infrared spectroscopy, FT-IR)分析精制生物油官能团构成,波数扫描范围400~4 000 cm-1,分辨率0.1 cm-1。
采用赛默飞世尔的Trace DSQ-Ⅱ气相色谱-质谱联用仪(Gas chromatography/mass spectroscopy, GC/MS)仪测定精制生物油分子组成。GC条件:载气(He),流量1 mL/min,进样口温度250 ℃,不分流,进样量1 μL;MS条件:MS传输线温度250 ℃,电离方式EI,轰击能量70 eV,扫描质量范围30~500(质荷比),扫描时间1 s。升温程序:50 ℃保持2 min,以20 ℃/min升至100 ℃,然后以15 ℃/min升至280 ℃保持2 min。溶剂CH2Cl2延迟时间为3 min。
2 结果与讨论
2.1 响应面法试验
按照Box-Behnken响应面法设计方案,进行了12个析因试验和3个中心试验。试验组合及结果如表3所示。
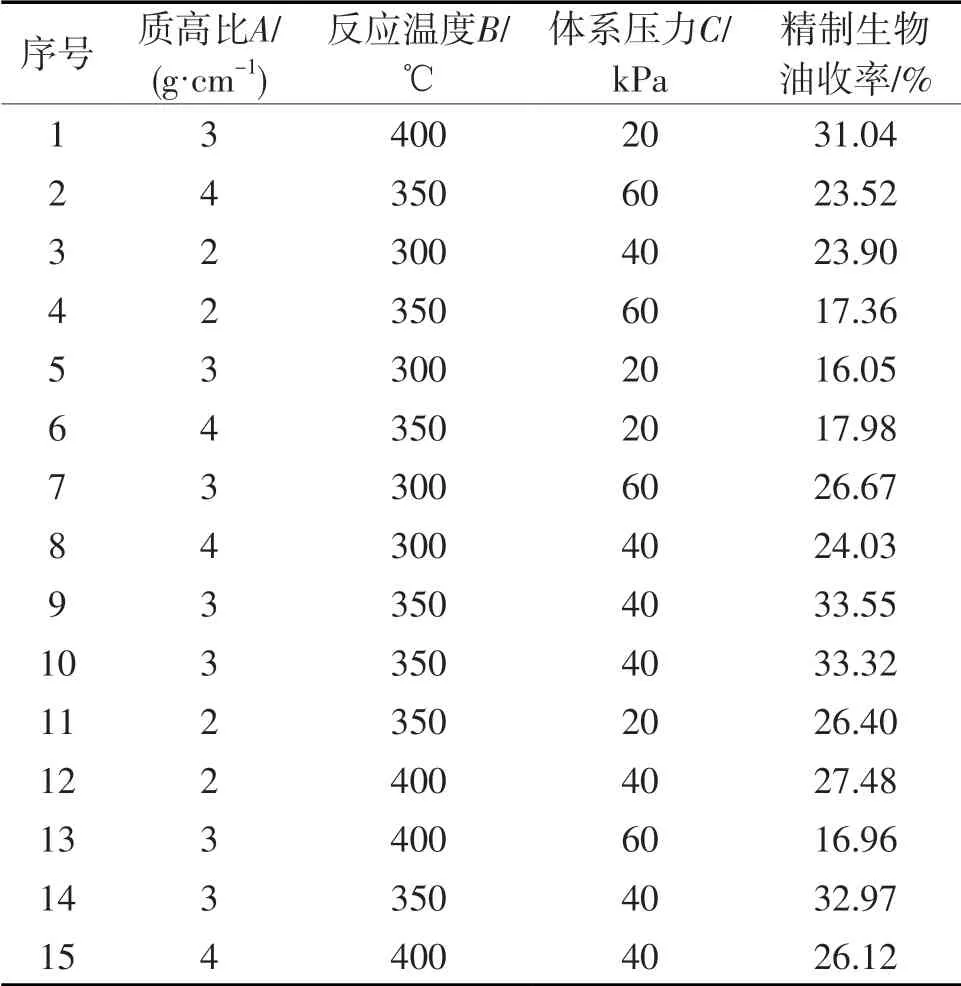
表3 试验组合及结果
使用Design-Expert软件对试验数据进行分析与拟合,得到回归模型如下:

回归模型的方差分析如表4所示。

表4 回归方程方差及显著性分析
由表4可见:模型的检验p值小于0.000 1,表明该模型极显著;失拟项p=0.676 9>0.05,表明失拟不显著。模型的确定性系数R2=0.999 4,调整后的确定性系数RAdj2=0.998 2,表明该模型符合99.82%的响应值,拟合度较好,可以有效预测最优条件。模型中一次项A、B和C的p<0.01,极显著;交互项AC和BC的p<0.01,极显著;交互项AB的p<0.05,显著;二次项A2、B2和C2的p<0.01,极显著。因此,质高比、反应温度和体系压力3个因素对精制生物油收率影响显著,并且三因素之间交互作用显著。
各因素对精制生物油收率影响的响应曲面和等高线如图2所示。
由图2(a)可见:当反应温度不变时,精制生物油收率随质高比的增大先升高后降低;当质高比不变时,精制生物油收率随反应温度的升高而缓慢升高。质高比过小,热解气容易被过度催化而二次裂解,产生更多不可冷凝的气体,导致精制生物油收率降低;质高比过大,热解气催化不完全,精制生物油收率降低。随着反应温度的升高,精制生物油收率的上升速率由急至缓,这归因于生物质热解催化程度逐渐完全。而反应温度过高会增大热解气二次裂解机率,从而导致精制生物油收率出现下降趋势。

图2 各因素对精制生物油收率影响的响应曲面和等高线
由图2(b)可见:当质高比不变时,精制生物油收率随体系压力的增大先升高后降低;当体系压力不变时,精制生物油收率随质高比的增大先升高后降低。体系压力过低,热解气停留时间短,不利于冷凝,导致精制生物油收率较低;体系压力过高,热解气停留时间过长,热解气二次裂解程度高,导致精制生物油收率降低。
由图2(c)可见:当反应温度不变时,精制生物油收率随体系压力的降低先升高后缓慢降低;保持体系压力不变,体系压力在较高值时升高,精制生物油收率随反应温度的升高而降低,归因于热解气的二次裂解程度高;体系压力在较低值时升高,精制生物油收率随反应温度的升高而升高,归因于较低的体系压力使得热解气停留时间短,减少了热解气二次裂解的机率。此外,质高比、反应温度和体系压力之间存在交互作用,三者在适宜的范围内有利于提高精制生物油的收率。
2.2 响应面优化分析
在参数约束范围内进行精制生物油收率最大化分析,获得最佳工艺条件为:质高比为2.799、反应温度为376.899 ℃和体系压力为33.291 kPa。为验证试验的可靠性,并考虑到实际操作的控制精度,取质高比为2.8、反应温度为377.0 ℃、体系压力为33.3 kPa。并在此条件下进行2次验证试验,获得精制生物油的平均收率为33.71%,与预测值相差0.13%,误差较小,表明该模型较为准确。赵勃等[11]采用木质素炭与HZSM-5联合原位催化热解木质素,当木质素与ZSM-5质量均为1.0 g,热解温度为500 ℃时,生物油最高收率为26.00%。李小华等[12]采用HZSM-5为催化剂,500 ℃下对油菜秸秆进行异位热解-催化反应,所得生物油收率仅为22.22%。与HZSM-5单一催化相比,NTP协同热解催化有效降低了催化热解所需温度,产生了更多的活性自由基,有利于提高转化率,获得更多精制生物油。
2.3 精制生物油产物分析
2.3.1 精制生物油元素组成
元素分析结果表明,精制生物油含质量分数71.14%的碳,8.27%的氢和20.59%的氧(差减法)。由式(2)计算得到理论QHHV为32.46 MJ/kg。获得的精制生物油热值较高,优于其他热解方法制得的精制生物油。董良秀等[13]以油菜秸秆为原料,500 ℃终温下在两段式固定床反应器上进行异位催化热解试验,发现直接热解所得生物油高位热值为28.36 MJ/kg,以HZSM-5为催化剂所得生物油高位热值为31.02 MJ/kg。相比较而言,NTP协同生物质真空热解-HZSM-5催化制备的精制生物油高位热值明显提升,且NTP的协同作用明显降低了反应温度。
2.3.2 FT-IR分析
对所制备的精制生物油进行FT-IR分析,结果如图3所示。
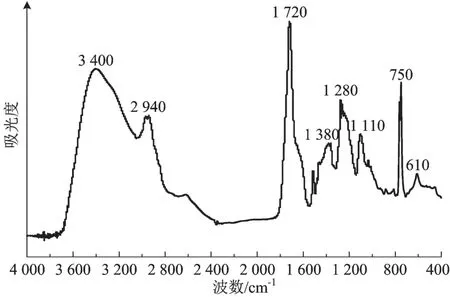
图3 精制生物油的红外光谱
由图3可见:3 200~3 500 cm-1处存在一个吸收峰,归因于O—H的伸缩振动;2 900~3 000 cm-1存在的吸收峰归因于饱和C—H的伸缩振动,表明精制生物油中含有烷烃基团;1 700~1 730 cm-1处尖锐的峰归因于C=O的伸缩振动,表明精制生物油中可能含有酮、醛或酸等物质;1 500~1 520 cm-1处的峰归因于C=C伸缩振动,表明精制生物油中可能含有烯烃结构类的双键;1 480 cm-1、1 350~1 470 cm-1处的吸收峰归因于C—H键的弯曲振动,表明精制生物油中含有烷烃基或脂肪基团;1 000~1 300 cm-1处的吸收峰则归因于苯环基团,表明精制生物油中含有大量芳香族物质。
2.3.3 GC-MS分析
根据有机物类别,将精制生物油中检测到的化合物分为轻质脂肪烃(Light aliphatic hydrocarbon, LAHs)、 单 环 芳 香 烃(Monocyclic aromatic hydrocarbons, MAHs)、多环芳香烃(Polycyclic aromatic hydrocarbons, PAHs)和含氧化合物,结果如表5所示。
由表5可见:精制生物油中期望的目标产物LAHs和MAHs的总质量分数达50.10%。LAHs主要是4-亚甲基庚烷(6.57%)一种,而MAHs中主要有邻二甲苯、1-甲基-3-乙基苯和1-甲基-4-丙烯基苯,质量分数都在7%以上。PAHs为环境污染物,其主要成分包括甲基萘、1,4-二甲基萘和1,5-二甲基萘,质量分数在4%以上。与HZSM-5催化热解[14]相比,精制生物油中未检测到酸类物质和醛类物质,表明NTP协同热解催化脱羧反应较彻底,酸类得以转化,醛类裂解更加充分,转化为酚类,NTP明显提高了催化活性。此外,含氧有机物主要包括酚类和酮类,其中酚类为主要成分,其质量分数为20.29%,进一步验证了FT-IR分析结果。一般而言,生物质直接热解所得生物原油中烃类产量极低,甚至不含烃类产物[15]。冯学东等[16]采用HZSM-5对生物质进行500 ℃催化裂解,发现烃类产物质量分数仅为27.32%。试验制备的精制生物油中增加了大量的烃类物质,总质量分数达74.71%,除了HZSM-5的催化选择作用外,主要归因于NTP的协同作用,NTP激发高能电子解离反应物,产生更多的活性自由基,提供更多的碳正离子,促进芳构化反应,同时NTP在催化剂表面形成微放电等离子体鞘,促进了催化位点活性提高,并提升了催化剂稳定性。带有苯环的有机大分子裂解产生芳香烃,而小分子碳氢化合物则通过聚合、芳构化等反应形成芳香烃,使芳香烃收率大幅增加。

表5 精制生物油主要成分
对精制生物油中的有机物分类和碳数分布进行统计,结果如图4所示。

图4 精制生物油中有机物分类及碳数分布
由图4可见:NTP协同生物质一段式热解-催化对MAHs的选择性较高,达到43.53%,含氧有机物总质量分数较低,仅为25.26%。此外,所有化合物碳原子分布为C5~C16,根据汽油(C4~C12)和柴油(C10~C22)的碳数分布,精制生物油中碳原子分布位于C5~C12,化合物总质量分数达到94.43%,这与汽油的主要碳数分布高度重合,表明精制生物油具有制成汽油组分或添加剂的潜力。
3 结论
采用响应面法对NTP协同生物质热解-催化制备精制生物油的工艺参数进行了分析和优化。质高比、反应温度和体系压力对精制生物油收率具有显著影响,且三者交互作用显著。精制生物油收率最高时的制备工艺为:质高比2.8、反应温度377.0 ℃和体系压力33.3 kPa,平均收率为33.71%,与预测值33.84%较为接近。所得精制生物油高位热值达到32.46 MJ/kg。NTP协同有效降低了反应温度,增强了生物质热化学转化率。精制生物油中烃类总质量分数达74.71%,含氧有机物总质量分数较低,仅为25.26%。期望产物LAHs和MAHs质量分数达50.10%;并且化合物主要碳数分布为C5~C12,与汽油碳数范围高度重合,可进一步作为汽油组分或添加剂使用。

