神经导航引导下无框架立体定向穿刺引流治疗脑干出血的临床疗效及治疗经验
韩昊锦,牛光明,刘展,娄金峰
脑干是生命中枢,位置极其重要,该部位一旦出血则患者容易出现昏迷,其致残率和致死率极高[1]。既往研究表明,高血压性脑干出血发病人数占高血压性脑出血患者总数的5%~10%[2]。血肿体积是预测脑干出血患者预后的重要因素,其中血肿体积>5 ml者致死率为75%[3-4]。但采取哪种治疗方式治疗高血压性脑干出血一直存在争议[5],尽管有脑干出血患者采用手术获益的相关临床报道[6],但目前仍以保守治疗为主。近年随着神经导航系统和立体定向系统的不断完善,其因简便、创伤小、快捷等优势而在脑干出血患者治疗中得到进一步实践[7-8]。郑州大学第二附属医院神经外科采用神经导航引导下无框架立体定向穿刺引流治疗19例脑干出血患者并获得一定临床疗效及治疗经验,现报道如下。
1 资料与方法
1.1 一般资料 选取2018年2月—2020年1月郑州大学第二附属医院神经外科收治的脑干出血患者48例,均于入院后行CT检查并确诊为脑干出血,有原发性高血压病病史,出血原因排除瘤卒中、创伤及血管畸形。48例患者中19例接受神经导航引导下无框架立体定向穿刺引流治疗(观察组),29例不同意手术而采取内科保守治疗(对照组)。两组患者性别、年龄、出血量及出血部位比较,差异无统计学意义(P>0.05),见表1。所有患者对本研究知情并签署治疗知情同意书。
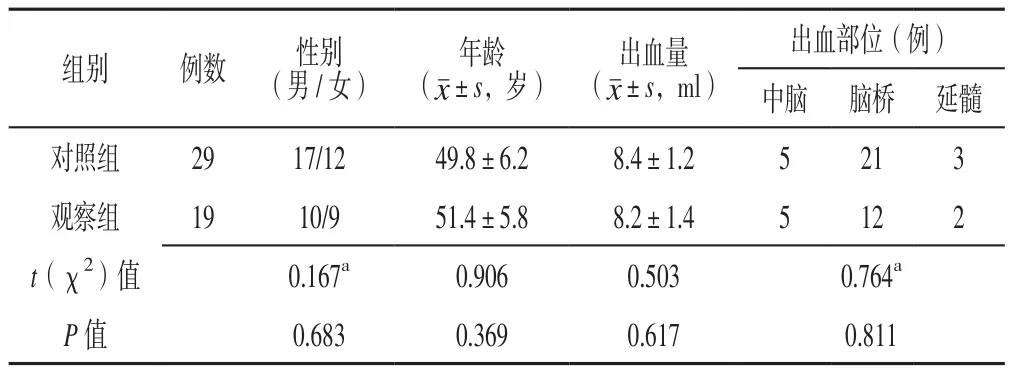
表1 两组患者一般资料比较Table 1 Comparison of general information between the two groups
1.2 纳入与排除标准 纳入标准:(1)多田公式结合3D Slicer三维重建软件计算血肿量>6 ml;(2)入院时格拉斯哥昏迷量表(Glasgow Coma Scale,GCS)评分≤8分;(3)发病距入院时间≤6 h。排除标准:(1)入院时自主呼吸消失且血压、心率不稳定者;(2)合并肝肾功能障碍、凝血功能障碍者;(3)临床资料不完整者。
1.3 治疗方法
1.3.1 对照组 对照组患者参照《自发性大容积脑出血监测与治疗中国专家共识》[9]中的常规内科治疗方法,给予吸氧、特级护理、控制血压稳定〔血压维持140/90 mm Hg(1 mm Hg=0.133 kPa)〕、镇静、降颅压、促醒、护胃、维持内环境稳态、抗感染、营养神经、改善脑功能、营养支持、改善全身情况等治疗;维持昏迷患者气道通畅,给予雾化化痰、预防呼吸抑制、改善呼吸功能,必要时气管切开,密切关注患者病情变化,积极对症治疗;定期复查颅脑CT以了解患者颅内情况,根据是否伴脑室积血、梗阻性脑积水行侧脑室穿刺引流术(患者均同意必要时行侧脑室穿刺引流术)。
1.3.2 观察组 观察组患者接受神经导航引导下无框架立体定向穿刺引流治疗,具体如下:(1)术前准备:患者行薄层颅脑CT扫描,层厚1 mm,扫描范围自头顶以上至鼻尖以下,将影像数据结合3D Slicer三维重建软件等构建三维成像,进行精准术前设计,构建术前三维可视化模型。完成术前设计方案后部分患者须备皮后于头部粘贴4个Mark标识点(位置选择在手术侧枕部、乳突、顶结节),之后行薄层颅脑CT扫描,将术前三维重建及CT数据导入美敦力S7神经导航系统无框架立体定向穿刺模块,三维融合,设计手术靶点,计算坐标值,规划穿刺路径、确定头部穿刺点。依据血肿部位及形状选择不同入路,确定每例患者具体穿刺方向及穿刺路径距离等参数。(2)手术过程:采取两种穿刺路径,血肿位于中脑及脑桥上部者选择幕上穿刺路径,患者取仰卧位,头部穿刺点选在术侧冠状缝前、中线旁部分区域,幕上穿刺途径沿额叶(额中回中部)-放射冠-丘脑外侧部-中脑或脑桥上端路径。血肿位于脑桥下部及延髓上部者选择幕下侧方穿刺路径,患者取仰卧位,术侧垫肩,头偏向对侧45°,头部穿刺点选在手术侧乳突内侧、横突下方部分区域,幕下穿刺途径建议沿小脑半球外下部-小脑中脚-脑桥下部或延髓上部路径。具体操作如下:患者全麻后取仰卧位,Mafierd头架固定头部,进行导航系统注册及空间配准,常规消毒铺巾,钻孔,电凝止血,切开硬脑膜,在导航系统无框架立体定向穿刺模块引导下缓慢将引流管引导至靶点,少量抽吸血肿,固定引流管。术中通过导航系统无框架立体定向穿刺模块可视化穿刺位置、方向、路径、靶点距离等信息。穿刺过程中避免反复进出蛛网膜下腔,以免穿刺过程中脑脊液丢失而导致管头未置于血肿腔正中,并严密监测患者心率、血压变化,尤其经小脑中脚穿刺,在进针前必须备好阿托品等急救药品。根据有无脑室系统积血、梗阻性脑积水表现同期行侧脑室穿刺外引流术。(3)术后处理:术后第2天复查颅脑CT,根据残余血肿量酌情使用尿激酶以辅助溶解血肿并调整引流管深度,每10 ml血肿可注入含1万U尿激酶的0.9%氯化钠溶液1 ml,再使用0.9%氯化钠溶液2 ml冲管,关闭引流管2 h后打开;每日使用1~2次尿激酶注入引流管以促进血肿排出。留置引流管3~5 d后拔除。其他治疗同对照组。
1.4 观察指标 比较两组患者入院时及治疗1周后GCS评分;治疗后3个月进行电话随访,询问患者存活情况并采用改良Rankin量表(modified Rankin Scale,mRS)评估存活患者预后,mRS共5个分级,0级:完全无症状;1级:有症状,但无明显功能障碍,能完成所有日常活动;2级:轻度残疾,不能完成病前所有活动,但不需要帮助,能照顾自己的事务;3级:中度残疾,需部分帮助,但能独立行走;4级:中重度残疾,不能独立行走,日常生活需别人帮助;5级:重度残疾,卧床,二便失禁,日常生活完全依赖他人[10]。比较两组患者治疗2周血肿清除量。
1.5 统计学方法 应用SPSS 19.0统计学软件进行数据处理。计量资料以(±s)表示,组间比较采用两独立样本t检验;计数资料比较采用χ2检验;等级资料比较采用秩和检验。以P<0.05为差异有统计学意义。
2 结果
2.1 神经导航引导下无框架立体定向穿刺引流的准确性 神经导航引导下无框架立体定向穿刺系统最大误差为2.8 mm、最小误差为0.9 mm,平均误差为(1.8±1.1)mm,空间坐标误差X轴为(1.2±0.3)mm、Y轴为(1.1±0.1)mm、Z轴为(0.8±0.3)mm。术后复查颅脑CT证实,引流管精准位于血肿腔内,见图1。
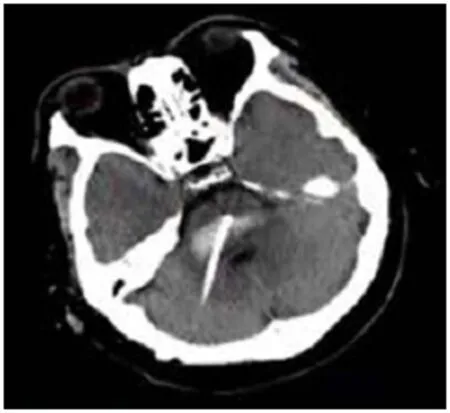
图1 颅脑CT检查结果Figure 1 Results of brain CT examination
2.2 治疗效果 两组患者入院时GCS评分比较,差异无统计学意义(P>0.05);观察组患者治疗1周后GCS评分高于对照组,治疗后3个月mRS分级优于对照组,治疗后3个月内死亡率低于对照组,治疗2周血肿清除量大于对照组,差异有统计学意义(P<0.05),见表2。
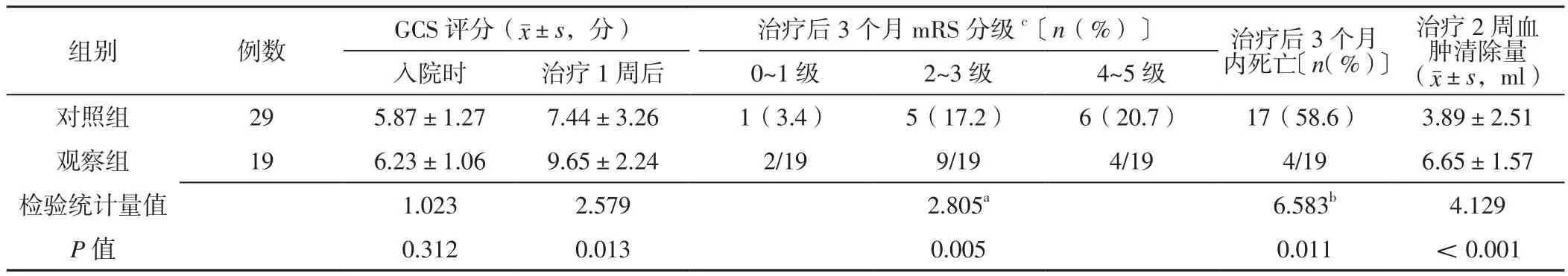
表2 两组患者治疗效果比较Table 2 Comparison of treatment effect between the two groups
3 讨论
据统计在高血压脑干出血中脑桥出血占80%,中脑出血占15%,延髓出血占5%[11]。脑干出血初期损伤为血肿压迫脑干造成轴向扭曲或纵向位移等[12];后期损伤为血肿挤压临近脑组织及血肿降解产物、血红蛋白的毒性作用导致脑组织水肿、缺血,进而造成严重的继发性损伤[13]。因此,脑干出血治疗重点是尽快清除血肿、解除占位,减轻脑干临近组织受压,中断脑干出血后继发性损伤的恶性循环,以提高患者生存率,改善患者预后。
3.1 神经导航引导下无框架立体定向穿刺系统的优势 目前,神经内镜下手术清除血肿、显微镜下手术清除血肿、传统有框架立体定向技术穿刺抽吸血肿均具有一定临床疗效[8,10,13],其中显微镜下和神经内镜下手术清除血肿是可行的方法,但二者手术时间均相对较长,手术难度相对较高;传统有框架立体定向手术受定位框架限制,对入颅点的选择有一定影响,且患者需要局麻下安装定位框架后行CT扫描,一定程度上增加了创伤。神经导航引导下无框架立体定向穿刺系统不但具有传统立体定向精确度高的特点,还能避免定位框架的限制,可不受限地选择入颅点[14-15]。
3.2 治疗经验
3.2.1 脑干出血穿刺路径的选择 本研究在神经导航引导下无框架立体定向穿刺系统辅助下穿刺引流治疗脑干出血,术后使用尿激酶促进引流。采取的穿刺路径无关键神经、血管,可有效防止手术造成的不可逆损伤,其中幕上穿刺途径为笔者在200余例帕金森病立体定向核团毁损术和脑深部电刺激植入术及神经导航下无框架立体定向丘脑病变穿刺活检术的基础上总结而来,该术式可到达中脑和桥脑,避免刺破小脑幕,具有较高的安全性与精准度。而幕下穿刺途径也有相关报道,有较好的安全性[7]。此外,依赖于影像三维重建模型制定的穿刺方案在减少穿刺部位出血、置管位置合理性以及管头平行于血肿长轴方面具有优势。本研究中观察组患者术中无一例死亡,术后存活率为78.95%,高于既往研究报道的60%[16]。
3.2.2 手术时机选择得当 脑干出血后10~20 min出血量达高峰,1~2 h不再出血,6~7 h后血肿压迫及其降解产物损伤临近组织,导致临近组织变性坏死、血管周围出血等损伤,脑水肿于24~48 h达峰值[17-19]。目前,支持脑干出血后6~7 h内行手术治疗的原因如下:尽早手术尽早解除压迫,且目前没有证据证明超早期手术增加再出血风险[13,20-21]。支持脑干出血7~24 h内行手术治疗的原因如下:尽管单纯出血大多数在2 h内停止,但超早期脑干出血患者因躁动、搬动、血压波动等因素可能导致脑内血肿不稳定,而发病6~7 h后各种因素趋于稳定,血肿也随之稳定。李建国等[22]采用立体定向手术治疗20例高血压脑干出血患者的手术时机选择为6~24 h内,并取得较好的疗效。由于脑干出血具有特殊性,且需要考虑患者转移、气管插管、中心静脉置管、影像学检查、精确计算穿刺路径等因素,本研究观察组患者手术时间均在发病 6~24 h内。
3.2.3 穿刺抽吸血肿还是注入尿激酶溶解、引流血肿? 对于脑干出血患者,穿刺抽吸是否能导致新的出血尚无定论;基于脑干出血量较小、形态多呈椭圆形,笔者认为如果穿刺过程中脑脊液丢失而导致管头未置于血肿腔正中,则负压抽吸时可能导致血肿扩大。既往研究报道,抽吸少量血肿可有效缓解占位情况,但清除血肿壁残余血块常导致再出血[22]。尿激酶可激活纤溶酶原为纤溶酶,通过酶促反应分解纤维蛋白,但其速率受酶、底物浓度影响,而给予适量尿激酶可提高速率[23-25]。目前,尿激酶的量效关系尚未完全明确,根据既往研究[26]及笔者治疗经验,1万U尿激酶/10 ml血肿(多田公式)注入血肿腔,夹闭2~3 h,留置引流管3~5 d安全有效。但鉴于使用尿激酶在血肿纤溶期(出血48 h后)效果更佳,因此常规在术后第2天复查引流管位置后再使用尿激酶,本研究观察组患者均于术中少量抽吸血肿以缓解占位,术后注射尿激酶辅助引流并获得较好的治疗效果,且注射过程中未出现不良反应。
3.2.4 昏迷程度在手术指征中是否非常重要? 中脑和间脑的尾侧区是网状上行激活系统的关键位置[27]。与常见的中晚期脑疝导致的昏迷不同,脑干出血昏迷常发生于出血初期,分析其原因为血肿导致网状上行激活通路直接损伤(中脑出血)或上行纤维受压(脑桥出血),且脑干出血所致昏迷并不能像其他颅内占位病变一样可反映全脑功能的损伤程度,因此需要对意识障碍在脑干出血手术指征中的作用重新进行评价[28]。根据临床经验,脑干出血初始至就诊时生命体征的动态改变是决定是否手术的重要因素,本研究观察组中2例患者均为入院后8 h内复查颅脑CT提示血肿量变大,且昏迷程度加重、双瞳孔针尖样改变、自主呼吸微弱,遂行急诊神经导航引导下无框架立体定向穿刺引流,术后效果较好。
3.2.5 哪种生命体征紊乱是手术禁忌证? 呼吸中枢以延髓和脑桥最为重要,延髓是引起原始呼吸节律的主要位置。血管舒张区位于延髓网状结构的腹内侧部(主要为孤束核),接受颈动脉窦神经及主动脉神经的传入,可发出纤维抑制巨细胞网状核和兴奋迷走疑核,进而引起血管舒张和心率减慢[29]。血管收缩区(其内混合心跳加速中枢神经元)位于延髓脑桥网状结构背外侧部分(主要为巨细胞网状核),兴奋时会提高心率、收缩血管、升高血压。迷走神经背核也是心跳抑制中枢。因此,应根据疾病演变、血肿位置和形态判断延髓背侧中央区呼吸、血压和心跳中枢是受压还是直接破坏,如血压下降和呼吸暂停同时存在,则考虑延髓背侧出血范围广泛,不考虑手术治疗;如单纯存在呼吸暂停,则可以考虑手术治疗。
3.2.6 术中如何避免漂移造成的穿刺失败? (1)本研究中所用神经导航下无框架立体定向穿刺系统具有较高的精准度,系统误差很小,能够精准到达脑深部病变位置,尤其是较小病灶,基本没有漂移。黄俊等[30]认为神经导航在神经外科手术中发生位置漂移的原因主要考虑以下几点:①患者术前与术中体位不一致以及术中头颅的旋转造成的偏差(本研究中患者术前、术中均为仰卧位,术中不涉及头颅的旋转);②术中部分肿瘤组织的切除以及脑脊液、血液丢失后周围组织因重力作用塌陷而造成的漂移〔本研究中不涉及部分肿瘤组织切除,且采用的穿刺术仅在硬脑膜做一5 mm切口,出血和脑脊液丢失均较少(<10 ml)〕;③术中使用甘露醇及骨瓣去除后颅内压下降导致脑组织塌陷(本研究术中未使用甘露醇,且磨除的骨孔较小,直径为1 cm,故降颅压作用有限)。(2)韩磊等[31]在神经导航10年应用经验总结中指出:由于脑干非常重要,故手术时切开部位要非常精确;由于脑干位置相对固定,基本可以忽略漂移的影响。(3)本研究选取的患者血肿量均>7 ml,且术后复查颅脑CT证实与术中导航设计的穿刺通路及引流管位置一致,无一例穿刺失败,精确度较高;此外,本研究使用的美敦力S7神经外科导航系统及其配套的先进无框架立体定向穿刺活检软件模块精准度均较高,可精准到达脑深部位置。
3.2.7 脑干是重要神经核团密集区域,术前根据CT检查结果设计导航穿刺计划能否辨析核团位置? 本研究选取的患者血肿量均>7 ml,其脑干局部结构已经受损,包括局部脑干神经核团,因此CT检查较难辨析这些核团位置。脑干出血为高死亡率疾病,手术可能挽救患者生命,故没有将核团功能作为首要考虑的问题,但本研究选择的入路可避开重要结构、脑内大血管,与脑深部大血管及重要结构保持平行的空间位置关系,极大地避免了继发性损伤、出血的发生。
3.2.8 采用“额叶(额中回中部)-放射冠-丘脑外侧部-中脑或脑桥上端”入路穿刺脑桥和中脑血肿,如何避免因穿刺导管直径较粗而造成继发性损伤? (1)GILARD等[32]指出,为了尽量避免引流管置入过程中损伤脑实质,常规使用的脑室外引流管直径一般较小(内径为1.5 mm),但引流管直径较小又易造成堵塞,从而影响治疗效果;该研究在脑室内出血患者手术中使用粗脑室外穿刺引流管(内径为2.3 mm),降低了导管堵塞的可能,且未增加导管置入相关脑出血风险;此外,粗引流管还可以降低相关感染风险。本研究使用的是内径为2.4 mm的法国SOPHYSA DE-306软引流管,相对于更细的引流管,其不会增加继发出血风险,但可以降低导管相关感染风险和堵管率。(2)林岩崇等[33]和王晓锋等[34]采用经额或顶-侧脑室-基底核或丘脑-中脑或脑桥入路,孙喜山等[35]采用经顶上小叶-大脑弓状纤维-胼胝体压部-四叠体池-中脑或脑桥入路,上述两种入路为中脑及脑桥上部血肿穿刺提供了新的思路。本研究所用幕上穿刺路径可更精准地到达中脑和脑桥上部,对脑干及其周围重要结构损伤更小,可避免损伤侧脑室、基底核等结构。
综上所述,采用神经导航引导下无框架立体定向穿刺引流治疗脑干出血是有效的,可在一定程度上降低患者死亡率、改善患者预后,但需要注意的是,手术时应合理选择穿刺路径、手术时机、血肿引流方式、引流管直径等。本研究样本量较小,可能影响结果的可靠性,未来仍需开展大样本量、前瞻性随机对照试验进一步验证本研究结论。
作者贡献:韩昊锦、牛光明、刘展、娄金峰进行文章的构思与设计,研究的实施与可行性分析;韩昊锦进行数据收集、整理、分析,并撰写论文;韩昊锦、刘展、娄金峰进行结果分析与解释;牛光明负责文章的质量控制及审校;韩昊锦、牛光明对文章整体负责、监督管理。
本文无利益冲突。

