SOX与XELOX方案对术后复发性胃癌患者血清肿瘤标志物、生存期及耐受性的比较研究
蒋 冬 孙 晓 樊宏伟
胃癌作为消化系统常见恶性肿瘤之一,目前仍以根治性外科手术为最有效的治疗措施,但由于其流行病学多表现为早期诊断率、手术切除率、5年存活率低而根治术后复发转移率高的“三低一高”特点[1],化疗仍在胃癌治疗策略中占据主导地位。对胃癌晚期患者而言,体质状况相对较差,综合考虑器官功能、并发症、安全性方面,美国国立综合癌症网络与欧洲肿瘤医学协会均推荐采用口服氟尿嘧啶类与奥沙利铂联用方案[2],且其疗效优于三联药物方案。替吉奥与卡培他滨均属于典型的口服氟尿嘧啶类药物,可分别与奥沙利铂联合为SOX、XELOX方案,临床已有多项研究对其各自疗效、安全性进行探讨[3-5],然而二者临床应用效果缺乏对比。对此,本研究旨在探索SOX与XELOX方案对术后复发性胃癌患者血清肿瘤标志物、生存期及耐受性的影响差异,取得一定成果,现报告如下。
1 材料与方法
1.1 一般资料
回顾性分析2017年1月至2019年3月期间,于我院接受治疗的192例术后复发性胃癌患者临床资料,采用SOX方案者纳入S组(n=98),采用卡培他滨联合奥沙利铂(XELOX)方案者纳入X组(n=94)。纳入标准:①临床表现、影像学检查与内镜活检组织学检测结果均符合术后复发性胃癌相关诊断标准者[6];②年龄为40~80岁者;③手术至复发时间≤2年者;④预计生存期≥4个月者。排除标准:①治疗前血象或肝肾功能存在异常者;②合并精神疾病、意识障碍而无法配合治疗者;③伴有其他部位恶性肿瘤或活动性感染者;④对相关化疗药物有过敏反应者;⑤改变治疗方案或临床资料不完整者。S组男性53例,女性45例;年龄为43~79岁,平均(63.81±9.26)岁;Ⅲa期11例,Ⅲb期33例,Ⅲc期36例,Ⅳ期18例;胃体部癌22例,胃窦癌47例,胃底贲门癌29例;乳头状腺癌41例,管状腺癌29例,黏液腺癌18例,低分化腺癌10例;手术至复发时间为6~22个月,平均(15.75±4.31)个月。X组男性53例,女性41例;年龄为46~77岁,平均(64.12±8.87)岁;Ⅲa期4例,Ⅲb期36例,Ⅲc期39例,Ⅳ期15例;胃体部癌21例,胃窦癌43例,胃底贲门癌30例;乳头状腺癌41例,管状腺癌26例,黏液腺癌19例,低分化腺癌8例;手术至复发时间为8~23个月,平均(15.94±4.20)个月。两组一般临床资料比较均无统计学意义(P>0.05),后续观测指标具有可比性。
1.2 方法
S组予以替吉奥胶囊(生产企业:山东新时代药业有限公司,规格:25 mg,国药准字:H20080803)按体表面积给药,体表面积<1.25 m2者服用40 mg/次,体表面积为1.25~1.5 m2者服用50 mg/次,体表面积>1.5 m2者服用60 mg/次,bid,早晚餐后温水送服,d1~d14+注射用奥沙利铂(生产企业:齐鲁制药(海南)有限公司,规格50 mg,国药准字H20093167)130 mg/m2,稀释于生理盐水后2 h内静脉滴注完毕,d1,以21 d为1个化疗周期。X组予以卡培他滨片(生产企业:上海罗氏制药有限公司,规格:500 mg,国药准字H20073024),每次100 mg/m2,bid,早晚餐后温水送服,d1~d14+注射用奥沙利铂130 mg/m2,稀释于生理盐水后2 h内静脉滴注完毕,d1,以21 d为1个化疗周期。两组均常规给予止呕、保肝药物,持续随访至治疗开始后1年。
1.3 观察指标
于治疗前及治疗6个周期后,常规采集患者肘静脉血样,低温下充分凝血并离心后,提取上层清液,分别采用糖类抗原125(carbohydrate antigen 125,CA125)、糖类抗原19-9(carbohydrate antigen 19-9,CA19-9)、癌胚抗原(carcinoembryonic antigen,CEA)对应试剂盒,经由酶联免疫吸附试验(enzyme-linked immuno sorbent assay,ELISA)测定上述物质在血清中的浓度。回顾两组无进展生存期(progression-free survival,PFS)情况并纳入统计。
1.4 评估标准
1.4.1版实体肿瘤疗效评价标准(Response Evaluation Criteria in Solid Tumors 1.1,RECIST1.1)评估治疗效果[7]。完全缓解(CR):靶病灶完全消失,病理淋巴结短径<10 mm;部分缓解(PR):靶病灶长径总和减小>30%;疾病进展(PD):靶病灶长径总和增大>20%,增大绝对值>5 mm,或出现新病灶;疾病稳定(SD):病灶直径变化在PR、PD所述标准之间。客观缓解率(ORR)=CR+PR。采用胃癌患者生活质量问卷(Quality of Life Questionnaire of Stomach 22(QLQ-STO22))评估生活质量[8],通过对吞咽困难、疼痛、返流、焦虑等共22项问题进行评价,每项问题按对生活影响严重程度计为1~4分,满分为88分,分数越高则说明生活质量越差。采用不良事件通用术语标准4.0版(Version 4.0 of Common Terminology Criteria for Adverse Events,CTCAE v4.0)评估毒副反应[9],针对最常见的胃肠道症状、血液和淋巴系统症状及手足综合征进行评级,以1~4级表示“发现症状但无需治疗”~“症状危及生命”,将3~4级定义为中重度毒副反应进行统计。
1.5 统计学方法
数据均录入SPSS 23.0软件进行统计处理,分类变量以百分率的形式描述,无序分类变量组间比较根据理论频数所处范围,对应选用Pearson卡方检验、连续性校正卡方检验或Fisher精确概率检验,有序分类变量采取Mann-Whitney U检验;连续变量先实施方差齐性与正态性检验,具备方差齐性且近似服从正态分布变量以平均值±标准差的形式描述,前者组间同期比较采取独立样本t检验,组内不同时间比较采取配对样本t检验;生存分析以Kaplan-Meier曲线描述,组间生存期比较采取Log Rank检验;上述检验均采用双侧检验法,无特殊说明均以P<0.05为有统计学意义。
2 结果
2.1 两组患者治疗效果比较
治疗6个周期后,两组ORR与死亡率比较均无统计学意义(P>0.05),见表1。

表1 两组患者ORR及死亡率比较(例,%)
2.2 两组患者血清肿瘤标志物及生活质量比较
治疗6个周期后,两组血清CA125、CA19-9、CEA水平均较治疗前有显著下降(P<0.05),而组间同期比较则均无统计学意义(P>0.05);两组QLQ-STO22评分均较治疗前有显著下降,且S组明显低于同期X组,差异均有统计学意义(P<0.05),见表2。

表2 两组患者治疗前后血清CA125、CA19-9、CEA水平及QLQ-STO22评分比较
2.3 两组患者PFS比较
S组中位PFS为281.0天(95%CI=253.088~308.912),与X组的247.0天(95%CI=157.374~336.626)比较无统计学意义(Log Rank χ2=0.128,P=0.720),见图1。

图1 两组患者PFS比较
2.4 两组患者不良反应严重程度比较
治疗6个周期内,两组胃肠道症状、血液和淋巴系统症状严重程度比较均无统计学意义(P>0.05),而S组手足综合征严重程度明显轻于X组,差异有统计学意义(P<0.05),见表3。
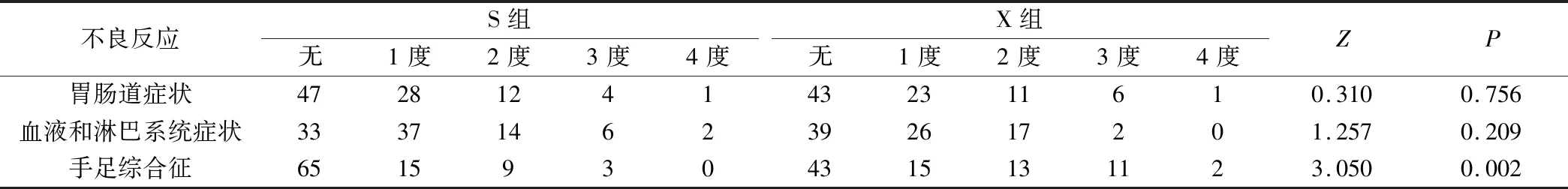
表3 两组患者不良反应严重程度比较/例
3 讨论
由于早期诊断率较低,胃癌患者确诊时通常已发展至中晚期,手术效果欠佳,术后转移与复发率均较高,预后不甚理想,因此采取有效的化疗方案改善预后至关重要。
铂类化疗药物进入细胞后发生水解,水合阳离子可以共价键的形式紧密嵌合于多处DNA腺嘌呤与鸟嘌呤碱基之间特定位点,造成脱氧核酸链内交联、链间交联及与蛋白大分子交联结构剧变,从而使其发生解旋、扭曲或断裂[10],直接阻断复制与转录过程,最终促成细胞凋亡。其中第三代的奥沙利铂化学结构空间位阻相对第二代的卡铂更大,抗肿瘤活性与抗肿瘤谱不完全相同,因此并未形成交叉耐药性,加之其代谢动力学模型中,分布相迅速而排出相缓慢,半衰期可达24 h[11],肝肾毒性较小且疗效尚佳,尤其适合于身体状况较差的晚期胃癌患者治疗。本研究结果显示,两组近期疗效、FPS均无显著差异,这表明SOX与XELOX方案应用于术后复发性胃癌均有一定疗效,初步猜测认为,由于卡培他滨与替吉奥均属于5-氟尿嘧啶(5-fluorouracil,5-Fu)前体制剂的口服药物,其抗肿瘤机制均有赖于5-Fu对RNA、蛋白质合成过程的抑制作用,倘若二者生物利用度相仿,则对总体治疗效果影响较小。有关学者得到与之不同的结论,发现晚期胃癌患者完成2个周期治疗后,SOX方案可获得47.6%总有效率,显著高于XELOX方案的25.0%[12],由于本研究纳入样本量相对较大,治疗周期数较多,并已开展生存分析,统计学上存在较强说服力,但仍有待后续研究加以验证。
肿瘤标志物是当代肿瘤学、分子生物学与临床检验医学共同发展的前沿性成果,已逐渐在肿瘤筛查、早期诊断、疗效判定、预后评估等方面发挥重要作用。相关研究表明,CA125检测既往多应用于卵巢癌诊疗工作,近年研究发现其也能反映出化道恶性肿瘤进展趋势,由于除卵巢、输卵管上皮细胞表面外,还大量分布于腹膜与胸膜间皮细胞表面[13],因此对胃癌复发转移有较高灵敏度。CA19-9则广泛存在于胃肠道肿瘤细胞表面,且已证实术后其水平升高是胃癌复发的高危因素[14]。本研究发现,两组治疗后血清CA125、CA19-9、CEA水平均出现显著下降,但组间比较未见显著性差异,提示两种化疗方案均能从本质上控制术后复发性胃癌患者肿瘤生长,对改善预后有积极意义。邢瑞青等[15]认为,CEA尽管在多种恶性肿瘤患者血清中表现出升高趋势,但对胃癌根治术后生存期、肝转移率与复发率均有较高独立预测价值。
卡培他滨转化为5-Fu需经由胞苷脱氨酶、羧酸酯酶及胸苷磷酸化酶依次作用[16],其中胸苷磷酸化酶在肿瘤细胞中丰富表达且酶活性较高,肿瘤细胞内激活概率大,因此该药物具有一定抗肿瘤靶向性,对药物毒性进可起到一定控制作用。替吉奥则是替加氟、吉美嘧啶与奥替拉西钾以1∶0.4∶1摩尔比例制备的复合型药物,前体物质替加氟在肝脏经由细胞色素P450加工成为5-Fu[17],吉美嘧啶则通过拮抗二氢嘧啶脱氢酶活性,抑制5-Fu分解代谢而维持有效生理作用浓度,而奥替拉西钾则在口服后作用于消化系统内乳清酸磷酸核糖基转移酶以避免5-Fu胃肠道毒副作用。本研究中,两组下胃肠道症状、血液和淋巴系统症状严重程度均无统计学意义,而S组手足综合征严重程度明显低于X组,且生活质量明显较好,这说明SOX方案与XELOX方案控制毒副反应效果均属良好,但由于卡培他滨部分代谢产物可经由汗腺排出,因而更易于富集与皮肤组织造成损害,最终触发手足综合征并使其加重,不利于改善患者生活质量,故SOX方案安全性相对XELOX方案更为理想。该结论与多数临床研究相符,为保障患者坚持参与化疗,通常以调整化疗药物剂量,加服维生素B6、维生素E、环氧化酶-2(Cyclooxygenase-2,COX-2)特异性抑制剂或外用角质层分离剂对其进行缓解[18]。
综上所述,SOX方案与XELOX方案治疗术后复发性胃癌疗效均较为理想,二者对生存期延长效果接近且对血清肿瘤标志物水平减低幅度相当,但SOX方案安全性相较于XELOX方案更佳,对改善患者生活质量有一定帮助。

