自蔓延燃烧法制备Pd0.01CuxCe(1-x)/2Zr(1-x)/2Oy催化剂催化NO制NH3反应的性能研究
闫瑞宁,王一男,赵旭腾,刘旻,刘兴,胡琨,石福禄,王涛,林赫,黄震
(1.上海交通大学新能源动力研究所教育部重点实验室,上海 200240;2.上汽汽车乘用车公司技术中心,上海 201804;3.北京市机动车排放管理中心,北京 100176)
与传统的化学计量发动机相比,稀薄燃烧发动机不仅具有更好的燃油经济性,而且二氧化碳排放也更低[1]。然而,如何有效地减少稀薄燃烧废气中的氮氧化物(NOx)仍然是汽车工业面临的挑战。NOx作为主要的大气污染物,会导致酸雨和城市烟雾的形成,对自然和人类健康造成灾难性的影响[2]。因此,最新发布的排放法规如EURO 6[3]和China 6a[4]对NOx排放有严格的限制。三效催化剂(TWC)在当量空燃比(λ=1±0.01)下对化学计量发动机排气中NOx,CO和HC的同时控制非常有效,但在稀薄燃烧条件下性能较差。当λ大于1.2时,由于TWC的衰减效应,NOx排放急剧增加[5]。因此,需要采用新的后处理系统来满足严格排放法规的要求。
通用电气公司(General Electric Company)首次提出了这种被称为“被动式”或“无尿素”SCR的新技术[6]。在传统TWC的基础上,增加了SCR脱硝,在周期性富燃运行过程中,由TWC供给NH3并将其储存在SCR催化剂上。而在贫燃运行期间,通过SCR上储存的NH3降低了NOx。这种所谓的TWC+PSCR法消除了传统的SCR尿素罐,降低了成本。
具体地说,在富燃过程中,在TWC催化剂上NO与H2及HC生成NH3储存在下游SCR中;储存的NH3在稀燃时与NOx发生SCR反应产生N2[7]。被动SCR法的关键反应是生成NH3[8]。然而,对TWC催化剂上NH3生成的研究较少。事实上,NH3一直被视为环境的副产品甚至污染物,在TWC反应过程中肯定会产生NH3,并从车上逃逸,这一点已经得到了后续反应器筛选、发动机底盘测功机研究和风洞调查等试验的证实[9]。Heeb等[10]进一步论证了NH3作为二次污染物应纳入今后的法规中。相反,对于被动式SCR脱硝方法,其主要目标是通过TWC生产NH3并输送到下游SCR催化剂,此反应中NH3是有益的中间产物,用于后续NOx的去除。
自蔓延燃烧合成法由于其能效高、反应时间短、产率高、净化能力强,在金属氧化物催化剂领域中受到广泛的关注[11]。因此,本研究采用自蔓延燃烧合成法对催化剂进行制备,得到纯净及高产率的催化剂。采用Pd/Ce0.5Zr0.5Ox催化剂模拟TWC催化剂的主要成分,并掺杂Cu进行改性,从而提高NOx转化为NH3的催化能力。
1 实验
1.1 催化剂制备
采用自蔓延燃烧合成法[12]制备Pd0.01CuxCe(1-x)/2Zr(1-x)/2Oy型贵金属催化剂。首先按照不同的Pd,Cu,Ce,Zr配比制作前驱液,将Pd(NO3)2·xH2O,Cu(NO3)2·9H2O,Ce(NO3)3·6H2O,Zr(NO3)4·5H2O粉末溶于20 ml去离子水中,并按照一定的化学计量比(甘氨酸与硝酸根离子比例为5∶9)加入甘氨酸(C2H5NO2)作为助燃剂。将混合溶液在60 ℃下充分搅拌1 h后转移至坩埚内,在马弗炉中迅速升温到600 ℃并持续焙烧4 h,最终将坩埚内燃烧所得的粉末经过压片、研磨等处理后筛分至40~80目大小的颗粒备用。按照不同的Pd,Cu,Ce,Zr配比,将催化剂标记为Pd0.01CuxCe(1-x)/2Zr(1-x)/2Oy(x=0,0.1,0.2,0.4)。
1.2 催化剂性能评价
NO与H2的产氨反应在固定床流动反应器中进行,将经过压片处理的催化剂置于石英管反应器中,反应器置于程序升温管式炉内,炉温由PID控制器进行调节。反应器中的进气反应物由500×10-6NO,2 000×10-6H2及平衡气N2组成,控制空速为30 000 h-1。待反应器出口处气体成分稳定后,出口气体中的NO,NO2及NH3浓度通过FTIR光谱仪(Thermo Nicolet 10)以1 Hz的采样率进行测量。催化剂的性能评价通过NO向NH3的转化率(SNH3)来表示[13],其定义如下:
SNH3= [NH3]out/[NO]in。
式中:[NH3]out为出口处的氨浓度;[NO]in为入口处一氧化氮浓度。
1.3 催化剂性能表征
使用Quantachrome NOVA 2000e自动气体吸附仪来测量样品的比表面积。使用N2作为吸附气在77 K下进行吸附。在进行样品比表面积测试之前,将样品在300 ℃的真空下脱气4 h以除去杂质。比表面积通过BET法进行测定。使用CuKα辐射(λ=1.540 6 Å)通过粉末X射线衍射(XRD,D8 ADVANCE DA VINCI)分析样品的晶体结构。
在20°~80°的2θ范围内获得了XRD曲线,并通过Scherrer方程确定了催化剂的晶体尺寸。在Kratos AXIS Ultra DLD光谱仪上使用X射线光电子能谱法(XPS)分析催化剂表面的元素组成。C 1s光谱从278至298 eV收集,Cu 2p从923至958 eV收集,Ce 3d从330至350 eV收集,O 1s从765至815 eV收集。在Micromeritics Chemisorb 2720设备上进行了H2-TPR测试,以研究样品的还原性。首先将样品在600 ℃的N2中处理1 h,然后冷却至室温。H2-TPR在100~800 ℃的温度下以10 ℃/min的斜率暴露于5%H2/N2的气体混合物中,采用GC 2014气相色谱仪和TCD检测器监测氢气含量变化。使用MAIA3 model 2016高分辨扫描电子显微镜来测试催化剂表面的光谱发射情况。采用Nicolet 6700型红外光谱仪,通过原位漫反射红外傅里叶变换技术(in-situ FTIR) 分别探究催化剂表面NO吸附情况及催化剂表面的反应过程。
2 结果与讨论
2.1 催化剂性能
催化剂的产氨效率曲线见图1。由图1可见,当不掺杂铜时,没有NO转化为NH3。掺杂铜后,Cu负载对产氨效率的提高具有显著作用,催化活性顺序从大到小依次为x=0.1,x=0.2 ,x=0.4,随着Cu掺杂量的增加,催化剂活性先增高后降低。当掺杂比例x=0.1时,在250~350 ℃温度窗口内,催化剂能实现NO到NH3的全部转化;对于掺杂比例x=0.2的催化剂,其活性相对降低,在275~350 ℃的温度窗口内转化率超过92%;掺杂比例x=0.4时,催化活性进一步降低,催化活性在250~350 ℃区间接近90%。结果表明,催化剂的产氨效率并不完全取决于掺杂量,而是取决于催化剂的结构、表面组成、氧空位及酸性位点等因素[14]。

图1 NO在不同催化剂上的氨转化效率
2.2 催化剂表征
不同比例的Pd0.01CuxCe(1-x)/2Zr(1-x)/2Oy(x=0,0.1,0.2,0.4)催化剂的XRD图谱见图2。纯Ce0.5Zr0.5O2样品的反射主要位于29.25°,33.70°,34.03°,48.725°,48.90°和58.02°,分别对应于(1 0 1),(0 0 2),(1 1 0),(1 1 2),(2 0 0)和(2 1 1)Ce-Zr-O固溶体的平面。随着铜含量的增加,衍射峰向更高的方向偏移。在Cu负载量x=0.1的样品轮廓上未观察到Cu或CuO峰。这表明铜氧化物的良好分散和固溶体的形成将增强铜氧化物与铈锆载体Ce0.5Zr0.5O2之间的相互作用,并促进反应的发生[15]。此外,由表1可见,催化剂的晶粒尺寸略有降低,这归因于配位的Cu+和Cu2+的尺寸比Ce3+或Ce4+的尺寸小,以及铜氧化物与载体Ce0.5Zr0.5O2晶格中的结合。对于Cu负载量为x=0.2及x=0.4的样品,检测到35.4°和38.9°处发生了弱反射,这归因于块状CuO的存在,这对催化活性没有好处[16]。
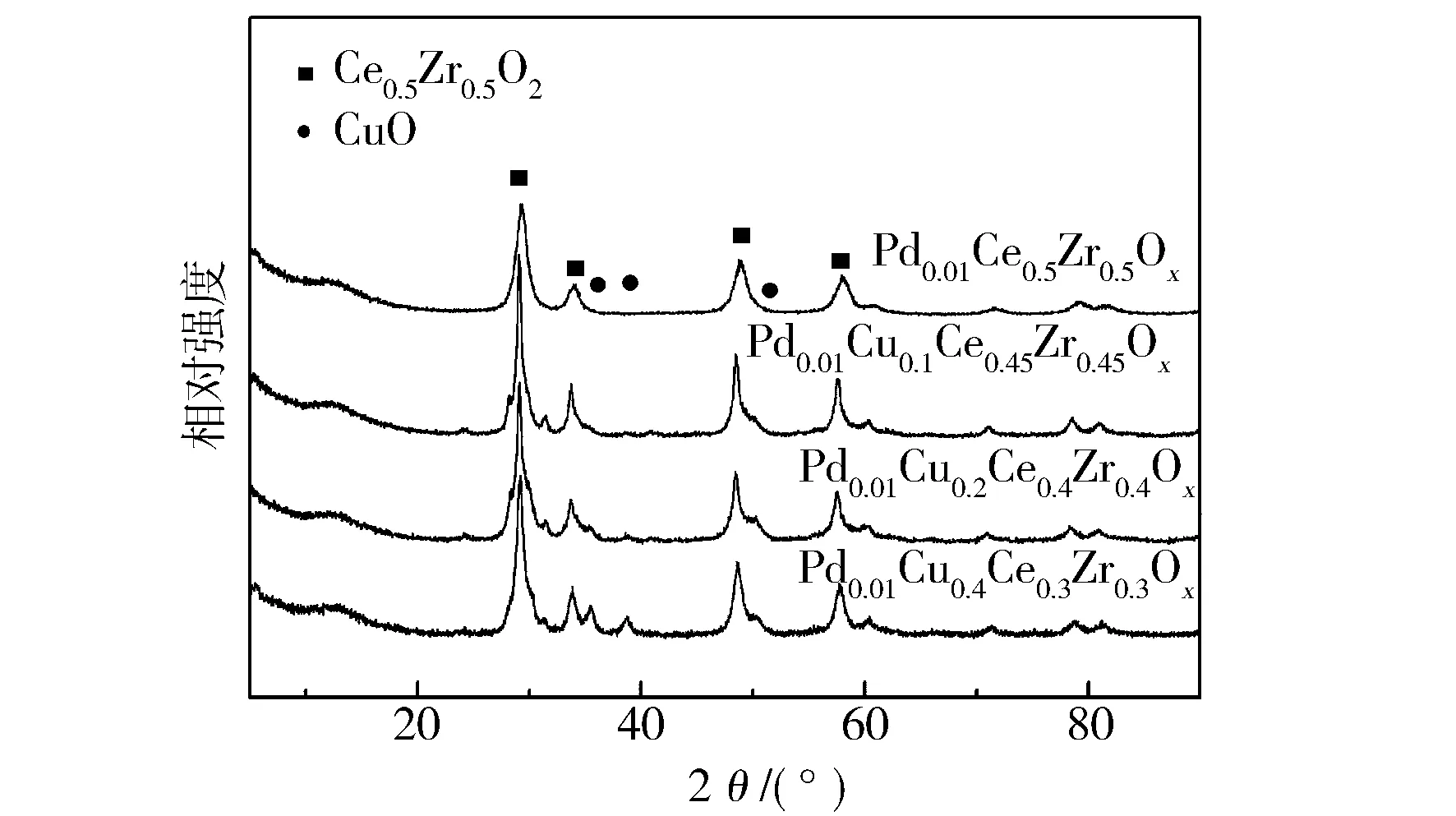
图2 不同催化剂的XRD谱图
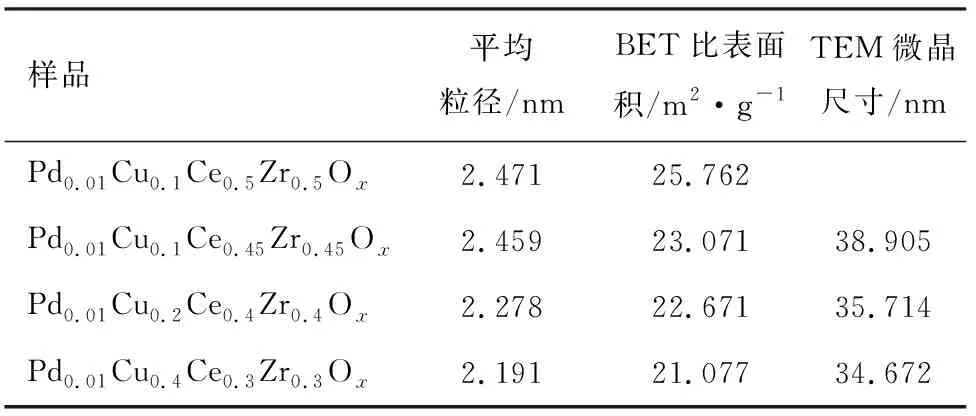
表1 不同催化剂的物理特征
图3示出了不同比例的Pd0.01CuxCe(1-x)/2Zr(1-x)/2Oy(x=0,0.1,0.2,0.4)催化剂样品的TEM图像。从图中可以看到很多颜色较深的黑点,这表明钯物种的存在。随着铜掺杂比例的增加,黑点逐渐聚集成大片的黑块,表明钯的聚集对催化活性不利[17]。当铜掺杂比例小于0.1时,钯物种在催化剂表面高度分散。综上所述,铜的掺杂会改变钯的分散性,从而在一定程度上影响催化剂的催化活性。样品的平均粒径随着铜的掺杂而略有降低,这表明将铜离子掺入萤石晶格有助于减小晶体尺寸[18]。这可以归因于6个配位的Cu2+(0.073 nm)与Ce4+(0.10 nm)和Zr4+(0.084 nm)相比半径较小。样品的HRTEM形态见图4。间隔值为0.310 nm和0.306 nm的晶格条纹分别对应于(1 1 1)平面的Ce0.5Zr0.5O2和Cu-Ce-Zr-O固溶体。在铜含量为x=0.1的样品上未观察到CuO的晶格条纹,这可能是由于Cu含量低所致。间隔为0.230 nm的晶格条纹对应于(1 1 1)平面的CuO(见图4b和图4c)。

图4 不同催化剂的HRTEM图像
结果表明催化剂中的Cu主要以Cu氧化物和Cu-Ce-Zr-O固溶体两相存在[19]。Cu掺入Ce0.5Zr0.5O2受限制,高的Cu负载量将导致催化剂表面上形成大量的氧化铜,这在产氨反应中的活性较低,导致Cu负载量x=0.2及x=0.4的催化性能较差。
2.3 XPS光谱
图5示出Pd0.01CuxCe(1-x)/2Zr(1-x)/2Oy(x=0,0.1,0.2,0.4)催化剂样品的XPS分峰光谱。图5a反映了Pd0.01CuxCe(1-x)/2Zr(1-x)/2Oy(x=0,0.1,0.2,0.4)样品的Ce 3d光谱。光谱可分为8个不对称峰,883.9 eV,888.9 eV,897.8 eV,903.1 eV,907.8 eV和916.7 eV对应的峰为Ce4+特征峰,885.6 eV和903.8 eV对应的峰为Ce3+特征峰。Ce3+与Ce4+的比例可反映催化剂表面氧空位情况,这与催化剂性能高度关联[20]。由表2可见,在Cu负载量x=0.1和x=0.2时,表面Ce3+与Ce4+的比例与Cu负载量没有直接关系。Cu负载量超过x=0.2时,Ce3+的含量降低,这可能是由于高分散性CuO的形成使催化剂表面的Ce3+再氧化,从而降低了Ce3+含量[21]。
图5b 示出了Pd0.01CuxCe(1-x)/2Zr(1-x)/2Oy(x=0,0.1,0.2,0.4)催化剂样品的Cu 2p光谱。可以将Cu XPS信号分解为以934.3 eV为中心的Cu 2p 3/2和以954.1 eV为中心的Cu 2p 1/2的两个不对称峰。在934.0 eV和953.7 eV处的主峰可以识别为Cu2+,而在940.1~945.1 eV范围内的摇动峰归因于Cu+。Cu+和Cu2+的同时存在可归因于分散的CuO氧化催化剂表面上的Ce3+形成Cu+[22]。随着Cu掺杂量的增加形成大量的CuO,使得Cu2+在Cu负载量x=0.4样品中要低得多。
图5c示出的O 1s光谱可以拟合到两个主峰中。在529.6~529.9 eV范围内的氧对应于来自催化剂晶格的氧(OL),而另一个以531.0~531.5 eV为中心的氧来自于表面化学吸附的氧(OA)。在催化剂上,OA与(OL+OA)的比率随着Cu负载量的增加而减少。这表明在晶格中掺入Cu促进了铜离子与表面吸附氧OA的结合[23],从而使OA量减少。OA的减少降低了催化剂表面的氧化还原能力,降低了催化剂样品对该反应的催化活性。

图5 不同催化剂的XPS谱图

表2 不同催化剂表面的原子组成
2.4 H2-TPR

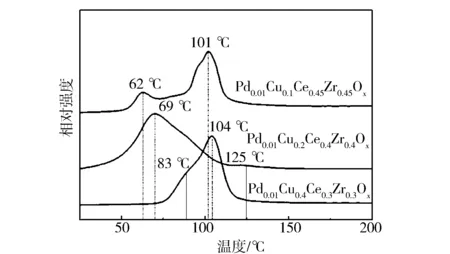
图6 不同催化剂的H2-TPR谱图
2.5 拉曼光谱
图7示出Pd0.01CuxCe(1-x)/2Zr(1-x)/2Oy(x=0,0.1,0.2,0.4)催化剂样品的拉曼光谱测试结果。在589,543,474,309,257,210 cm-1处的峰形特征为四方相结构Ce0.5Zr0.5O2的Raman振动峰[27]。随着Cu负载量的增加,Ce0.5Zr0.5O2在257 cm-1和474 cm-1处的特征峰逐渐红移,这表明引入Cu后形成Cu-Ce-Zr-O固溶体,使得Ce-Zr-O键长增加[28];此外,处于589 cm-1处的特征峰随着Cu负载量的增加逐渐蓝移,这可以看作是氧空位的产生[29]。这些结果表明,Cu2+可能结合到了Ce-Zr载体的晶格内。值得一提的是,对于Cu负载量为x=0.2及x=0.4的催化剂,在大约292 cm-1处出现了CuO的特征峰,而Cu负载量为x=0.1的催化剂特征峰并不明显,这表明过量的CuO累积在催化物的表面,并与Cu-Ce-Zr-O固溶体产生了很强的相互作用。而这种过强的相互作用对产氨反应并没有积极影响。
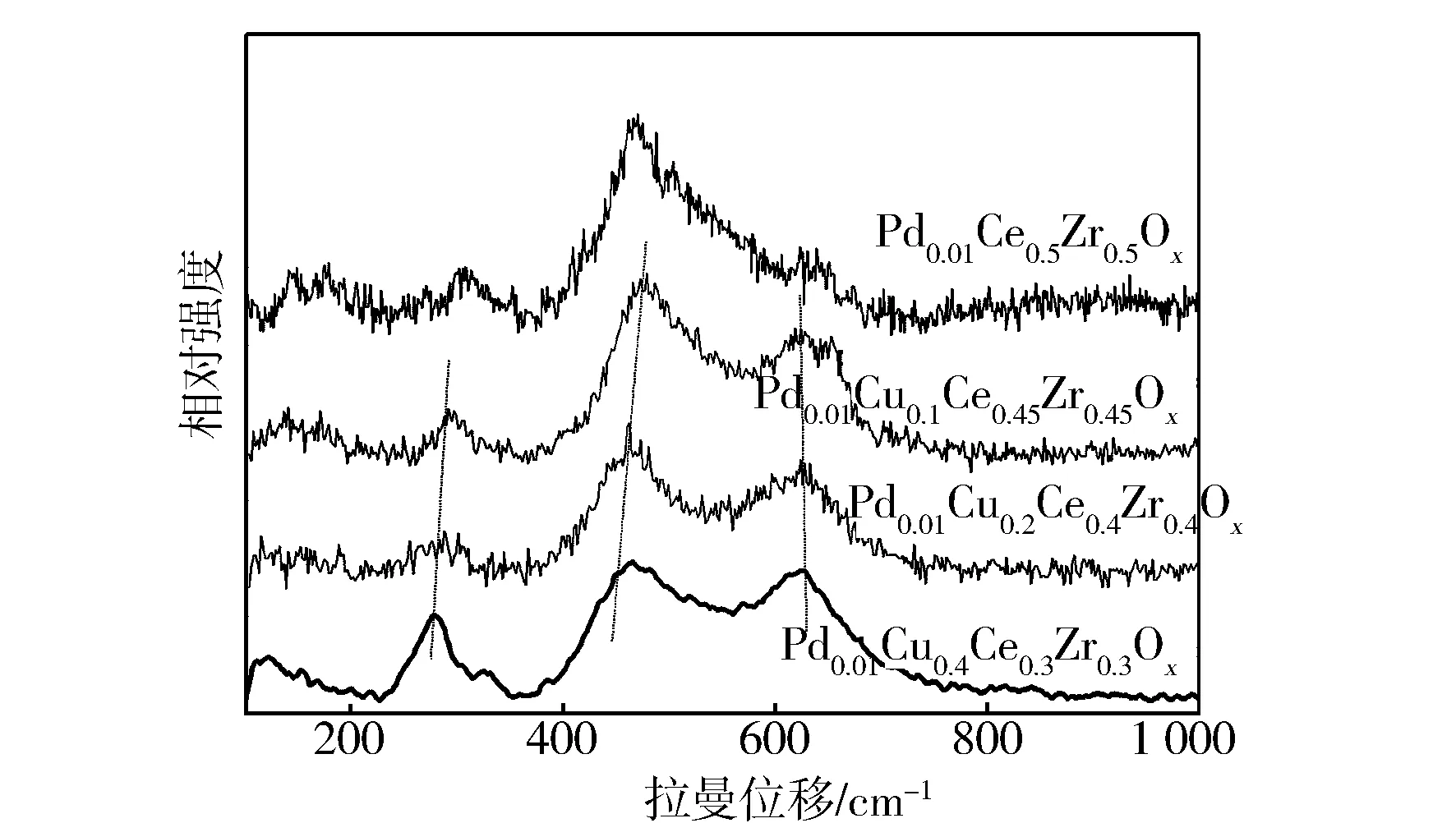
图7 不同催化剂的拉曼谱图
此外,632 cm-1和463 cm-1处的两个峰面积(表示为A632和A463)的比值可反映出相对的表面氧空位数量[30]。不同催化剂的632 cm-1和463 cm-1的峰面积比拟合结果见表3。当Cu掺杂量为0.1时,A632/A463的值最高,表明催化剂表面存在较多的氧空位。催化剂的氧空位数量从大到小依次为Pd0.01Cu0.1Ce0.45Zr0.45Ox,Pd0.01Cu0.2Ce0.4Zr0.4Ox,Pd0.01Cu0.4Ce0.3Zr0.3Ox, Pd0.01Cu0.1Ce0.5Zr0.5Ox,与催化剂的活性变化一致。由此可见,Cu掺杂过多或过少都会对表面氧空位产生不利影响。众所周知,氧空位的产生将促进铜和Ce0.5Zr0.5O2载体之间形成强大的金属-载体相互作用。因此,当Cu的掺杂量为0.1时,氧空位的最大数量导致Cu与Ce0.5Zr0.5O2的相互作用更强,从而促进催化剂的转化效率。

表3 不同催化剂的A632/A463比值
2.6 原位表征


图8 不同催化剂的NO吸附in-situ FTIR谱图
此外,对Pd0.01Cu0.1Ce0.45Zr0.45Ox催化剂样品的NO与H2反应性也进行了研究(见图9)。

图9 不同催化剂产氨反应的in-situ FTIR谱图
在250 ℃下用NO预吸附饱和后,向催化剂通入H2,并测定其0~15 min的原位红外光谱。当开始通入H2后,催化剂表面的各种硝酸盐物种随着H2通入时间的增加逐渐减少,在1 min时只剩下强度较弱的吸附峰,说明表面吸附的NOx物种以较快的反应速度消耗;在15 min时只剩下很弱的吸附峰,说明大部分吸附的NOx物种均可参与NO与H2的产氨反应[33]。
3 结论
a) 随着Cu负载量的增多,催化剂表面的Ce3+含量减少,Ce4+的相对含量增加,而Cu2+相对含量减少,催化剂表面化学吸附氧的比例减少;结果表明,OA的含量及Cu2+与Ce4+的竞争关系是决定该反应的重要因素;
b) 铜与铈锆之间的过强相互作用,使得随着Cu负载量的增加,CuO在催化剂中形成,对反应不利,过多的Cu负载量抑制了Pd0.01CuxCe(1-x)/2Zr(1-x)/2Oy催化剂的低温还原能力;
c) 拉曼图谱部分特征峰的蓝移及红移,在催化剂表面产生了更多的氧空位;过量的CuO累积在催化物的表面,并与Cu-Ce-Zr-O固溶体产生了很强的相互作用,对反应不利;
d) 酸度在该反应中也起到重要的作用;铜掺杂可以产生更多的酸性位点,有效地改善了NO的活化,从而促进NO向NH3的转化;Pd0.01Cu0.1Ce0.45Zr0.45Ox催化剂样品的氧化还原能力强,但其对NOx的吸附能力较弱,且该反应的反应速率较高;
e) Cu的掺杂改善了催化剂表面物种的分布,提高了活性物质的分散度,增强了催化剂的催化还原能力,并增加表面化学吸附氧及催化剂表面的酸性位点,从而在多方面改善了催化剂的性能,这种新式催化剂有希望成为改进TWC催化剂实现被动SCR脱附NOx的一个非常有效的方案。

