唑来膦酸联合局部放疗对原发性肝癌骨转移患者血清miR-21、TNF-α和骨代谢水平的影响
徐晓美,沈预程,邵春燕
南通大学附属海安医院肿瘤科,江苏 海安 226600
原发性肝癌(primary liver cancer,PLC)是一种发病率和恶性程度较高、预后较差的恶性肿瘤,在疾病早期常无特异性症状和体征,部分患者以转移灶为首发,其中骨转移的发生率为3%~28%[1]。PLC骨转移病灶处骨骼疼痛进行性加重,易发生病理性骨折和压迫脊髓神经导致局部剧烈疼痛和截瘫,有报道称,PLC骨转移患者的生存期一般不超过10个月,严重影响患者的生活质量和疾病预后[2]。对于骨转移患者局部放疗是一种有效的治疗手段,可抑制转移性病灶的进展,但对减轻骨痛和压迫症状并不理想[3]。唑来膦酸是最新一代双膦酸盐类药物,可抑制成骨细胞产生炎症细胞因子,诱导破骨细胞的凋亡,抗骨质吸收,延缓和减轻骨转移性病灶的破坏,减轻骨痛[4]。微小RNA(miRNA)是一种非蛋白编码转录分子,通过多种机制抑制mRNA的表达,发挥调控抑癌基因的表达,是新型恶性肿瘤标志物,在评估肝癌和发生远处转移中具有较高的临床价值[5]。近年来,我们对PLC骨转移患者在局部放疗的基础上加用唑来膦酸治疗,观察血清miRNA表达水平及疾病预后,现报道如下。
1 资料与方法
1.1 病例选择(1)诊断标准:经病史、影像学、手术和病理组织学检查确诊为PLC;出现骨转移灶,经PECT检查确诊。(2)纳入标准:年龄45~75岁;预测生存期超过3个月,具有唑来膦酸和局部放疗的适应证;经医学伦理审批,患者知情同意。(3)排除标准:肝功能失代偿期,其他多处转移,恶液质期;骨代谢性疾病,风湿性、免疫性疾病;重要脏器功能衰竭,严重糖尿病、高血压;1个月内使用双膦酸盐、皮质激素、放疗和化疗等治疗;妊娠、哺乳期妇女,药物过敏史;智力和精神障碍不能配合,中途死亡或失访者。
1.2 一般资料选择2018年1月至2019年6月收治的符合入选标准的PLC骨转移患者76例作为研究对象;根据数字表示法将患者分成观察组和对照组,各38例。观察组中男25例,女13例;年龄(61.7±5.8)岁(46~75岁);体质量(57.6±4.2)kg(41~75 kg);PLC病史(4.3±2.1)个月(0.5~28个月);Child-Pugh分级A级11例,B级24例,C级3例;骨转移部位为脊柱转移26例,骨盆转移8例,四肢转移4例。对照组中男26例,女12例;年龄(61.4±5.6)岁(46~74岁);体质量(57.8±4.3)kg(42~76 kg);PLC病史(4.2±2.3)个月(0.6~27个月);Child-Pugh分级A级12例,B级23例,C级3例;骨转移部位为脊柱转移25例,骨盆转移9例,四肢转移4例。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.3 研究方法(1)对照组:在一般治疗的基础上给予局部放疗。给予相应营养支持和对症治疗,疼痛较剧者给予非甾体镇痛药治疗;给予活血化瘀、清热解毒、软坚散结、理气止痛等中医药辅助治疗。根据影像学检查结果,采用模拟透视机下定位;照射范围为脊椎转移性病灶包括上下相邻的各1个椎体,长骨和扁骨尽量包括整块骨头,骨盆转移性病灶应超越病灶周围2~3 cm;照射剂量为2~3 Gy/次,1周4~5次,总剂量为50~75 Gy。(2)观察组:在对照组治疗的基础上加用唑来膦酸(厂商:正大天晴制药;国药准字:H20041346;规格:4 mg/5 ml)治疗。于放疗第1天时,将唑来膦酸注射液4 mg加入生理盐水100 ml中稀释后缓慢静滴,输注时间不低于20 min;间隔1周后重复使用1次,连续使用4~6次。
1.4 观察指标(1)血清学指标:分别于治疗前和治疗3个月时采集清晨外周静脉血,采用反转录定量PCR法(生产商:上海碧云天生物技术公司;生产批号:20161003)检测miR-21与正常人群的相对表达量(2-△△Ct),ELISA法(生产商:北京北奥莱博科技公司;生产批号:20180080)检测肿瘤细胞因子α(TNF-α)等肿瘤标志物水平;采用EIA法(生产商:武汉明德生物科技公司;生产批号:20170326)检测骨钙素(OST)和骨碱性磷酸酶(BAP)等骨代谢水平;采用奥利巴斯AU400全自动生化分析仪和上海景源医疗器械有限公司生产的配套试剂盒,检测丙氨酸氨基转移酶(ALT)、碱性磷酸酶(ALP)和总胆红素(TBIL)等肝功能水平。(2)分别于治疗前和治疗3个月时,评价疼痛指数和生活舒适度评分等生活质量指标。疼痛指数采用视觉模拟评分法(VAS)测评,总分0~10分,0分为无痛,10分为最痛。生活质量评分采用改良Barthel指数评定量表测评,包括进食、如厕、洗浴、活动等10个日常生活项目,每项0~10分,总分100分,得分越低表示生活能力越差。(3)不良反应:观察和处理药物不良反应。

2 结果
2.1 肿瘤标志物水平变化的比较治疗前两组的血清miR-21和TNF-α水平差异无统计学意义(P>0.05);3个月后观察组的下降幅度显著高于对照组(P<0.05)(见表1)。
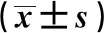
表1 两组肿瘤标志物水平的比较
2.2 骨代谢水平的比较治疗前两组的血清OST和BAP水平差异无统计学意义(P>0.05);3个月后观察组的升高幅度显著高于对照组(P<0.05)(见表2)。
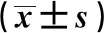
表2 两组骨代谢水平的比较
2.3 肝功能指标的比较治疗前两组的ALT、ALP和TBIL水平差异无统计学意义(P>0.05);3个月后观察组的改善幅度显著高于对照组(P<0.05)(见表3)。

表3 两组肝功能指标的比较
2.4 生活质量的比较治疗前两组的VAS和Barthel评分差异无统计学意义(P>0.05);3个月后观察组的改善幅度显著高于对照组(P<0.05)(见表4)。

表4 两组生活质量评分的比较
2.5 不良反应的比较两组均发生嗜睡、恶心、口干、便秘、低热、皮疹轻度脱发和血细胞下降等一般性不良反应,经处理后缓解,未出现剥脱性皮炎、二重感染、肝肾功能损伤、粒细胞缺乏、药物过敏等严重不良反应。观察组7例(18.42%),对照组6例(15.79%),不良反应率组间比较,差异无统计学意义(P>0.05)。
3 讨论
现代医学研究证实[6],miRNA通过与靶基因的3′非翻译区与碱基配对,调控下游基因转录后翻译,从而发挥促癌作用。miR-21在PLC术前、病灶直径≥5 cm和远处转移等患者血清和组织液中表达水平较强,是PLC的发生、发展、转移、复发等过程中的独立危险因素,可作为PLC的诊断、远处转移、预后评估等重要的标志物。肝肿瘤细胞随血行到达骨髓并定植于局部骨组织,释放出多种炎症细胞生长因子,与骨基质、成骨和破骨细胞作用,形成局灶性骨组织破坏和重塑,使骨组织释放更多的炎症细胞因子,使肿瘤细胞不断增殖,形成转移灶[7]。TNF-α是由单核-巨噬细胞在炎症和免疫反应中分泌的多向性细胞因子,可促进肝细胞增生和血管生成,诱发蛋白多糖合成从而加剧肝细胞炎症坏死和纤维化,是肝癌的诱发因素,还可刺激骨质吸收,在肝癌骨转移中异常表达[8]。唑来膦酸为第三代含氯双膦酸盐制剂,可直接抑制成骨细胞介导的IL-6、TNF-α等炎症细胞因子的生成,减轻肝细胞和骨组织细胞的炎症应激反应,减少骨组织细胞的乳酸生成等生化反应,阻止了破骨细胞的修复[9]。本研究中,观察组治疗3个月后的miR-21、TNF-α等肿瘤标志物水平较对照组显著下降,明显改善了肿瘤基因和应激水平,降低了肿瘤转移和复发的危险系数。
在正常生理情况下,机体的成骨细胞与破骨细胞之间维持着骨代谢平衡,当PLC发生骨转移后,骨代谢平衡被打乱,成骨细胞和破骨细胞功能亢进,骨转换速率增快,骨溶解吸收明显,局部骨质钙化下明显,出现骨质破坏、骨折等病理性改变[10]。OST和BAP是由成骨细胞分泌合成的非胶原蛋白和糖蛋白,可将磷酸酯水解成磷酸,促使骨基质的沉积,水解焦磷酸盐抑制骨盐形成,在调节骨钙代谢中起着重要作用,反映了骨组织转化率和全身骨骼的代谢情况,在肝癌骨转移患者中的表达显著增加,是骨代谢特异性标志物[11]。唑来膦酸与骨基质的羟磷灰石结合后,直接干扰骨吸收;能选择性结合于破骨细胞骨内膜的活性位点,改变破骨细胞的形态,诱导破骨细胞凋亡;可抑制破骨细胞介导的细胞因子,阻断炎症刺激和肿瘤等因素导致的骨质破坏和吸收[12]。本研究中,观察组治疗3个月后的OST、BAP等骨代谢水平较治疗前升高,改善幅度显著高于对照组,明显改善了机体的骨代谢水平。
在我国大部分的PLC是在慢性乙型肝炎和肝炎后肝硬化等肝脏反应炎症的基础上发展来的,炎症细胞因子在炎症反应过程中产生大量的活性氧和活性氮等物质,诱导肝细胞DNA和血管内皮损伤,促进了肝细胞的变性坏死和肝组织再生,直接导致慢性肝功能损伤。在PLC的中晚期,机体的炎症应激反应和骨转移病灶组织释放的炎症细胞因子直接导致肝组织细胞大量变性坏死和纤维组织增生;肿瘤病灶的梗阻压迫使肝脏血流动力学异常,肝脏代谢能力下降,大量代谢产物在肝内堆积,对肝组织细胞产生持续性刺激,均可导致肝脏功能受损[13]。唑来膦酸能通过抑制肝脏肿瘤组织和骨转移病灶的炎症细胞因子生成,减轻炎症应激反应对肝组织细胞的损伤,改善了肝脏功能[14]。本研究中,观察组治疗3个月后的ALT、ALP、TBIL等肝功能指标对照组显著改善,说明唑来膦酸抑制了PLC骨转移的进展,对肝功能有一定的改善作用。
PLC肿瘤细胞转移至骨后,骨组织代谢紊乱释放可溶性介质,导致骨质增生和破坏;大量释放的炎症细胞因子、分泌的前列腺素等痛性物质,以及肿瘤细胞浸润骨膜和压迫周围软组织,均可刺激末梢神经,引发顽固性骨痛,严重降低了患者的生活质量[15]。唑来膦酸通过抑制炎症反应,阻止骨质破坏、吸收等作用,显著减轻了骨转移病灶带来的顽固性骨痛症状,有效提高了患者的生活质量,病情减缓骨转移性病灶的进展速度,提高了局部放疗的效果,改善了患者的疾病预后[16]。本研究中,观察组治疗3个月后的VAS评分显著低于对照组,Barthel评分显著提高,有效地减轻了患者骨转移病灶的疼痛症状,提高了生活舒适度和治疗效果。有报道[17]称,唑来膦酸的不良反应为流感样症状、关节肌肉疼痛和胃肠道反应等,大多是可逆性的,尚未发现不可逆的肝肾功能损伤、血液及淋巴系统异常表现。本研究中,观察组发生数例一般性不良反应,经处理后缓解,未影响治疗进程,不良反应率与对照组比较,差异无统计学意义,用药安全性较高。
综上所述,PLC骨转移患者的骨痛症状明显,生活质量较差,对该类患者在局部放疗的基础上加用唑来膦酸治疗,能降低癌症基因表达水平和炎症应激状态,改善骨代谢水平,减轻骨痛症状,提高生活质量,改善了疾病预后,用药安全性较高。

