CH4在原油体系中溶解规律及影响机理
李秉繁,刘刚,陈雷
(中国石油大学(华东),山东省油气储运安全省级重点实验室,山东青岛 266580)
随着石油资源的不断消耗,轻质原油的储量日益减少,含蜡原油的勘探开发越来越重要。但含蜡原油具有密度大、黏度高、流动阻力大等特点,使得其开采、输送问题十分突出[1-3]。含蜡原油溶气改性技术研究越来越重要[4-6],气体溶解对原油降凝、降黏的影响主要取决于气体在原油中的溶解能力以及气体溶解后原油体系性质的变化。因此,研究甲烷(CH4)在原油中的溶解能力具有重要意义。
目前,国内外学者[7-12]对溶气原油溶解度开展了相应研究,发现气体在原油中的溶解度通常随溶气压力的增加而增大,随温度升高而降低。Saboorian[7]通过试验发现,在温度90℃、压力为7.65MPa条件下,CO2在稠油中的饱和溶解量高达914mol/m3,气体溶解使得稠油体系密度减小,即气体对稠油具有较好的稀释作用,降低了稠油黏度;Yang等[8]研究了常压到2MPa压力范围内溶气原油的流变性,结果表明:在测试压力范围内,随着压力的增加,气体溶解量呈现幂律增长;溶气原油的倾点、黏度、平衡黏度及屈服应力均随着溶气压力的增加而减小,并指出溶气原油流变特性的改善主要是由于气体溶解的稀释作用;鲁彦伯[9]研究了不同条件下长10溶气原油溶解度的变化情况,发现溶解度随着压力的增加而增大,但随着温度的降低溶解度先减小后增大。文献[10]同样观察到相似的试验现象,认为温度降低,蜡晶析出,原油中液相体积减少,使得气体溶解度下降。气体溶解度不仅与温度、压力有关,还与溶剂的分子结构有关[11],相同条件下气体在直链烷烃中的溶解度稍大于支链烷烃溶解度;李传宪等[12]对比了CO2和CH4两种气体在原油中的溶解度,发现CO2在原油中的溶解度是CH4的两倍,且降黏效果优于CH4。目前,相关研究主要集中在宏观层面不同压力、温度条件下气体溶解度规律研究,而CH4溶解的微观作用机制尚不明确。
分子动力模拟以经典牛顿力学为基础,能够分析分子间作用力、分子形态等微观性质的变化[13-15],可以作为宏观试验的补充。目前,分子动力学模拟已经成功应用于描述黏土[16-17]、煤表面[18-20]、有机物[21-22]等材料的气体吸附溶解行为。因此,本文以正庚烷为基础油,蜡、胶质、沥青质含量为影响因素,按照L16(43)正交表构建相应的原油体系,并构建胜利原油和南阳原油两种特定比例的原油体系,共18种原油体系。利用分子动力学方法模拟考察不同温度、压力条件下,CH4在原油体系中的溶解过程以及溶解量,根据原油体系的等量吸附热、自由体积以及CH4与原油分子间的相互作用能,分析CH4溶解的作用机制,以期获得CH4在原油中溶解的分子层面的解释。
1 试验部分
1.1 试验油样
试验所用测试油样为胜利原油和南阳原油,油样预处理温度为70℃,常压条件下油样基本物性见表1。

表1 常压条件下油样基本物性
1.2 试验仪器及方法
(1)饱和溶气原油溶解度的测量装置及方法[23]图1为饱和溶气原油溶解度测量装置。利用该装置测试不同温度、饱和溶气压力条件下CH4的溶解度。首先对装置进行密闭性检测,并通过排水法记录装置及管线的总体积V0;其次进油、排气,注入CH4恒温2h,形成饱和溶气原油,记录带压试管内饱和溶气原油的体积V1、压力P1和温度T1;最后,脱气并利用排水集气法记录气体体积Vx以及此时原油体积V2、压力P2和温度T2。

图1 饱和溶气原油溶解度测量装置
假设气体溶解析出过程符合理想气体状态方程,则有式(1)、式(2)。
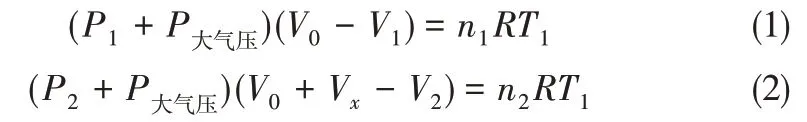
式中,n1、n2分别为脱气前后气体的物质的量,mol。
溶解气体的物质的量Δn见式(3)。

因此,饱和溶气原油溶解的气体体积ΔV见式(4)。

(2)黏温测试 试验所用仪器为MARS60高压流变仪,将预处理的油样加至仪器中,加热到70℃,利用CH4对密闭压力单元进行扫气、加压,试验压力分别为常压、1MPa、2MPa,恒温剪切2h,剪切速率为10s-1,在CH4溶解过程需持续注入一定气体以维持密闭压力单元内压力恒定,随着剪切的进行,密闭压力单元内压力、原油黏度变化趋于平衡,两个参数在2h内保持不变,认为混合体系达到饱和状态。之后对原油恒温20min,消除原油的剪切“记忆”效应,然后以0.5℃/min的冷却速率对油样降温,在油样降温过程中,施加相应的恒剪切速率进行动态降温测试,剪切速率为10s-1。
(3)分子动力学模拟数值试验 利用美国Accelrys公司开发的Materials Studio软件Sorption模块,对CH4在不同原油体系中的溶解进行巨正则蒙特卡洛计算。计算过程采用周期性边界条件,任务选择Adsorption isothem,平衡步数(equilibration steps)为2000000,产出 步数(production steps)为1000000,力场为COMPASS,静电交互和范德华交互分别采用Ewald和Atom Based方法,溶质为CH4,控制压力为0~20MPa,模拟温度分别为20~80℃,采用Metrolis算法计算CH4分子在原油体系中的溶解量。
2 实验结果与讨论
2.1 CH4在含蜡原油中的溶解规律及降黏效果
通过试验测试了不同溶气压力条件下CH4在胜利原油(20~50℃)和南阳原油(30~60℃)中的溶解度,由于试验器材的承压限制,只测试了0~2MPa条件下的CH4饱和溶解度。
图2为胜利原油和南阳原油的饱和溶解度曲线,表2为不同溶气压力条件下原油平均降黏率(30℃)。由图2、表2可知,在试验压力范围内,CH4在两种原油中的溶解度均随温度升高而下降,随溶气压力增加而增大,且随着溶气压力的增加,溶气原油的平均降黏率逐渐增大,降黏效果较好,这与前人[23]研究规律一致。值得注意的是,蜡、胶质和沥青质的总体含量(53.2%)较高的南阳原油中CH4饱和溶解度低于含量(42.65%)较低的胜利原油。下文将借助分子模拟手段,探索不同组分体系中CH4的溶解规律。

图2 原油饱和溶解度曲线
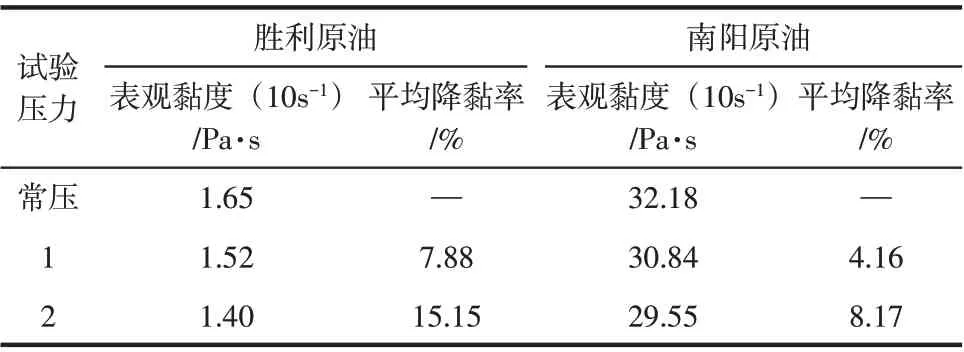
表2 不同溶气压力条件下原油平均降黏率(30℃)
2.2 CH4在原油体系中溶解的分子动力学模拟
2.2.1 原油组分模型体系构建及评价
含蜡原油的主要成分为烷烃、环烷烃、芳香烃、胶质和沥青质等,鉴于原油化学组成、结构的复杂性,建立与原油组成和性质完全对应的模拟体系几乎不可能。目前,实验室含蜡模拟油主要通过基础油、切片石蜡、胶质、沥青质混合配制而成[24],借鉴实验室含蜡模拟油配置方法,选取实验室所用的基础油正庚烷(C7H16)作为溶剂油,其20℃密度为0.684g/cm3;根据实验室切片石蜡的碳数平均值选取正构C24H50模拟蜡分子,20℃密度为0.798g/cm3;胶质是原油中分子量相对较重的组分,通常为长支链稠环化合物或极性芳香环稠环化合物,但胶质中芳香环的个数均小于7个[25],20℃密度在1.070g/cm3左右,胶质平均分子模型选用Modified R-benzo-thio-S分子模型[26];沥青质是原油中密度和分子量最大的组分,均高于胶质,但两者化学结构相似,20℃密度在1.150g/cm3左右,沥青质平均分子模型选用At-N+2S+O分子模型[27]。选取的原油各组成分子模型如图3所示。
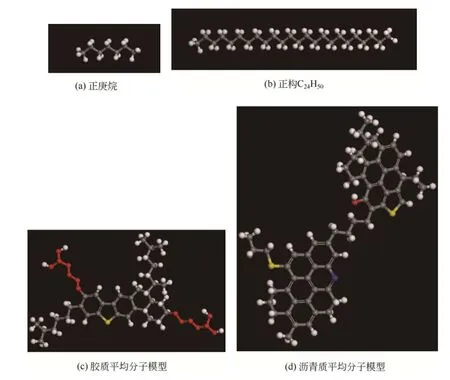
图3 原油组分分子模型
根据文中选用的正庚烷、正构C24H50、胶质、沥青质平均分子模型,利用Materials Studio中Visualize模块分别建立相应的分子模型,并对每一个分子模型进行几何优化以及能量最小优化得到原油分子模型的最优化结构构型,同时构建CH4分子模型。
本文以导致原油高黏、高凝特性的蜡、胶质、沥青质含量为影响因素,配制具有单一或混合组分的原油体系,其中基础油为正庚烷,体系内正庚烷分子个数均为100个。其中蜡分子为影响因素1、胶质为影响因素2、沥青质为影响因素3,不同影响因素的混合比例(物质的量分数)均取4个水平,依次为:0(分子个数为0个)、4.8%(分子个数为5个)、10%(分子个数为11个)、20%(分子个数为25个)。如表3所示,按照L16(43)正交表构建相应的原油体系,并根据表1中胜利原油和南阳原油蜡、胶质、沥青质的质量分数换算为相应的物质的量分数,构建胜利原油和南阳原油两种特定比例的原油体系,共18种原油体系。利用Geometry Optimization模块和Anneal模块对18种原油体系进行结构优化和退火优化,如图4所示,其中灰色为正庚烷、红色为蜡分子、蓝色为胶质、绿色为沥青质。

图4 原油体系

表3 原油体系
密度是原油基础物性之一,是评价所建立原油体系合理性的重要依据。利用Forcite模块中Dynamics对原油体系进行密度计算,通过对比模拟密度值与试验参考密度值,验证所构建原油体系的合理性。动力学模拟参数为:NPT系综,CPMPASS力场,温度为20℃,压力为10-4GPa,静电交互和范德华交互分别采用Ewald和Atom Based方法,截至距离1.25nm,Anderson法控温,Berendsen法控压,步长为1fs,进行100ps(100000步)动力学模拟,每500步输出一次运行结果。
利用分子动力学模拟计算常压20℃条件下原油体系密度,如图5所示。由图可知,原油体系的密度随模拟时间逐渐趋于平衡(标准差小于0.001)。分子动力学模拟计算的时间为100ps,其中前40ps用于平衡原油体系,后60ps用于模拟密度数据采集,对40~100ps时间范围内原油体系密度求平均值,并与试验密度值进行对比,如表4所示。
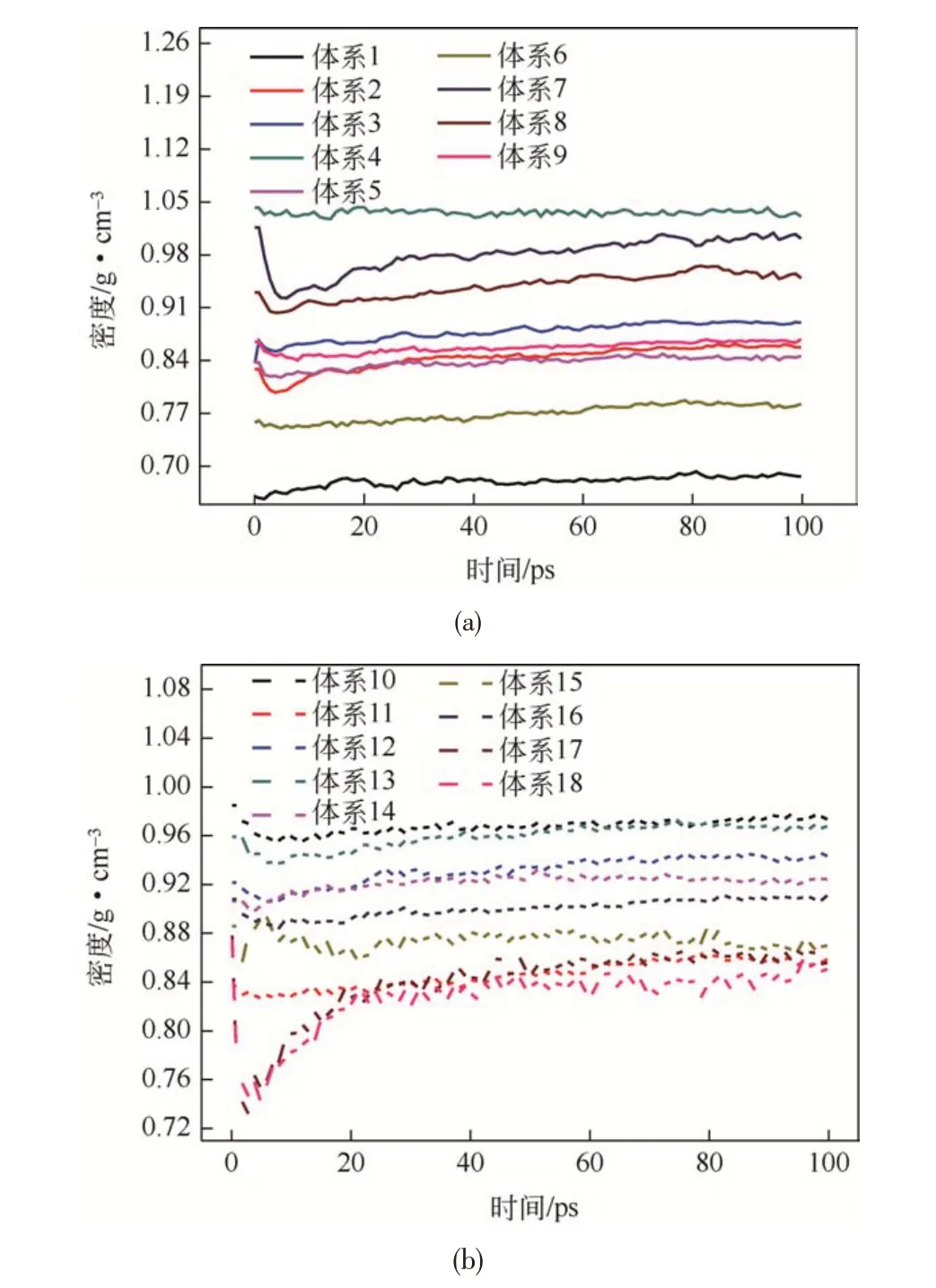
图5 原油体系密度随模拟时间变化关系
根据表4可知,分子动力学模拟计算的原油体系密度值接近试验密度值,相对误差均小于5.14%。组分越重、重质组分含量越多,密度越大。上述分析结果表明所建立的原油体系以及模拟流程的准确性。
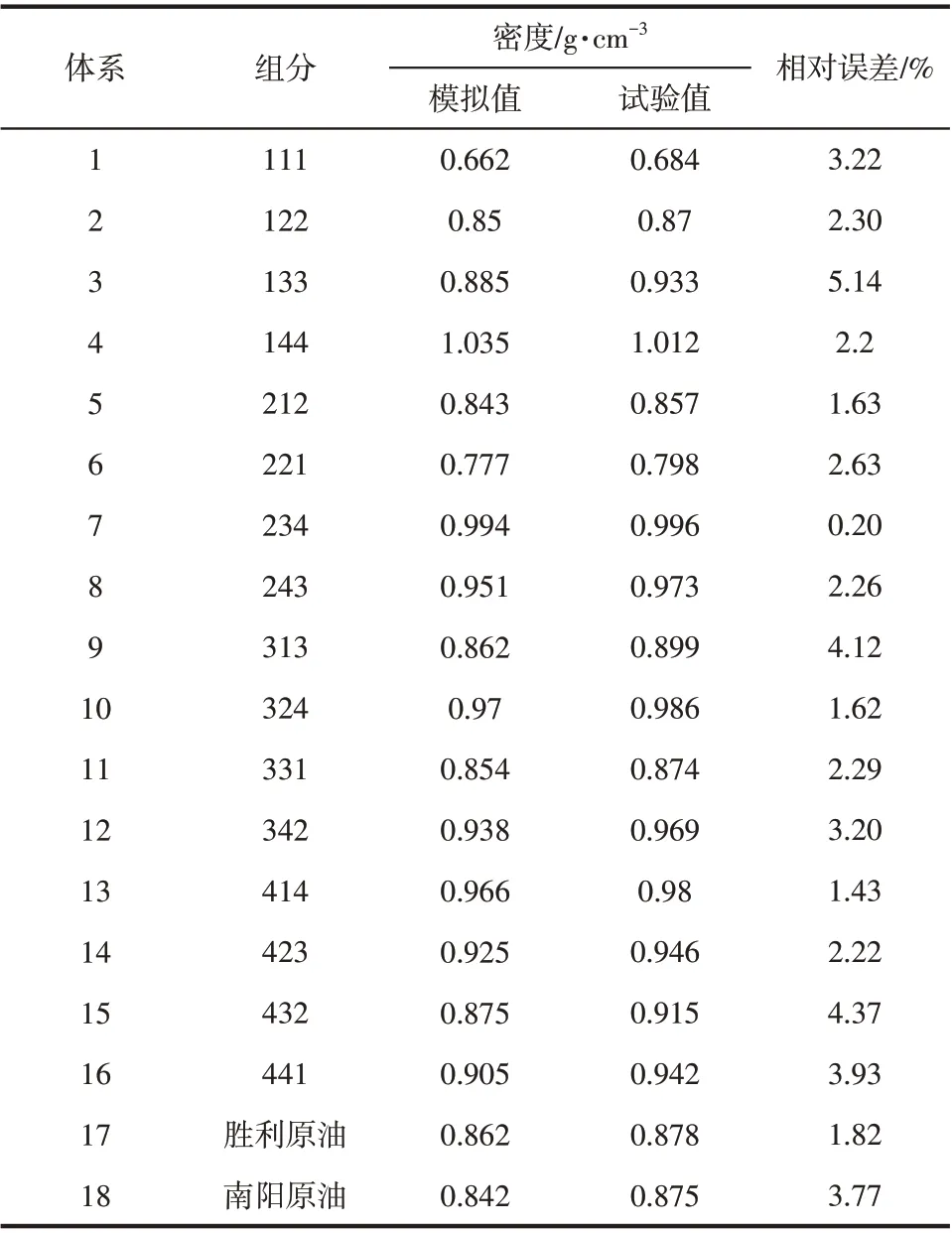
表4 模拟密度与试验参考密度对比
为了验证Sorption模块模拟方法的准确性,模拟计算25℃不同压力条件下CH4在正庚烷体系中的溶解度,并与文献[28]中的溶解度试验值进行对比,如表5所示。同时对比了40℃条件下试验溶解度和模拟计算溶解度,如表5所示。由表可知,正庚烷体系分子动力学模拟计算溶解度值接近试验溶解度值,且相对误差均小于7.246%,而胜利原油和南阳原油溶解度试验值与计算值相对误差平均值分别为9.129%和13.973%,且溶解度变化趋势类似,因此可以利用分子动力学方法模拟CH4在原油体系中的溶解过程。
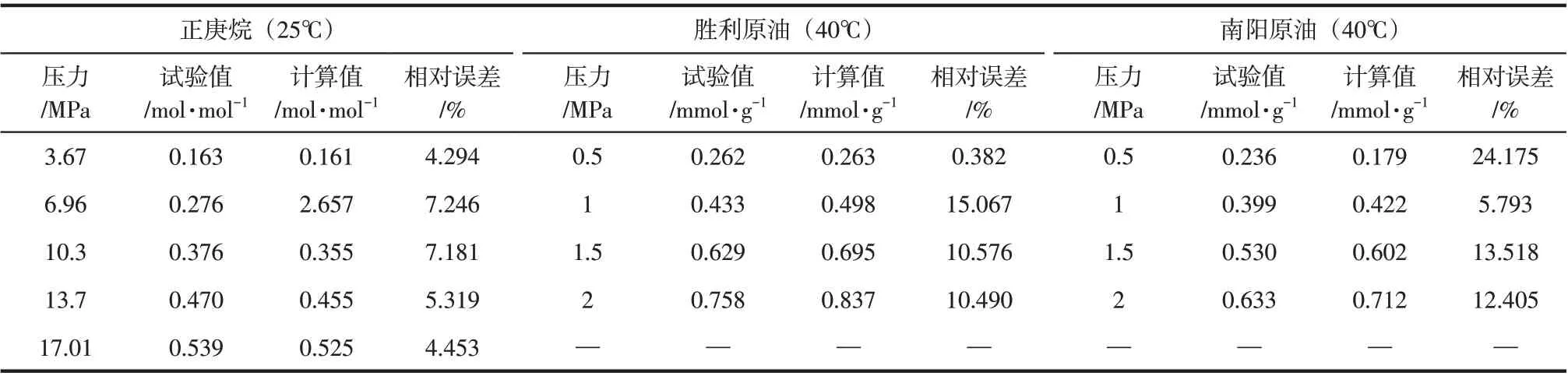
表5 模拟溶解度值与试验值对比
2.2.2 CH4溶解过程的分子动力学模拟
利用分子动力学模拟方法的优势在于能够观察CH4在原油体系中的微观溶解过程,定性地分析CH4分子在不同原油体系中的溶解位置和溶解量,有助于更好地认识CH4溶解机制。图6为16MPa压力条件下CH4在胜利原油体系和南阳原油体系中溶解的构型图,为了观察清晰,删除了氢原子,蓝色区域为体系的自由体积空隙,蓝色区域越大,自由体积越大。图7为温度20℃时不同压力条件下CH4在原油体系中溶解的构型图,由于CH4在不同原油体系中的溶解过程类似,因此以胜利原油体系和南阳原油体系为例,图中黄色球状为CH4分子、链状为原油分子。
由图6可知,不同分子组成的原油体系中存在较多的空隙,溶解的气体主要集中在这些空隙中。Everett等[29]通过计算狭缝孔中吸附原子的势能分布发现,随着空隙直径的减小,固体表面与吸附质分子相互作用势增大,CH4在原油体系中溶解,必须克服空隙壁产生的势垒。当溶气压力较小时,原油分子会吸引CH4,使其溶解到原油体系空隙的高能吸附位,CH4溶解位置多为空隙较大的地方;随着溶气压力的增大,CH4能够克服更高的势垒进入空隙较小的地方,即随着溶气压力的增加,CH4溶解量逐渐增多。如图7所示,随着溶气压力的增大,CH4溶解量逐渐增大,但溶解的位置可能发生变化,这是由于溶解的CH4分子仍处于振动状态,CH4分子的振动有可能摆脱碳原子的引力作用重新成为自由气体;当溶气压力较低时,CH4分子较为分散地分布在原油体系中;随着溶气压力的增加,CH4的溶解量逐渐增多,部分溶解的CH4分子会发生聚集,如图6所示。
2.2.3 温度、压力对CH4溶解量的影响
分子动力学模拟计算CH4的溶解量单位为N/uc,即CH4溶解的个数,N/uc,而试验上常用的单位为mmol/g,因此利用式(6)进行气体溶解量的单位转换[30]。

式中,n为气体溶解量,mmol/g;Nam为气体溶解的分子个数;N为阿伏伽德罗常数;M为原油体系质量,g。其中,M=ρV,ρ为体系密度,g/cm3;V为原油体系体积,Å3(1Å=10-10m)。表6为20℃条件下原油体系体积。
图8为不同温度、压力条件下CH4分子在原油体系中的溶解量。由图可知,在试验压力范围内,对于纯正庚烷(体系1),随着CH4溶解压力的增加,CH4在正庚烷中的溶解量基本呈现线性增加,服从Henry定律;对于体系2~体系18,随着CH4溶解压力的增加,CH4在原油体系(体系2~体系18)中的溶解量先增大后逐渐趋于平衡。这是由于原油体系中蜡、胶质、沥青质的存在占据了部分空隙,使得CH4溶解的有效空隙减小(如表6),当空隙填充满时,CH4溶解量逐渐趋于平衡。
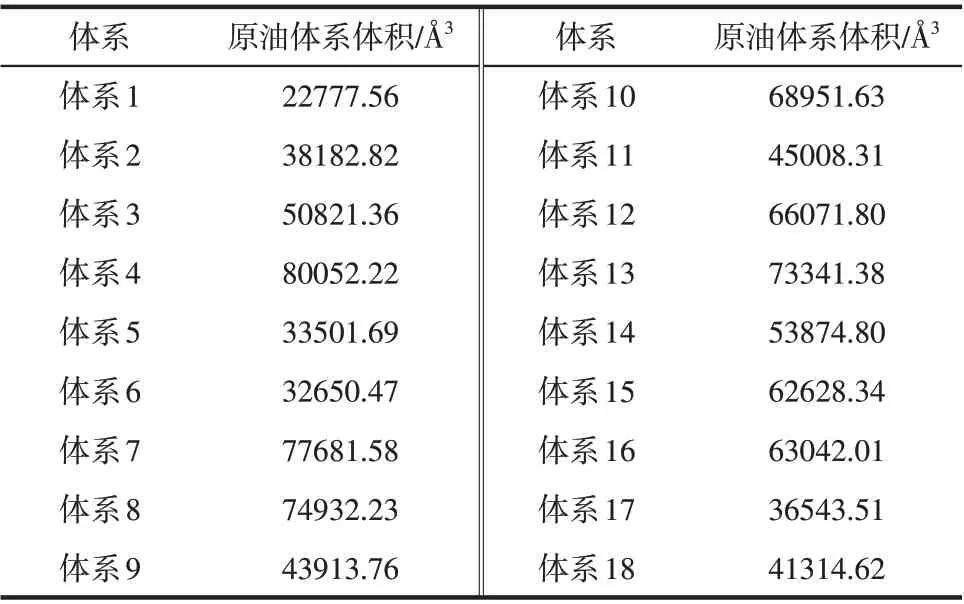
表6 原油体系体积
在试验溶气压力范围内,原油体系中蜡、胶质、沥青质的存在,使得CH4在原油体系(体系2~体系18)中的溶解行为存在一个极限值,即泡点压力,当压力小于泡点时,CH4在原油体系中的溶解量随压力的增加逐渐增大;当压力大于泡点压力时,CH4溶解量基本没有明显变化。如图7所示,CH4的溶解符合孔填充机制[31-32],随着溶气压力的增加,CH4在原油体系中不断填充,直至体系空隙填充满为止。由图8可以看出,相同温度、压力条件下,CH4分子在不同原油体系中的溶解量顺序大小依次为:体系1>体系6>体系17>体系5>体系2>体系11>体系18>体系9>体系15>体系3>体系16>体系14>体系12>体系8>体系13>体系10>体系7>体系4,CH4在原油体系中的溶解难易程度排序同上;通过对比相同压力条件下CH4分子在不同原油体系中的溶解量,发现由于温度升高增大了分子的布朗运动,使得CH4容易摆脱原油分子的吸附势垒,CH4溶解量减小,即低温有利于CH4的溶解。

图7 不同压力条件下CH4在原油体系中溶解过程的构型图
由图8可知,CH4分子在不同原油体系(体系2~体系18)中的溶解曲线符合Langmuir吸附特征。因此利用Langmuir方程进行拟合,其关系式见式(7),拟合参数如表7所示。

图8 不同温度、压力条件下CH4分子在原油体系中的溶解量曲线
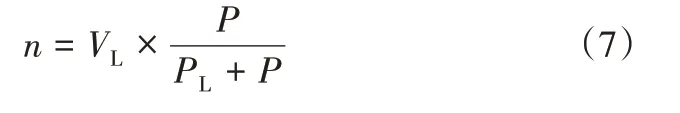
式中,n为CH4在不同原油体系中的溶解量,mmol/g;P为平衡压力,MPa;VL为Langmuir体积,mmol/g;PL为Langmuir压力,MPa。其中,Langmuir体积VL是衡量原油体系吸附溶解能力的参数,其值反映原油体系最大吸附溶解能力;Langmuir压力PL为溶解量达到0.5VL时的压力值,Langmuir压力PL越小,气体越容易溶解。
根据表7中VL、PL与温度的关系,以偶数体系为例作图9。由图9可知,随着温度的升高,Langmuir体积VL基本呈现线性减小规律,即原油体系最大吸附溶解能力随温度的升高而降低。随着温度升高,Langmuir压力PL基本呈现线性增大规律,温度越低,Langmuir压力PL越小,气体越容易溶解。

图9 VL、PL随温度变化关系

表7 不同温度下Langmuir方程拟合参数
通过正交表分析蜡、胶质、沥青质含量对CH4溶解量影响程度的大小,如表8所示。由极差R大小可知,因素主次为:沥青质>胶质>蜡,原油大分子的存在影响CH4溶解量。这是由于蜡分子为直链烷烃,而胶质、沥青质分子中存在较多的芳香环大分子,链状烷烃易发生弯曲缠绕,形成的空隙孔径大于芳香环形成的空隙。此外,链状烷烃对甲烷的作用力比芳香环的作用力大,因此原油分子体中沥青质的存在对CH4的溶解量影响程度最大。
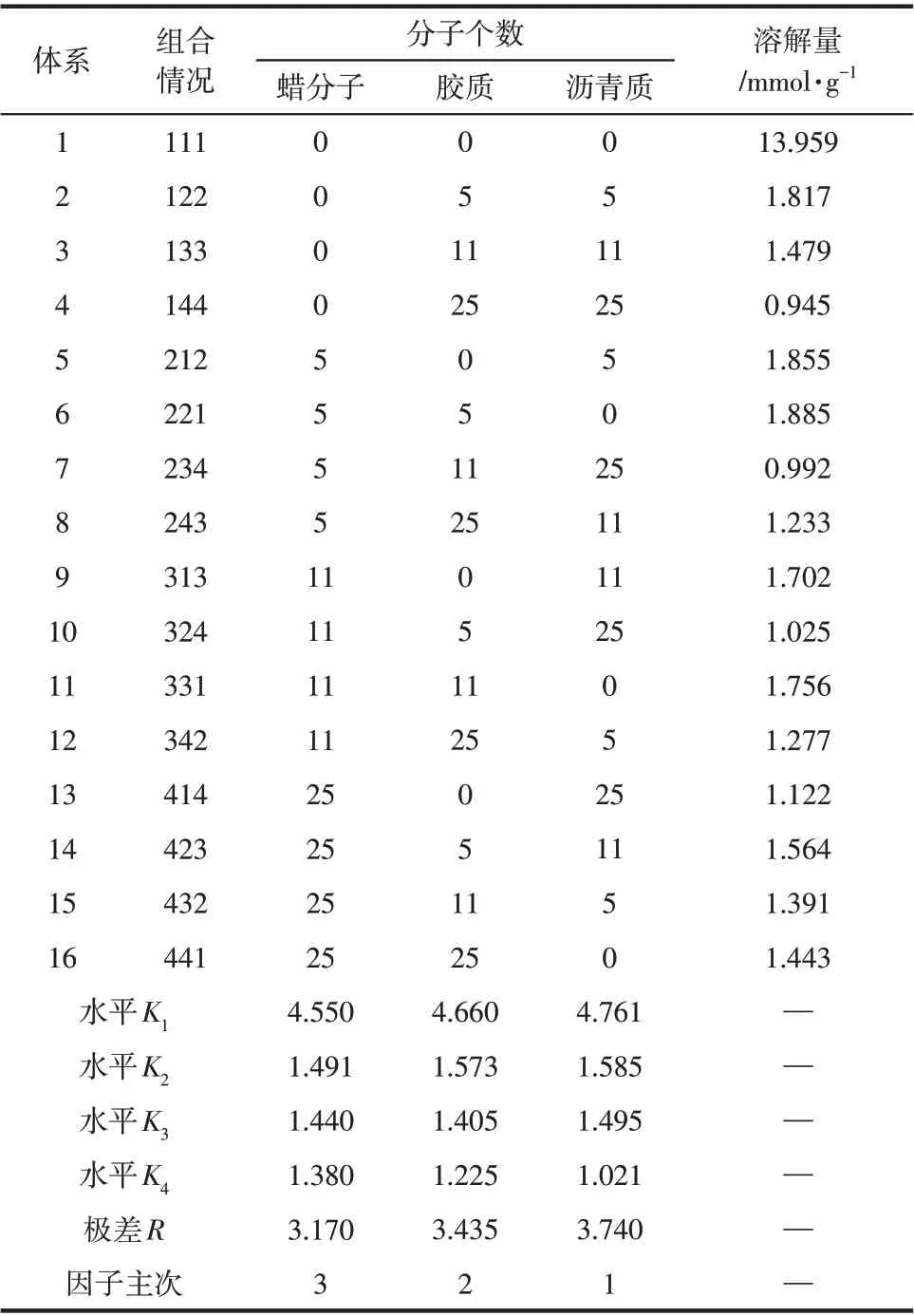
表8 正交实验方案
为了描述不同原油体系溶解CH4的能力,定义碳占比(C)=原油体系内碳原子个数/原油体系内分子个数。不同原油体系的碳占比如表9所示。20℃条件下,碳占比与VL的关系如图10所示。VL与体系碳占比基本呈现线性减小规律,即原油大分子(蜡、胶质、沥青质)的含量越多,CH4最大溶解量越小。
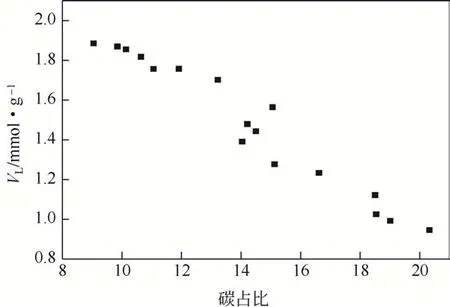
图10 碳占比与VL的变化关系

表9 不同原油体系的碳占比
2.2.4 CH4溶解的分子动力学机制
结合CH4在原油体系中的溶解特点,从原油体系的等量吸附热、原油体系的自由体积和相互作用能三个方面开展CH4溶解的作用机制研究。
(1)原油体系的等量吸附热 原油体系的等量吸附热是区分物理和化学吸附的一个重要热力学参数,是判断CH4溶解行为为化学溶解还是物理溶解的依据,同时能够评价原油体系的溶解能力。吸附热小于42kJ/mol时为物理吸附,吸附热大于42kJ/mol时为化学吸附[33-34]。
利用Clausius-Clapeyron等量吸附热方程[33-34]计算原油体系的等量吸附热,如表10所示,不同原油体系的等量吸附热均小于42kJ/mol。因此CH4在原油体系中的溶解为物理溶解过程。随着原油体系碳占比的增大,等量吸附热逐渐减小,不同原油体系对CH4等量吸附热顺序大小依次为:体系1>体系6>体系17>体系5>体系2>体系11>体系18>体系9>体系15>体系3>体系16>体系14>体系12>体系8>体系13>体系10>体系7>体系4,CH4在原油体系中的溶解难易程度排序同上,这与前文通过溶解量对比所得的溶解难易程度顺序一致。

表10 20℃、0~20MPa条件下原油体系的等量吸附热
图11为原油体系等量吸附热与CH4溶解量的关系曲线,对于纯正庚烷体系(体系1),等量吸附热随着CH4溶解量的增大呈线性增加,而体系2~体系18的等量吸附热随着CH4溶解量的增大先减小后增大,说明原油体系(体系2~体系18)的非均质性,原油大分子的存在使得正庚烷由均质性转化为非均质性。在CH4溶解初始阶段,CH4首先被吸附到能量较高的吸附位,随着溶解量的增多,CH4逐渐吸附在能量较低的吸附位,CH4分子和原油分子间的作用对吸附热起主要贡献,此过程原油体系的等量吸附热逐渐减小;随着溶气压力的继续增大,CH4溶解量逐渐增大,CH4分子间的作用增大,使得原油体系的等量吸附热增大,原油体系的等量吸附热变化趋势是这两个过程的叠加效果。
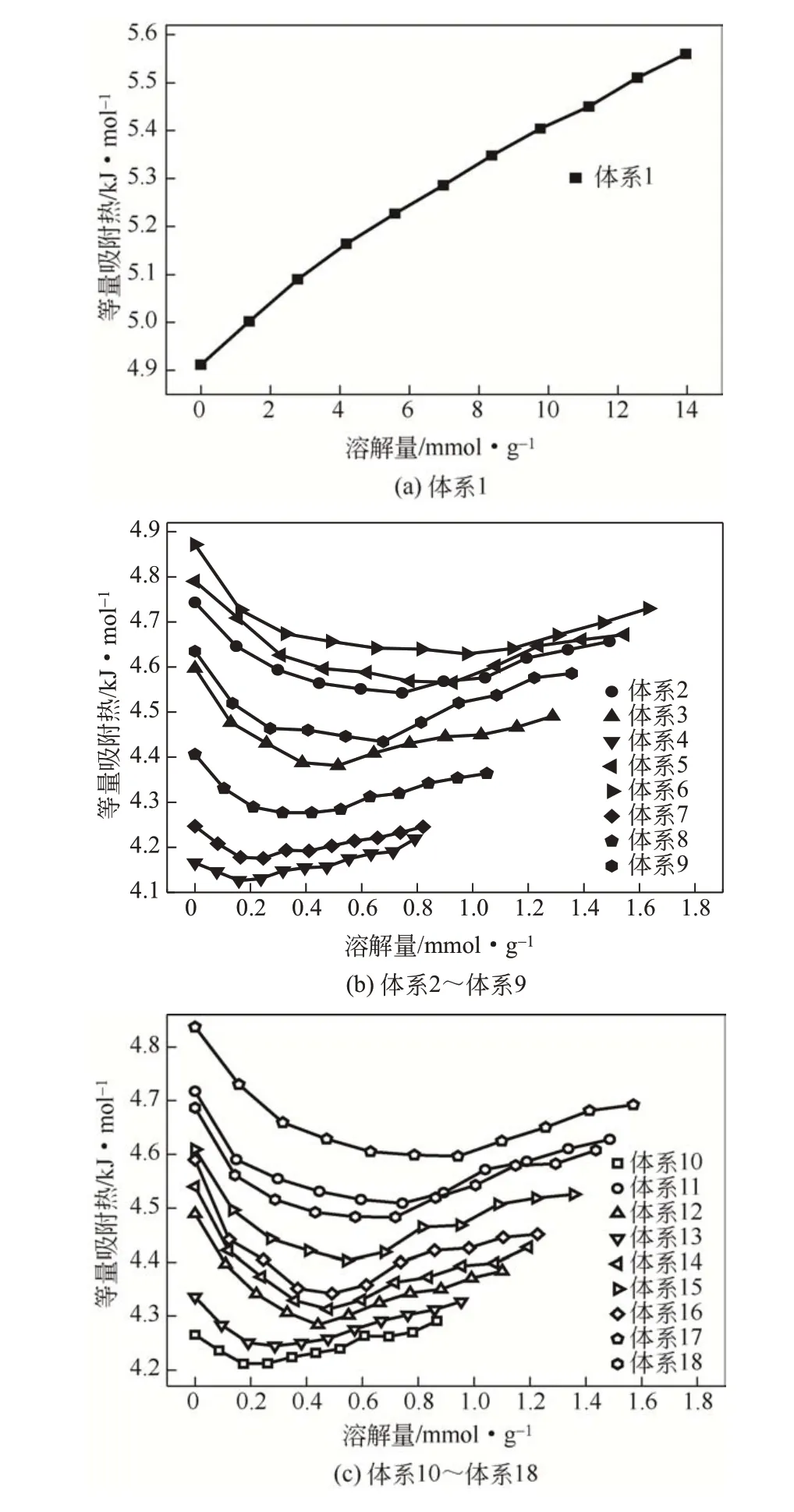
图11 原油体系的等量吸附热
(2)原油体系的自由体积 Fox和Flory[35]首次提出自由体积理论,认为聚合物由液体分子占有的体积V0和未被占有的或自由的体积Vf构成,自由体积分数f定义为自由体积与总体积的比值,可由式(8)计算。自由体积的拓扑形态与孔隙结构对气体的吸附溶解起着重要的作用[36]。不同于宏观自由体积及表面积计算方法,分子动力学方法采用吸附溶解分子作为探针探测材料计算自由体积及表面积,不同直径吸附质溶解分子对应着不同的自由体积及表面积[37]。

采用直径为0.38nm的CH4分子作为探测分子,考察原油体系自由体积所占比例。图12为常压、20℃条件下,原油体系的自由体积空隙及表面积示意图,灰色区域为骨架,蓝色区域为体系的自由体积空隙。利用式(8)求得原油体系的自由体积分数,如表11所示。

图12 原油体系自由体积空穴的模拟形貌

表11 原油体系结构模型的表征参数
图13为20℃条件下不同原油体系自由体积分数与VL的关系。原油体系的自由体积分数越大,溶解气体分子的空间越大,溶解的气体量越多。这是由于自由体积为CH4的溶解提供必要的扩散空间和运动空间,CH4分子在原油体系中是不断运动的,大部分条件下CH4分子的运动振幅较小,可认为是振动,但是CH4分子偶尔会从一个空隙跳跃到另个一空隙继续进行小振幅振动,这样的空隙即为自由体积,自由体积越大,CH4扩散溶解量越多。不同原油体系自由体积分数顺序大小依次为:体系1>体系6>体系17>体系5>体系2>体系11>体系18>体系9>体系3>体系16>体系15>体系14>体系12>体系8>体系13>体系10>体系7>体系4,CH4在原油体系中的溶解难易程度排序同上,这与前文通过溶解量、等量吸附热对比所得的溶解难易程度顺序基本一致。
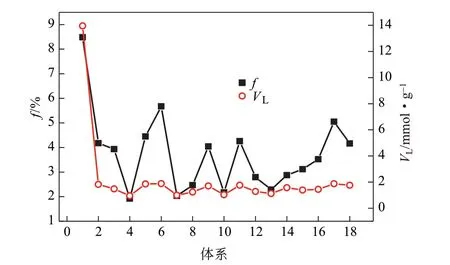
图13 原油体系自由体积分数与VL的关系
(3)相互作用能 为了明确CH4与原油分子间的相互作用,计算CH4与原油分子间的相互作用能(Einter)。分子间相互作用能反映CH4与原油分子间的结合强度,其绝对值越大,分子间相互作用越强,表达式如式(9)所示。
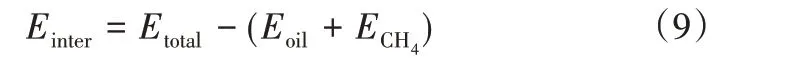
式中,Einter为气体分子与原油分子间的相互作用能,kJ/mol;Etotal为气体分子与原油体系的总能量,kJ/mol;Eoil为原油体系能量,kJ/mol;ECH4为CH4的能量,kJ/mol。相互作用能计算过程:选择一定的温度压力条件,计算CH4分子与原油体系的总能量,然后分别计算该构型下删除CH4分子的原油体系能量和删除原油分子后CH4分子的能量,利用式(9)计算CH4与原油分子间的相互作用能。
图14为20℃条件下CH4与原油分子间的相互作用能,原油分子与CH4之间的相互作用能主要有范德华作用能(EW)和静电作用能(Ee),CH4与原油分子间的静电作用能基本趋于零,说明CH4与原油分子间的库仑力作用很小,基本可以忽略不计。对于纯正庚烷体系(体系1),范德华作用能随着压力的增大而增大;而对于体系2~体系18,范德华作用能随着压力的变化呈幂函数变化趋势,且原油分子与CH4之间范德华作用能远大于静电作用能,这说明CH4在原油体系的溶解过程中范德华力作用起主要作用。随着溶气压力的增大,由于CH4溶解速度减慢,使得CH4与原油分子间相互作用能增加速度减慢,当溶气压力达到体系泡点时,随着溶气压力的增大,由于原油体系吸附CH4分子已经达到饱和,使得CH4原油分子间相互作用能不再发生变化。
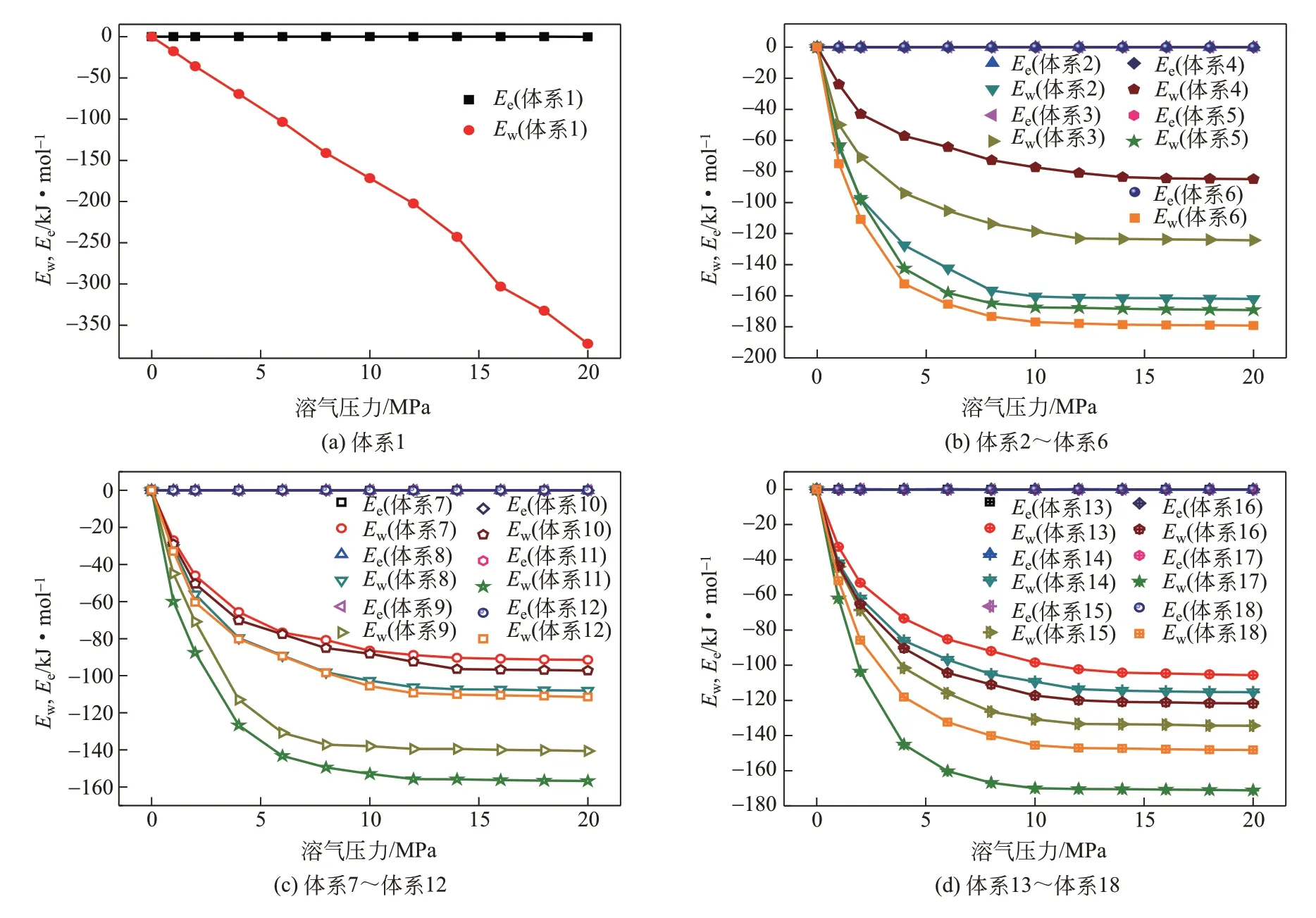
图14 CH4与原油体系间的相互作用能
通过对比相同压力条件下CH4与原油分子间的相互作用能发现,相互作用能越大,CH4的溶解量越多,且溶气压力达到泡点时,相互作用能趋于恒定值,可见CH4与原油分子间的相互作用能与溶解量具有直接关系。
原油体系中含有大量的孔隙,CH4溶解使其产生膨胀变形,降低渗透率,影响气体的运移,因此有必要对原油体系由于CH4溶解产生的形变进行研究。参数ε用于描述原油体系体积变化情况。针对材料体积应变的研究,Coussy[38]建立模型研究了游离态流体对孔隙介质体积变形的影响,但模型未考虑吸附引起的体积变形;Brochard等[39]在Coussy模型的基础上进行改进,考虑吸附对多孔介质体积的影响,得到体积应变表达式,见式(10)。

式中,ε为体积应变,%;p为原油体系压力,MPa;K0为原油体系体积模量,MPa;CCH4为气体耦合常数,CCH4=6.05[40];uCH4为气体的化学势;n为气体溶解量,mmol/cm3。由于dui=RTd lnfi,i=CH4,其中fi为气体的逸度。因此有式(11)。
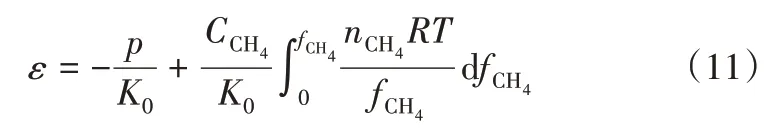
利用式(11)计算得到的原油体系体积应变结果如图15所示。对于体系1,随着溶气压力的增加,原油体系体积逐渐增大,相互作用能逐渐减小;对于体系2~体系18,随着溶气压力的增大,原油体系体积应变先逐渐增大,CH4与原油分子间的相互作用能逐渐减小,当溶气压力达到泡点时,原油体系体积应变达到最大,CH4与原油分子间的相互作用能达到最小,随着溶气压力的进一步增加,原油体系体积应变逐渐减小,CH4与原油分子间的相互作用能基本趋于平衡。

图15 相互作用能、体积应变随压力变化关系
在溶气压力达到泡点压力之前,Einter和ε存在一定的对应关系,当溶气压力达到泡点压力后,随着溶气压力的增加,相互作用能基本不变,体系体积应变逐渐减小。为了阐明在溶气压力达到泡点压力之前Einter和ε的对应关系,通过评价PΩP功进行描述,其中P为体系压力,ΩP为体积膨胀系数。Zhou等[41]认为体系压力决定体系体积的变化,且体系压力与体积变化之间的关系为式(12)。
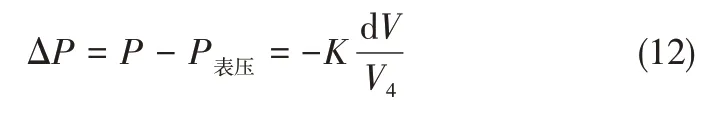
式中,K为溶气原油体系体积模量,其中原油体系的体积模量由Materials Studio软件计算。
相互作用能的计算见式(13)。
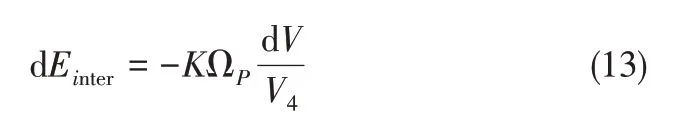
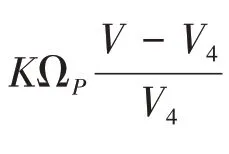

式中,V4为常压条件下原油体系体积,Å3;Einter0为常压条件下气体分子与原油分子间的相互作用能,kJ/mol。
如图16所示,基于方程(14)的拟合曲线基本与相互作用能变化情况相吻合,拟合参数如表12所示,其中Einter0为2.356kJ/mol,这种良好的一致性解释了Einter和ε之间对应的线性关系。
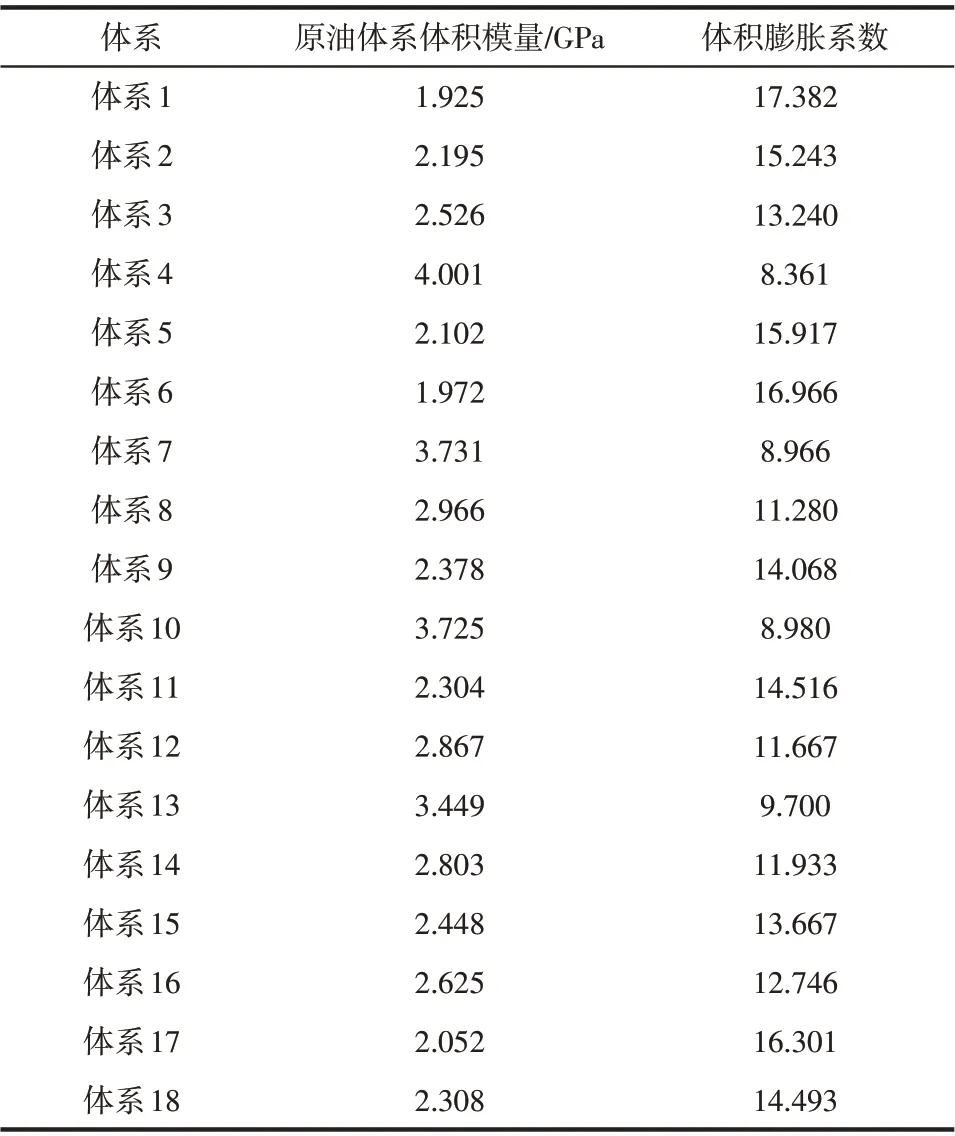
表12 原油体系的体积模量、体积膨胀系数值
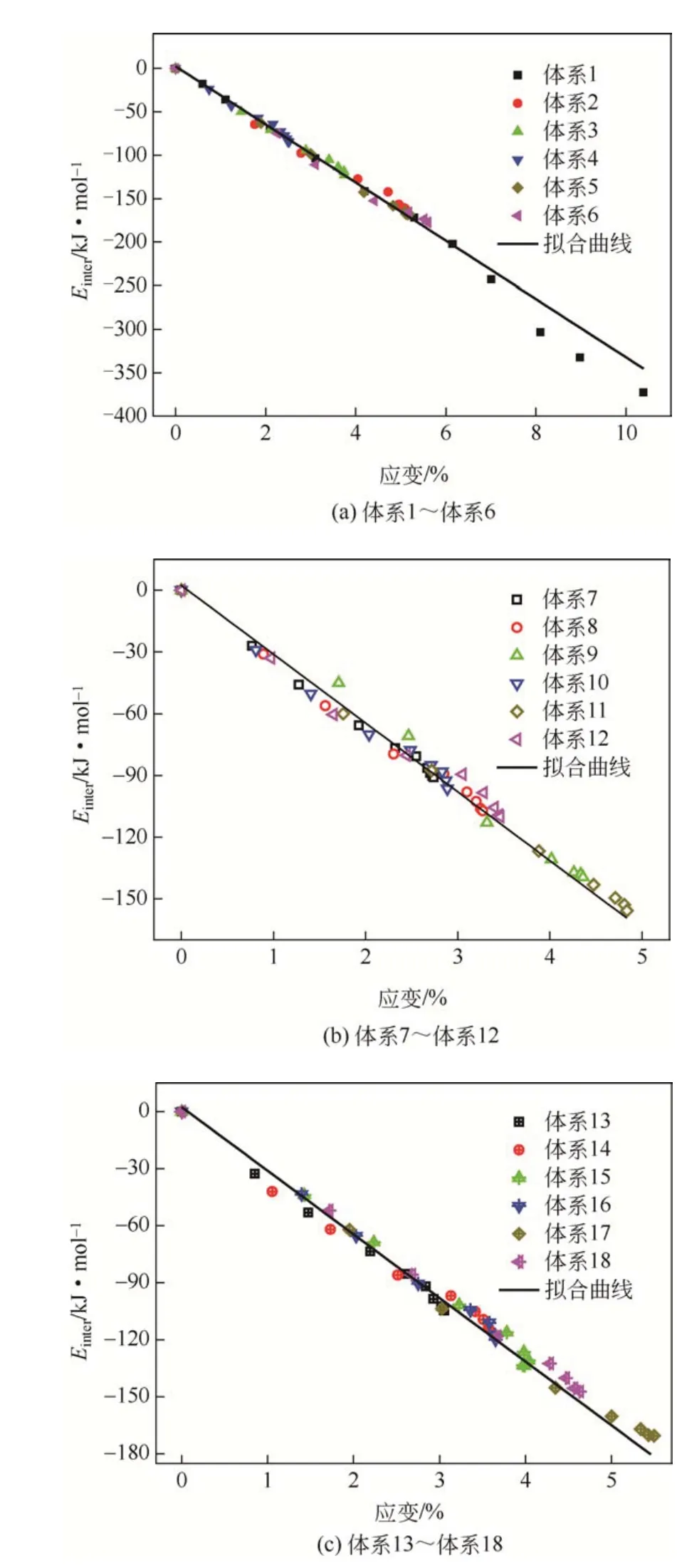
图16 相互作用能与体积应变的关系及拟合曲线
3 结论
(1)在试验压力范围内,随着溶气压力的增加,CH4在两种原油中的饱和溶解度均逐渐增大;随着温度的升高,CH4在两种原油中的饱和溶解度均逐渐减小。
(2)在泡点压力范围内,随着溶气压力的增加,CH4溶解量逐渐增大,其溶解的位置可能发生变化;当溶气压力较低时,CH4分子较为分散地分布在原油体系中;随着溶气压力的增加,CH4的溶解量逐渐增多,部分溶解的CH4分子会发生聚集;随着溶气压力的增加,原油大分子对CH4溶解量的影响程度逐渐增大,但未改变CH4溶解的力学作用方式,其中原油大分子对CH4溶解量的影响程度依次为:蜡<胶质<沥青质。
(3)通过原油体系等量吸附热、自由体积空隙和分子间的范德华作用分析CH4溶解机理,发现CH4在原油体系中的溶解为物理溶解过程,原油自由体积分数越大,能够为CH4提供的溶解空间越大,且CH4溶解过程中范德华作用为主要的力学作用方式,并通过力学公式揭示了相互作用能与原油体系体积变化量的线性关系,促进对CH4在原油体系中溶解的分子级理解,为含蜡原油溶气改性技术提供理论依据。
符号说明
——气体耦合常数,=6.05
Einter,Etotal,
EOil,,Einter0——气体分子与原油分子间的相互作用能、气体分子与原油体系总能量、原油体系能量、CH4的能量、常压条件下气体分子与原油分子间的相互作用能,kJ/mol
fi——气体的逸度,Pa
f——自由体积分数,%
K0,K——原油体系体积模量、溶气原油体系体积模量,GPa
M——原油体系质量,g
N——阿伏伽德罗常数
n——气体溶解量,mmol/g
P,P1,P2——平衡压力、脱气原油压力、溶气原油压力,MPa
PL——Langmuir压力,MPa
p——原油体系压力,MPa
Rs——气体溶解度,m3/m3
T1,T2——溶气原油温度、脱气原油温度,℃
——气体的化学势
V,V4,Vf——原油体系体积、常压条件下原油体系体积、自由的体积,Å3
V0,V1,Vx,V2——装置及管线的总体积、饱和溶气原油的体积、气体体积、脱气原油体积,mL
VL——Langmuir体积,mmol/g
ρ——原油体系密度,g/cm3
ε——体积应变,%
ΩP——体积膨胀系数

