HTPB/Cu/μAl 的制备及其对AP 热分解性能的影响
李廷润,郭春雨,包淑霞,赵洋洋,杜振国,吴瑞凤
(内蒙古工业大学化工学院,内蒙古 呼和浩特 010050)
1 引言
随着科学技术的不断发展,各种战术武器和航天飞机越来越先进,国防和航天科学技术领域对推进剂的能量性能要求越来越高[1-2]。其中提高固体推进剂性能的关键技术在于如何同时提高其能量利用率和燃烧速率[1],铝粉的加入为解决这一难题提供了新的思路。铝粉作为一种金属燃料,具有能量密度高、氧化性能好等特点,被广泛应用于涂料、火炸药、火箭推进剂等领域[2-3]。但铝粉较活泼,易和氧原子结合,生成一层氧化铝薄膜覆盖在铝粉表面,影响能量释放效果[4]。因此,如何防止铝粉表面发生氧化导致其活性含量下降成为了当今国内外的学者研究的重点。
铜由于具有良好的催化和反应活性,在固体推进剂中起着调节弹道性能和提高推进剂燃烧性能的作用[5]。有研究表明,加入少量铜粉,可以保证推进剂组分在多种阻力下继续稳定燃烧[6]。程志鹏[7]等人在以明胶为保护剂、氟离子为络合剂的水溶液中,采用Al直接置换还原铜盐的方法,制备出核壳结构的Cu/Al复合粉末。姚冰洁[8]等人用电爆炸铝粉和二水合氯化铜为原材料,以聚乙二醇400 为表面活性剂,以乙二胺四乙酸二钠和酒石酸钾钠为络合剂,同样采用置换反应法成功制备Cu/Al 复合材料。而汪靖凯[9]等人以柠檬酸钠和β-糊精为稳定剂、以抗坏血酸为还原剂,采用化学还原法制备Cu/Al 复合纳米粒子。这些方法虽然成功制备了Cu/Al 复合粒子,但制备过程中引入各种非推进剂组分,不利于推进剂组分的稳定燃烧。
端羟基聚丁二烯(HTPB)因价格低廉,综合性能好,常作为高聚物黏合剂用于复合推进剂中[10]。雷瑞琛[11]等人采用HTPB 通过悬浮法和溶剂蒸发法包覆RDX,研究了HTPB 的含量及工艺条件对包覆效果的影响。结果表明,悬浮法中HTPB 所占比例的增大会显著改善包覆效果,减小撞击感度;溶剂蒸发法中在HTPB 质量分数为10%和15%时,采用TDI 与HTPB一起加入会明显改善包覆效果。徐娟[12]等人采用陶瓷膜-反溶剂法制备纳米CuO/AP 复合颗粒,然后用溶剂蒸发法在其表面包覆HTPB,制得纳米CuO/AP/HTPB复合颗粒。用溶剂蒸发法将HTPB 包覆在粒子表面,不需要加入其它试剂,操作简单,所得样品包覆均匀[13]。
上述研究表明,Cu 包覆可以提高铝粉的燃烧性能,而HTPB 的包覆既可以阻止粒子的表面氧化和粒子的团聚,又有利于金属粉体的压装成型。为此采用一锅法,以甲醛和肼为还原剂制备了Cu/μAl复合物,又以推进剂黏合剂组分HTPB 为包覆剂制备了HTPB/Cu/μAl复合粒子。该方法在不加入各种稳定剂和络合剂的情况下,还原和包覆一锅完成,方法简便,可操作性强。
2 实验部分
2.1 试剂与仪器
试剂:Al 粉(μAl),1 μm,上海攀田粉体材料;乙酰丙酮铜(C10H14CuO4),天津永晟精细化工有限公司;端羟基聚丁二烯(HTPB),淄博齐龙化工有限公司;氢氧化钠(NaOH),上海实验试剂有限公司;甲醛(HCHO),中天精细化工有限公司;水合肼(N2H4·H2O),山东德享国际贸易有限公司;无水乙醇(CH3CH2OH),天津鑫铂特化工有限公司;无水乙醚(CH3OCH3),上海阿拉丁化学试剂公司。
仪器:红外测试仪器为日本岛津公司IRTracer-100 傅里叶红外光谱仪;XRD 测试仪器为日本理学(Rigaku)公司SmartLab 9KW 的X 射线衍射仪;SEM-EDS 测试仪器为荷兰Phenom 公司Phenom LE型场发射扫描电子显微镜;DSC 测试仪器为北京恒久科学仪器厂HSC-1 型热流式差示扫描量热仪。
2.2 Cu/μAl 复合粒子的制备
称取2.045 g 乙酰丙酮铜(C10H14CuO4)于250 mL烧杯中,加入25 mL 无水乙醇溶解,40 ℃下加入3 mL甲醛溶液,配成溶液A 放置备用;在另一个250 mL 烧杯中加入1 gμAl 粉,40 ℃下加入用无水乙醇溶解的NaOH 调节溶液的pH 至10,配成溶液B;将上述备用溶液A 用滴液漏斗滴入溶液B 中,15 min 滴加完毕。加入1 mL 水合肼进行二次还原。2 h 后用无水乙醇将样品反复离心洗涤,置于60 ℃烘箱中干燥2 h,得到粉末状复合材料Cu/μAl。制备流程见图1。
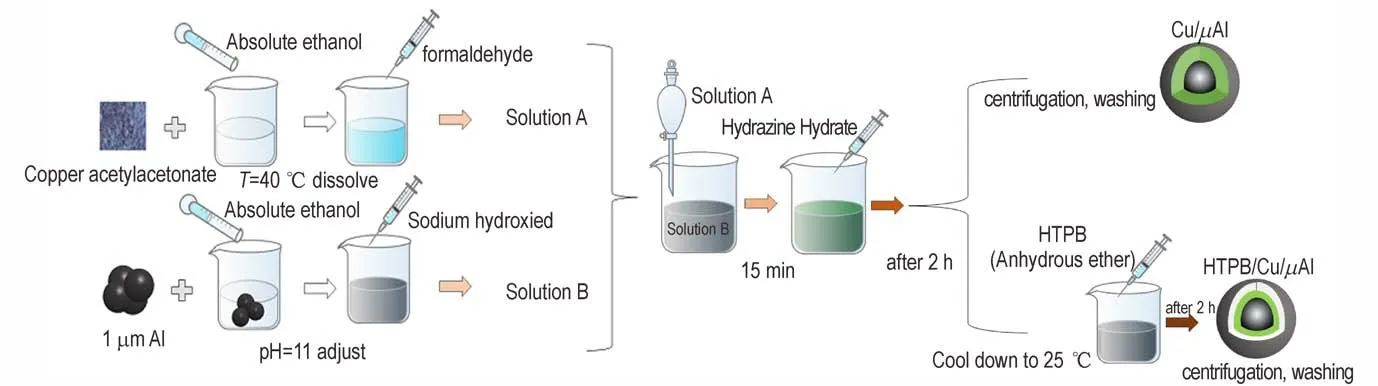
图1 Cu/μAl 和HTPB/Cu/μAl 复合粒子制备流程图Fig.1 Flow chart of preparation of Cu/μAl and HTPB/Cu/μAl composite particles
2.3 HTPB/Cu/μAl 复合粒子的制备
在上述反应进行2 h 后,将体系温度降至25 ℃,加入0.15 g 无水乙醚溶解的HTPB,持续搅拌反应。2 h 后用无水乙醇将样品反复离心洗涤,置于60 ℃烘箱中干燥2 h,得到双包覆复合材料HTPB/Cu/μAl 粉末。制备流程见图1。
2.4 对AP 热分解的影响
采用文献方法[14],将所得样品与AP 按1∶10 的比例置于玛瑙研钵中搅拌研磨,加入适量的无水乙醇混合均匀,使复合粉末充分接触,置于60 ℃烘箱中干燥2 h,得到μAl/AP、Cu/μAl/AP 和HTPB/Cu/μAl/AP 复合粉末。采用DSC 法探究所得样品对AP 热分解性能的影响。
3 结果与讨论
3.1 红外表征(FT-IR)
为研究HTPB 的包覆情况,对HTPB/Cu/μAl 的FT-IR 光谱进行了分析,如图2 所示。2845 cm-1和2915 cm-1分别对应了HTPB 中—CH2的C—H 键对称伸缩振动峰和反对称伸缩振动峰;1638 cm-1对应了HTPB 中—C=C—键的伸缩振动峰;1435 cm-1和3445 cm-1分别为HTPB 中—OH 的弯曲振动吸收峰和伸缩振动吸收峰;970 cm-1为—OH 的摇摆振动吸收峰。与Cu/μAl 相比,HTPB/Cu/μAl 中位于970 cm-1的—OH 摇摆振动吸收峰消失不见,推测认为HTPB 中的羟基与铝基金属发生反应。在767 cm-1和618 cm-1处出现两个新峰,分别推测为Al—O 和Cu—O 键。在1579 cm-1附近仍有明显的—C=C—键的特征吸收峰,说明包覆未改变HTPB 的骨架结构。因此,通过对比可初步证明HTPB 包覆到Cu/μAl 复合粒子的表面。
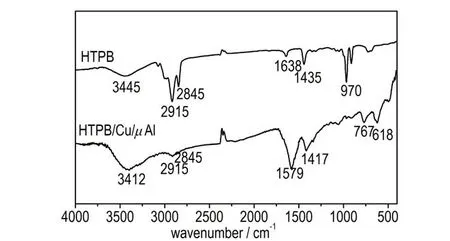
图2 HTPB 和HTPB/Cu/μAl 的FT-IR 谱图Fig.2 FT-IR spectra of HTPB and HTPB/Cu/μAl
3.2 X 射线衍射分析(XRD)
HTPB/Cu/μAl 和Cu/μAl 的XRD 图谱如图3 所示。从图3 中可以看出,在2θ=38.47°、44.74°、65.13°、78.28°、82.44°等归属于金属铝的衍射峰,这些衍射峰对应于面心立方(fcc)结构金属铝的(111)、(200)、(220)、(311)和(222)晶面的衍射,与标准相卡片(PDF#04-0787)相一致,说明复合材料中含有晶体物质铝。在2θ=43.30°、50.43°、74.13°等处归属于金属铜的衍射峰,这些衍射峰对应于面心立方(fcc)结构金属铜的(111)、(200)和(221)晶面的衍射,与标准相卡片(PDF#04-0836)相一致,说明铜离子被还原成单质铜。
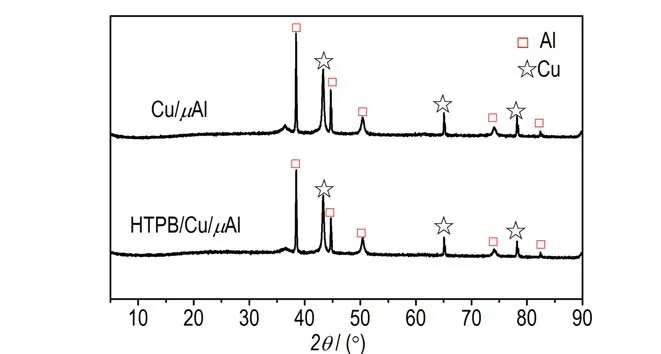
图3 Cu/μAl 和HTPB/Cu/μAl 的XRD 谱图Fig.3 XRD spectra of Cu/μAl and HTPB/Cu/μAl
3.3 扫描电子显微镜表征(SEM)
Cu/μAl 和HTPB/Cu/μAl 的SEM 照片如图4 所示。从图4a 可以看出Cu/μAl 粒子有颜色不同的物质存在,推测是还原出来的铜附着在μAl 表面,且部分颗粒间发生团聚。图4a 与图4b 对比可得,Cu/μAl 的外表面颜色较深,HTPB/Cu/μAl 的外表面颜色较浅,推测HTPB 包覆在Cu/μAl 复合粉末表面,导致颜色变浅。

图4 Cu/μAl 和HTPB/Cu/μAl 的SEM 照片Fig.4 SEM images of Cu/μAl and HTPB/Cu/μAl
3.4 能谱分析(EDS)
HTPB/Cu/μAl 复合粉末的EDS 表征结果如图5 所示。从元素分布图可以看出,单质铜在铝粉的表面分布不太均匀。由EDS 图可以看出,制备的HTPB/Cu/μAl 复合粉末中含有Cu、Al、C、O 4 种元素,其中Al 含量为49.61%,Cu 含量为16.76%。理论上还原出的单质Cu 与加入铝粉的质量比为1∶2,实际还原出Cu 的量低于理论值,推测导致铜含量较少原因可能是实验过程中未完全还原,且存在部分氧化。
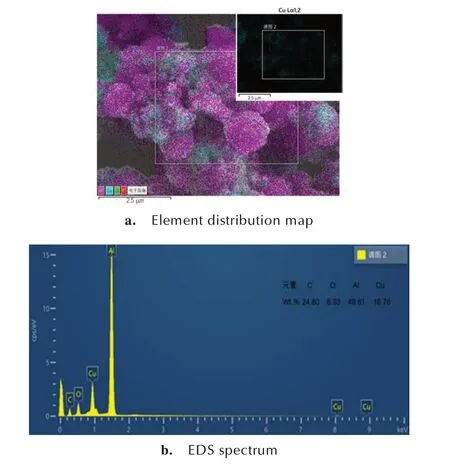
图5 HTPB/Cu/μAl 的EDS 谱图Fig.5 EDS spectrum of HTPB/Cu/μAl
3.5 差示扫描量热分析(DSC)
在空气气氛下,选取5 mg 样品,以10 ℃·min-1的升温速率对μAl、Cu、Cu/μAl 和HTPB/Cu/μAl 在50~720 ℃范围内的热行为进行探究,结果如图6 所示。
由图6 可见,μAl 的DSC 曲线在500~600 ℃之间有一放热峰,峰顶温度为555 ℃,放热量为1900 J·g-1,该峰为μAl 的氧化特征峰。相同反应条件下还原得到的单质Cu 的DSC 曲线在208 ℃和328 ℃存在两个氧化放热峰。从Cu/μAl 的DSC 曲线可以看出,在50~720 ℃范围内出现两个放热峰,其中在150~400 ℃之间存在一个比较宽的氧化放热峰,峰顶温度为280 ℃,放热量为2477 J·g-1,推测为复合物中铜的氧化放热峰;在500~600 ℃之间仍然存在μAl 的氧化放热峰,峰顶温度为571 ℃,放热量为1307 J·g-1。从HTPB/Cu/μAl 的DSC 曲线中可以发现,在200~450 ℃之间有三个放热峰,峰顶温度分别为233 ℃,289 ℃,352 ℃,总放热9513 J·g-1,推测其可能是铜的氧化与HTPB 的分解放热峰。在500~600 ℃之间的放热峰为Al 的氧化放热峰,放热量为1673 J·g-1。在Cu/μAl 样品制备中,理论上还原出单质Cu 的质量与μAl 的质量比为1∶2,HTPB/Cu/μAl 理论上还原出单质Cu、μAl 和HTPB 的质量比为10∶20∶3。因此,5 mg Cu/μAl 和HTPB/Cu/μAl 中μAl 的质量均低于5 mg,导致Cu/μAl和HTPB/Cu/μAl 中μAl 的放热量低于μAl 的放热量(1900 J·g-1)。将两者中的μAl 按质量比(总5 mg)衡算后发现,Cu/μAl 和HTPB/Cu/μAl 中μAl 的放热量分别为1960.5 J·g-1和3186.15 J·g-1,初步表明HTPB 包覆阻止了复合粒子的进一步氧化,提高了其氧化放热量。
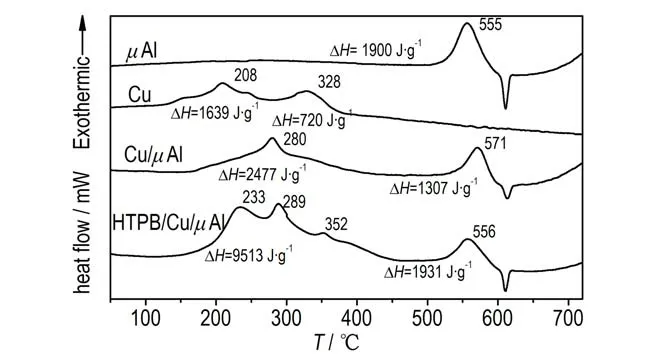
图6 Cu/μAl 和HTPB/Cu/μAl 的DSC 曲线Fig.6 DSC curves of Cu/μAl and HTPB/Cu/μAl
3.6 热氧化动力学性能分析
为对比研究包覆前后微米铝粉在550 ℃的氧化放热反应动力学,在空气气氛下,分别以5,10,15,20 ℃·min-1和25 ℃·min-11的升温速率测定了μAl、Cu/μAl 和HTPB/Cu/μAl 的DSC 曲线(见图7)。
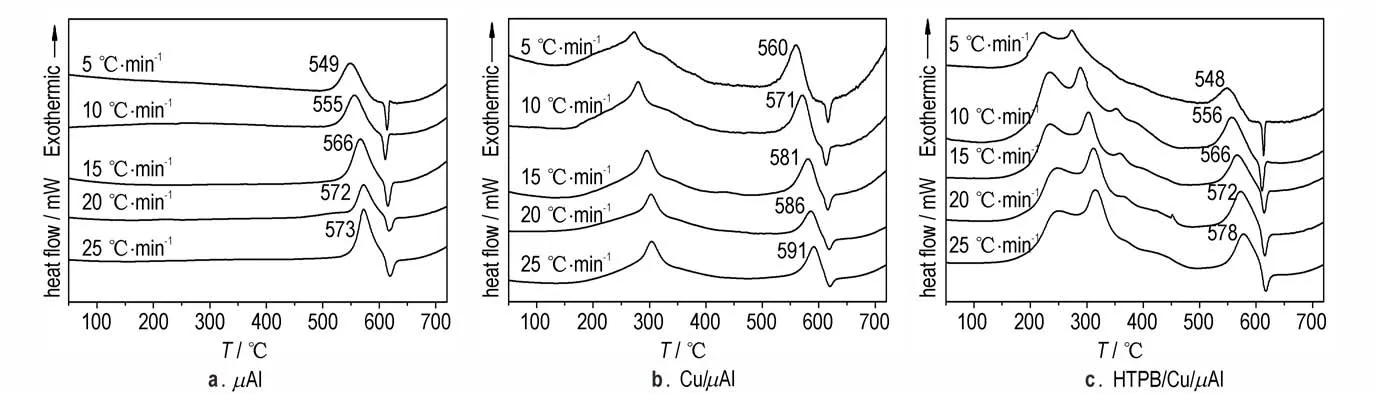
图7 μAl、Cu/μAl 和HTPB/Cu/μAl 不同升温速率的DSC 曲线Fig.7 DSC curves of μAl,Cu/μAl and HTPB/Cu/μAl at different heating rates
采用Ozawa 法和Kissinger 法分别对微米铝及包覆的微米铝粉在500~600 ℃的氧化过程进行动力学计算分析,其通式如(1)式[8]:

式中,R,普适气体常数,8.314 J·mol-1·K-1;β,升温速率,K·min-1;B,C为常数;Ea为表观活化能。当s=2,B=1 时为Kissinger 法方程;当s=0,B=1.0516 时为Ozawa 法方程。计算结果如表1 所示。
由表1 可得,μAl 粉的氧化放热峰主要集中在540~600 ℃之间,μAl的平均活化能为323.55 kJ·mol-1,Cu/μAl 的平均活化能为291.35 kJ·mol-1,相比μAl 平均活化能降低32.2 kJ·mol-1。HTPB/Cu/μAl的平均活化能为287.2 kJ·mo-1,相比μAl活化能降低36.35 kJ·mol-1,比Cu/μAl 平均活化能降低了4.15 kJ·mol-1,表明HTPB 和Cu 包覆可以显著降低铝粉的氧化活化能。

表1 μAl、Cu/μAl 和HTPB/Cu/μAl 的动力学参数Table 1 Kinetic parameters of μAl,Cu/μAl and HTPB/Cu/μAl
3.7 对AP 热分解性能分析
高氯酸铵(AP)作为复合固体推进剂的主要成分,一般占整个推进剂配方的65%~71%,其热分解特性与推进剂的燃烧特性密切相关[15]。因此,研究金属对AP 热分解的催化作用可以预估其对推进剂的催化效果[16]。采用DSC 法(升温速率为10 ℃·min-1)测定μAl、Cu/μAl 和HTPB/Cu/μAl 对AP 热性能影响分析,其DSC 曲线如图8 所示。
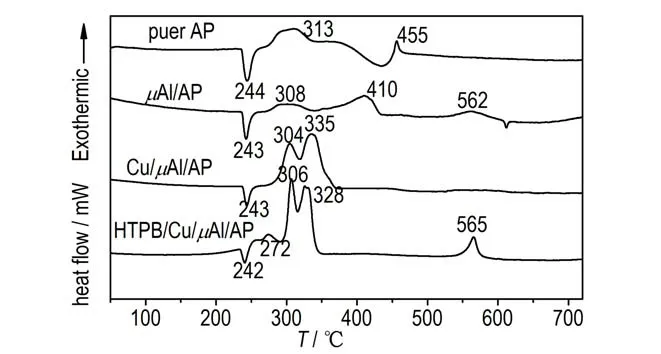
图8 AP、μAl/AP、Cu/μAl/AP 和HTPB/Cu/μAl/AP 的DSC 曲线Fig.8 DSC curves of AP,μAl/AP,Cu/μAl/AP and HTPB/Cu/μAl/AP
如图8 所示,可以看出纯AP 的热分解分为三个过程:第一个过程是晶型转变过程,由斜方晶型转为立方晶型,对应244 ℃处的吸热峰;第二个过程是低温分解过程,对应313 ℃的放热峰;第三个过程是高温分解过程,对应455 ℃的放热峰,直至AP 完全分解[17]。加入μAl、Cu/μAl 和HTPB/Cu/μAl 后,AP 的晶型转变温度没有发生明显的变化,复合物中AP 的热分解仍然分为高、低温两个连续的分解阶段;低温热分解温度仅发生微小的变化,而高温热分解温度则显著降低。相比于纯AP,μAl 使AP 的高温热分解温度由455 ℃降低到410 ℃;Cu/μAl 使AP 的高温热分解温度由455 ℃降低到335 ℃;HTPB/Cu/μAl 则使AP 的高温热分解温度由455 ℃降低到328 ℃。表明μAl、Cu/μAl 和HTPB/Cu/μAl 均对AP 的热分解产生了影响。
为了更好地探究μAl、Cu/μAl 和HTPB/Cu/μAl 对AP 的热分解机理,对上述样品加热至400 ℃的残渣进行XRD 分析,结果如图9 所示。
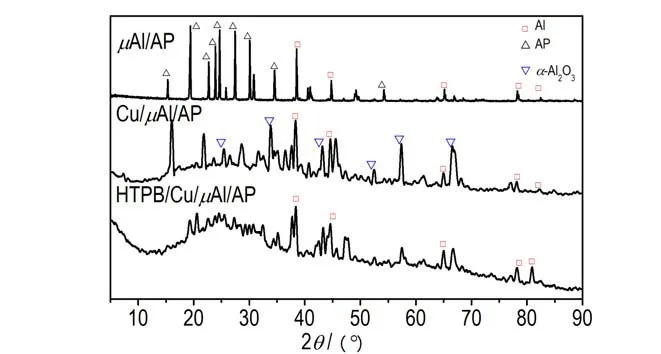
图9 μAl/AP 加热至400 ℃残渣的XRD 曲线Fig.9 The XRD curves of the residue of μAl/AP heated to 400 ℃
由图9 可见,μAl/AP 经过400 ℃加热后,残渣中仍然含有AP 与Al 的晶型结构,表明在400 ℃后AP 未完全发生分解,Al 同样未完全发生氧化,与图8 结果一致,即图8 中μAl/AP 曲线上位于410 ℃的放热峰为AP的高温分解峰。而Cu/μAl/AP 加热至400 ℃后的残渣仍含有Al 和α-Al2O3的晶型结构,HTPB/Cu/μAl/AP 加热至400 ℃后的残渣则只含有Al 的晶型结构,二者均未出现AP 的晶型结构,这表明加热至400 ℃时,AP 已完全分解,与图8 中Cu/μAl/AP 和HTPB/Cu/μAl/AP 的DSC曲线结果一致。α-Al2O3为六方紧密堆积结构,相比其它Al2O3晶型是最为稳定的[18]。HTPB/Cu/μAl/AP的400 ℃残渣中只含有Al 的晶型结构,未发现Al2O3晶型结构,推测所含残渣中Al2O3为无定形[19]。对比图8 和图9 推测认为,Cu/μAl/AP 和HTPB/Cu/μAl/AP均可对AP 产生一定催化作用,且HTPB 包覆后,所得样品HTPB/Cu/μAl 经400 ℃灼烧后残渣中未生成最稳定的α-Al2O3晶型。
4 结论
采用一锅法,以乙酰丙酮铜为铜源,液相还原制备了HTPB/Cu/μAl 复合材料,并对其结构、形貌和AP 的热分解性能影响进行分析,得出结论如下:
(1)结构和形貌表征结果表明,甲醛和肼作为还原剂可以将Cu2+还原成单质Cu,Cu 以粒子形式附着在μAl 的表面,HTPB 则均匀包覆在Cu/μAl 表面。
(2)动力学计算结果表明,Cu 包覆使μAl 平均活化能降低了32.2 kJ·mol-1,HTPB 的二次包覆使μAl 平活化能降低36.35 kJ·mol-1。因此无论是Cu 包覆还是HTPB 包覆,都会降低微米铝在550 ℃左右的氧化放热过程的活化能。还原出来的单质铜氧化过程和HTPB 的分解过程均会放出大量的热,表明用该方法包覆微米铝粉并不会降低铝作为能量成分的相对含量,还能提高能量释放率。
(3)相比于纯AP,μAl、Cu/μAl 和HTPB/Cu/μAl 的加入使AP 的高温热分解温度分别降低45 ℃、120 ℃和127 ℃,表明其促进了AP 的热氧化分解,降低了AP的热分解温度。

