超声引导下穿刺活检对获得性免疫缺陷综合征患者合并淋巴结肿大的病因诊断价值
刘建建, 黄晶晶, 张 晖,*, 马 鑫, 冯艳玲, 武 豆, 施 霞, 陆 清
1. 上海市公共卫生临床中心超声科,上海 201508 2. 复旦大学附属中山医院超声科,上海 200032 3. 上海市公共卫生临床中心病理科,上海 201508
获得性免疫缺陷综合征(acquired immunode-ficiency syndrome,AIDS)主要发病机制为人类免疫缺陷病毒(HIV)感染宿主后选择性地进入靶细胞(包括树突状细胞、巨噬细胞以及CD4+T淋巴细胞)大量复制,从而破坏CD4+T淋巴细胞,最终导致患者免疫功能缺陷[1]。
随着高效抗逆转录病毒疗法(highly active antiretroviral therapy,HAART)在AIDS治疗中的广泛应用,患者的预后获得显著改善,存活时间延长,但同时AIDS并发症发生率升高[2]。AIDS并发症病变复杂、多样,有些具有相似的影像学和临床特征,诊治难度较高,早期及时准确诊断有助于AIDS临床精准治疗和预后判断。
AIDS患者易发生各种HIV相关的机会性感染及相关性肿瘤,常累及全身多个器官,其中淋巴结肿大是临床最常表现形式。本研究回顾性总结上海市公共卫生临床中心近年来收治的AIDS合并淋巴结肿大患者的超声引导下穿刺活检结果,分析AIDS患者淋巴结肿大的病因及介入超声对该类淋巴结肿大的诊断率。
1 资料与方法
1.1 一般资料 2017年4月至2020年12月在上海市公共卫生临床中心由超声及其他影像学发现为AIDS合并淋巴结肿大需明确病因诊断患者130例,均行超声引导下病变淋巴结穿刺活检。其中住院患者116例、门诊患者14例,男性100 例、女性 30 例,年龄 7~83岁,平均(40.6±13.8)岁。AIDS由上海市疾病预防控制中心以及上海市公共卫生临床中心按照2015年中华医学会颁布的《艾滋病诊疗指南第三版》(2015版)标准[1]诊断。纳入标准:(1)超声检查显示淋巴结肿大病灶,并有安全进针途径;(2)凝血功能正常;(3)患者可耐受且愿意配合穿刺术。排除标准:(1)凝血功能障碍,出血风险大;(2)病情危重,无法耐受穿刺术。本研究获得上海市公共卫生临床中心伦理委员会批准(2019-S030-02),所有患者术前均签署知情同意书。
1.2 仪器与设备 采用彩色多谱勒超声诊断仪(美国Philips公司,型号IU-22、EPIQ 5型),高频探头(探头频率为5~12 MHz),低频探头(探头频率为1~5 MHz)。穿刺活检枪采用传统切割式半自动活检枪(MD公司)或意大利产Full-Opty抽吸式活检枪,规格18 G~16 G。
1.3 穿刺方法 常规超声结合彩色多普勒或超声造影确定病灶位置、大小、形态、回声、血供和病灶周围血管后定位。术者严格防护:戴防护眼罩及双层乳胶手套,穿防渗透手术衣。术中严格遵循无菌操作原则,进行常规消毒、铺巾,在探头表面涂耦合剂后用无菌塑料袋包裹,用1.0%利多卡因局部浸润麻醉后进针;针尖到达预定的病灶部位时,触发扳机获取组织后迅速退针。观察针槽内组织的颜色、质地和长度,将标本放入装有少许(5.0~6.0 mL)0.9%氯化钠溶液的无菌试管中。必要时可改变进针方向或深度后重复进行,但一般不超过3次;如使用Full-Opty抽吸式活检枪,当穿刺针尖达病灶合适位置时,激发活检枪扳机后,活检枪在不同角度反复进退4~5次,进退操作时针尖不超出病灶边界。拔针后按下按钮推出组织条,置于无菌试管,用少量0.9%氯化钠溶液冲洗穿刺针。摇晃振荡试管后,将上面液体行涂片、培养及基因X-Pert MTB/RIF等检测;沉淀组织用10.0%甲醛固定后送病理检查。如病灶伴有坏死液化,则先用穿刺针抽取脓液后再用活检枪穿刺。穿刺后门诊患者留院观察1 h。所有穿刺均徒手操作。
1.4 诊断评估标准 将淋巴结肿大病因分为3类:(1)良性病变,包括淋巴结结核,非结核感染性病变(如真菌、细菌及病毒感染)等;(2)恶性肿瘤,包括淋巴瘤、转移性肿瘤及卡波西肉瘤;(3)不确定。
淋巴结结核(在良性病变中占比最大)的诊断标准(满足以下任意1条即可确诊):(1)结核杆菌培养阳性;(2)基因X-Pert MTB/RIF检测阳性,涂片或病理可疑结核诊断;(3)典型上皮样肉芽肿形成、凝固性坏死、抗酸染色阳性。其他非结核感染性病变的病原体经涂片、培养及分子生物学检测明确诊断。实验室结果及病理诊断不明确者按不能明确诊断统计。门诊患者穿刺后3~6个月由高年资介入超声医师进行随访。 计算诊断阳性率及各种病变的发生率。
2 结 果
2.1 诊断结果 130 例患者中,淋巴结病灶位于颈部98 例(75.4%),腹股沟6例(4.6%),腋下11例(8.5%),腹腔内15例(11.5%)。穿刺病灶最大径11~100 mm。结果(表1)显示:良性病变82例(63.1%),恶性肿瘤36例(27.7%),病因类型不明确12例(9.2%)。其中17例淋巴瘤包括弥漫大B细胞淋巴瘤、Burkitt淋巴瘤各5例,浆母细胞淋巴瘤、小淋巴细胞性淋巴瘤及间变大细胞淋巴瘤各1例,未分型淋巴瘤4例。介入超声对AIDS合并淋巴结肿大病因诊断率达90.8%。
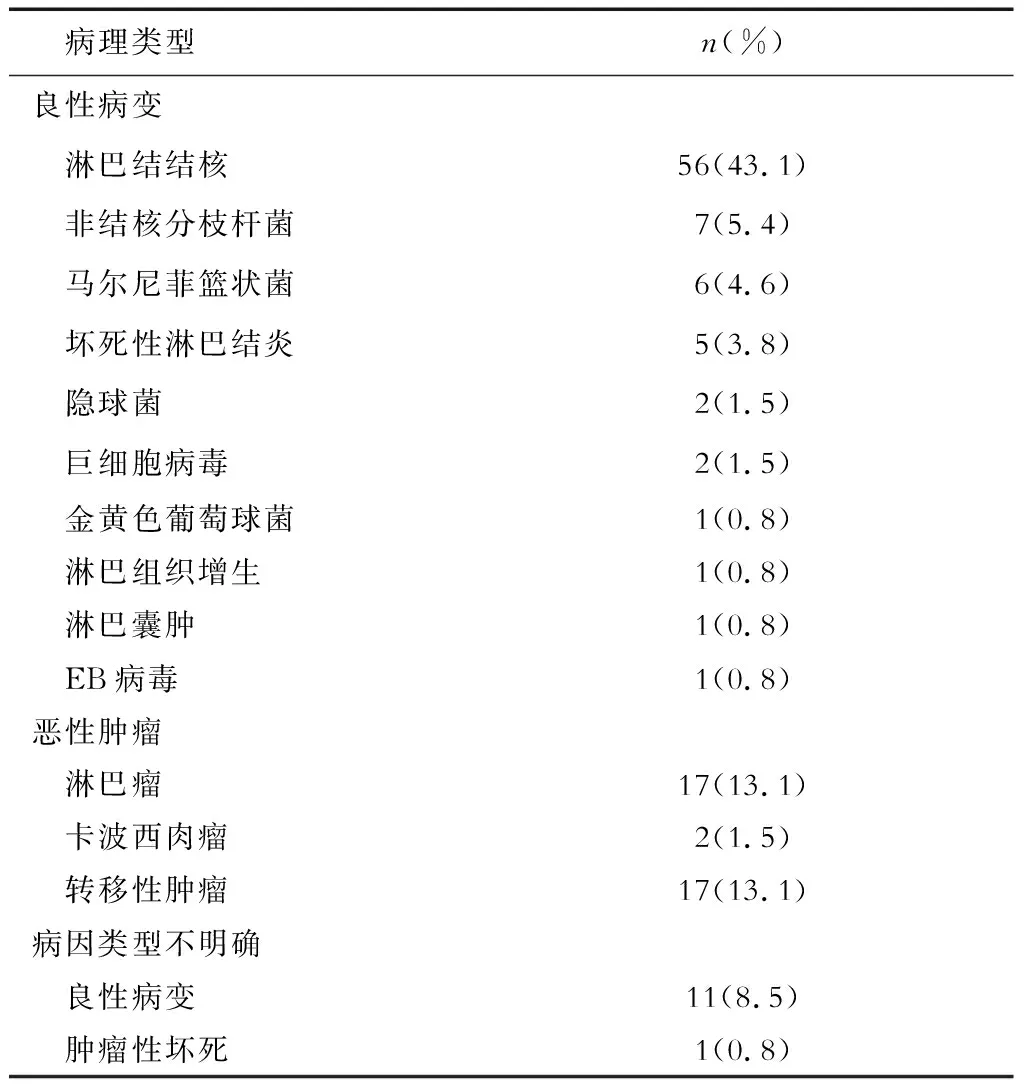
表1 AIDS合并淋巴结肿大患者淋巴结病变穿刺活检结果
2.2 部分典型病例超声及病理表现
2.2.1 淋巴结核 1例24岁男性患者腋窝下超声见1个30 mm×16 mm的低回声肿块,边界清,淋巴门结构模糊;彩色多普勒超声显示病灶内部短线状彩色血流,测及动脉频谱,阻力指数(RI)=0.72,不能除外淋巴瘤;超声引导下穿刺组织病理显示肉芽肿形成,干酪样坏死,抗酸染色(+),诊断为淋巴结结核(图1)。
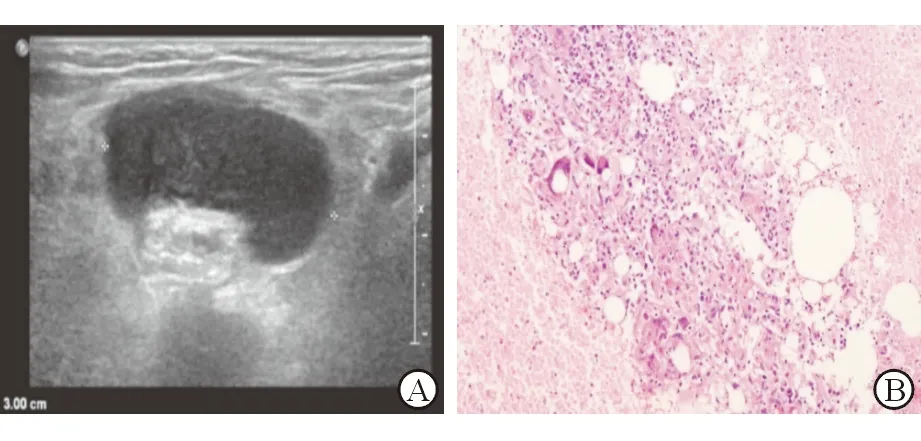
图1 AIDS患者合并腋窝淋巴结结核典型超声声像图与病理图片
2.2.2 马尔尼菲篮状菌感染 1例21岁男性患者腹部超声见腹腔多个长径20~30 mm的低回声肿块,部分融合,淋巴瘤可疑;超声引导下穿刺组织(图2)病理结果提示送检组织内炎性细胞浸润,组织细胞及上皮样细胞增多,肉芽肿形成,见大量真菌孢子,其形态提示为马尔尼菲篮状菌。
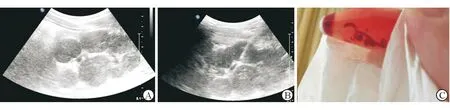
图2 AIDS患者合并腹腔淋巴结马尔尼菲篮状菌感染典型声像图、介入超声穿刺及穿刺标本图片
2.2.3 Burkitt淋巴瘤 1例53岁男性患者左颌下超声见97 mm×61 mm弱回声肿块,边界欠清,形态不规则,内见斑片状、条索状强回声,不能除外淋巴结核(图3)。穿刺后病理提示Burkitt淋巴瘤。
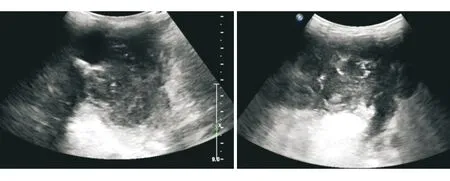
图3 AIDS患者合并颌下Burkitt淋巴瘤典型声像图
2.3 实验室资料 122例患者接受血常规检测,其中白细胞计数低于正常36例(29.5%),正常82例(67.2%),高于正常4例(3.3%);贫血98例(80.3%)。87例接受血沉检测,血沉>20 mm/h 70例(80.5%)。105例获得CD4+T淋巴细胞计数结果,其中大于500个/μL 7例,200~499个/μL 23例,100~199个/μL 28例,小于100个/μL 47例,其中低于正常值下限(410个/μL )94例(89.5%)。
3 讨 论
AIDS患者常见淋巴结肿大及软组织肿块,由于患者免疫功能差,病变性质复杂多样,发生感染时病原体种类多,可通过常规超声检查,根据病灶的大小、形态、回声、边界、血供及阻力指数等声像图特征初步判断病灶的良恶性,但临床精准治疗及预后判断还需要进一步检查。既往手术切除病灶活检是该类淋巴结肿大的主要临床诊断手段,但手术创伤大、费用贵,且病重患者不易耐受,而未经治疗的感染病灶术后可能感染播散甚至伤口不愈[3];同时对AIDS患者进行手术有职业暴露风险。国外有用细针穿刺抽吸细胞学检查诊断AIDS患者淋巴结病变的报道[4],但样本量较小。近年来,介入超声因其微创安全、操作便捷、价格低廉、有利于职业防护、无辐射等优点而受到临床广泛关注[5-6]。本研究总结了130例患者,男女比3.3∶1,病灶部位以浅表淋巴结尤其是颈部淋巴结为主,占75.4%;实验室检查中白细胞计数低于正常占29.5%(36/122)、血红蛋白低于正常占80.3%(98/122)、血沉升高占80.5%(70/87)、CD4+T细胞低于正常下限者占89.5%(94/105)、证实AIDS患者随着CD4+T淋巴细胞数量减少,免疫力降低,机会性感染及肿瘤发病率增加。
本研究显示,AIDS患者合并淋巴结病变的病因以感染为主,感染源种类多,其中淋巴结核占总数的43.1%,占首位。根据淋巴结核的病理类型,声像图可表现为以增生为主的“假肾征”、以结核性肉芽肿为主的低回声实质性肿块及多种病理表现并存的混合回声肿块。“假肾征”表现与淋巴组织反应性增生无法鉴别,结核性肉芽肿与淋巴瘤较难鉴别[7];混合回声肿块尤其当伴有钙化或窦道时往往提示结核病诊断,但HIV合并结核双重感染的患者中结核病灶内的钙化灶较少见[8]。因此,要明确病灶的病因诊断,需要行超声引导下穿刺活检。穿刺病理结果显示典型上皮样肉芽肿形成、凝固性坏死、抗酸染色阳性,提示结核感染,但有时病理检查不能发现结核的特征性改变,仅表现为非特异性的慢性炎症。为了提高诊断率,弥补单纯病理检查在感染性疾病诊断中的不足,本研究除对组织标本进行病理检查外,同时对穿刺组织液进行涂片、培养及基因X-Pert MTB/RIF等检测,进而明确除结核以外的非结核分枝杆菌、马尔尼菲篮状菌、隐球菌、金黄色葡萄菌、巨细胞病毒等病原微生物感染的诊断。
AIDS患者合并淋巴结肿大的另一个主要病因为肿瘤,尤其是淋巴瘤及卡波西肉瘤。其中,AIDS患者发生淋巴瘤的风险远高于普通人群,病灶可位于腹膜后和浅表淋巴结,超声表现为不均匀等回声或低回声肿块,病灶大者可表现为弱至无回声坏死灶,边界不清,不易与感染灶鉴别。本研究中恶性肿瘤占27.7%,其中淋巴瘤占13.1%。
综上所述,本研究利用超声引导下穿刺活检方法对AIDS患者合并淋巴结肿大的病因进行了初步探讨,除进行常规病理检查外,还进行组织液涂片、培养、相关基因等检测,提高了诊断率,仅9.2%(12/130)患者未明确病因诊断。获得病因诊断的患者中,良性病变主要为淋巴结核、非结核分枝杆菌、马尔尼菲篮状菌等感染,恶性肿瘤主要为淋巴瘤,淋巴瘤与转移性肿瘤比例相当。本研究说明对于该类患者,超声引导下穿刺活检技术可精准取材,微创安全,诊断准确率与手术活检相当[9],有助于AIDS机会性感染及相关性肿瘤的早期诊断及精准治疗。但本研究未能对患者的超声声像图特征进行比较分析,今后将进一步加以完善。此外,对不能明确病因诊断的患者可进行宏基因检测,进而提高诊断率。
利益冲突:所有作者声明不存在利益冲突。

