锰改性磁铁矿催化NH3-SCR脱硝性能研究
张少飞,李建军,舒松
(四川大学 建筑与环境学院,四川 成都 610065)
钢铁行业烧结、焦化、炼铁、炼钢及其附属环节都会产生NOx大气污染物[1]。工业上主要使用V2O5-WO3(MoO3)/TiO2,该催化剂的活性温度范围窄,为300~400 ℃[2],不适用于温度较低的烧结尾气中。铁基催化剂,具有突出的热稳定性、良好的中高温SCR活性,一直被广泛研究。但是,Fe基催化剂的低温活性仍需要改善。研究发现,锰与铁的强相互作用有利于提高铁基催化剂的低温脱硝效率[3-4]。
本文通过锰对磁铁矿型铁基催化剂改性,提高催化剂的低温脱硝性能。重点研究制备温度对催化剂脱硝性能的影响,通过XRD、BET、NH3-TPD等方法对催化剂的理化性质进行表征,构建催化剂结构与脱硝性能的构效关系。
1 实验部分
1.1 试剂与仪器
硝酸铁、硝酸锰、氢氧化钠均为分析纯;一氧化氮、氨气、氮气、氧气。
PHS-3C pH计;BSA224S分析天平;78HW-1恒温磁力搅拌器;SHZ-D(Ⅲ)循环水式真空泵;DHG-9070A电热鼓风干燥箱;TSXQ-4-10P(箱式)气氛保护炉;LLS Plus蠕动泵;PANalytical X’Pert PRO衍射仪;AUTOSORB-IQ型气体吸附仪;TP-5076化学吸附仪;AXIS UltraDLD X射线光电子能谱仪。
1.2 催化剂制备
准确称取20.201 0 g的Fe(NO3)3与相应的Mn2+离子盐混合,n(Fe3+)∶n(Mn2+)=2∶1,将其溶解于130 mL去离子水中,充分搅拌,配制成混合溶液A。NaOH溶于水中,制备5 mol/L的溶液B。在常温搅拌的条件下,使用蠕动泵将B溶液以 6 mL/min 的滴加速率加入到A溶液中,形成棕黑色胶体状混合物C,并调节pH值为11。将混合物C转移至密封好的内衬聚四氟乙烯的不锈钢反应釜中,分别在120,140,160,180,200 ℃烘箱中恒温反应8 h,制备批次催化剂样品,记为MnFe2O4-X(X=120,140,160,180,200)。常温冷却,用大量的蒸馏水反复抽滤、清洗,直到滤液为中性。在105 ℃下干燥12 h。放入马弗炉中,空气氛围中300 ℃下焙烧3 h,制得催化剂,研磨,筛分。
1.3 催化剂的表征
采用衍射仪对催化剂的晶体结构、物相组成进行分析。采用气体吸附仪测量催化剂的等温氮气吸脱附曲线。采用化学吸附仪测定催化剂的氧化还原能力和表面酸性。采用X射线光电子能谱仪测定催化剂的表面元素价态及各元素的含量。
1.4 催化剂活性评价
催化剂的脱硝活性测试装置见图1。
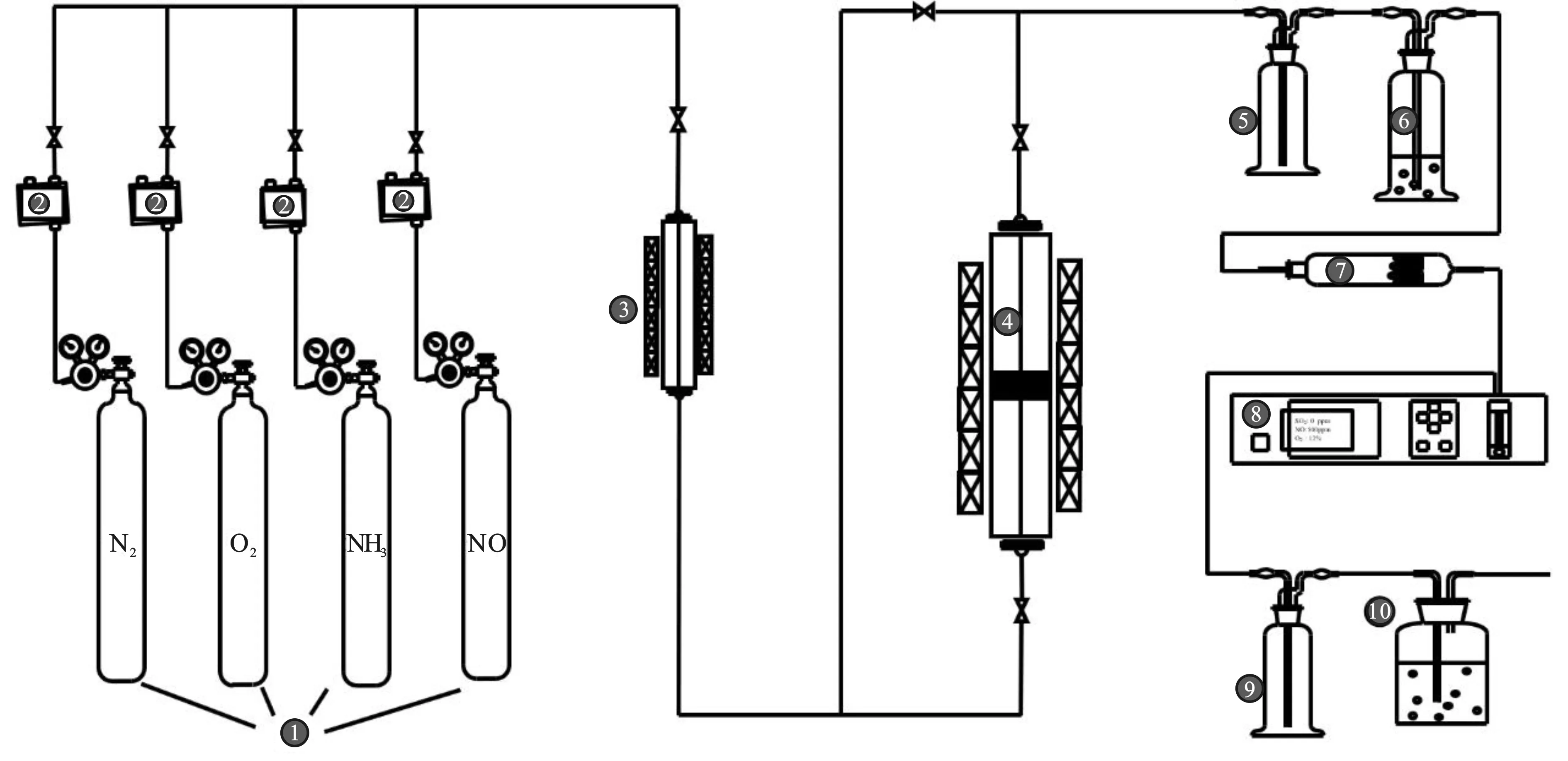
图1 NH3-SCR催化剂活性评价装置图Fig.1 Activity evaluation equipment diagram of NH3-SCR catalyst①气瓶;②质量流量计;③混器瓶;④催化反应器;⑤250 mL孟氏洗涤瓶;⑥氨吸收瓶;⑦干燥管;⑧烟气分析仪;⑨防倒吸瓶;⑩尾气吸收瓶
控制NO、NH3、O2、及N2以不同的流量从钢瓶中流出到预热器进行加热,之后流入到混合器,让气体充分混合形成模拟烟气。模拟烟气通过主要以内径为10 mm的石英玻璃反应管和加热炉组成的反应系统与催化剂发生反应。反应后的气体进入到烟气分析仪中进行NO的检测。最后气体通过尾气处理将有害废气吸收后排入大气中。
实验模拟烟气按照钢铁厂中烧结过程中排放的烟气特点进行配制,500×10-6NO,500×10-6NH3,12%O2,N2作为平衡气,气体总流量为 700 mL/min,催化剂的填装体积为1 mL,空速GHSV为 42 000 h-1。实验测试温度梯度60~260 ℃(每隔20 ℃一个温度点)下催化剂的催化效率,并在每个温度点停留 30 min,待烟气分析仪上示数稳定后记录数据。NO去除效果(ηNO,%)计算公式如下:
式(6)中,fst表示卫星发射的下行信号频率。地面站综合基带接收信号由于受到下行多普勒的影响,接收频率为:
2 结果与讨论
2.1 脱硝性能测试
图2显示了催化剂的脱硝性能。
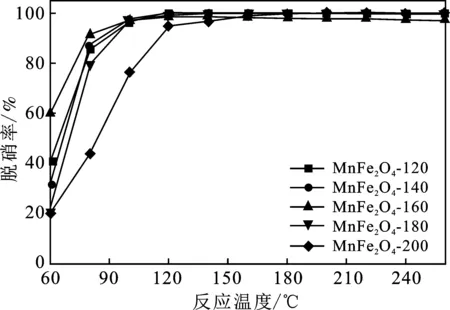
图2 不同水热反应温度催化剂脱硝效率Fig.2 Denitration efficiency of catalyst at differenthydrothermal reaction temperatures
由图2可知,反应温度越高所有样品活性越高。制备过程中合成温度越高,样品的催化能力越强,并在160 ℃制得的催化剂达到最大的活性,反应温度80 ℃下,可以达到90%的脱硝率,随后随着合成温度进一步升高,样品的活性不断的降低。活性最差的样品(水热200 ℃)在80 ℃时催化效率仅有44%的脱硝效率。不同的水热温度制备催化剂的活性从高到低顺序为:水热160 ℃>水热140 ℃>水热 120 ℃>水热180 ℃>水热200 ℃。
2.2 催化剂的物相结构分析
图3为5种样品的XRD图谱。
由图3可知,主峰30.2,35.6,43.3,57.3°代表了磁铁矿Fe3O4(220)、(311)、(400)、(422)、(511)和(440)面,与立方尖晶石结构具有良好的匹配[5]。5种样品峰位置相近,并且均与标准卡片磁铁矿Fe3O4(PDF#99-0073)的位置一致,说明合成了锰改性的磁铁矿。其中没有发现锰氧化物的衍射峰,说明锰进入到氧化铁的晶格中,成为结构中的一部分,或者合成的氧化物比较少,没有达到检测限。在水热温度160 ℃时的峰没有那么尖锐,说明160 ℃时样品中无定型的MnFe2O4比较多,催化剂活性比较高,与活性测试一致[6]。
2.3 催化剂的氧化还原性能分析
H2-TPR结果见图4。
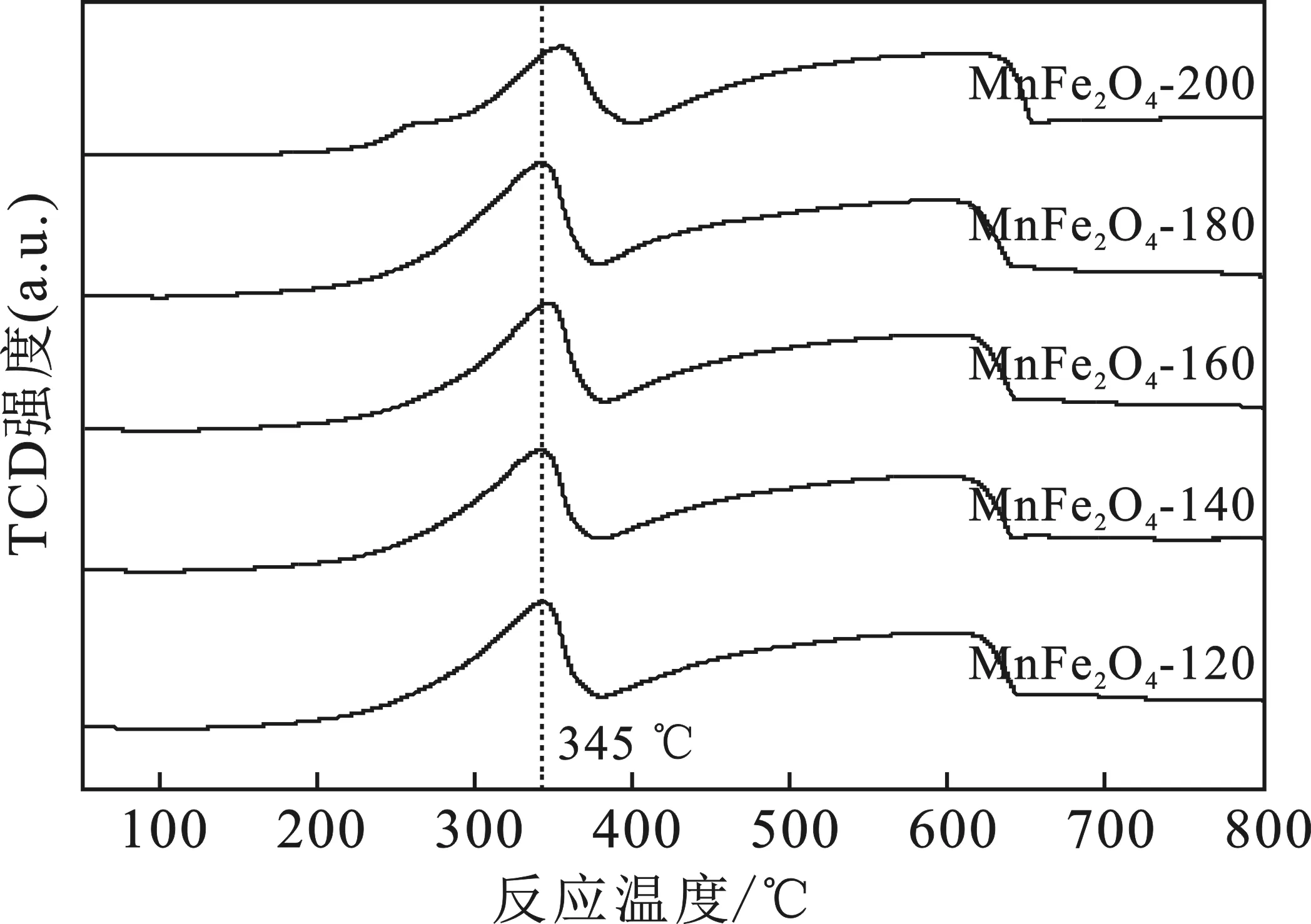
图4 不同水热合成温度制备样品H2-TPR图谱Fig.4 Different hydrothermal synthesis temperatures wereused to prepare H2-TPR profiles of the samples
由图4可知,样品均在160 ~ 395 ℃和380 ~ 675 ℃两个位置有明显的宽峰,前者是MnO2还原为Mn2O3,Mn2O3还原为Mn3O4,Fe2O3还原为Fe3O4[6-7],而后者Mn3O4还原为MnO,Fe3O4还原为FeO[4,8]。在200 ℃的水热反应制备条件下的样品,在250 ℃位置有一个小的还原峰并且在345 ℃左右的峰位置较靠后,可能是由于制备时水热温度较高,产生了其他氧化物在催化剂表面,形成的MnFe2O4减少,使其氧化还原过程分成两部分。
2.4 催化剂的NH3程序升温脱附分析

图5 不同水热反应温度下的NH3-TPD测试结果图Fig.5 NH3-TPD test results at different hydrothermalreaction temperatures
由图5可知,不同样品展示出了相似的氨气脱附峰,分别在80~140 ℃和400~650 ℃范围内,第一个峰属于物理吸附NH3或者部分NH4+在弱Brönsted酸位点上的解吸。第二个峰是一个重叠峰,可以分为480 ℃和590 ℃左右位置的两个峰,因此样品中存在吸附氨的中强酸位点和强酸位点,强酸位点归属于Lewis酸位点上氨的解吸[10-13]。180 ℃ 和200 ℃的水热反应条件下制备的样品中在低温下峰面积较小,氨气吸附量少,表面酸性较差,不利于NH3的吸附活化,所以催化反应活性比较差。其他样品的脱附峰的峰形与面积相似,且出现的位置也相差不大,所以表面酸性相近。
2.5 催化剂氮气吸附-脱附表征分析
图6为5个样品的N2吸附-脱附等温曲线,图7是其相应的孔径分布曲线图。
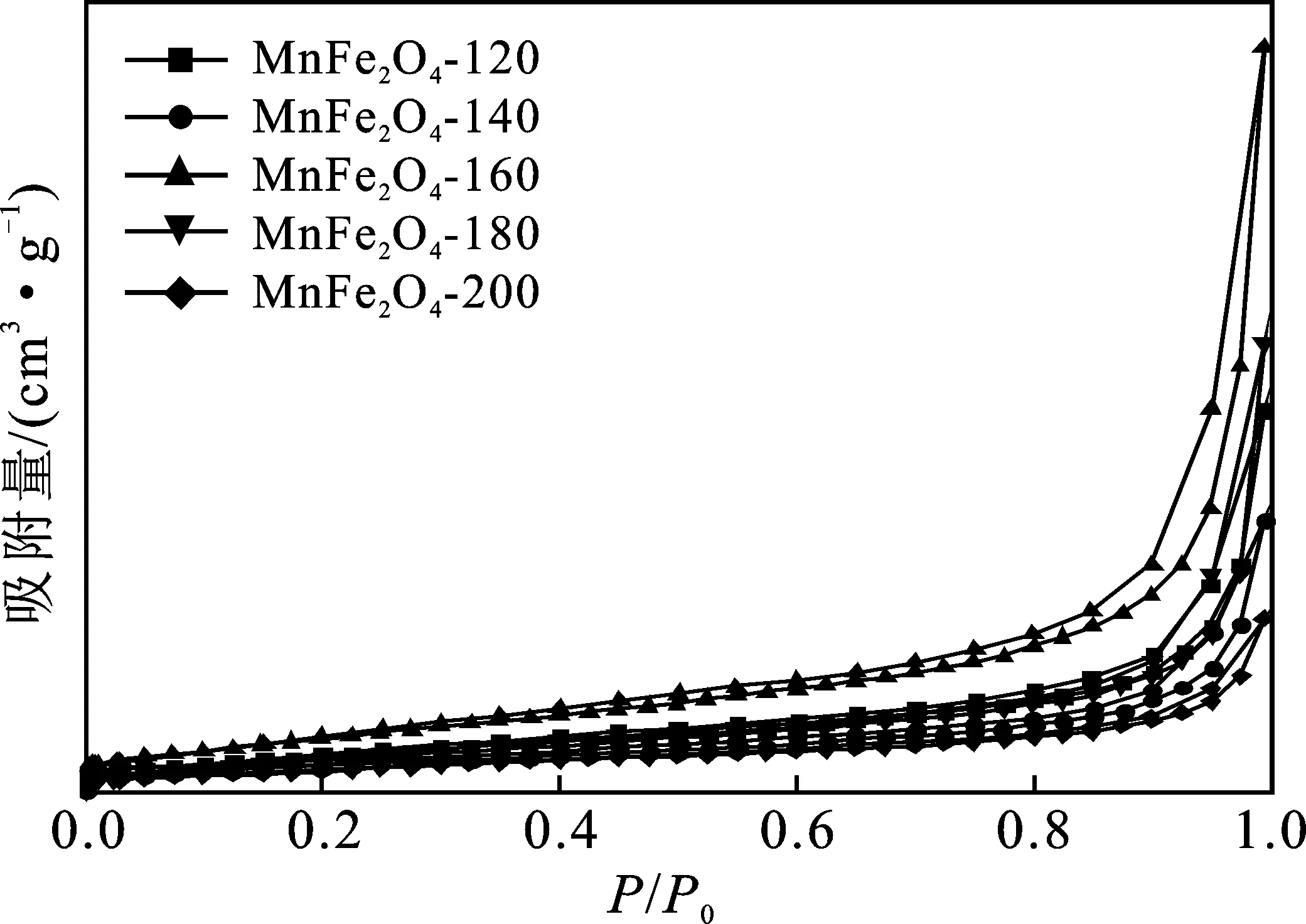
图6 不同水热反应温度条件下制备催化剂的N2吸附-脱附等温曲线Fig.6 N2 adsorption-desorption isotherm curves ofcatalysts prepared at different hydrothermalreaction temperatures
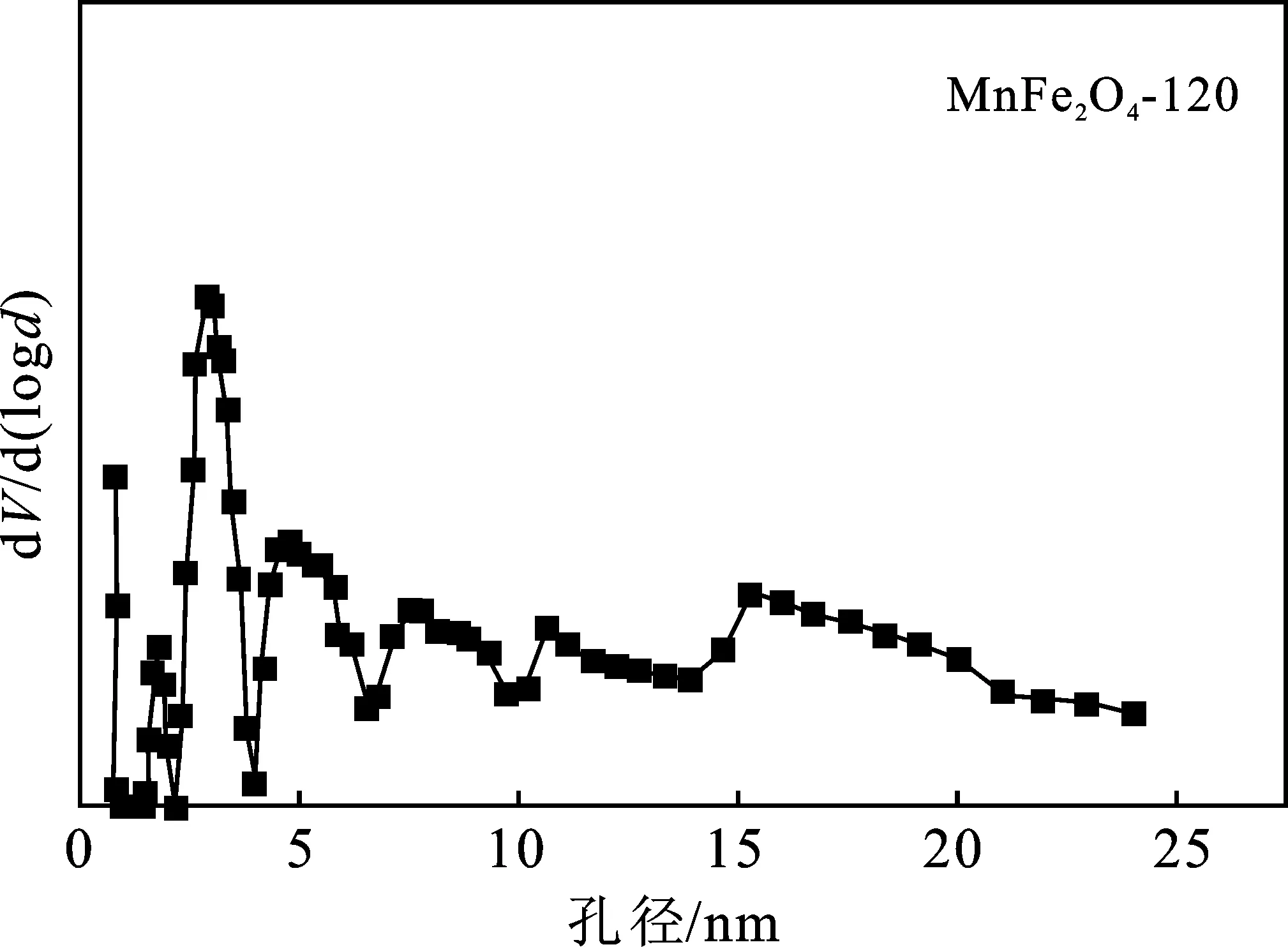
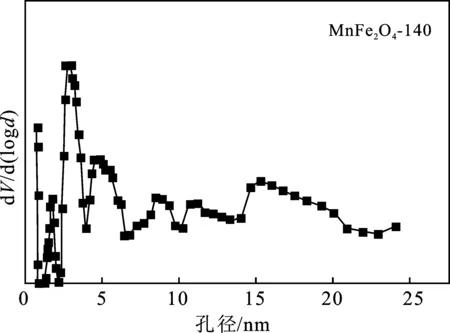
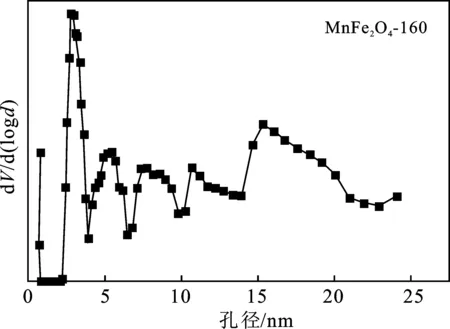
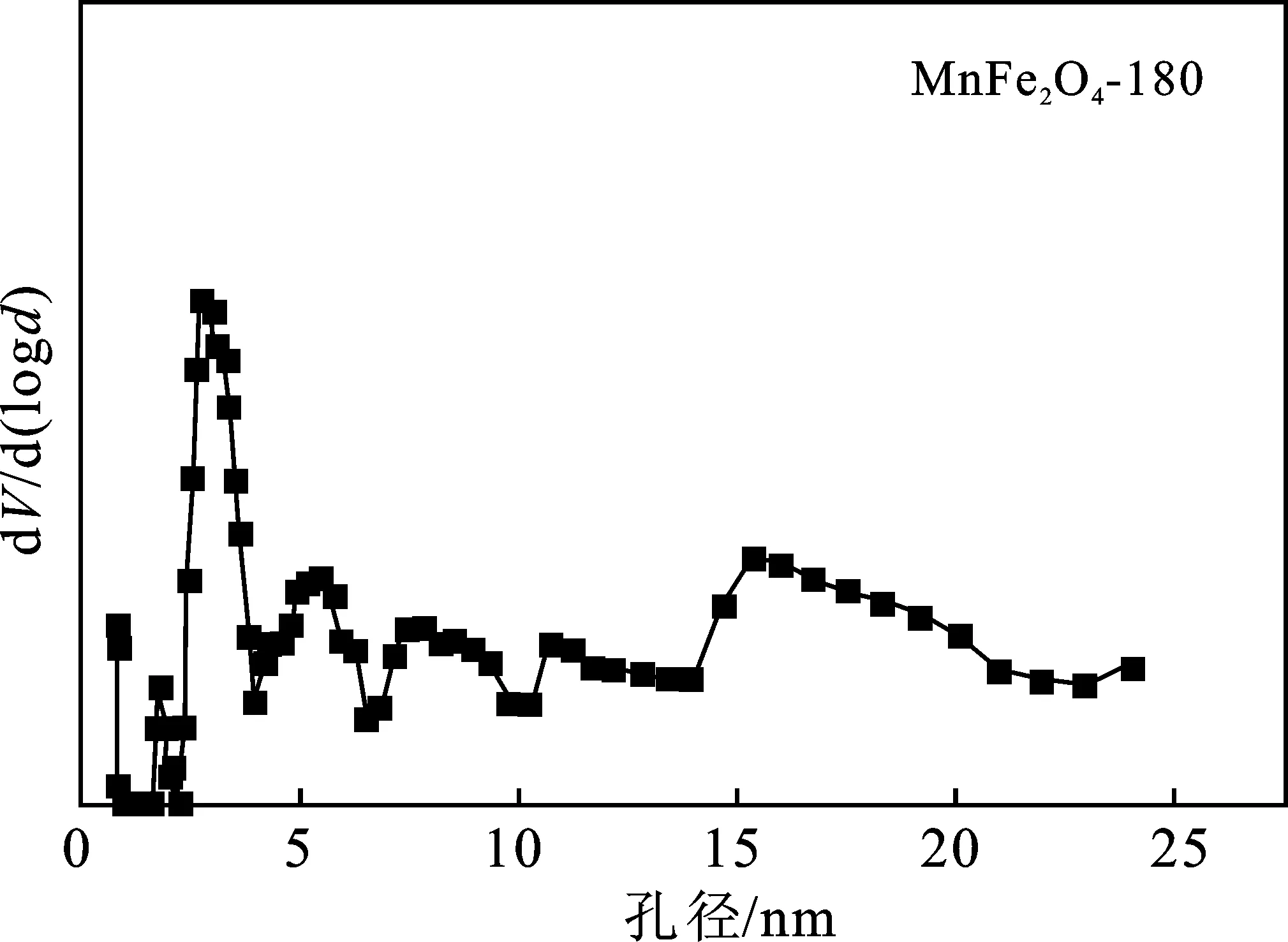
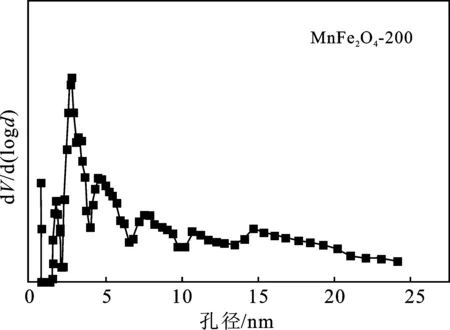
图7 不同水热反应温度制备催化剂孔径分布图Fig.7 Pore size distribution of catalysts preparedat different hydrothermal reaction temperatures
由图6可知,它们都有闭合的回滞环,且催化剂均呈现IV型等温线(IUPAC分类),伴随着H3滞后环,表明颗粒松散组合导致形成裂缝状孔洞和介孔的存在[14]。此外,无论是在低还是高的相对压力下,吸附量都急剧增加,表面存在微孔和大孔结构。由图7可知,在介孔范围内(2~50 nm)的孔的分布比较广泛,而微孔范围(<2 nm)内也出现孔径分布峰,与等温线的分析一致。表1为催化剂织构参数。
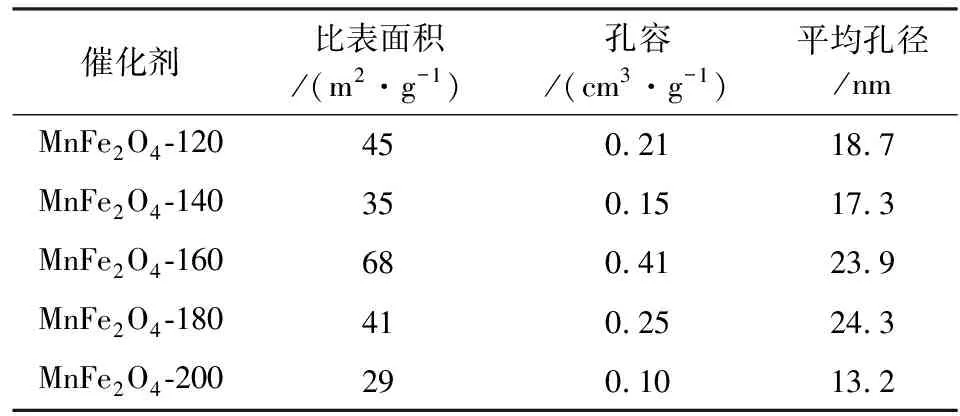
表1 不同水热反应温度制备催化剂的织构参数Table 1 Texture parameters of catalysts prepared atdifferent hydrothermal reaction temperatures
由表1可知,在160 ℃下制备的催化剂具有最大的比表面积(68 m2/g),这也是其表现出最好的催化剂活性的原因之一。
2.6 催化剂XPS分析
图8表示催化剂Fe 2p(a)、Mn 2p(b)和 O 1s(c)的XPS 图谱。
由图8a可知,结合能711,724 eV附近两处的峰分别对应于Fe 2p3/2和Fe 2p1/2。同时,在714,717,730 eV附近均观察到卫星峰,说明样品Fe2+和Fe3+同时存在[15]。通过对XPS图谱进行分峰拟合后,可分为在711.1~711.6 eV对应于Fe3+的标准峰和处于709.6~709.8 eV对应于Fe2+的标准峰[16],各价态Fe元素的峰位置与相对比例见表2。
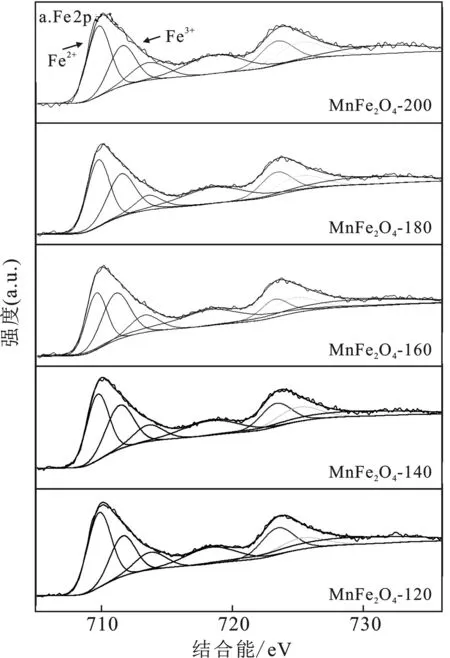
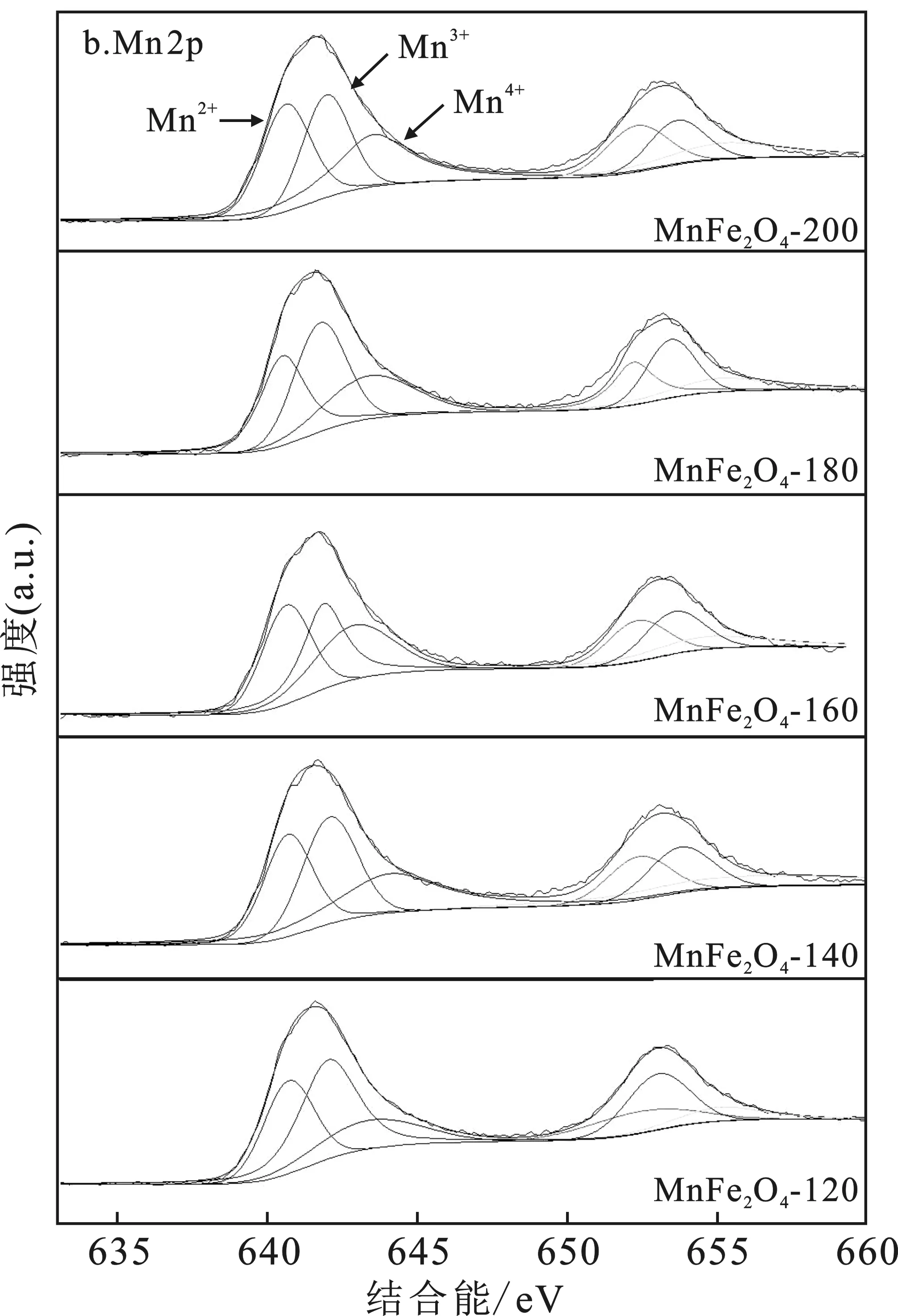
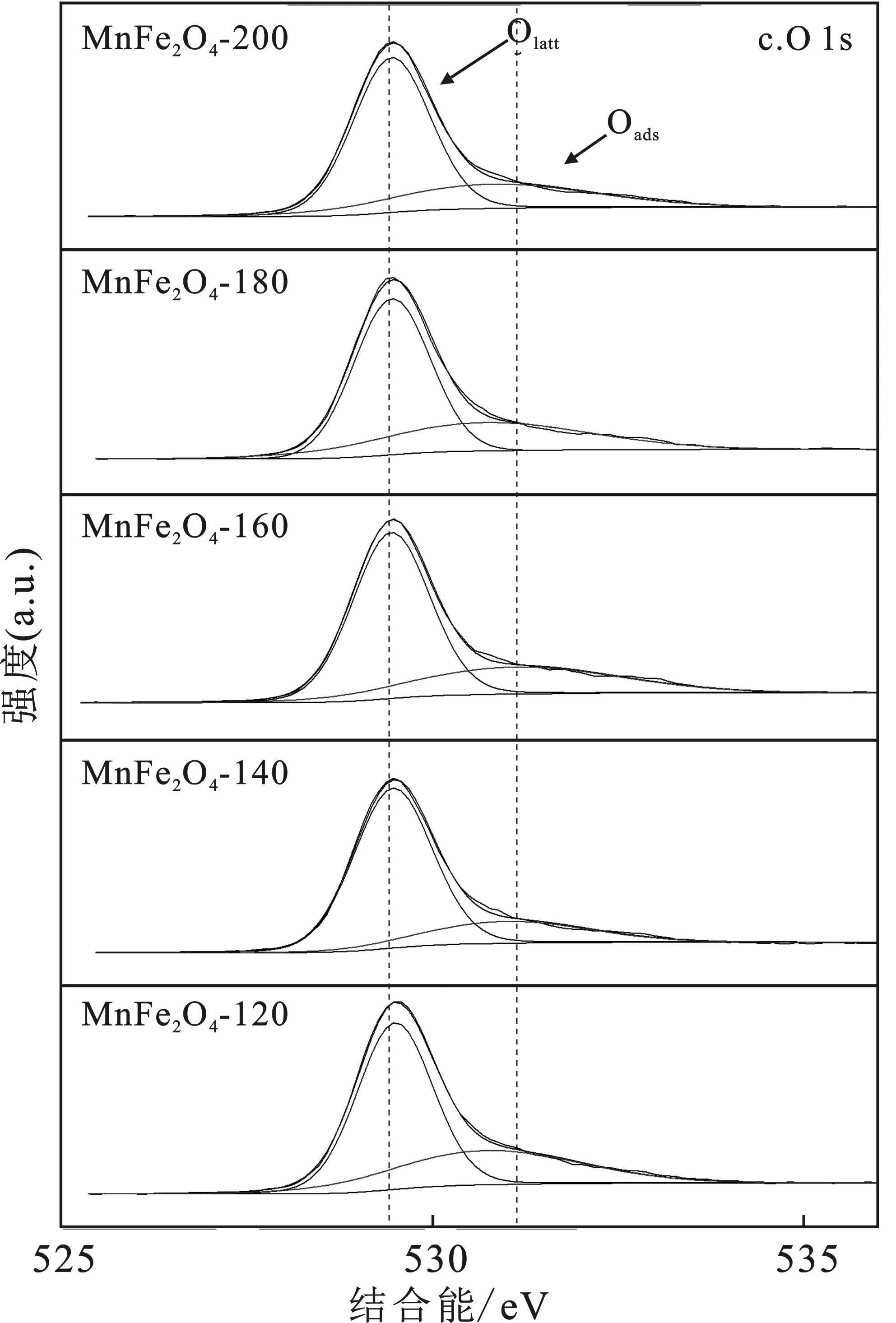
图8 不同水热反应温度制备的催化剂的Fe 2p(a)、Mn 2p(b)和 O 1s(c)XPS 图谱Fig.8 XPS spectra of Mn 2p (a),Fe 2p (b) andO 1s(c) catalysts prepared at different hydrothermalreaction temperatures were obtained
由表2可知,水热反应温度升高时,Fe2+和Fe3+的结合能均先降低后升高,并且在160 ℃时制得的样品具有最低的结合能。随着水热反应温度的升高,样品表面的两种价态Fe的相对比例,呈现出先增大后减小的趋势,并在160 ℃时达到最大。较多的Fe3+能够提供更多的酸性位点有利于NH3的吸附与活化,提高SCR的反应活性。
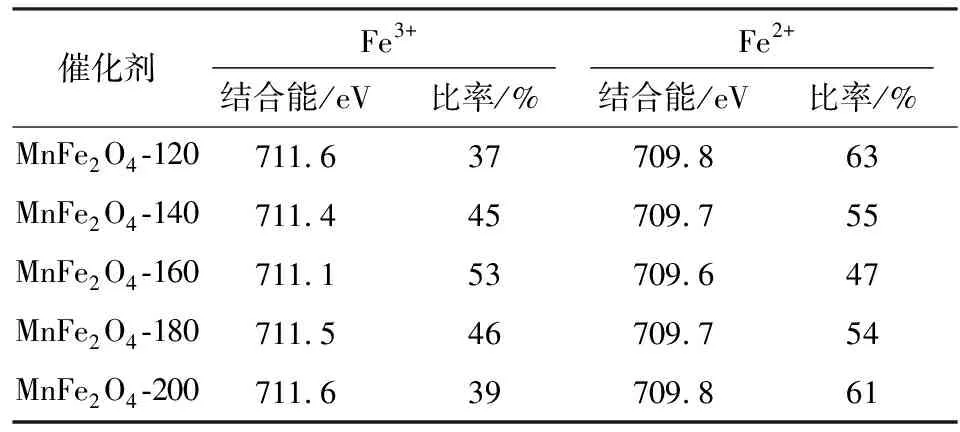
表2 不同水热反应温度下合成催化剂样品中不同价态铁的结合能和相对占比Table 2 The binding energies and relative proportionsof Fe with different valence states in catalyst samplesunder different hydrothermal reaction temperatures
由图8b可知,642,653 eV附近两个特征峰分别代表了Mn 2p3/2和Mn 2p1/2。分峰拟合后,可将每个样品的Mn 2p3/2的峰分成三个独立的峰,它们的结合能分别在640.5~640.8,641.8~642.1,643.2~644.0 eV范围内,对应于Mn2+、Mn3+和Mn4+[17-18],说明三种价态的锰元素均存在于样品的表面上,对拟合后的峰面积进行计算,不同价态的锰以及其相对比例,见表3。
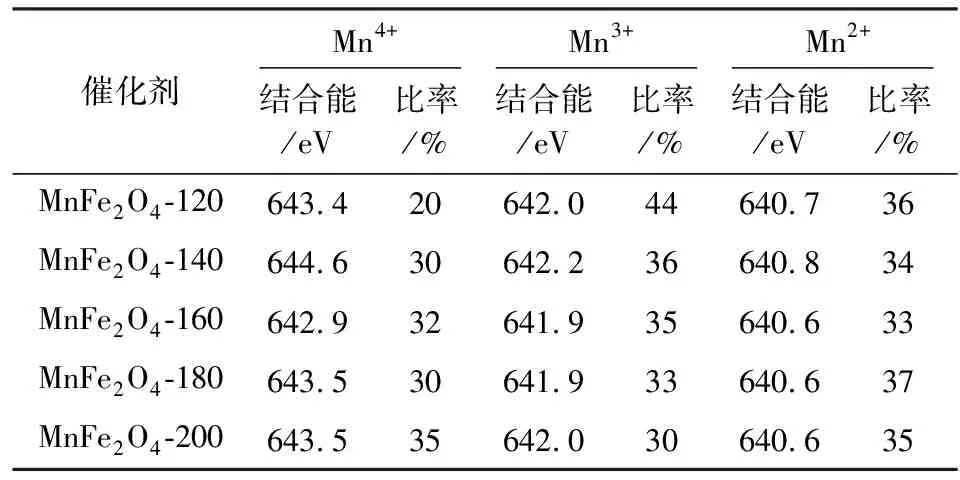
表3 不同水热反应温度下合成催化剂样品中不同价态锰的结合能和相对占比Table 3 The binding energies and relative proportionsof manganese with different valence states in catalystsamples under different hydrothermal reaction temperatures
由表3可知,锰元素没有单独形成具有晶体结构的氧化物,所以锰只能是在具有尖晶石结构的MnFe2O4中占据了Fe3+或者Fe2+的位置,从而表现出多种不同的价态[19]。由于锰的电负性比铁的弱,所以电子云会向铁的位置偏移,从而使锰的价态偏高。高价态的锰能够将NO氧化为NO2,为“快速SCR反应”创造条件。水热反应160 ℃时的结合能最低,有利于SCR的反应。此外,随着水热反应温度的升高,Mn的比例先增大,在160 ℃时达到最大,之后便不断的减小。根据文献可知[20-21],高价态的锰越多,越有利于低温下的SCR反应,Mn2+的增多表明高价态的锰含量减少,所以该结果与催化剂的活性结果表现一致。
由图8c可知,O 1s图谱中有一个不对称的峰,对其进行峰形拟合解卷积,可将其分峰为两个峰,其中529 eV附近的峰对应于催化剂样品的晶格氧,记为Olatt,而531 eV附近的峰对应于催化剂的表面吸附氧,用Oads[22-23]表示。催化剂表面氧物种的类型与占比见表4。

表4 不同水热反应温度下合成催化剂样品中不同氧物种的结合能和相对占比Table 4 The binding energy and relative proportion ofdifferent oxygen species in catalyst samples underdifferent hydrothermal reaction temperatures
由表4可知,样品表面吸附氧含量由高到低的顺序依次为MnFe2O4-160>MnFe2O4-140>MnFe2O4-120>MnFe2O4-180>MnFe2O4-200,与其活性结果一致。说明化学吸附氧在催化反应中起着至关重要的作用,因为Oads在催化反应中比Olatt更具活性和更高的流动性[24]。此外,水热160 ℃制备的样品拥有更多的高价态表面Mn、Fe元素,可能是因为价态越高,表面的晶格氧缺陷越多,形成更多的氧空位,从而拥有更多的表面吸附氧。
3 结论
(1)锰改性不会破坏Fe3O4的尖晶石结构,锰取代铁进入Fe3O4晶格,锰铁之间的相互作用有利于SCR催化反应。
(2)催化剂水热制备温度对催化剂脱硝性能影响较大,水热反应温度160 ℃时制备的催化剂脱硝性能最佳,80 ℃的反应温度即可达到90%的脱硝效率。160 ℃水热合成的催化剂中锰的平均价态最大,催化剂表面吸附氧量与比表面积最大。

