盐酸林可霉素可溶性粉含量测定方法
董书香,王 峻,陈向丹,丁 阳
(湖北省兽药监察所,武汉 430070)
林可霉素(lincomycin)是由链霉菌产生的一种林可胺类碱性抗生素,其作用机制与红霉素非常相似,通过抑制微生物蛋白质的合成而产生作用[1]。对革兰氏阳性球菌[2],如葡萄球菌、溶血性链球菌和肺炎球菌作用较强,对厌氧菌如破伤风梭菌、产气荚膜芽孢杆菌也有抑制作用[3];对支原体螺旋体有效,对弓形体也有一定作用,兽药临床上广泛用于敏感菌所致的畜禽细菌性疾病的治疗,且效果显著[4]。盐酸林可霉素在治疗各种感染中得到了广泛应用,因此建立盐酸林可霉素快速而有效的含量检测方法尤为重要。目前,盐酸林可霉素的含量测定方法有色谱法、质谱法、光谱法[5,6]。兽用盐酸林可霉素可溶性粉,收录于《兽药质量标准》(2017年版)化学药品卷[7],其中采用高效液相色谱法对含量进行测定。该方法使用的流动相为0.05 mol/L硼砂溶液(用85%磷酸溶液调节pH至6.0)-甲醇(4∶6,V/V),在实际试验过程中,发现该流动相中使用了高浓度硼砂盐溶液,硼砂是含10个水分子的化合物,放置时间过长容易失水风化,导致配制的流动相中硼砂浓度超过标准浓度[8],且高浓度盐溶液对色谱柱和液相系统都有较大的损害,长期处于高浓度盐溶液环境中,将大大缩短色谱柱和仪器的使用寿命[9]。研究一种新的液相色谱方法来改善以上问题,即可提高检测效率,又可以延长仪器和耗材寿命。本研究优化了高效液相色谱流动相,探讨了高效液相色谱法测定盐酸林可霉素可溶性粉含量的方法,并对方法进行了验证。
1 材料与方法
1.1 试剂与材料
林可霉素对照品(中国兽医药品监察所,含量:84.6%,批号:K0101503);甲醇、乙腈(安徽天地高纯溶剂有限公司)为色谱纯;硼砂(国药集团化学试剂有限公司)为分析纯;磷酸氢二铵(国药集团化学试剂有限公司)为分析纯;水为二次纯化水;盐酸林可霉素原料,辅料,10%盐酸林可霉素可溶性粉样品(批号为201905311、202005081、202005201)均由武汉某兽药公司提供。
1.2 仪器
岛津20AD高效液相色谱仪配紫外检测器;Met⁃tler AE240电子天平;MILIPORE超纯水处理器等。
1.3 试验方法
1.3.1 色谱条件 色谱柱:Agilent Eclipse XDB-C18色谱柱,4.6 mm×150 mm,粒径5μm;流动相:0.02 mol/L磷酸氢二铵-乙腈(75∶25,V/V);流速:1.0 mL/min;检测波长:214 nm;柱温:30℃;进样量:10μL。
1.3.2 溶液的配制 精密称取林可霉素对照品20 mg,置25 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,作为对照品溶液。精密称取盐酸林可霉素可溶性粉供试品0.2 g,置25 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,滤过,作为供试品溶液。
1.3.3 线性试验 精密称取林可霉素对照品100 mg,置25 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,作为4 mg/mL贮备液。分别精密量取贮备液适量,用流动相分别稀释至浓度为0.1、0.2、0.4、0.8、1.6、2.0、2.4、4.0 mg/mL的溶液,各取10μL进样,记录色谱峰面积,以浓度(C,mg/mL)为横坐标,峰面积(mV)为纵坐标,绘制标准曲线。
1.3.4 专属性试验 按“1.3.1”色谱条件,分别取供试品辅料空白溶液、对照品溶液以及供试品溶液注入液相色谱仪,考察专属性。
1.3.5 精密度试验 精密吸取对照品溶液(林可霉素0.8 mg/mL)10μL,按“1.3.1”色谱条件,连续重复进样6次,记录色谱峰面积,计算相对标准偏差RSD,考察精密度。
1.3.6 稳定性试验 取同一供试品溶液(批号201905311)(林可霉素0.8 mg/mL),按“1.3.1”色谱条件,在不同时间(0、1、2、4、6、8、10、12、24 h)分别进样10μL,记录色谱峰面积,计算相对标准偏差RSD,考察稳定性。
1.3.7 重复性试验 精密吸取同一供试品溶液(批号201905311)(林 可 霉 素0.8 mg/mL)10μL,按“1.3.1”色谱条件,连续重复进样6次,记录色谱峰面积,计算相对标准偏差RSD,考察重复性。
1.3.8 回收率试验 配制10%的盐酸林可霉素可溶性粉,分别精密称取16、20和24 mg的林可霉素对照品及0.2 g的辅料置25 mL容量瓶中,加流动相溶解并稀释至刻度,摇匀,滤过,按“1.3.1”色谱条件进行测定,按外标法计算林可霉素的含量,计算回收率。
1.3.9 样品的测定 分别取同一厂家不同批号的盐酸林可霉素可溶性粉,按“1.3.1”色谱条件进行测定,每个样品制备2份,计算样品中林可霉素的含量,取平均值。同时与《兽药质量标准》(2017年版)化学药品卷的色谱条件比较。
2 结果与分析
2.1 线性试验
以浓度为横坐标,峰面积为纵坐标进行线性回归(图1),得回归方程:y=2×106x+473 55,R2=0.999 7。可见在此色谱条件下林可霉素在0.1~4.0 mg/mL范围内线性良好。

图1 林可霉素的线性回归
2.2 专属性试验
色谱图中林可霉素峰与各杂质峰分离效果好,含量测定不受其他杂质峰的干扰,色谱图见图2、图3、图4。

图2 林可霉素可溶性粉辅料空白溶液的HPLC图

图3 林可霉素对照品溶液(0.8 mg/mL)的HPLC图

图4 林可霉素可溶性粉供试品溶液(0.8 mg/mL)的HPLC图
2.3 精密度试验
连续进样6次,测得林可霉素峰面积平均值为1 841 314,RSD为0.3%。该方法表明精密度良好。
2.4 稳定性试验
在不同时间(0、1、2、4、6、8、10、12、24 h)分别进行测定,测得林可霉素峰面积平均值为1 886 971,RSD为0.4%,表明供试品溶液在室温下24 h内性质稳定。
2.5 重复性试验
连续进样6次,测得林可霉素峰面积平均值为1 890 536,RSD为0.2%,表明该方法重复性良好。
2.6 回收率试验
加样回收率考察结果见表1。结果表明,林可霉素峰平均回收率为99.5%,RSD为1.2%,表明该法符合试验分析要求,准确度高。

表1 盐酸林可霉素可溶性粉的回收率试验结果(n=9)
2.7 样品的测定
分别取同一厂家不同批号的样品,采用“1.3.1”色谱条件进行测定,试验结果见表2。样品测定结果中可以看出,该方法与其他两个色谱条件测定的结果基本一致。
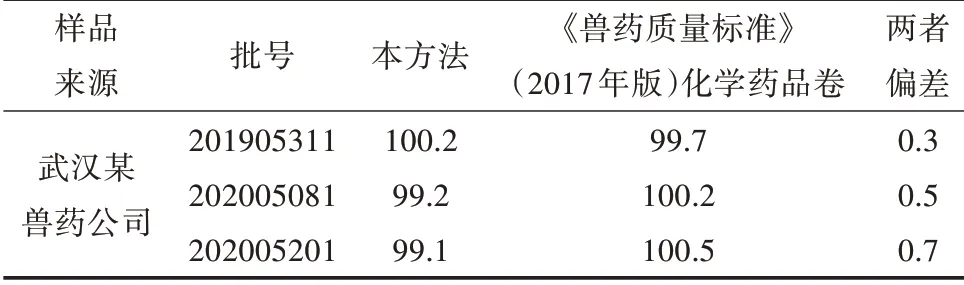
表2 样品含量测定结果(标示量//%,n=2)
2.8 耐用性
比较了InertSustain C18(4.6 mm×150 mm)和Agi⁃lent Eclipse XDB-C18(4.6 mm×150 mm)色谱柱。结果表明,两者均可使林可霉素分离度,理论塔板数良好,选择温度为25℃和35℃时,除出峰时间发生变化外,其余变化很小;将流动相水相和有机相比例调整为(70∶30,V/V)和(80∶20,V/V)进行测试,表明流动相比例的微调也仅能影响出峰时间,对峰形和理论塔板数影响甚小。不同品牌的色谱柱、不同流动相、有机相与水相比例以及不同温度,均能满足试验需要,该方法耐用性较好。
3 小结
在波长选择上,由于林可霉素在200 nm有最大吸收,但该处容易受溶剂干扰[10],因此本研究沿用《兽药质量标准》(2017年版)化学药品卷的214 nm作为检测波长。该方法测定盐酸林可霉素可溶性粉的含量,与《兽药质量标准》(2017年版)化学药品卷方法比较,结果基本一致。该方法使用了溶解性较好的磷酸氢二铵作为水相溶质,且配制流动相时不需要调节pH,缩短了时效,减少了盐溶液对色谱系统的污染,提高了色谱系统的稳定性,同时操作简便、快速,重现性好,专属性强,结果准确可靠,可作为该制剂的含量测定方法的参考,特别是在兽药企业内部质量控制方面也有一定的指导作用。

