康艾注射液干预乳腺癌的网络药理学研究
杨满英,陈雪珍,朱蓉,谢婷,胡金辉
1.湖南中医药大学,湖南 长沙 410208;2.湖南中医药大学第一附属医院,湖南 长沙 410007
乳腺癌是威胁女性健康的主要恶性肿瘤之一。研究表明,中医药制剂在改善乳腺癌患者症状、调控精神心理状态等方面具有明显的疗效。康艾注射液(以下简称“康艾”)作为临床应用广泛的中药抗肿瘤制剂[1],药物安全性及有效性明确,取得了较好的临床效果。康艾是由人参、黄芪、苦参中有效组分制成的中药制剂,其中最关键的成分是苦参素[1-3]。苦参素又称氧化苦参碱,有研究显示,其能够有效调节乳腺癌肿瘤细胞周期、促进肿瘤细胞凋亡、抑制肿瘤细胞的侵袭转移、逆转乳腺癌的多药耐药、调控肿瘤细胞的代谢水平等[4-5],进而达到抗肿瘤的效果。Lin 等[6]研究用氧化苦参碱介导人乳腺癌MCF-7 细胞Bax 和Bcl-2 的表达,可诱导乳腺癌细胞凋亡。临床亦有报道康艾可有效治疗乳腺癌[7-9]。本研究采用网络药理学方法探讨康艾治疗乳腺癌的潜在作用机制,为临床应用提供依据。
1 资料与方法
1.1 康艾注射液活性成分收集与筛选
通过中药系统药理学数据库与分析平台( TCMSP , http://www.tcmsp.com/tcmsp.php ) 和SwissTargetPrediction 数据库(http://www.swisstarget prediction.ch/)检索人参、黄芪、苦参的活性成分,获取分子信息,包括活性成分的分子名称、口服生物利用度(OB)、类药性(DL)等。以OB≥30%和DL≥0.18 为条件筛选主要活性成分。
1.2 康艾注射液活性成分相关靶蛋白获取
根据筛选得到的活性成分,在TCMSP 中点击“ Related Targets ” , 获取成分的“ Targets Information”,得到该成分作用的靶蛋白名。在UniProt(http://www.uniprot.org/)中,使用UniProt KB 检索功能,在检索框中输入靶蛋白名,检索条件为“organism: homo sapiens”和“reviewed: yes”,获取基因名称和UniProt ID。
1.3 康艾注射液治疗乳腺癌靶点收集
通过GeneCards数据库( http://www.genecards.org/ ) 和 OMIM 数据库(http://www.omin.org/),以“breast cancer”为关键词检索乳腺癌相关基因和蛋白靶点信息,根据Relevance score≥9.67 筛选核心基因。借助R 语言,获得康艾活性成分靶蛋白与乳腺癌靶蛋白的交集靶点。
1.4 中药-活性成分-靶点网络构建
使用Cytoscape3.6.1 软件构建康艾治疗乳腺癌的“中药-活性成分-靶点”网络,图中以“节点”(node)表示活性成分和靶点基因,用“边”(edge)表示两者之间的关系,并进行网络特征分析,以筛选其中较为重要的活性成分。
1.5 交集基因蛋白相互作用网络构建与核心靶点筛选
通过STRING 数据库(https://string-db.org/),点击“Multiple Proteins”,限定物种为人,获取交集基因的蛋白相互作用(PPI)网络。对数据进行预读后设置置信度为0.9,隐藏孤立蛋白,将数据导入Cytoscape3.6.1 软件绘制交集靶点网络图,进行网络拓扑结构分析,以节点degree 值反映基因作用大小,依据degree≥19 和介度中心性≥0.022,获得核心靶点。
1.6 GO 功能与KEGG 通路富集分析
将交集靶点导入Metascape平台(http://metascape.org/)进行分析,设置物种为“Homo Sapiens”,进行GO 功能和KEGG 通路富集分析。
1.7 分子对接
为进一步验证活性成分与蛋白靶点之间的结合活性,选取“中药-活性成分-靶点”网络中degree值排前3 位的活性成分,与PPI 网络筛选出的核心靶点进行分子对接。 在 PDB 数据库(http://www.rcsb.org/)中下载靶点的3D 结构,保存为“.pdb”格式文件,在TCMSP 中下载化合物的“.mol2”格式文件。在AutoDock1.5.6 软件中导入靶点和化合物的结构文件,经过去水、加氢、分配电荷等处理,运用Grid 模块设置蛋白原配体为对接盒子中心,将准备好的蛋白文件、配体文件、化合物文件及脚本放入相应文件夹,利用AutodockVina1.1.2 分子模拟软件进行分子对接,并使用Discovery Studio(2016 版)绘制最佳匹配结果图。
2 结果
2.1 康艾注射液活性成分及治疗乳腺癌靶点筛选
通过TCMSP 和SwissTargetPrediction 及相关文献补充检索,以OB≥30%、DL≥0.18 为条件筛选得到黄芪、人参、苦参活性成分共43 个,其中黄芪20 个、人参22 个,苦参1 个,见表1。利用UniProt 数据库选取活性成分对应的靶点,其中共有22 个活性成分未能查到对应靶点基因,删除重复项目后获得靶点295 个。通过GeneCards、OMIM 数据库收集到乳腺癌相关靶点并筛选核心基因共3670个,将康艾和乳腺癌相关靶点进行映射并取交集得到204 个交集靶点,即康艾治疗乳腺癌的潜在作用靶点,见图1。

图1 康艾-乳腺癌基因靶点韦恩图

表1 康艾注射液活性成分基本信息

续表1
2.2 中药-活性成分-靶点网络
使用Cytoscape3.6.1 软件绘制康艾治疗乳腺癌的中药-活性成分-靶点网络,见图2。该网络图可直观反映康艾通过多成分、多靶点治疗乳腺癌的作用机制。运用CytoNCA 插件对网络进行分析,根据degree 排序,主要活性成分有氧化苦参碱、槲皮素、山柰酚、豆甾醇、β-谷甾醇、异鼠李素、常春藤皂苷元、佳罗醇等。

图2 康艾注射液治疗乳腺癌中药-活性成分-靶点网络
2.3 蛋白相互作用网络
将交集基因上传至STRING,设置信度为高置信度(0.9),得到 PPI 网络图,将结果导入Cytoscape3.6.1 进行网络可视化,见图3。网络图中包含 174 个节点、853 条边,使用“network analyzer”功能计算degree 值,用CytoNCA 对网络进行拓扑分析,根据degree 值大小排序,颜色越深,节点越大,说明该靶点在治疗中的作用越大。排名前5 位的靶点分别为MAPK1、AKT1、JUN、TP53(即P53)、 ESR1。

图3 康艾注射液治疗乳腺癌作用靶点PPI 网络
2.4 GO 功能富集分析
将204 个交集靶点导入Metascape 平台进行生物过程(Biological Process,BP)、细胞成分(Cellular Component,CC)、分子功能(Molecular Function,MF)富集分析。GO 功能富集分别得到BP、CC、MF 各10 项(见图4),BP 主要涉及对毒性物质的应答(response to toxic substance)、细胞脂质反应(cellular response to lipid)、脂多糖反应(response to lipopolysaccharide)等,CC 有膜筏(membrane raft)、细胞外基质(extracellular matrix)、转录因子复合体(transcription factor complex)等,MF 有转录因子结合(transcription factor binding)、核受体活性(nuclear receptor activity)、蛋白结构特异性结合(protein domain specific binding)等。
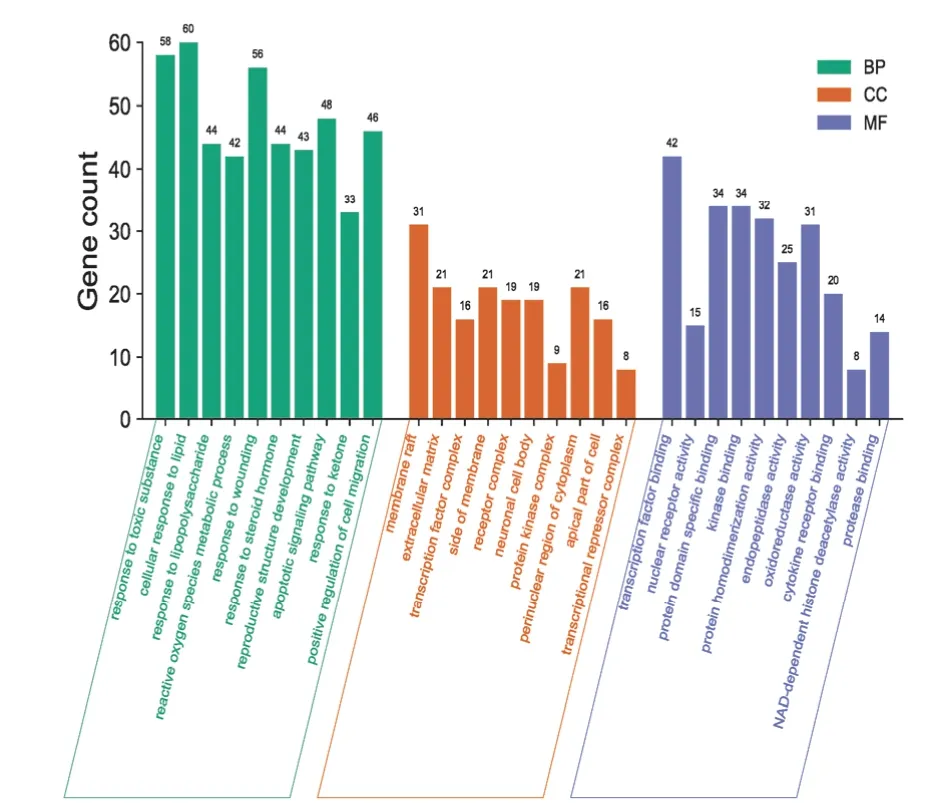
图4 康艾注射液治疗乳腺癌靶点GO 功能富集分析
2.5 KEGG 通路富集分析
将上述204 个交集靶点在Metascape 平台进行KEGG 通路富集分析,获得康艾治疗乳腺癌的20 条信号通路,其中关键通路有TNF 信号通路、MAPK信号通路、铂类药物耐药信号通路、肿瘤糖代谢、细胞衰老、JAK-STAT 信号通路、FOXO 信号通路、雌激素信号通路等。见图5。

图5 康艾注射液治疗乳腺癌靶点KEGG 通路富集分析
2.6 分子对接
根据度值、介度中心性从PPI 网络中筛选得到排名前 5 位核心靶点 MAPK1、AKT1、JUN、TP53、ESR1 作为治疗乳腺癌的潜在靶点,与中药-活性成分-靶点网络中度值排名前3 位的活性成分氧化苦参碱(oxymatrine)、槲皮素(quercetin)、山柰酚(kaempferol)进行分子对接,评分见图6;分子对接结合能<-5 时,认为药物和靶点蛋白结合稳定,可起到治疗作用。靶点蛋白和化合物的结合能均小于-5,表明受体和配体结合能力高。Vina Score 评分显示山柰酚、氧化苦参碱和JUN 靶点结合能最低,说明山柰酚、氧化苦参碱和JUN 的结合活性最强;槲皮素的最佳结合靶点是MAPK1,见图7~图9。

图6 分子对接Vina Scroe 热图

图7 槲皮素-MAPK1 分子对接模型及受体-蛋白质2D 结合图

图7 山柰酚-JUN 分子对接模型及受体-蛋白质2D 结合图

图8 氧化苦参碱-JUN 分子对接模型及受体-蛋白质2D 结合图
3 讨论
随着对乳腺癌发病及治疗相关机制的研究不断深入,其病理机制逐渐被揭示。现代医学认为,乳腺癌的形成机制包括肿瘤雌激素受体机制、干细胞形成机制及炎性刺激相关机制等。在治疗方面,较长时间的西药治疗易出现各类临床不良反应且易复发。隋代医家巢元方有云:“积聚者,由寒气在内所生也。血气虚弱,风邪搏于腑脏,寒多则气涩,气涩则生积聚也。”《医宗必读•积聚》记载“积之成者,正气不足,而后邪气居之”。乳腺癌在中医又称为“乳岩”“乳石痈”“翻花乳”等。中医认为乳腺癌的病机以气血亏虚为本,气滞血瘀、痰火毒结为标,整体属虚,局部属实,虚实夹杂[10]。手术治疗易内耗气血,致气血更亏;化疗、放疗更为攻伐之术,驱邪同时也损伤正气,灼伤阴津。故中医治疗时多以扶正祛邪为治疗大法,兼顾养阴。康艾具有益气养阴、扶正抗癌的作用,初始研究多用以治疗肝癌、肺癌、结肠癌、妇科相关恶性肿瘤,或化疗后导致的骨髓抑制、白细胞减少症;从中医辨证论治角度看,康艾配方基础契合乳腺癌“益气养阴、扶正抗癌”的治疗原则,且近年来,临床上把康艾扩展运用于治疗手术后化疗患者亦取得良好的临床效果。
网络药理学网状式地阐述药物有效成分与疾病各个靶点的内在关系,这与中药复方多成分、多途径、多靶点协同作用原理不谋而合[11-13]。本研究分析显示,康艾关键成分为氧化苦参碱、槲皮素、山柰酚、异鼠李素、β-谷甾醇、人参皂苷等成分起到协同作用。槲皮素、山柰酚属于植物来源的黄酮类化合物,是一类具有抗癌活性且毒副作用小的天然多酚类化合物[14]。槲皮素、山柰酚抗乳腺癌机制包括阻滞细胞周期[15-18]、促进细胞凋亡[19-21]、抑制侵袭转移[22]、调节肿瘤细胞糖代谢[21,23]、化疗增敏及逆转耐药[19,24-25]抑制乳腺癌细胞的生长与增殖。氧化苦参碱不仅具有类黄酮类化合物的抗癌活性,还能诱导癌细胞发生自噬[26],但其对乳腺癌细胞的自噬作用目前暂未见报道。
康艾治疗乳腺癌主要作用蛋白为 MAPK1、AKT1、JUN、TP53、ESR1。MAPK1 属于丝裂原活化蛋白激酶家族,MAPK 在乳腺癌中被明显激活,持续活化最终导致细胞的增殖和恶性转化。邵建斌等[27]体外实验研究显示,miR-198 靶向MAPK1 能抑制人乳腺癌MCF-7 细胞的增殖并促进其凋亡。本研究分子对接中3 种核心有效成分与MAPK1 结合活性仅次于最高结合点JUN,说明康艾有效成分能稳定结合在乳腺癌MAPK1 靶点上,起到治疗作用。AKT1 又称蛋白激酶B,是PI3K/AKT 信号通路中重要的下游靶标,参与的生物过程包括调控细胞存活、代谢、生长、增殖、转录及蛋白质合成。Li等[28]研究表明,大黄素干扰AKT1 介导的DNA 损伤并降低乳腺癌细胞对化疗药物的耐药性。Capivasertib(AZD5363)是一个高选择性的AKT1-3 亚型抑制剂,一项双盲、随机临床试验表明,Capivasertib 联合紫杉醇治疗三阴性乳腺癌,其治疗效果使无进展生存期增加1 倍以上,且显著提高客观缓解率和总生存期[29]。JUN 属于激活蛋白(AP-1)的蛋白家族之一,当受到细胞张力变化、DNA损伤、氧化应激、紫外线照射、细菌及病毒感染等刺激时,活化后的AP-1 作为转录因子参与调控细胞增殖、分化和凋亡等生物过程。Song 等[30]研究发现,AP-1 在三阴性乳腺癌中高表达,靶向阻断AP-1 家族蛋白成员可增加三阴性乳腺癌患者对PARP 抑制剂的敏感性。癌症患者对化疗药物不敏感或耐药是临床治疗重大难题之一,康艾关键有效成分氧化苦参碱、槲皮素、山柰酚均被证实具有化疗增敏及逆转耐药的作用[4,15,31]。分子对接结果显示,氧化苦参碱、山柰酚与JUN 有最佳的对接结果,说明康艾不仅有抗乳腺癌效果,联合化疗药还起到化疗增敏及减少耐药的作用,与多项临床观察实验[7,9]得出结论一致。突变后的P53 失去原有的抑癌功能,对细胞的生长失去调控作用,Rong 等[32]对958 例转移性乳腺癌患者的血液标本进行ctDNA 检测,发现突变肿瘤基因P53 约54%,P53 与较差的临床结局相关。
GO 功能富集分析显示,康艾干预乳腺癌细胞膜筏、细胞外基质、转录因子复合体。膜筏主要生物功能有信息传导、膜组分分迭、腺癌细胞的定向迁移等[33]。肿瘤细胞的侵袭转移是影响恶性肿瘤预后及总生存(OS)的关键因素,细胞外基质是阻止肿瘤转移的重要组织屏障,一项系统评价分析表明,MMP2、MMP9 过度表达与不良OS 相关,细胞外基质在癌症患者生存期发挥重要角色[34]。转录因子对基因的表达起抑制或增强作用,陆慧敏等[35]研究发现三七总皂苷可激活AP-1,对4T1 乳腺癌模型小鼠有抑制作用。说明康艾治疗乳腺癌可能和转录因子对相关通路靶点的调控相关。
KEGG 通路富集分析显示,MAPK 信号通路起到主要作用。通路之间相互交叉,又相互作用,其治疗特点是在乳腺癌通路网路上多位点阻滞或激活,相比单一靶点的药物,或许能得到更好的疗效。
综上所述,本研究揭示了康艾治疗乳腺癌的主要活性成分为氧化苦参碱、槲皮素、山柰酚,涉及的关键分子功能有转录因子结合、核受体活性、蛋白结构特异性结合,其参与的作用机制主要与MAPK 通路相关,提示康艾治疗乳腺癌有效物质-关键靶点作用的网络关系,为进一步的药效物质研究及作用机制研究提供方向。
本研究仍存在不足之处,网络药理学所得到的有效成分及靶点均从数据库中匹配信息得到,但目前现有的中药数据库对收集药物的信息存在差异性,代谢分布不统一,中药的生物利用度、组织分布等无法客观量化等,因此本研究下一步将依据网络药理学预测的药物物质基础和通路展开实验验证研究。

