低氧分压下PtO2的分解机理研究
朱天梦, 潘家荣, 孙建平, 李 婷, 李 旭, 王成科
(1.中国计量大学,浙江 杭州 310018; 2.中国计量科学研究院,北京 100029)
1 引 言
标准铂电阻温度计(standard platinum resistance thermometer,SPRT)是现行90国际温标(ITS-90)中规定的重要内插仪器之一,也是实现温标量值传递的必要仪器。在温度计的使用过程中,作为SPRT传感元件的铂丝会在不同热工况与氧气分压的影响下发生氧化分解反应,影响温度计的稳定性[1~3]。为持续推进ITS-90国际温标的完善与发展,基于微观层面开展提升SPRT测温性能的氧化分解特性研究已成为当前重要议题之一。
SPRT的结构是将纯度为99.999%的铂丝均匀缠绕在石英骨架上并置于密封绝缘套管中,向套管内填充氧气与惰性气体(氦气或氩气)组成的混合气,最高工作温度下的氧气分压约为5~10 kPa。氧气的充入能有效避免测温元件组件材料及外界带入的微量杂质污染铂丝,但同时也会使铂丝发生氧化及分解反应,影响温度计的稳定性。Berry R J最先提出了铂的氧化模型:随着温度升高,铂与氧气反应依次生成二维或三维PtO2[4~6],氧化物的生成会使铂电阻温度计阻值升高,氧化物分解则会使温度计阻值降低[7],三维PtO2的生成和分解温度与氧气分压呈正相关[4]。Sakurai H等认为铂的氧化产物为PtO2和PtO[8,9]。德国PTB和中国NIM分别开展了在合成空气中PtO2分解温度的研究,认为在580~600 ℃下,PtO2开始分解,低氧环境下分解温度提前;800~830 ℃下PtO开始分解,低氧环境下氧化和分解过程均会被强烈抑制[2,3,10]。上述研究详细论述了空气环境下铂的氧化和分解过程及其对温度计阻值变化趋势的影响,然而,针对低氧分压下铂的氧化还原机理依然缺少较为一致的阐述和系统全面的研究,且已有的氧化分解模型尚未通过微观实验给予证实。
本文采用差示量热法与X射线光电子能谱分析,开展了铂的主要氧化产物在氧气分压10 kPa和 3 kPa下微观分解机理的研究,参考当前国际通用的标准铂电阻温度计制作方法,以明确氧气分压和温度对SPRT性能的影响,优化和完善SPRT的制作工艺,进一步提高SPRT的测量稳定性,为铂电阻温度计计量检定规程的修订提供数据参考和理论支持。
2 实验原理及样品制备
相对于其它金属,铂具备较强的抗氧化特征,正向氧化实验耗时长,因此本文选择了样品纯度为95%的PtO2粉末为研究对象,开展氧化铂的分解逆向实验研究。实验用电子天平称取样品放置于差示量热扫描仪(differential calorimetry scanner,DSC)的待测样品端,参比端使用氧化铝材质空坩埚,向仪器加热炉内以一定的气体吹扫率通入氧气与氩气的合成气体,测试时加热炉以设定的速率升温至不同温度点,得到在不同氧压和温度下的粉体样品及加热过程中的热流曲线。
受氧化铝坩埚和使用气氛导热性能的影响,测量温度tm与样品实际温度ts之间会产生一定程度的偏差Δt,因此在实际测量中需对tm进行信号校正(扣除Δt)后才能得到样品真实温度ts[12]。信号校正即温度和热焓校正。本文选取5种已知熔点的金属标准物质进行测定,见表1,得到实测熔点值与已知熔点值之间的偏差Δti,绘制Δti-t散点图并做拟合曲线,最终得到DSC校正曲线,见图1。校正后的温度误差为0.5 ℃。

表1 金属标准物质理论熔点与实测熔点值对照Tab.1 Comparison of theoretical melting point and measured melting point value of standard metal materials ℃

图1 DSC测试温度校正拟合曲线Fig.1 DSC test temperature correction fitting curve
将DSC加热后获得的粉体样品制成压片粘贴在X射线光电子能谱仪(X-ray photoelectron spectroscopy, XPS)测试样品台上,如图2所示。使用Thermo Escalab 250XI型XPS观测PtO2样品表面的元素种类、化学价态以及相对含量。X射线源为单色化Al靶,灵敏度1×106cps,发射电压15 kV,靶功率150 W,XPS光电子谱的获得采用Al Kα(能量为1 486.68 eV)的X射线光源,采用脉冲计数模式,通能为20.00 eV。

图2 XPS测试样品台及PtO2压片Fig.2 XPS test sample table and PtO2
不同元素的原子轨道具有不同的结合能,由此可以定性物质的元素种类。当铂原子与氧原子形成共价键后,原子所处化学环境不同,其内壳层电子结合能会发生变化,产生化学位移,在谱图上表现为谱峰位移。一般地,氧化作用使内层电子结合能上升,氧化中失电子越多,上升幅度越大[13,14]。因此根据能谱图中谱峰的横坐标位置(结合能)即可鉴定元素的组成及其化学价态,查阅美国国家标准技术研究院NIST X射线光电子能谱数据库获得4f 5/2和4f 7/2轨道的铂及其氧化物的电子结合能数据,见表2[15]。为避免因操作方法和仪器自身产生的误差,在实验前首先选取高纯铂片和PtO2进行XPS测试,分别获取2项谱图(见图3、4)。

表2 铂及其氧化物的电子结合能Tab.2 Electron binding energy of platinum oxide eV
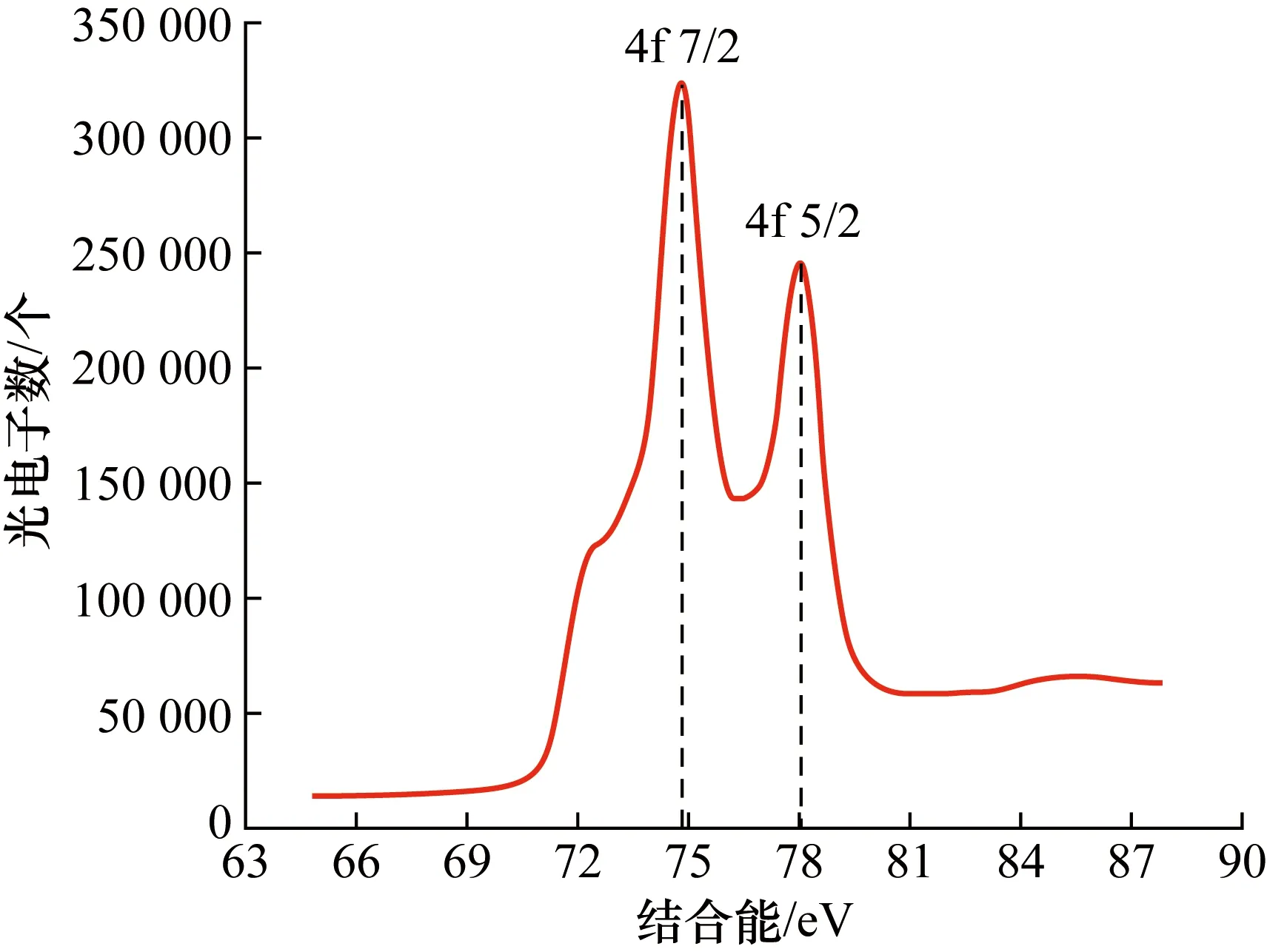
图3 PtO2的4f轨道电子能谱Fig.3 The electron energy spectrum of 4f orbit of PtO2

图4 Pt的4f轨道电子能谱Fig.4 The electron energy spectrum of 4f orbit of Pt
并将表3中数据与文献数据进行比对。通过对高纯铂片和PtO2样品的XPS谱图分析可知:Pt的4f轨道结合能分别为71.1 eV和74.5 eV;PtO2的4f轨道结合能分别为78.1 eV和74.8 eV,与文献查得数据最大误差为0.4 eV,实验结果可靠。

表3 实验获得铂及其氧化物的电子结合能Tab.3 Experimentally obtain the electron binding energy of platinum and its oxide eV
3 实验及分析
3.1 不同氧气分压下PtO2的DSC热流曲线
将高纯PtO2粉末样品称重20 mg置于DSC中,分别向加热炉内通入氧气与氩气的合成气体,氧气分压分别为21,10,3 kPa。测试时气体吹扫速率为1.6 mL/min,设置10 ℃/min的速率从20 ℃线性升温至1 000 ℃,获得不同氧气分压下的热流曲线见图5~图7所示。
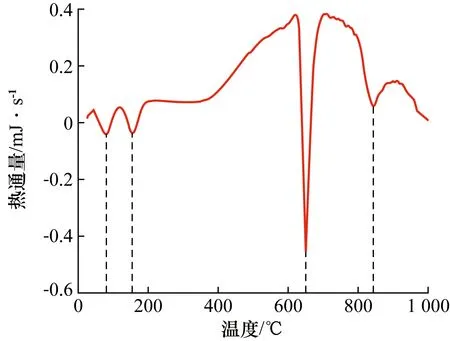
图5 氧分压21 kPa下PtO2的热流曲线Fig.5 Heat flow curve of PtO2 at the oxygen partial pressure of 21 kPa

图6 氧分压10 kPa下PtO2的热流曲线Fig.6 Heat flow curve of PtO2 at the oxygen partial pressure of 10 kPa

图7 氧分压3 kPa下PtO2的热流曲线Fig.7 Heat flow curve of PtO2 at the oxygen partial pressure of 3 kPa
3条曲线中均出现了4个明显的吸热峰,其中第1个峰出现在100 ℃附近,判断是由于样品暴露在空气中吸附了水分子,当温度接近100 ℃时水分蒸发而产生吸热过程;第2个峰出现在150 ℃附近,分析由于升温过程中坩埚吸收了部分能量。第3个峰表现出较强的吸热过程,氧分压为21 kPa时,峰值对应温度为650 ℃;氧分压为10 kPa时,峰值对应温度为630 ℃;氧分压为3 kPa时,峰值对应温度为610 ℃。第4个峰同样表现出较为明显的吸热过程,氧分压为21 kPa时,峰值对应温度为840 ℃;氧分压为10 kPa时,峰值对应温度为820 ℃;氧分压为3 kPa时,峰值对应温度为780 ℃。
在PtO2的加热过程中,随着温度升高,热流曲线反应出了两段明显的分解吸热过程,并且峰值温度附近的反应速率最大。根据文献[8,9]中提出铂氧化分解的反应路径:Pt→PtO2→PtO可判断,600 ℃附近主要为PtO2分解,800 ℃附近主要为PtO分解。由图8可以看出,氧气分压对于2种氧化物的分解峰值温度具有明显影响。

图8 氧化物分解温度随氧气分压变化曲线Fig.8 Oxide decomposition temperature change curve with oxygen partial pressure
3.2 不同氧气分压下PtO2的XPS实验
图9为氧气分压10 kPa下,PtO2粉末样品在各个温度点下加热维持8 h后Pt元素的XPS曲线。图10为氧气分压10 kPa下,PtO2粉末样品在各个温度点下加热维持8 h后O元素的XPS曲线。由图可知:550 ℃以下样品加热后的峰位与未经处理的原始样品峰位保持基本一致,Pt元素电子结合能分别位于74.9 eV和78.2 eV左右,根据文献[15],4f 7/2轨道74.9 eV附近的信号与4f 5/2轨道78.2 eV附近的信号均为Pt2+。另外O的电子结合能位于531.0 eV左右,也没有表现出明显的变化趋势,因此在氧气分压10 kPa的气氛环境下,低于550 ℃时PtO2基本不发生分解。当温度升高至570 ℃,Pt元素的谱峰增加,分峰处理后获得电子结合能分别为:74.9 eV、78.2 eV;72.0 eV、76.5 eV,其中72.0 eV的4f 7/2信号对应为Pt单质,76.5 eV的4f 5/2信号对应为Pt+,74.9 eV、78.2 eV的信号对应为Pt2+,同时O1s轨道信号经分峰后的结合能为530.5 eV和531.8 eV,表明了此时PtO2已经分解,样品中存在分解产物Pt单质、少量PtO以及未完全反应的PtO2。

图9 氧气分压10 kPa时PtO2原样于不同温度下加热8 h的Pt元素XPS谱Fig.9 XPS spectra of Pt element when PtO2 is heated at different temperatures for 8 h at the oxygen partial pressure of 10 kPa

图10 氧气分压10 kPa时PtO2原样于不同温度下加热8 h的O元素XPS谱Fig.10 XPS spectra of O element when PtO2 is heated at different temperatures for 8 h at the oxygen partial pressure of 10 kPa
氧气分压3 kPa时PtO2在不同温度下加热维持8 h的XPS曲线见图11、图12所示,与10 kPa不同的是,Pt元素谱峰的增加和位移在540 ℃时已经出现,分峰处理后各峰值相应的电子结合能分别为:74.9 eV、78.1 eV;72.7 eV、71.6 eV,其中71.6 eV的4f 7/2信号和74.9 eV的4f 5/2信号对应为Pt单质,72.7 eV的4f 7/2信号对应为Pt+,78.1 eV对应为Pt2+,O1s轨道信号经分峰后的结合能为530.6 eV和532.3 eV,表明此时PtO2已经分解为PtO和Pt 单质。

图11 氧气分压3 kPa时PtO2原样于不同温度下加热8 h的Pt元素XPS谱Fig.11 XPS spectra of Pt element when PtO2 is heated at different temperatures for 8 h at the oxygen partial pressure of 3 kPa

图12 氧气分压3 kPa时PtO2原样于不同温度下加热8 h的O元素XPS谱Fig.12 XPS spectra of O element when PtO2 is heated at different temperatures for 8 h at the oxygen partial pressure of 3 kPa
图13为氧气分压3 kPa下,PtO2原样在500 ℃下加热24 h后的XPS曲线,由图可知,曲线的峰位和结构均未发生明显变化,表明在此条件下PtO2基本不发生分解反应。

图13 氧气分压3 kPa时PtO2原样在500 ℃下不同加热时间的Pt元素谱Fig.13 Pt element spectrum of PtO2 at 500 ℃ for different heating time at the oxygen partial pressure of 3 kPa
图14为氧气分压3 kPa下,PtO2原样在520 ℃下加热不同时间,XPS测试得到的Pt元素曲线,可以看出:520 ℃下加热8 h,Pt4f轨道对应结合能分别位于75.0 eV和78.2 eV,表明此时样品中主要为PtO2,基本没有发生分解反应,图中峰值的相对位移可能是由于测量位置变化而造成的。随着加热时间延长,PtO2对应谱峰强度逐渐减弱,位于72.5 eV处的谱峰逐渐增强,同时71.3 eV附近也出现了明显的肩峰,表明此时PtO2开始分解,样品中含有大量分解产物PtO和少量Pt单质。

图14 氧气分压3 kPa时PtO2原样在520 ℃下不同加热时间的Pt元素谱Fig.14 Pt element spectrum of PtO2 at 520 ℃ for different heating time at the oxygen partial pressure of 3 kPa
图15在氧气分压3 kPa下,PtO2原样在高于起始分解温度之上的3个不同温度下加热8 h的XPS曲线,其中4个较为明显的谱峰分别位于70.8、72.1、74.2,77.6 eV附近。其中接近70.8 eV的信号表明了Pt单质的存在,接近72.1 eV和74.2 eV的信号表明了PtO的存在,接近77.6 eV的信号则表明样品中仍然含有部分PtO2。另外,根据谱峰强度还可以判断,在565 ℃以下,PtO2谱峰较强,表明样品中未反应的PtO2较多,565 ℃以上,PtO的谱峰强度相比Pt开始逐渐减弱,表明生成PtO的速度开始减缓。因此认为在氧气分压3 kPa下565 ℃附近为PtO的最佳生成温度。

图15 氧气分压3 kPa时PtO2原样在不同温度下加热8 h的Pt元素谱Fig.15 Pt element spectrum of PtO2 is heated at different temperatures for 8 h at the oxygen partial pressure of 3 kPa
综上所述:PtO2的分解产物为PtO和Pt单质。在氧气分压为10 kPa下,低于550 ℃ PtO2基本不发生分解,当温度升高至570 ℃附近时,PtO2已经完全分解为Pt以及少量的PtO。当氧气分压降低至 3 kPa时,在520 ℃附近PtO2开始缓慢分解,在此温度下反应程度随着时间的延长而不断加深,24 h内仍然持续分解,另外,PtO的最佳生成温度在565 ℃附近,高于此温度分解生成Pt的速率快于PtO。
由此可见,氧气分压对PtO2由氧化态到还原态的转变温度有明显的促进作用,PtO的生成和分解温度也会随氧分压的减小而提前。SPRT检定规程JJG160-2007中规定,使用在600 ℃以上的温度计需在660 ℃退火,而使用在600 ℃以下的温度计在600 ℃退火[16]。660 ℃的退火温度会使PtO更易分解,导致SPRT阻值减小,而600 ℃的退火温度会由于不同的氧气分压造成PtO2的分解程度不同,进而使SPRT阻值发生改变。2种铂氧化物的状态共同影响着铂电阻温度计的阻值,因此在实际工作中,需考虑绝缘套管内填充的氧气比例,选择不同的退火温度、划分温度计的工作温区,以此保证温度计的长期稳定性。
4 总 结
采用差示量热扫描法和X射线光电子能谱共同分析了铂氧化物在1 000 ℃内的分解过程,研究了在不同氧气分压下氧化物的分解机理。由DSC热流曲线可以看出铂氧化物的分解主要包括两步:PtO2的分解和PtO的分解,氧气分压由21 kPa降低至3 kPa的过程中,2种氧化物的分解温度对氧气分压的依赖较为明显。在氧分压为10 kPa下570 ℃附近,PtO2基本已经完全分解为Pt单质和PtO;在氧分压为3 kPa下PtO2的起始分解温度约为520 ℃。根据XPS曲线可知,在PtO2的分解过程中会持续生成少量的PtO,3 kPa时,565 ℃以上PtO2大量分解为Pt单质,并且当温度达到585 ℃时,PtO2分解为Pt的速度达到最快。
PtO的来源有两种途径:PtO2的分解与高温下Pt的直接氧化[9]。考虑到PtO自身的不稳定性,在PtO2的分解过程中,也可能伴随着PtO的部分分解,这同样会对铂电阻温度计在400 ℃~600 ℃温区内的阻值造成影响。在评估温度计的性能时,需要考虑不同氧气分压下铂氧化物分解与氧化温度的变化;温度计工作过程中产生的氧化层则可通过在不同温度下退火使其分解,由此保证SPRT的稳定性[17,18]。研究结果还可为铂电阻温度计的制作工艺、计量检定规程的完善提供数据参考和理论支持。

