Ag,O共掺实现p型氮化铝纳米管电子结构的第一性原理研究
熊明姚,张 锐,文杜林,苏 欣
(1.伊犁师范大学物理科学与技术学院,伊宁 835000;2.伊犁师范大学新疆凝聚态相变与微结构实验室,伊宁 835000)
0 引 言
AlN是一种宽带隙半导体材料,在室温下直接带隙为6.2 eV,具有良好的光学、电学特性[1-2]。这些优异的性能使AlN成为一种很有前景的材料,被广泛应用于发光二极管、激光二极管、光电探测器和太阳能电池等领域[3-6]。
自碳纳米管被Iijima[7]发现以来,碳纳米管以其独特的结构、电学性能引起了人们的广泛关注[8-9]。在此背景下,科研工作者们提出了元素周期表中第三主族(Ⅲ:B、Al和Ga)和第五主族(V:N、P和As)基团的对应原子作为碳纳米管的可能替代品[10-12]。Hao等[13]和Zhao等[14]对(6, 0)氮化铝纳米管的电子结构进行了研究,虽然得到的氮化铝纳米管的带隙不同,但最终计算结果都表明(6, 0)氮化铝纳米管是直接带隙。
通过掺杂金属和非金属原子对氮化铝纳米管进行化学修饰能够有效地改善其电学性能。如Baei等[15]研究发现非金属Si分别取代(6, 0)氮化铝纳米管中的Al和N表现出n型和p型半导体特性且导电性能得以提高。Zhang等[16]采用3d过渡金属掺杂氮化铝纳米管,发现经过V和Ni修饰的(5, 5)和(8, 0)氮化铝纳米管具有半金属特性。袁娣等[17]研究了金属Ag和非金属S共掺氮化铝,发现共掺能够实现高浓度的p型氮化铝。Huang等[18]研究了金属Mg与非金属O共掺氮化铝纳米管,发现O的存在可以大大提高氮化铝纳米管中Mg的掺杂效率,且价带顶的电荷分布具有p型特征,有助于实现高效的p型氮化铝纳米管。再参照其他p型纳米管的研究结果[19-21],氮化铝纳米管的p型掺杂问题如果能够得以解决将大大扩展其应用范围。获得p型氮化铝纳米管对于其在纳米尺度电子器件中的应用是非常重要的,这样只需在一根纳米管上便可实现p-n结或p型纳米尺度场效应晶体管等,进而形成更加复杂的器件结构。本文利用基于密度泛函理论的第一性原理对Ag-O共掺氮化铝纳米管的电子结构和p型特性进行一定的理论实践,期望能够成为一种制备p型氮化铝纳米管的有效方法并促进氮化铝纳米材料在光电器件领域的研究工作。
1 理论模型与计算方法
采用(6, 0)氮化铝纳米管的原胞,共包含72个原子的1×1×3超胞如图1所示,为避免纳米管之间相互影响,建立1 nm的真空层。Ag和O原子替代图中标记Al和N原子的位置。用一个Ag替代图中的Al原子,形成Ag掺杂氮化铝纳米管体系,再用一个O替代一个N原子,形成Ag-O共掺氮化铝纳米管体系。本文采用Materials Studio软件中的CASTEP[22]模块完成。几何结构优化的截断能为400 eV,自洽精度(SCF)为1.0×10-6eV/atom。电子间相互作用的交换关联能采用广义梯度近似(generalized gradient approximation, GGA)的PBE[23](Perdow Burke Emzerhof, PBE)方案处理,最外层电子和离子实间的相互作用势选择超软赝势[24](ultrasoft pseudopotential, USP),K点采用1×1×7进行设置。迭代时收敛精度为1×10-5eV/atom,作用到原子上的力小于0.3 eV/nm,内应力收敛精度为0.05 GPa,最大位移收敛精度为1×10-4nm。
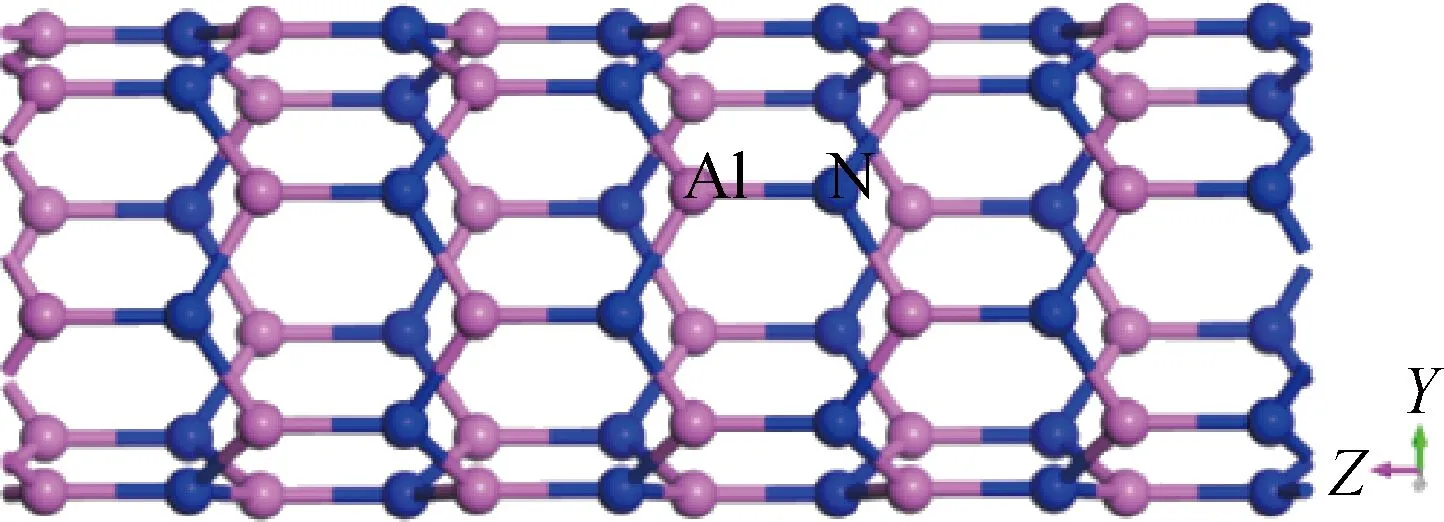
图1 氮化铝纳米管超胞模型Fig.1 Supercell model of AlN nanotubes
2 结果与讨论
2.1 几何结构优化结果
计算所得相应体系的总能量、形成能、禁带宽度以及跃迁形式如表1所示。其中,E为体系的总能量,Ef为形成能,Eg是禁带宽度。跃迁形式可分为直接跃迁和间接跃迁[25]。形成能Ef可以判断形成单掺和共掺体系的相对难易程度。
Ag单掺、Ag-O共掺体系的计算公式分别为:
Ef(AlN,Ag)=EAlN,Ag-EAlN-μAg+μAl
(1)
Ef(AlN,Ag,O)=EAlN,Ag,O-EAlN-μAg-μO+μAl+μN
(2)
式中:EAlN、EAlN,Ag和EAlN,Ag,O分别为本征、单掺和共掺体系的总能量,μX(X=Ag,Al,O,N)分别表示Ag、Al、O以及N原子在T=0所对应的化学势大小。在实验上制备氮化铝材料时,制备条件会在富Al(Al-rich)和富N(N-rich)之间发生变化,对Al-rich和N-rich两种极端情况进行了研究,这也是缺陷计算中常用的方式[26],结果如表1所示。在Al-rich条件,Al的化学势:μAl=μAl(bulk)=EAl(bulk),而N-rich条件,N的化学势:μN=μN(molecule)=1/2EN2。其中,EAl(bulk)和EN2分别为一个 Al原子在Al块材和氮气分子放置在(1.5 nm×1.5 nm×1.5 nm)的立方体中的总能量[27]。而正形成能代表了材料的不稳定性,表明在平衡条件下复合生长较为困难。从表1可以看出,Ag单掺和Ag-O共掺在N-rich条件下的形成能均为负且Ag-O共掺体系形成能低于Ag单掺体系。这意味着在N-rich条件下,Ag和O原子很容易融入到氮化铝纳米管中,易于在实验中制造Ag-O共掺氮化铝纳米管材料。

表1 氮化铝纳米管掺杂前后的总能量、形成能、禁带宽度以及跃迁形式Table 1 Total energy, formation energy, band gap and transition form of AlN nanotubes before and after doping
2.2 本征氮化铝纳米管的电子结构
为比较Ag和O对氮化铝纳米管电子结构的影响,如图2所示,首先计算讨论了本征氮化铝纳米管的能带结构和态密度。图2(a)能带结构的计算结果表明氮化铝纳米管的禁带宽度较大,通过轨道分析得到禁带宽度为2.49 eV,与相关研究[28]结果(2.50 eV)较为接近。但和实验值(6.20 eV)相比偏小,这是由于DFT是基态理论,禁带宽度和能带结构具有激发态特性,导致计算结果被低估(采用相同的参数处理,并不会对正确结果产生影响)。氮化铝纳米管的导带底以及价带顶均处于布里渊区的G点,且G点带隙最小,表明(6, 0)氮化铝纳米管是直接跃迁。由图2的分波态密度可以看出,氮化铝纳米管的价带大概可以分成两部分,即-14.34~-11.77 eV的下价带、-5.38~0 eV的上价带区。而导带主要位于2.49 eV到5.09 eV之间。价带顶由N-2p占据,上价带主要由Al-3p态和N-2p态贡献。下价带主要由N-2p态以及Al-3s和3p态贡献,在上述的能量区间内拥有较强的局域性。在位于导带的部分,主要由Al-3p和Al-3s态以及少量的N-2p和N-2s贡献。
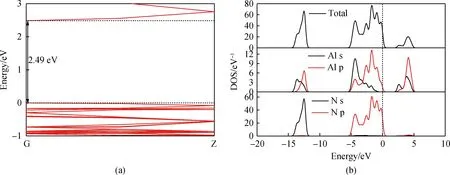
图2 氮化铝纳米管的(a)能带结构与(b)态密度Fig.2 (a) Energy band structure and (b) DOS of AlN nanotubes
2.3 Ag掺杂氮化铝纳米管的电子结构
图3是Ag掺杂氮化铝纳米管的能带结构和分波态密度图。由图3(a)能带结构可以得出,Ag掺杂氮化铝纳米管的价带顶贯穿费米能级从而形成简并态,这使得多余的空穴载流子出现在氮化铝纳米管价带顶附近,在费米能级附近引入了受主能级。计算所得禁带宽度为1.84 eV,低于本征体系,电子跃迁所需能量减小,导电性能提高。由图3(b)的分波态密度可知,Ag掺杂氮化铝纳米管提高了空穴浓度,也就是说Ag的掺入能够实现氮化铝纳米管的p型掺杂。但是从Ag原子的分波态密度来看,Ag原子在费米能级附近拥有较强的局域性分布,使得在费米能级处引入一窄深受主能级,费米能级附近的空穴载流子数目增多,各原子之间相互排斥作用力以及单掺体系的能量增加,导致单掺体系不稳定。所以Ag单掺体系虽然是p型电导,但较难实现理想的p型氮化铝纳米管。

图3 Ag掺杂氮化铝纳米管的(a)能带结构与(b)分波态密度Fig.3 (a) Energy band structure and (b) PDOS of Ag doped AlN nanotubes
2.4 Ag-O共掺氮化铝纳米管的电子结构
图4为Ag-O共掺氮化铝纳米管的能带结构和分波态密度图。从图4(a)中能够看出,Ag-O共掺后,价带顶同样贯穿费米能级形成简并态,在费米能级附近产生多余的空穴载流子从而引入了受主能级。禁带宽度进一步减小为1.80 eV,带隙得到了较好的调整,大小低于单掺体系,电子跃迁所需要的能量进一步减小,导电性能再次得到改善。从图4的分波态密度来看,在氮化铝纳米管的价带部分,上价带主要由Ag-4d 态与N-2p态杂化形成的。显然O原子的掺入使得Ag-4d态与Ag原子临近的 N-2p态电子轨道杂化增强,使得轨道重叠加剧,同时减弱了相互排斥效应,提高了掺杂浓度。再结合图5可以看出,共掺纳米管体系相较于单掺纳米管体系的总体态密度峰值有所降低,整体向深能级移动,费米能级附近的态密度减小,空穴间的库仑作用力减弱,使得共掺纳米管体系的形成能降低,体系变得更为稳定。这时施主O原子并非p型材料的有效复合中心,只是对Ag原子起激活作用,从而为实验上实现氮化铝纳米管的p型掺杂提供一定的理论支持。这与前面稳定性讨论的结果一致。
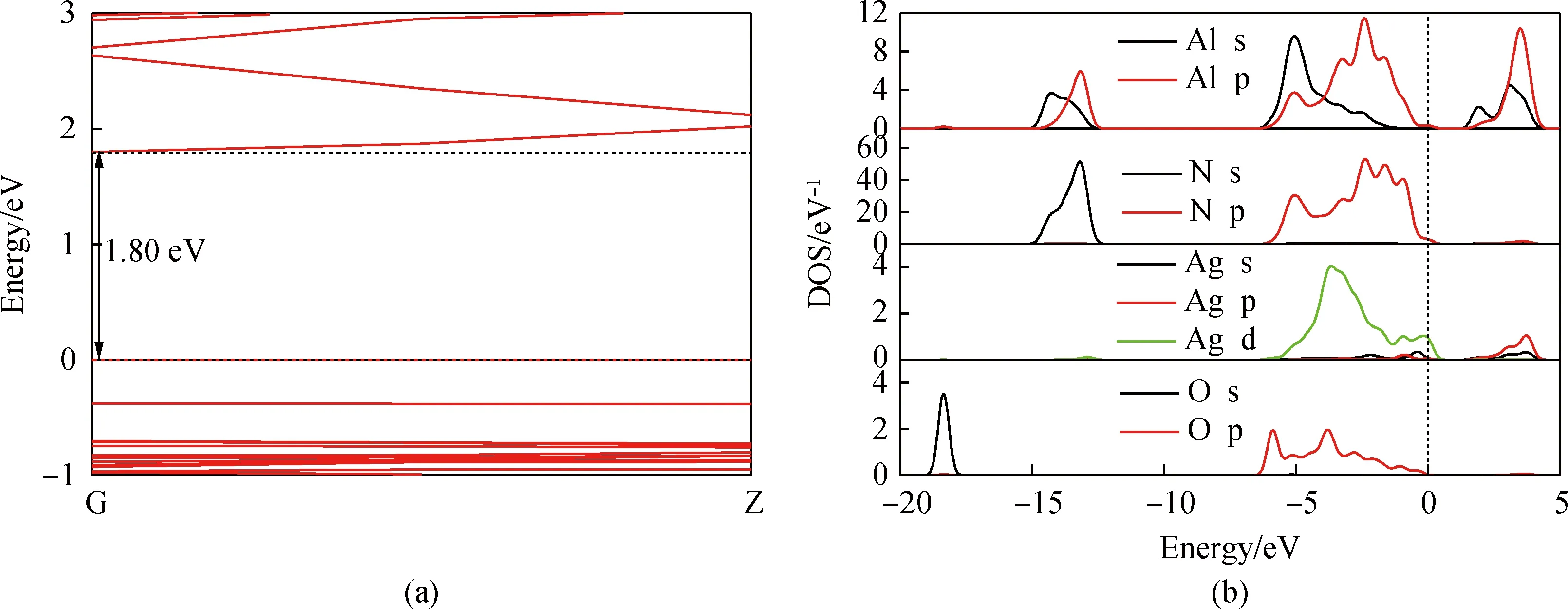
图4 Ag-O共掺氮化铝纳米管的(a)能带结构与(b)分波态密度Fig.4 (a) Energy band structure and (b) PDOS of Ag-O co-doped AlN nanotubes
2.5 差分电荷密度和布局分析
为了更加直观了解纯氮化铝纳米管、Ag掺纳米管以及Ag-O共掺杂纳米管的内部电子相互作用,对三种体系进行电荷差分密度分析。从差分电荷密度分布图能够得到纳米管中原子间的电荷转移、电荷分布、成键类型等情况。从图中可以看出掺杂纳米管相比于纯纳米管的成键类型有较大差异,原子之间的相互作用同样发生了较大的变化,进而影响到整个体系的电荷重新分布情况。
在纯氮化铝纳米管中,Al原子周围的电荷密度减小,N附近的增大。N得到电子而Al则失去电子。从成键角度来看,Al原子和N原子之间的重叠布居为0.64,如表2所示,说明Al—N成键的共价性强于离子性,Al—N键是包含离子键成分的共价键,另外,优化后的键长长度与相关研究结果相近[28],说明相关参数选取的合理性。在Ag单掺氮化铝纳米管体系中,由于Ag离子的半径(0.115 nm)大于Al离子的半径(0.054 nm),使得Ag—N键的键长变大,相互排斥作用力将变高。从图6(c)共掺纳米管体系可以看出,掺杂Ag原子与近邻原子之间相互作用有所加强,电荷分布具有明显的方向性。Ag—O键中电子更容易从Ag原子向O原子转移,这是由于O原子更容易得电子。共掺体系中由于O的离子半径(0.14 nm)大于N的离子半径(0.13 nm)导致Ag—O键相较于Ag—N键更长,重叠布居仅为0.03,Ag—O键表现出极强的离子性。共掺后Ag与O之间的吸引作用可克服原子间产生的相互排斥作用力,使得Ag原子与其近邻原子形成较为稳定的键合态,有效提高受主掺杂浓度以及系统稳定性,有利于实现氮化铝纳米管p型掺杂,上述分析与前面的结果是一致的。

图5 掺杂体系总体态密度对比Fig.5 Comparison of total density of states of doped systems
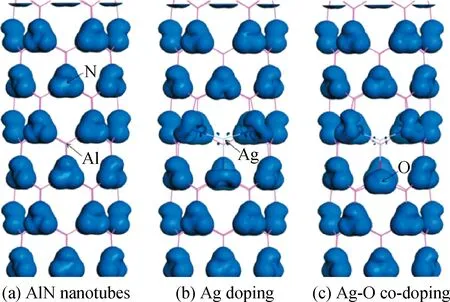
图6 电荷差分密度Fig.6 Electron density differences

表2 各个原子间的电子键长和重叠布居Table 2 Electronic bond lengths and overlapping populations between atoms
3 结 论
本文利用基于密度泛函理论的第一性原理对纯氮化铝纳米管、Ag掺杂和Ag-O共掺纳米管的电子结构进行了计算讨论,得到以下结果:
(1)本征氮化铝纳米管的带隙为2.49 eV,Ag掺杂纳米管之后,价带顶上移,带隙窄化,带隙减小为1.84 eV。且Ag-O共掺杂纳米管后,带隙进一步减小为1.80 eV,导电性增强。
(2)Ag掺杂氮化铝纳米管提高了空穴浓度,Ag的掺入实现了氮化铝纳米管的p型掺杂,但Ag-4d态和N-2p在价带顶形成一条局域性较强的窄深的受主能级,导致原子之间相互排斥作用力增大,单掺体系不稳定。
(3)O原子的掺入,有效地激活了Ag原子,使得Ag原子与其近邻原子形成较为稳定的键合态,有效提高了受主掺杂浓度以及系统的稳定性,有利于实现氮化铝纳米管的p型掺杂,为实验合成提供了理论依据。

