超微血流成像与超声造影成像对慢性肾功能不全患者颈动脉粥样硬化斑块内新生血管的诊断价值
李晓蕾
天津市北辰医院 (天津 300400)
慢性肾功能不全多是由于各种慢性肾脏疾病迁延不愈所致,会累及多种脏器或组织,早期患者血压升高,随着病情进展,可发生全身动脉硬化,并引起心、脑等脏器病变,甚至诱发脑梗死、心肌梗死等脏器疾病[1]。颈动脉斑块是全身动脉粥样硬化形成的窗口,斑块形成与脑梗死的发病、进展关系密切;具体机制为斑块形成会导致血管管腔狭窄,供血动脉远端血液缺乏,进而诱发脑梗死。而斑块内新生血管是斑块发展和不稳定性增加的危险因素之一[2],因此,通过检测斑块内新生血管的形成,对预测斑块稳定性,评估脑梗死风险具有重要的临床意义。超微血流成像(superb microvascular imaging,SMI)是一种新型血流成像技术,具有高灵敏度、高分辨力、低伪像的特点,可准确分离血流信号与周围组织运动重叠伪像,有效检测低速流动的血流信号[3]。超声造影成像(contrastenhanced ultrasound,CEUS)通过注射造影剂,可实时、动态观察斑块内血流分布,时间分辨力及空间分辨力高。基于此,本研究探讨SMI、CEUS 对慢性肾功能不全患者颈动脉粥样硬化斑块内新生血管的诊断价值,现报道如下。
1 资料与方法
1.1 一般资料
选取2019年1月至2021年8月我院收治的120例慢性肾功能不全患者,其中男68例,女52例;年龄38~75岁,平均(58.83±5.82)岁;肾功能分期,Ⅱ期85例,Ⅲ期35例。本研究经医院医学伦理委员会批准。
纳入标准:患者均经常规超声发现低回声或以低回声为主的混合回声斑块,且有多于1个的斑块厚度≥2.0 mm;具有完整的临床诊断资料;无超声检查过敏史;对本研究知情,并签署知情同意书。排除标准:伴有甲状腺功能亢进、脑梗死、心肌梗死等疾病;存在超声造影剂应用禁忌证;合并不稳定性缺血性心脏病或心功能不全。
1.2 方法
选用东芝Aplio 500型超声诊断仪,高频线阵变频探头,频率为4~11 MHz。检查时,患者取仰卧位,头部稍微后仰,保持颈部放松,头部转向检查对侧,充分暴露待检侧颈部;先行常规二维超声检查,探头横向、纵向扫描患者颈总动脉及动脉分支,观察及记录斑块的回声、部位、直径、面积等;随后开启SMI 扫查模式,将探头固定在目标斑块,通常选取动脉斑块最厚的位置,设置机械指数为1.50,深度为3.0~5.0 cm,在SMI 模式下进行颈部横切、纵切扫查,使用灰阶模式,于斑块近心端开始扫描至远心端,扫描时应完全覆盖斑块与周围组织,在行纵切扫描时,详细探查及记录斑块顶部、基底部等处的血流信号,观察斑块表面是否有溃疡,并获取图像保存,新生血管的诊断标准为斑块内存在短线或条状高回声;在SMI 检查结束后,采用CEUS 检查,患者保持平静呼吸,经肘静脉快速注射2 ml Sono Vue 微泡造影剂(意大利Bracco 公司,批号181204,规格59 mg 六氟化硫微泡),随后立即推注5 ml 0.9%氯化钠注射液,启动计时器,进行颈动脉斑块造影,确保探头固定,持续3 min,存储动脉腔内出现造影剂前3个心动周期及造影剂注射后15个心动周期的图像,并实时、动态分析图像,观察是否存在新生血管,即斑块内存在短线或条状高回声。
1.3 观察指标
以颈动脉内膜斑块剥脱术后病理结果为金标准,分析两种方法对新生血管的诊断价值。新生血管分级诊断标准如下[4]。(1)SMI:0级,斑块内无血流信号;1级,斑块顶部或基底部存在血流信号;2级,斑块顶部、基底部同时出现血流信号。(2)CEUS:0级,斑块内无明显微气泡;1级,斑块顶部或基底部一层局部有微气泡出现;2级,斑块内出现弥漫性微气泡。
1.4 统计学处理
采用SPSS 20.0统计软件分析数据。计数资料以率表示,采取χ2检验;一致性采用Kappa分析,Kappa>0.80为高度一致,>0.60但≤0.80为中度一致,≥0.40但≤0.60为低度一致,<0.40为不具有一致性。P<0.05为差异有统计学意义。
2 结果
2.1 两种方法对新生血管的诊断价值比较
颈动脉内膜斑块剥脱术后病理结果显示,120例患者244个斑块共96个斑块发现新生血管。以颈动脉内膜斑块剥脱术后病理结果为金标准,SMI对新生血管的诊断灵敏度为85.42%(82/96),特异度为97.97%(145/148),准确度为93.03%(227/244);CEUS对新生血管的诊断灵敏度为89.58%(86/96),特异度为98.65%(146/148),准确度为95.08%(232/244);两种方法对新生血管的诊断灵敏度、特异度及准确度比较,差异无统计学意义(P>0.05),见表1~2。

表1 SMI 对新生血管的诊断结果(个)
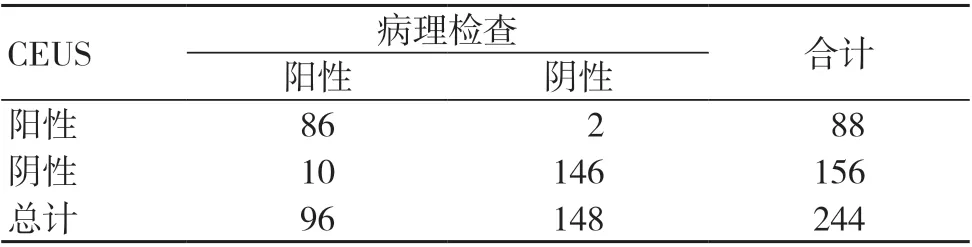
表2 CEUS 对新生血管的诊断结果(个)
2.2 两种方法对斑块内新生血管的诊断分级结果比较
SMI 与CEUS 对斑块内新生血管诊断分级结果的一致性高(Kappa=0.842),见表3。

表3 两种方法对斑块内新生血管的诊断分级结果比较(个)
3 讨论
慢性肾功能不全患者由于脂质代谢紊乱,物质沉积,极易导致动脉粥样硬化,动脉狭窄明显。当慢性肾功能不全患者合并颈动脉粥样硬化斑块形成后,颈动脉内膜异常增厚,血管管腔狭窄,或易损斑块溃疡形成,或斑块脱落阻塞远端血管,严重时甚至会导致缺血性脑血管病,危及患者生命安全,因此,有效预测疾病危险程度,预估疾病发生风险,对防治疾病发生,确保患者生命安全具有重要的意义。斑块成分为预测疾病发生的主要指标。当前,临床根据斑块性质将其分为稳定斑块及易损斑块,其中,易损斑块具有偏心脂质核心较大、纤维帽较薄、炎性细胞浸润明显、斑块出血、新生血管形成、斑块表面溃疡形成等特点,上述特点有助于医师判断易损斑块性质。斑块内新生血管形成是预测斑块破裂的独立因子,其形成机制为多种因素作用导致血管内皮细胞损伤,血浆内血液成分不断沉积在血管壁上,并逐渐形成斑块,导致局部缺氧,此时为了缓解局部缺氧状态,故有大量新生血管形成。新生血管常是由内皮细胞组成,周围无结缔组织支撑,故大量炎性细胞、血液成分容易透过新生血管管壁,增加斑块不稳定性[5],因此,准确监测斑块内新生血管形成,对评估斑块易损性具有重要的意义。
本研究结果显示,以颈动脉内膜斑块剥脱术后病理结果为金标准,SMI 对新生血管的诊断灵敏度为85.42%,特异度为97.97%,准确度为93.03%,与CEUS 的89.58%、98.65%、95.08%比较,差异无统计学意义(P>0.05);SMI 与CEUS 对斑块内新生血管诊断分级结果的一致性高(Kappa=0.842)。此结果与杨德斌等[6]及陈显荣和张晓[7]的研究结果相似,证实了SMI 与CEUS 对慢性肾功能不全患者颈动脉粥样硬化斑块内新生血管均具有较高的诊断价值。采用CEUS 诊断斑块内新生血管时,操作无创、可重复,可实时显像,无造影剂外溢至血管外,并可直观、动态显示斑块内新生血管形成过程,但该技术需要注射造影剂,可能会诱发造影剂肾病,加重肾脏负担。SMI 是一种新型的超声显像技术,可清晰显示组织内低速血流信号,消除背景组织信号,并可提高极低速血流显像灵敏度,且SMI技术无创、重复性好,无需注射造影剂,适用范围广,可有效预测斑块的稳定性及新生血管形成[8]。因此,虽然SMI、CEUS 均可有效诊断斑块内新生血管形成,但CEUS 技术检查费用高、致敏风险高,会限制其应用。
综上所述,采用SMI 与CEUS 诊断慢性肾功能不全患者颈动脉粥样硬化斑块内新生血管均具有较高的临床价值,临床在应用超声技术诊断颈动脉粥样硬化斑块内新生血管时,可根据患者病情、特点,选择一种安全、有效的超声模式。

