硫化氢对顺铂致犬肾脏氧化损伤及炎症的缓解作用
王 爽,刘星尧,贾昊天,刘 云
(东北农业大学动物医学学院,黑龙江省实验动物与比较医学重点实验室,哈尔滨 150030)
急性肾损伤(acute kidney injury,AKI)是一种以肾功能迅速下降的临床综合征,同时AKI是住院患者最常见的并发症之一,使患者死亡风险增加10~15倍[1]。研究表明,AKI的发病机制主要与肾脏组织炎症反应、坏死和氧化应激损伤等有关[2-3]。顺铂是临床上一种常见的抗肿瘤化学药物,其代谢毒副作用能够损伤肾小管细胞并诱导肾脏组织炎症,最终导致AKI发生[4-5]。在兽医临床上,犬AKI发病急、发病快,且病犬更易在药物代谢毒副作用下发展成为肾衰竭,严重时可导致病犬死亡。因此,探究预防和治疗犬AKI的有效方法对兽医临床具有重要意义。
硫化氢(hydrogen sulfide,H2S)是一种无色、剧毒、酸性气味的有害气体,能够引起机体多种器官发生损伤[6-7]。随着研究的深入,人们发现动物体内存在H2S气体分子[8],它成为动物体内继一氧化氮(NO)和一氧化碳(CO)之后的第3种气体信号分子,在不同组织中发挥着重要的生理功能。内源性H2S具有很强的抗氧化作用,它能清除活性氧(ROS),提高细胞内谷胱甘肽(GSH)的水平[9]。另外,H2S具有明显的抗炎作用,能够下调炎症因子,如白介素-1β(IL-1β)、肿瘤坏死因子-α(TNF-α)、核转录因子-κB(NF-κB)等[10]。研究发现,给予结肠炎小鼠H2S可降低炎症因子TNF-α的表达,而抑制小鼠体内H2S的合成易诱发小鼠结肠炎。硫氢化钠(NaHS)是外源性H2S供体,外源给予NaHS能够明显改善大鼠气道炎症[11]。此外,近几年有报道称阿托伐他汀可通过提高内源性H2S缓解小鼠肾脏组织炎症、细胞凋亡和过度的氧化应激,进而缓解AKI[12]。但H2S能否在犬AKI的防治中发挥抗氧化和抗炎作用还未可知。鉴于此,本试验通过静脉注射顺铂建立犬AKI模型,探究H2S对顺铂诱导的犬肾脏组织功能、抗氧化水平和炎症因子等变化的影响,以期为缓解AKI提供新的方法。
1 材料与方法
1.1 试验动物
18只2~3岁、体重为8~12 kg的健康成年雄性比格犬饲养于清洁干燥、通风良好、室温(20±2)℃的动物房中,自由进食和饮水。
1.2 主要试剂及仪器
注射用顺铂(冻干型)购自齐鲁制药有限公司;NaHS由东北农业大学动物医学学院临床外科教研室提供;肌酐(Scr)、尿素氮(BUN)、GSH、过氧化氢(H2O2)和NO试剂盒均购自南京建成生物工程研究所;Trizol购自Invitrogen公司;反转录试剂盒及SYBR Green荧光染料均购自宝日医生物有限公司;HE染液购自武汉塞维尔生物科技有限公司;IL-1β、IL-6、TNF-α、NF-κB、环氧合酶2(COX2)、诱导型一氧化物合酶(iNOS)、IL-4和IL-10抗体均购自万类生物科技有限公司;GAPDH和辣根过氧化酶标记羊抗兔IgG均购自北京博奥森生物技术有限公司。Epoch酶标仪(LD-96A)购自BioTek公司;体视显微镜(TE2000-U)购自Nikon公司;化学发光呈像仪(Tanon 5200)购自上海天能公司;荧光定量PCR仪(罗氏480)购自Roche公司。
1.3 试验动物分组与处理
18只健康成年比格犬随机分为对照组(C)、顺铂组(cis)和硫化氢+顺铂组(H+cis)3组,每组6只。对照组犬经头静脉注射生理盐水;顺铂组犬经头静脉注射5 mg/kg顺铂[13];硫化氢+顺铂组(H+cis)犬在注射顺铂前30 min,经头静脉注射1 mg/kg NaHS溶液,并且每隔24 h注射1次,共3次。
1.4 样品采集与处理
注射顺铂72 h后对犬进行麻醉,静脉采血,4 ℃放置2 h,3 500 r/min离心10 min后收集血清,-20 ℃保存备用。收集血液样本后以外科方式无菌采集左侧部分肾脏组织,用生理盐水漂洗后,一部分肾脏组织固定于4%多聚甲醛,用于制备肾脏组织病理切片,剩余组织-80 ℃保存备用。
1.5 测定指标与方法
1.5.1 生化指标检测 使用生化试剂盒检测血清中Scr和BUN含量,评价犬肾脏组织损伤程度。通过生化试剂盒检测犬肾脏中GSH、H2O2和NO的含量,评价顺铂致犬肾脏氧化损伤的程度以及H2S对犬肾脏抗氧化能力的影响。所有操作均按照试剂盒说明书进行。
1.5.2 肾脏病理学检测 将肾脏组织于4%多聚甲醛中固定24 h后,无水乙醇脱水,石蜡包埋并进行切片,脱蜡,HE常规染色,于显微镜下观察肾脏组织的病理变化。
1.5.3 RNA的提取及实时荧光定量PCR 采用Trizol法提取各组肾脏总RNA。 按照反转录试剂盒说明书操作合成cDNA。 根据GenBank中犬IL-1β、IL-6、IL-4、IL-10、TNF-α、NF-κB、COX2、iNOS基因序列,使用Primer Premier 5.0软件设计引物,引物信息见表1。引物均由广州擎科生物有限公司合成。以GAPDH为内参,进行实时荧光定量PCR反应。PCR反应体系20 μL:RNA 2 μg,2×SYBR Green Mix 10 μL,上、下游引物各0.4 μL,RNase-free ddH2O补至20 μL。PCR反应条件:95 ℃ 3 min;95 ℃ 5 s,60 ℃ 30 s,共40个循环;95℃ 5 s,60 ℃ 1 min;50 ℃ 30 s。采用2-ΔΔCt法计算基因mRNA的相对表达量。
1.5.4 总蛋白提取和Western blotting 称取1 g犬肾脏提取总蛋白,用BCA法检测蛋白浓度,PBS调节蛋白浓度一致,取400 μL蛋白样品加入100 μL SDS-PAGE蛋白上样缓冲液,沸水煮15 min,分装后-80 ℃保存备用。取等量蛋白样品进行SDS-PAGE,转印到PVDF膜上,用5%脱脂乳封闭1 h,一抗IL-1β(1∶1 000)、IL-6(1∶1 000)、TNF-α(1∶500)、NF-κB(1∶500)、COX2(1∶1 000)、iNOS (1∶500)、IL-4 (1∶500)、IL-10 (1∶500)及GAPDH (1∶50 000)于4 ℃孵育过夜,室温孵育二抗(1∶10 000)1 h,ECL显影检测蛋白表达。使用Image J 1.48软件分析蛋白条带灰度值。
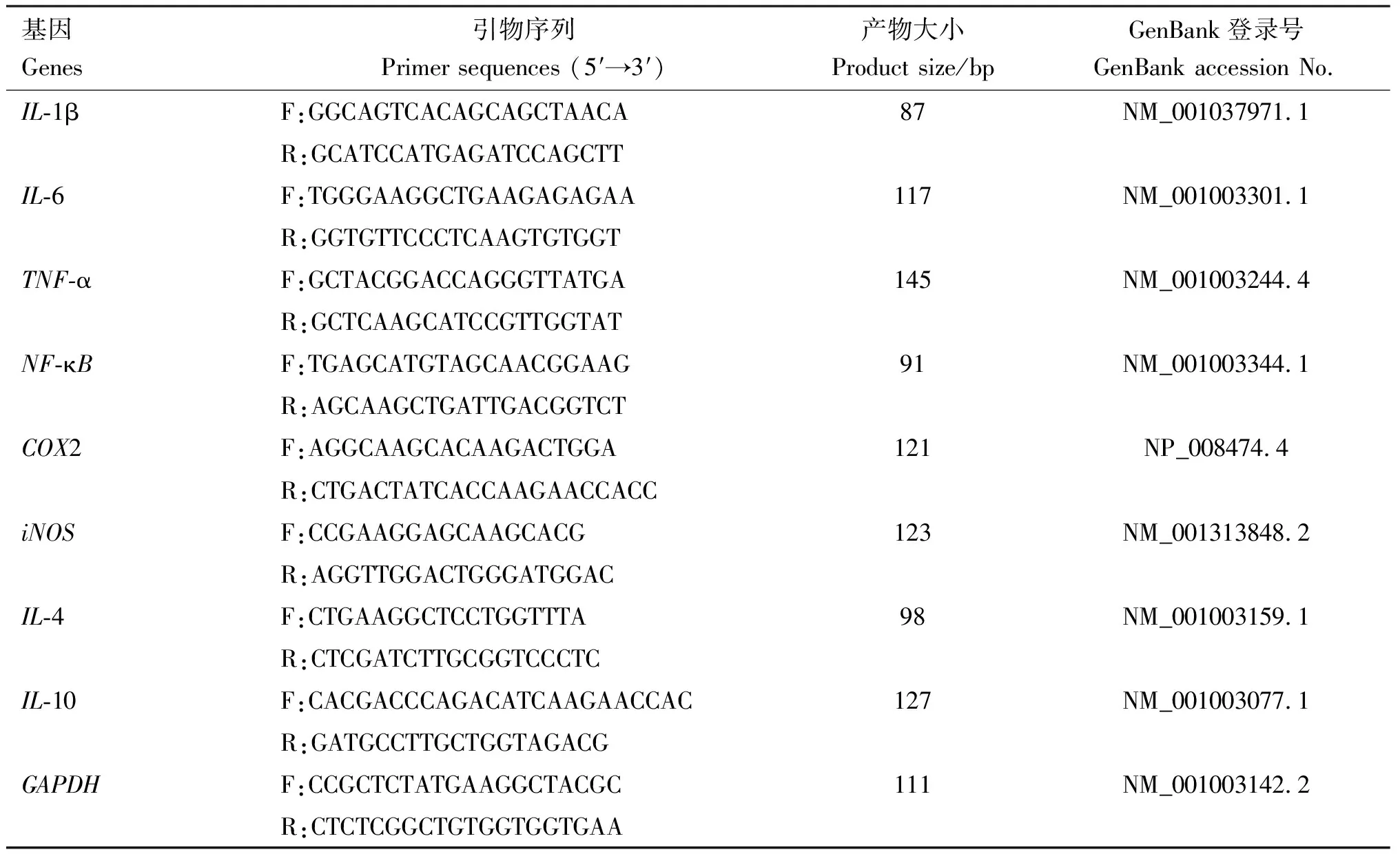
表1 引物信息
1.6 数据统计分析
用GraphPad Prism 8.0统计软件进行单因素方差分析(One-Way ANOVA),组间差异采用t检验。结果用平均值±标准差表示。P<0.05表示差异显著,P<0.01表示差异极显著。
2 结 果
2.1 H2S对犬血清BUN和Scr的影响
由图1可知,与C组相比,cis组犬血清中BUN和Scr含量均极显著增加(P<0.01),H+cis组Scr含量极显著增加(P<0.01);与cis组相比,H+cis组犬血清中BUN和Scr含量均极显著降低(P<0.01)。
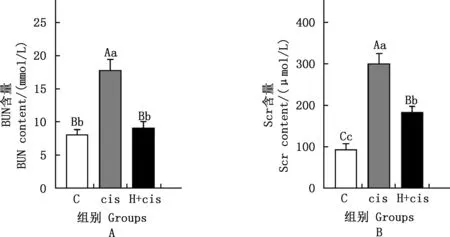
肩标不同小写字母表示差异显著(P<0.05);肩标不同大写字母表示差异极显著(P<0.01);肩标相同字母表示差异不显著(P>0.05)。下同Values with different small letter superscripts mean significant difference (P<0.05);And with different capital letter superscripts mean extremely significant difference (P<0.01);While with the same letter superscripts mean no significant difference (P>0.05).The same as below图1 各组犬血清中BUN和Scr含量Fig.1 Contents of BUN and scr in serum of dogs in each group
2.2 H2S对顺铂处理犬肾脏组织病理变化的影响
由图2可知,C组肾脏组织肾小球和肾小管结构正常,球囊腔明显(a),血管壁清晰,未观察到明显病变。而cis组犬肾脏组织出现大量的炎性细胞浸润(b),肾小管上皮细胞变性,管腔内有蛋白性物质(c),间质血管明显充血(d)。H+cis组犬肾脏组织可见肾小球囊腔狭窄(e),肾小管上皮细胞变性(f)。

图2 各组犬肾脏组织病理学观察(200×)Fig.2 Histopathological observation of dog kidney tissues in each group (200×)
2.3 H2S对犬肾脏中GSH、H2O2和NO含量的影响
由图3可知,与C组相比,cis组犬肾脏中GSH含量极显著降低(P<0.01),而H2O2和NO含量均极显著增加(P<0.01);H+cis组犬肾脏中GSH、H2O2和NO含量均无显著差异(P>0.05)。与cis组相比,H+cis组犬肾脏中GSH水平极显著增加(P<0.01),H2O2和NO含量极显著下降(P<0.01)。
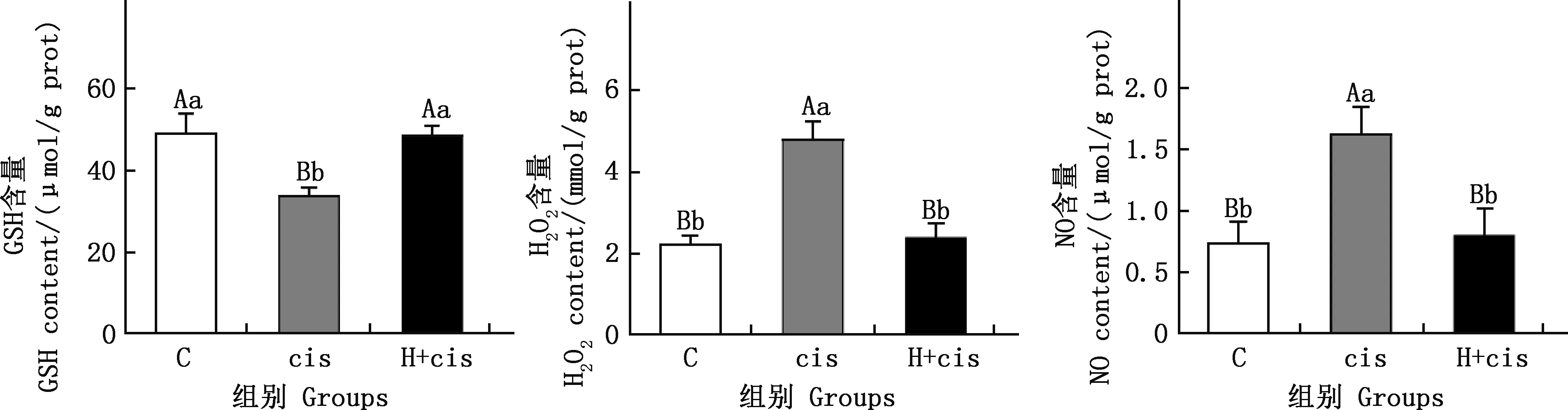
图3 各组犬肾脏组织GSH、H2O2和NO含量Fig.3 Contents of GSH,H2O2 and NO in kidney tissues of dogs in each group
2.4 H2S对犬肾脏组织中炎症相关因子mRNA表达的影响
由图4可知,与C组相比,cis组犬肾脏组织中IL-1β、IL-6、TNF-α、NF-κB、COX2和iNOS的mRNA相对表达量均极显著增加(P<0.01),IL-4和IL-10的mRNA相对表达量均极显著下降(P<0.01);H+cis组IL-1β、IL-6、TNF-α、NF-κB和COX2的mRNA相对表达量均显著或极显著增加(P<0.05;P<0.01),IL-10的相对表达量极显著下降(P<0.01),IL-4和iNOS的mRNA相对表达量无显著差异(P>0.05)。与cis组相比,H+cis组犬肾脏组织中IL-1β、IL-6、TNF-α、NF-κB、COX2和iNOS的mRNA相对表达量均极显著下降(P<0.01),IL-4和IL-10的mRNA相对表达量均极显著增加(P<0.01)。IL-10的mRNA相对表达量极显著下降而IL-4的mRNA相对表达量无显著性差异(P>0.05)。
2.5 H2S对犬肾脏组织中中炎症相关因子蛋白表达的影响
由图5可知,与C组相比,cis组犬肾脏组织中IL-1β、IL-6、TNF-α、NF-κB、COX2和iNOS蛋白相对表达量均极显著增加(P<0.01);IL-4和IL-10蛋白的相对表达量均极显著降低(P<0.01);H+cis组犬肾脏组织中IL-1β、IL-6、TNF-α、NF-κB和iNOS蛋白相对表达量均极显著增加(P<0.01),COX2蛋白相对表达量无显著性差异(P>0.05),IL-4和IL-10的蛋白相对表达量显著或极显著降低(P<0.05;P<0.01);与cis组相比,H+cis组犬肾脏组织中IL-1β、IL-6、TNF-α、NF-κB、COX2和iNOS蛋白相对表达量均极显著降低(P<0.01),IL-4和IL-10蛋白相对表达量均极显著升高(P<0.01)。
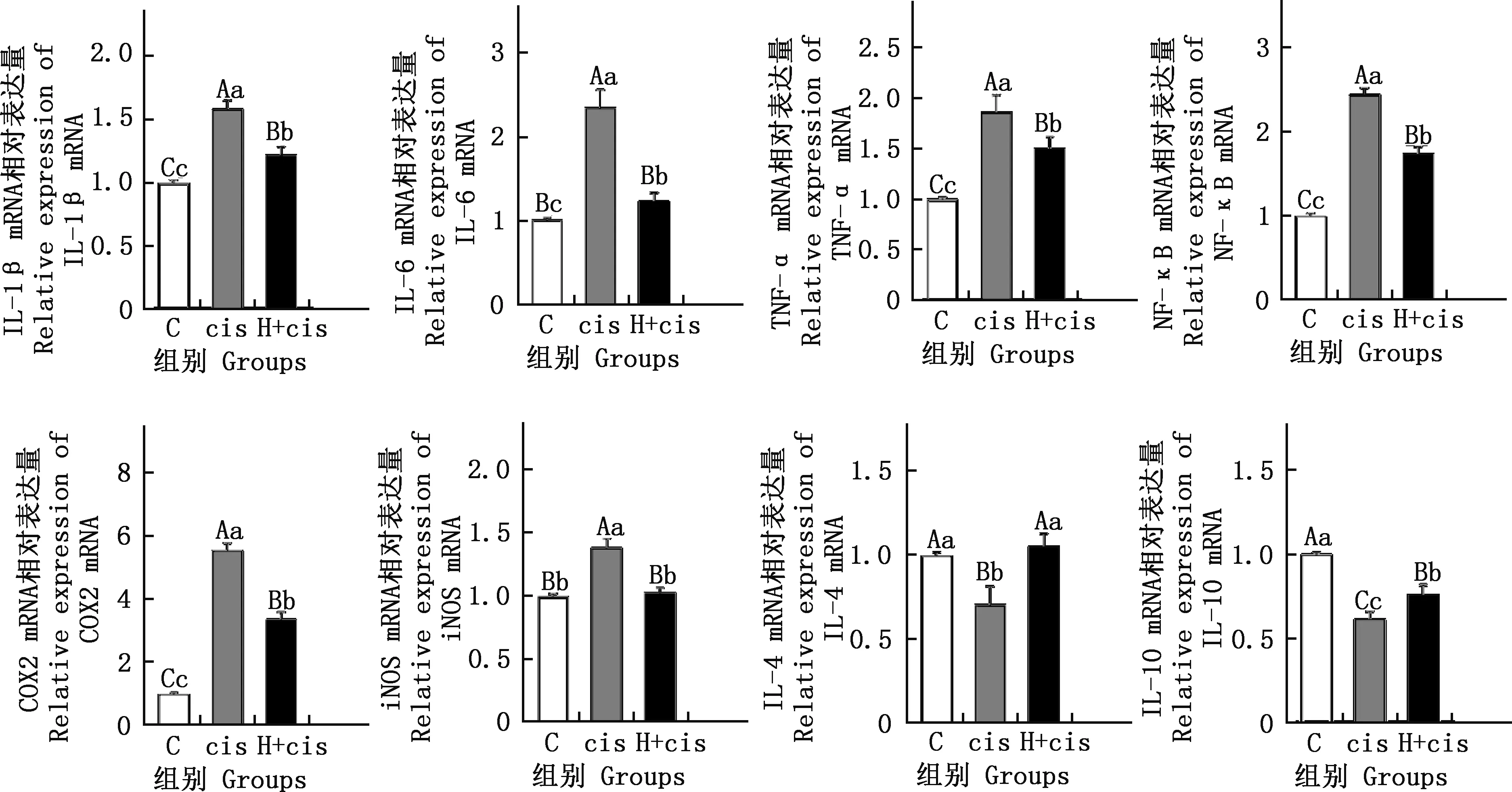
图4 各组犬肾脏组织中炎症因子mRNA表达水平Fig.4 Expression levels of mRNA of inflammatory factors in dog kidney tissues in each group
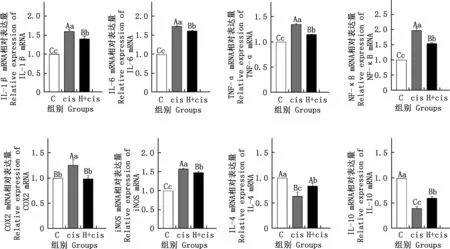
图5 各组犬肾脏组织中炎症因子蛋白的表达水平Fig.5 Expression levels of protein of inflammatory factors in dog kidney tissues in each group
3 讨 论
H2S最初被认为是一种无色、剧毒、具有特殊臭鸡蛋味的气体,低剂量就能对机体造成损伤。直到1996年,Abe等[8]研究发现,H2S作为一种神经调节介质而发挥重要作用,自此关于动物体内气体分子H2S的研究成为生物医学领域的热点。已有研究证实,H2S参与哺乳动物多种组织的各种病理生理过程并发挥重要作用。外源给予H2S能够通过减轻氧化应激和线粒体功能障碍来防止心肌结构破坏,缓解心肌缺血再灌注损伤[14]。崔永华等[15]研究发现,外源性H2S可以通过激活海马组织硫氧还原蛋白系统来降低氧化应激水平,进而缓解蛛网膜下腔出血引起的早期脑损伤。此外,H2S能下调IL-1β、IL-6、TNF-α等炎性因子来减轻细胞炎性损伤,发挥抗炎作用[16]。 Sidhapuriwala等[17]研究发现,给予10 mg/kg NaHS可下调小鼠胰腺和肺脏的炎症反应,并减少促炎趋化因子和黏附因子的表达。Zhang等[18]研究发现,H2S可以降低细胞因子TNF-α、IL-6以及IL-1β的表达来缓解臭氧诱导的小鼠气道炎症。然而在兽医领域中,关于H2S对犬肾脏组织的保护作用鲜有报道。基于此,本研究首次从顺铂造成犬肾脏氧化损伤的角度出发,利用H2S抗氧化、抗炎的特性,探究H2S对顺铂引起的犬AKI是否具有保护作用。
AKI是临床上常见的疾病,一般治疗包括透析和肾脏移植。由于治疗成本高导致很难应用到兽医临床上,因此探究有效预防AKI手段对兽医临床十分重要。血液Scr和BUN是反映肾脏功能的重要指标,当血液Scr和BUN水平短时间内升高,提示AKI的发生[19]。本试验结果显示,静脉注射顺铂72 h后犬血液中Scr和BUN极显著升高,说明犬AKI模型构建成功。而H2S能下调犬血液中Scr和BUN水平,同时结合组织病理切片结果,提示H2S能有效缓解顺铂诱导的犬AKI。此外,生化指标检测发现,cis组犬肾脏组织中GSH含量极显著降低,而H2O2和NO含量极显著上升。GSH是动物体内一种重要的还原剂,能够清除动物体内自由基,参与机体多种氧化还原反应。ROS和活性氮(RNS)是动物体内主要氧化物,包括H2O2、羟自由基(·OH)、NO和过氧化亚硝酸盐(ONOO-)等。正常生理情况下,机体内氧化与抗氧化处于一个动态平衡,当氧化物在机体内累积过多会引起机体氧化应激[20- 21]。本试验结果显示,顺铂诱导犬肾脏组织发生氧化应激,而H2S能够下调H2O2和NO水平,提高GSH含量进而提高犬肾脏组织抗氧化能力。此外,氧化应激能够激活免疫活性蛋白如细胞因子和转录因子等[22]。NF-κB是动物体内重要的转录因子,它不仅可以调控免疫细胞的激活,还广泛参与机体的应激和炎症等反应。许多外部刺激如H2O2、TNF-α等均能激活NF-κB通路,进而诱导促炎因子IL-1β和IL-6的生成和释放。IL-1β是动物体内炎症反应的核心细胞因子,主要体现在它能诱导其他炎性因子如IL-6、趋化因子和黏附分子等的合成。AKI常表现为肾脏组织发生炎症反应,Prasada等[23]观察到AKI患者体内TNF-α、IL-1β和IL-6显著上升。TNF-α主要是由巨噬细胞产生的一种促炎因子,它可以诱导白介素和干扰素等多肽物质引起炎症反应[24]。Zhu等[25]报道在小鼠AKI模型中,肾脏中NF-κB、TNF-α、IL-1β和IL-6水平均显著上升。与Zhu等[25]报道相似,本试验结果显示,顺铂处理后犬肾脏中促炎因子IL-1β、IL-6、TNF-α和NF-κB相对表达量明显升高,提示肾脏组织发生炎症。COX2是合成前列腺素的关键酶,正常生理情况下在动物体内几乎检测不到,当机体受到炎性因子刺激可激活COX2,而抗炎因子如IL-4和IL-10则可抑制机体COX2水平[26]。与COX2相似,正常情况下,细胞内iNOS水平相对较低,但在炎症等病理情况下其表达会显著升高[27],并诱导细胞产生大量的NO,NO又会与超氧阴离子结合生成过氧亚硝基阴离子而引起氧化应激反应[28],进而损伤组织细胞。本试验结果显示,cis组犬肾脏组织中COX2和iNOS相对表达量较对照组明显升高,进一步表明顺铂诱导犬肾脏组织发生炎症反应。IL-4和IL-10是动物体内重要的抗炎因子,能限制促炎因子的表达[29-30]。H2S可通过调节细胞因子产生抗炎作用。Li等[31]研究发现,给予外源性H2S能够降低大鼠肺脏组织中IL-6水平,同时提高抗炎因子IL-10表达进而减轻肺损伤。杨永华等[32]研究发现,用H2S处理大鼠肢体缺血再灌注损伤模型后,大鼠血清中促炎因子IL-1、IL-6及TNF-α水平明显下降,提示H2S减轻大鼠局部炎性反应。本试验结果显示,H2S预处理可以下调炎性因子IL-1β、IL-6、TNF-α、NF-κB、COX2和iNOS水平,提高IL-4和IL-10相对表达量,说明H2S能够缓解顺铂诱导的犬肾脏组织炎性损伤。
4 结 论
本试验结果表明,顺铂通过诱导犬肾脏组织氧化应激,促进肾脏中NF-κB、TNFα、IL-1β、IL-6、COX2和iNOS的表达,并下调IL-4和IL-10水平,导致犬AKI的发生,而H2S预处理可通过提高肾脏组织抗氧化抗炎能力缓解顺铂引起的犬AKI。

