脉冲放电等离子体甲烷氯化制氯代甲烷实验研究
许 平
(集宁师范学院 化学与化工学院,内蒙古乌兰察布 012000)
石油、天然气等能源是社会发展、生存的重要条件,是开展各种经济活动和日常生活的重要基础。如今能源开发和环境问题,已困扰各国的社会进步、经济发展。我国天然气储量较为丰富,但开发水平、利用水平、消费水平均较低,甲烷作为天然气主要成分,利用价值高,利用技术也较简单,费用低廉,以甲烷等原料制作的甲醇、二氯甲烷等产品也具有广阔应用前景,但甲烷作为温室气体也产生了严重的环境问题。因此,需要合理的利用甲烷,才能在获得更多经济价值的同时,有效控制甲烷排量,减少其对环境的负面影响。
1 脉冲放电甲烷氯化实验的相关概念
1.1 甲烷基本概念
自然中的甲烷分布广泛,天然气、沼气、煤气主要成分就是甲烷。甲烷可作为制造氢气、甲醛、炭黑、乙炔等物质的原料。甲烷作为简单有机物,空间结构为正四面体,难溶于水,但易溶于乙醇等溶剂,化学性质稳定,与H2SO4等强酸、NaOH 强碱等、强氧化剂一般不发生反应。一定条件下甲烷会发生氧化、卤代等反应。甲烷作为温室气体,增温效应明显,近百年来大气中甲烷浓度大幅提升,对环境的影响颇大。
甲烷来源多样,沼泽、化石燃料及动物消化过程、有机物分解、生物加热或燃烧等过程均会产生大量甲烷。天然气、油田气等物质可直接分离出天然气,对石油加工产生的气体、焦炉气进行分离,也能得到甲烷。甲烷对各个国家而言均是重要的燃料、化工原料。我国对天然气较为依赖,而甲烷氯化能得到各种氯代甲烷,均是重要的化工原料。甲烷作为重要资源,可创造巨大经济效益,相关技术不复杂,但需要合理利用甲烷,避免加剧全球气候变暖。
1.2 甲烷转化方法
天然气中甲烷含量高达95%,因此转化甲烷时一般以天然气为主体进行甲烷的化学转化和利用。甲烷C-H 键和CH3-H 键的解离能均较高,这使活化甲烷分子较为困难,目前常用的活化方法有热活化、催化活化、等离子体活化。甲烷分子在活化后转化为甲醇等易被利用的原料,如合成气、甲醇、C2烃等。热活化等方法为常规的转化方法,依据转化途径又可分为直接转化、间接转化两种。直接转化指将甲烷一步转化为甲醇、甲醛等产物,如采用气相催化氧化技术,将甲烷合成为甲醇,利用氧化偶联技术制作乙烯,利用热裂解技术生成炭黑、乙炔等;还有甲烷转化为甲烷氯化物、氢氰酸等产物。间接转化指将合成气进行重整以制作合成气,或利用合成气制作甲醇、二甲醚及液体燃料等,首先需要将甲烷重整反应为合成气,如对甲烷水蒸气进行重整,指以甲烷水蒸气作为原料,进行转化生成合成气,或对甲烷进行部分氧化、联合重整,然后需要对重整得到的合成气进行再次转化,以合成甲醇、二甲醚及液体燃料。间接转化的技术存在费用高、流程复杂、成本较高等缺点,因此工业上尚未大规模应用。近年来对利用天然气制各种化学原料的研究较为活跃,但常规工艺均要使用各种催化剂,且需要高温高压等特殊环境,这极大增加了催化成本,同时对金属废物的处理也成为难题。
非常规的甲烷转化法、等离子体转化法、光催化转化法等技术,避免了常规转化中存在的能耗高、催化剂易失活等问题。其中等离子体活化甲烷十分有效,具有很高的能量足以使甲烷分子激发、离解、电离,进而转化为氯代甲烷等产物。
1.3 等离子体
1808 年,Dawy 对等离子体进行最初的研究,Langnuir 于19 世纪30 年代正式提出等离子体概念,20 世纪70 年代其成为物理学独立分支,等离子体化学则是研究其相态下化学反应,于1967 年被正式提出。等离子体化学,利用物质等离子态时的化学活性,进行许多常规条件下物质无法进行的反应。等离子体化学越来越被科学家重视,目前等离子体主要被应用于废气处理、金属切割、固体废物处理等方面。等离子体,指通过放电、辐射等方式迫使气体电离,从而使粒子数达到一定数值,形成含电子、离子、原子、分子、自由基等的导电性流体,其正、负电荷数相等时即为等离子体。等离子体处于特殊气体状态的,此流体有特殊的化学反应特性,被称为固、液、气态之外的第四种物质形态,具有导电性,但整体保持电中性。与普通气体相比,等离子体可导电,粒子间存在库仑力,且会受外加电磁场影响。等离子体在进行气态转化时需要电子摆脱原子核的束缚。因此和人们熟悉的三种物质状态相比,等离子体无论是组成上还是在性质上主要依据其空间、时间尺度,德拜长度衡量等离子体电中性的尺度下限,若等离子体容积小于德拜长度空间范围,则表明存在电荷分离,但等离子体不处于电中性状态。根据热力学温度,可将等离子体划分为平衡态、非平衡态下的离子体,若电子温度、离子温度、中性粒子温度相同时,表明离子体处于平衡状态,反之则为非平衡态。平衡态粒子温度常大于在5×103K,又称为热等离子体,在常压、高压等条件下电弧放电、高频放电,会离子温度大于中性粒子的温度,成为分平衡态离子体,温度一般大于104K,但表观温度依然较低,所以又称冷等离子体。甲烷转化所用的等离子体一般为冷等离子体,稀薄气体激光及射频、微波等方式激发放电,以产生冷等离子体,以有效激活甲烷分子的化学反应。而等离子体产生方式也有很多种,主要有辐射、放电两类,放电法又包括辉光放电、电晕放电、介质阻挡放电、频射放电、微波放电等。
2 实验过程
2.1 研究对象
实验选取甲烷、氯气作为研究材料。氯气是黄绿色带刺激性的气体,主要用于漂白及氯化合物、聚氯乙烯等物质的制造,氯气可通过电解食盐获得,在冶金、造纸、染料、制药、橡胶、塑料等化工生产中广泛应用。甲烷氯化反应产生的氯代甲烷均有很大市场应用价值,以二氯甲烷为例,国内对其需求量很大,基于其不可燃等特性,被用来代替乙醚等物质,在胶片、医药、家电制造等领域具有广泛前景,而天然气氯化是目前生产二氯甲烷的主要方法。另外,实验使用氩气作为稀释剂,基于其不燃烧、不助燃、氩气击穿电压与起晕电压较低等特性,能使实验获得较好转化效果,同时节省成本。
2.2 实验流程
实验使用的装置及实验流程如图1所示,包括配气、高压电源、脉冲反应器、分析检测等部分,钢瓶3为氯气与氩气的混合气,前者体积分数为28.75%。各类气体经减压阀进行相应流程的反应,最终在缓冲罐6中混合,然后进入脉冲电晕等离子体的反应器,最后经过干燥装置得到最终产物,利用傅里叶红外光谱仪对产物进行分析,最后将产物通入氢氧化钠溶液以避免排入环境。
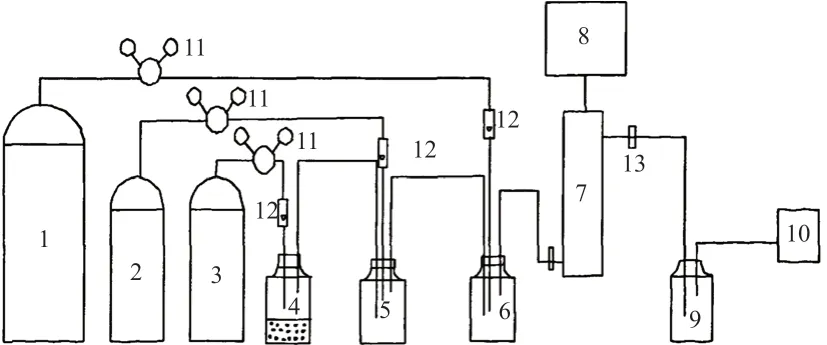
图1 脉冲放电甲烷氯化实验流程图
2.3 实验材料
脉冲反应选择的高压电源是产生等离子体的关键设备,本实验选用机械火花开关的脉冲方式,对电容器进行交替充电、放电,以在反应器上得到脉冲高压。电晕反应器选择线筒式样的反应器,反应器玻璃管需要有进气出气口、电晕线、采样口等结构。其他设备包括气体进样器、小口瓶、流量计、干燥管等,气体药品有无水氯化钠、氢氧化钠等。
3 结果与讨论
3.1 峰值电压对反应的影响
基于电晕反应器的原理,其电场强度与峰值电压相互关联,而电场强弱直接影响脉冲所获自由电子的能量。当自由电子达到一定水平,才能与甲烷、氯气等气体分子进行非弹性碰撞,使气体分析电离、解离。因此,提高峰值电压利于反应的开展。
实验主要观察不同峰值电压下甲烷转化率及产物中二氯甲烷浓度等数据。实验控制脉冲频率为35Hz,甲烷、氯气、氩气的流量比为2∶l∶7,总流量控制为300ml/min,反应器处理时间控制为40s,峰值电压设置10kV、12.5kV、15kV、17.5kV,数据显示峰值电压提高,甲烷转化率、二氯甲烷浓度也大幅增加,各峰值下甲烷转化率分别为:18.9%、21.3%、23.7%、25.4%,各峰值下二氯甲烷浓度分别为1.1mol/m3、1.8mol/m3、4mol/m3、4.7mol/m3,增速由慢至快再变慢。峰值电压对甲烷转化率的影响,主要是因为低放电时甲烷分子被解离的数量少,电压峰值增大,反应体系内总能量成级数增大,自由电子数量、能量大幅增大,因此有更多甲烷被解离为自由基。而电压峰值对二氯甲烷浓度的影响,整体显示峰值电压增高有利于产生二氯甲烷,这是由于体系内能量增加,更多甲烷分子离解成自由基,其增速的变化,是由于反应初期,生成物中三氯甲烷的选择性更高,而随着能量增加,使三氯甲烷被快速降解,其生成速率却下降,二氯甲烷的选择性提高,但电压进一步增高,产物产率与选择性均会减小。可见,若目标产物为二氯甲烷,17.5kV 是最好的选择。
3.2 脉冲频率对反应的影响
脉冲频率升高,电流增加,反应功率增加。因此脉冲等离子体反应可通过调节脉冲频率改变反应功率。实验控制峰值电压17.5kV,气体比例、流量、反应时间的控制同上,转化后控制为2∶l∶7,气体在反应器中的停留时间为40s,将脉冲频率控制为20Hz、25Hz、30Hz、35Hz、40Hz,测量并分析不同脉冲频率时甲烷转化率、二氯甲烷含量的变化情况。数据表明,脉冲频率提高,甲烷转化率随之提升,各脉冲频率下甲烷转化率分别为23.8%、26.6%、29.4%、31.2%。这是由于当放电频率提高时,自由基生成速率随之提高,更多的甲烷分子被解离。脉冲频率提高,二氯甲烷浓度也不断提高,各脉冲频率下二氯甲烷浓度分别为0.3mol/m3、0.7mol/m3、1.6mol/m3、3.9mol/m3、4.4mol/m3,可见更高的脉冲频率有利于生成二氯甲烷,这是因为脉冲频率提高,更多甲烷变成自由基,但二氯甲烷浓度增加速率先慢后快再慢,这是由于反应初期,反应物中自由基大幅增加,但产物浓度低,因此各产物生成速率较低,随着反应进行,反应器中产物浓度大幅增加,因此产物增长速率大幅增加,但随着自由基大幅减少,产物增加速率也会减缓,但脉冲频率处于30~35Hz 时,二氯甲烷选择性增速最快,三氯甲烷选择性随脉冲频率升高而下降。
3.3 甲烷、氯气流量比对反应的影响
实验时控制电压峰值17.5kV、脉冲频率35Hz,反应时间、总气体流量等条件同上,甲烷与氯气比例调节为2∶1,2.5∶l,3∶1,3.5∶1,4∶1。实验结果显示,不同甲烷与氯气比例下,甲烷转化率分别为29%、27%、23%、21%、19%,提升两种气体的比例,甲烷转化率反而降低,这是因为二者气体比例升高,反应器中自由电子数量、能量过量,甲烷量过剩。不同的甲烷与氯气比例下,二氯甲烷浓度分别 为2.4mol/m3、3.6mol/m3、3.8mol/m3、3.7mol/m3、4.2mol/m3,整体上两种气体比例增加,二氯甲烷的生产量是增加的,但比例为3.5∶1,甲烷转化率不升反低,且后期增长率大幅减低,这是由于甲烷量过多,可见二者比例过高,不仅对提升产物含量见效甚微,还不利于提高原料利用率。另外,二者比例变化,也影响产物的分布,整体而言,二氯甲烷选择性会随比例提高而增加,而三氯甲烷选择性随比例提高而减小。
4 结束语
甲烷氯化的技术多样,而利用脉冲等离子体促使甲烷氯化反应进行,是可行且具有诸多优势。通过实验,可以发现峰值电压、脉冲频率等因素均会对甲烷转化率及生成物含量产生复杂影响。实际生产中,还应根据目标产物,合理的设置峰值电压等参数,以在提高目标产物转化率的同时,提升反应效率和原料利用率。另外,为实现该技术的工业化,需要合理地放大反应装置,以满足工业化生产的要求。

