床旁预处理及先端部刷洗在十二指肠镜清洗中的应用
林玉湘 黄 倩
福建医科大学附属第二医院消毒供应中心,福建省泉州市 362000
随着十二指肠镜技术的不断成熟以及相关器械、附件的创新发展,内镜逆行胰胆管造影术(Endoscopic retrograde cholangiopancreatography,ERCP)已成为临床胆胰疾病诊断、治疗不可或缺的工具。ERCP操作过程中,十二指肠镜需要经人体体腔进入体内,操作使用之后内镜的表面以及内部管道等都会被人体体腔的细菌污染。相比于其他类型的内镜,十二指肠镜的设计结构复杂、材质特殊,清洗难度较大,尤其是先端部的抬钳器裂隙较多而且位置隐蔽,容易残留细菌,显著增加了十二指肠镜的清洗难度[1]。研究表明,十二指肠镜清洗不彻底容易导致细菌污染,使十二指肠镜消毒后细菌菌落数超标,导致交叉感染和医院感染的风险升高[2]。国内一项针对1 743例ERCP患者的研究指出,ERCP术后并发胆道感染是最常见的并发症,发生率超过4%[3],十二指肠镜清洗相关因素是经十二指肠镜行ERCP后感染的因素之一[4]。如何更好地对十二指肠镜进行清洗,已成为当下研究热点。我院也一直积极探索、研究相关改进方法,通过研究十二指肠镜构造和特点,采用床旁预处理和先端部刷洗的清洗方式清洗十二指肠镜,取得了较好效果,现报道如下。
1 材料与方法
1.1 材料 选择2019年5月—2020年12月我院操作使用后的480条十二指肠镜(奥林巴斯株式会社,TJF-160V)。内镜清洗器械:管道开口清洗刷(奥林巴斯株式会社,MH 507)、AW通道清洁适配器(奥林巴斯株式会社,MH-948)、冲洗管(奥林巴斯株式会社,MH-974)、内镜清洗刷(日本奥林巴斯株式会社,BW-20T)。清洗剂:医疗器械内镜多酶清洗剂(山东新华医疗器械有限公司)、2%戊二醛消毒液(朗索医用消毒剂有限公司)。将480条十二指肠镜随机分为对照组和实验组,每组240条。
1.2 清洗方法
1.2.1 对照组:按照《软式内镜清洗消毒技术规范》(2016年版)要求[5]按照如下步骤进行常规清洗:(1)首先将内镜置于水槽内,用湿测法进行内镜测漏试验检查;(2)清水冲洗、纱布擦洗;(3)取下吸引器及送气按钮进行清洗,高压水枪冲洗各孔道;(4)清洁毛刷刷洗孔道和导光软管的管道;(5)正确启动内镜自动清洗消毒机。
1.2.2 实验组:在对照组基础上增加先端部标准刷洗和床旁预处理,分别由消毒供应中心护士和操作医生执行。相关人员均接受十二指肠镜制造商、医院感染管理科和医院消毒供应中心的严格理论培训和实践操作考核,且均考核合格。(1)床旁预处理。ERCP诊疗后即对十二指肠镜进行床旁预处理:①十二指肠镜从口腔退出,未拆离主机前,即用含多酶清洗剂的无菌纱布对十二指肠镜表面进行擦拭;②将灭菌水从气道和钳道注入进行冲洗;③将十二指肠镜身置入多酶清洗剂容器内,进行吸引冲洗;④盖上防水帽,放入专用容器,送至消供中心。(2)先端部刷洗。①先端帽清洗:先用多酶液对先端帽内侧面进行冲洗,用刷子刷洗或纱布擦洗外侧面,再用多酶清洗浸泡6min,最后用超声破碎清洗5min;②先端部刷洗:先刷洗先端部表面,再刷洗内部结构,注意各种凹槽、间隙的刷洗。依据《医院消毒供应中心管理规范》中的清洗标准,应用放大镜进行检查,查看先端部内部结构,表面光洁,无污渍和杂质为合格,不合格则继续刷洗;③抬钳器刷洗:按侧面→内部凹槽→中轴顺序刷洗抬钳器;配合活动抬钳器按钮,从各个方向对内部间隙进行多次刷洗。
1.3 评价方法和指标 每条操作使用过的十二指肠镜清洗后用气枪吹干,使用一次性使用注射器分别从抬钳器道和气道入口注入20ml含0.3%甘氨酸的采样液,在出口处用无菌试管收集洗脱液,密封后由专人送检验科备检。检验科人员严格按照《内镜清洗消毒技术操作规范》和《医院消毒卫生标准》[6]对标本进行接种培养72h,采用平板菌落计数法在显微镜下观察、记录观察细菌菌落形成单位(cfu)。抬钳器道和气道任一洗脱液标本培养出细菌,则判断为十二指肠镜细菌培养阳性。根据《软式内镜清洗消毒技术规范》(2016年版)标准[5],细菌总数<20cfu/件表示清洗合格。
2 结果
2.1 两组细菌计数及清洗合格率比较 实验组抬钳器道和气道洗脱液培养细菌计数均少于对照组,且十二指肠镜清洗合格率高于对照组,差异有统计学意义(P<0.05)。见表1。

表1 两组细菌计数及清洗合格率比较
2.2 两组细菌培养阳性率比较 实验组抬钳器道洗脱液细菌培养阳性率、气道洗脱液细菌培养阳性率以及二者同时阳性率均低于对照组,差异有统计学意义(P<0.05)。见表2。
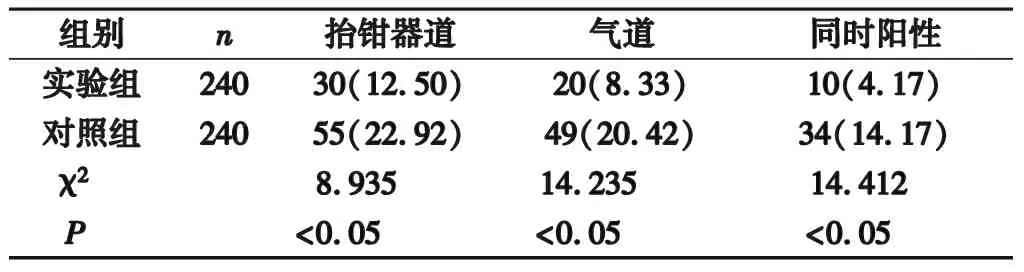
表2 两组细菌培养阳性率比较[n(%)]
2.3 清洗后常见细菌分布 两组清洗后总体细菌培养阳性率为22.08%(106/480),其中69条(65.09%)残留革兰氏阴性菌,37条(34.91%)残留革兰氏阳性菌,残留细菌以大肠杆菌、柠檬酸杆菌等革兰氏阴性菌为主。两组均检出克雷伯氏杆菌,且阳性例数差异不明显。
3 讨论
清洗是消毒灭菌必需的前期工作,也是灭菌成功与否的前提。影响器械清洗效果的因素较多,包括器械污染情况、器械结构复杂性、清洗方式等[7]。十二指肠镜钳道纤细、抬钳器构造特殊,使用时反复进行取石等操作使其表面容易残留各种消化液,容易使胆泥、黏稠胆汁潴留在抬钳器的间隙及凹槽部位,集聚形成污染物。此外,十二指肠镜本身材质特殊,电子光学纤维不耐高温且化学消毒剂对其易产生腐蚀,常用的高压蒸汽灭菌法和消毒浸泡法均不适宜于十二指肠镜长久的清洗消毒。因此,如何有效地对十二指肠镜进行清洗消毒,是内镜消供中心面临的难题。
Kehoe等[8]研究指出,使用后的手术器械在1h内清洗,合格率可达99.21%,而如果放置超过1h再清洗,合格率则降低到63.92%。该研究提示,包括十二指肠镜在内的医疗器械在使用后应尽量在较短时间内进行清洗,去除大部分污染物。如十二指肠镜操作使用后放置过久,消化液内含有的纤维蛋白原就会凝固成为纤维蛋白附着于十二指肠镜表面,成为细菌滋生的有利场所。由于我院ERCP主要是由外科医生在手术室操作完成,并未配备专门的内镜护士,这部分的工作往往容易被忽视。因此我们加强了对手术医生的培训,强化他们的院感意识,由手术医生在十二指肠镜使用后用内镜专用多酶清洗剂完成预处理的操作,缩短了预处理时间,提高了效率。而内镜专用多酶清洗剂则能够较好地处理、分解人体液中的各类有机物。相关研究指出,十二指肠镜相关医院感染暴发的主要污染源来自抬钳器和内镜腔道[9]。十二指肠镜先端部位置隐蔽、体积小、附着微生物多,清洗不彻底的情况下血迹和体液等分泌物在该部位表面和缝隙中形成可影响灭菌机穿透的生物膜,最终导致灭菌失败。针对十二指肠镜先端部、抬钳器的特殊性,我们在日常工作中持续改进,逐步完善清洗细节,形成了我院标准的清洗流程。尤其是在先端部的凹槽缝隙刷洗方面,还特别注重洗刷用具的选择和保养,选择专用的清洗刷,做到凹槽“无缝隙”的刷洗。
本文结果显示,通过床旁预处理和先端部刷洗的清洗流程,十二指肠镜细菌菌落计数明显少于传统清洗方法,清洗合格率也高于传统清洗方法,提示床旁预处理和先端部刷洗可以提高十二指肠镜的清洗效果。根据细菌培养的菌属来看,以阴性菌为主,其中大肠杆菌和柠檬酸杆菌最多见,这与相关文献报道的急性胆管炎时胆汁培养的结果相符合[10]。本文结果表明,增加床旁预处理和先端部刷洗的方法可以减少细菌的残留,从而减少了发生院感的风险。但笔者也发现了克雷伯氏杆菌属的残留,且实验组与对照组相比未见明显减少,是否与该菌属耐刷性较高有关,有待进一步研究。
综上所述,增加床旁预处理和先端部刷洗可减少十二指肠镜清洗后细菌的残留,提高清洗质量。

