胰酶肠溶微丸的制备及体外释药特性研究
冯洋洋,陈章宝
(1.西南大学药学院,重庆 400715;2.西安思源学院护理学院,陕西 西安 710038)
胰酶是从哺乳动物的胰腺中提取并分离得到的一种混合酶,由多种酶组成,主要包括胰脂肪酶、胰蛋白酶、胰淀粉酶等消化酶[1]。胰蛋白酶可促进人体蛋白质分解,胰淀粉酶将淀粉转化成麦芽糖等二糖,胰脂肪酶具有帮助消化人体脂肪的能力[2]。因此,胰酶在临床应用中占据一定地位。胰酶存在自身的缺点,酸性条件下,胰脂肪酶会很快失去活性,中性和碱性条件下,则保持较高活性[3]。为此,要求胰酶制剂应具备耐酸的能力,同时保证在肠道中必须有较高释放度的特性,从而达到助消化作用。目前,关于胰酶制剂上市的产品有多酶片、胰酶肠溶片剂和胶囊剂[2]。多酶片硬度大,口服之后很难分解成小颗粒,不能与食糜同步进入十二指肠,导致胰酶中胰脂肪酶的稳定性差,活性降低[4];胰酶肠溶片针对有吞服困难的患者不适合[2];胰酶肠溶胶囊里面的内容物为胰酶肠溶微丸,在胃中释放出分散体系的胰酶肠溶微丸,到达小肠后快速释放胰酶发挥作用[5]。微丸粒径小,属于多元体系,有缺陷的个别微丸不会影响整体药物释放特性,药物的稳定性得到保证[6]。另外,它属于分散体系,在胃肠道分布面积较大,刺激性小,提高了药物的安全性[7]。关于胰酶制剂的活性和含量评价指标,胰脂肪酶起着决定性作用[8]。因此,在评价市售胰酶制剂时,通常选择以胰脂肪酶的活性和含量作为关键指标[9]。
1 仪器与试药
1.1 仪器
JBZ-300离心式包衣制粒机(中国辽宁.医药新药技术研究所);D-800LS药物溶出仪(天津市天大天发科技有限公司);TG16-W高速离心机(湖南湘仪实验室仪器开发有限公司);UV-2700紫外分光光度计 (日本岛津);sartoriUs普及型pH计(PB-10)(赛多利斯);680酶标仪(美国伯乐);DF-101S恒温加热磁力搅拌器(巩义市予华仪器有限责任公司)。
1.2 试剂
胰酶(武汉三恒医药化工有限公司,胰蛋白酶活力≥1800U/g,胰淀粉酶活力≥21000U/g,胰脂肪酶活力≥12000U/g);胃蛋白酶(1:3000,北京鼎国昌盛生物技术有限责任公司);微晶纤维素(MCC)(上海风泓药用辅料技术有限公司);交联羧甲基纤维素钠(CCNa)(上海风泓药用辅料技术有限公司);羟丙基甲基纤维素(HPMC)(安徽山河药用辅料股份有限公司);滑石粉(成都市科龙化工试剂厂);柠檬酸三乙酯(东京化成工业株式会社);EUdragit L30D -55(德固赛);盐酸、硫酸均为分析纯。
2 方法与结果
2.1 人工胃液对胰酶活力的影响
依据《中国药典》2015年版·二部中胰酶[6]项下关于活力的测定方法,称取适量的胰酶粉3份,分别与人工胃液作用0.5 小时、1 小时、2 小时、3 小时、4 小时后,分别测定胰脂肪酶、胰蛋白酶和胰淀粉酶活力[10],观察人工胃液对三种酶活力的影响,结果见图1。

图1 人工胃液对胰酶活力的影响
从图1可知,在4小时内,胰蛋白酶活力始终保持在0左右,说明活力很低;胰淀粉酶活力基本保持不变,约为20U/mg,人工胃液对胰淀粉酶活力无影响;胰脂肪酶在30分钟时,活力由17U/mg变为0,完全失去活性,说明胰脂肪酶活力相对较高,但是不耐酸,需要抗酸保护,这一结果与相关文献中采用胰脂肪酶活力表示胰酶肠溶制剂的溶出度结果相一致。因此,本实验拟采用胰脂肪酶活力表示胰酶肠溶微丸中胰酶的溶出度。
2.2 载药微丸处方
根据文献和前期预实验设计4个处方。以微丸是否成实心球型及微丸在18~24目(0.8~1.2mm)之间的收率为依据,确定处方。
处方1:MCC∶CCNA∶HPMC:胰酶=8:2∶0.5∶4.5
处方2:甘露醇∶交联聚维酮∶HPMC∶胰酶=8∶2∶0.5∶4.5
处方3:甘露醇∶CCNA∶HPMC∶胰酶=8∶2∶0.5∶4.5
处方4:MCC∶交联聚维酮∶HPMC∶胰酶=8∶2∶0.5∶4.5
结果表明:处方1和处方4可以成丸,微丸硬度较好,收率分别为85%和69%;处方2和处方4都难以成丸,因此考虑选用处方1用 来制备微丸。
2.3 载药微丸制备工艺
2.3.1 制备工艺流程
将处方中涉及到的胰酶粉、MCC、HPMC、CCNA等辅料分别过100目筛,随后分别称取处方比例用量,混合均匀,加适量水制成具有一定可塑性的软材(手握成团、手松即散)[2],立即投入到挤压机中,经1.0毫米孔径筛板挤成细条状,迅速分批次加入到滚圆机内进行制粒和滚圆工艺,调节转盘转速、滚圆时间等因素,待颗粒完全滚圆时停止操作,取出制备的微丸放置于40℃烘箱中干燥20h,整粒后,即得胰酶微丸。
2.3.2 微丸评价指标
① 圆整度:将1.0 g胰酶微丸置一平板上,平板一侧缓慢抬起,测量并记录微丸滚动前倾斜平面与水平所夹的角(Φ),Φ值越小,说明胰酶微丸流动性越好,圆整度越好。
② 收率:通过18~24目(0.8~1.2mm)筛孔的胰酶微丸质量记为m1,总投入量记为m,收率=m1/m*100%,收率越大越好[2]。
2.3.3 工艺条件优化
3个制备工艺影响因素,即软材挤出转速(A)、微丸滚圆转速(B)和时间(C),采用 L9(34) 正交设计实验优化工艺条件(见表1),用圆整度和收率两个指标来评价工艺质量,要求收率(y1)值越大越好,圆整度(y2)越小越好,综合评分采用y=y1-y2表示,y值越大,代表相应的工艺条件越好,结果见表 2和表3。

表1 因素水平表

表2 正交试验结果
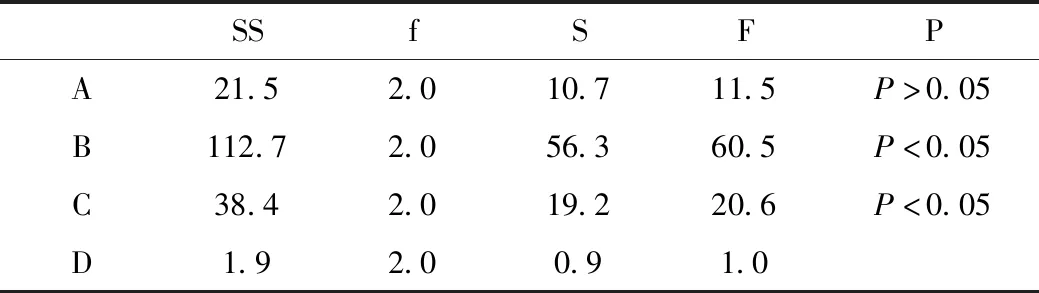
表3 方差分析
由表2和表3可知,影响胰酶微丸制备工艺因素大小的顺序依次是B>C>A,B、C因素为显著因素,挤出速度:924rpm>812rpm>700rpm,滚圆速度:504rpm>560rpm>616rpm;滚圆时间:8min>2min>5min,故最佳工艺为A3B1C3。
2.3.4 工艺验证实验
按照上述确定的胰酶微丸制备最佳工艺参数,同步制备3批小试试验进行验证,结果表明制备工艺参数可靠,具体见表4。

表4 验证实验
2.4 载药微丸的包衣
2.4.1 肠溶层包衣液的配置
取Eudragit L30D-55聚合物水分散体适量,用纯化水稀释至聚合物浓度为15%,搅拌均匀,备用。用纯化水制备浓度12%的柠檬酸三乙酯混悬液,备用。将后者缓慢倒入前者溶液,加水稀释至聚合物浓度为7.5 %,缓慢搅拌30min后,过80目筛网,滤液即肠溶层包衣液。
2.4.2 包衣工艺流程
采用离心式包衣制粒机进行包肠衣。根据预实验可知,向包衣锅中加入适量整粒后的胰酶微丸,用浓度为1% HPMC混悬液包隔离层,包衣过程动态加入适量滑石粉。当隔离层厚度约为10%时,停止包衣,并取出包隔离层后的胰酶微丸于40℃烘箱中干燥约10min,随后,将干燥过的包有隔离层的胰酶微丸再用肠溶层包衣液包衣,当肠衣层达到一定厚度,停止包衣,取出胰酶肠溶微丸,并于40℃烘箱干燥2h,即得。
2.4.3 肠溶层包衣液处方单因素考察
包衣增重对胰酶累计释放度影响:分别称取5份120g包有隔离层的胰酶微丸置于离心式包衣制粒机的包衣锅内进行包衣,包衣增重分别设置为25%、30%、35%、40%、45%,固其他条件不变,滑石粉适量,制备胰酶肠溶微丸,备用。选取《中国药典》2015版·四部通则0931溶出度与释放测定法的第二法,测定胰酶肠溶微丸的体外释放度;采用《中国药典》2015版·二部中胰酶项下的活力测定方法,测定不同包衣增重后胰酶肠溶微丸中胰脂肪酶活力,用活力来计算胰酶累计释放度,见图2。
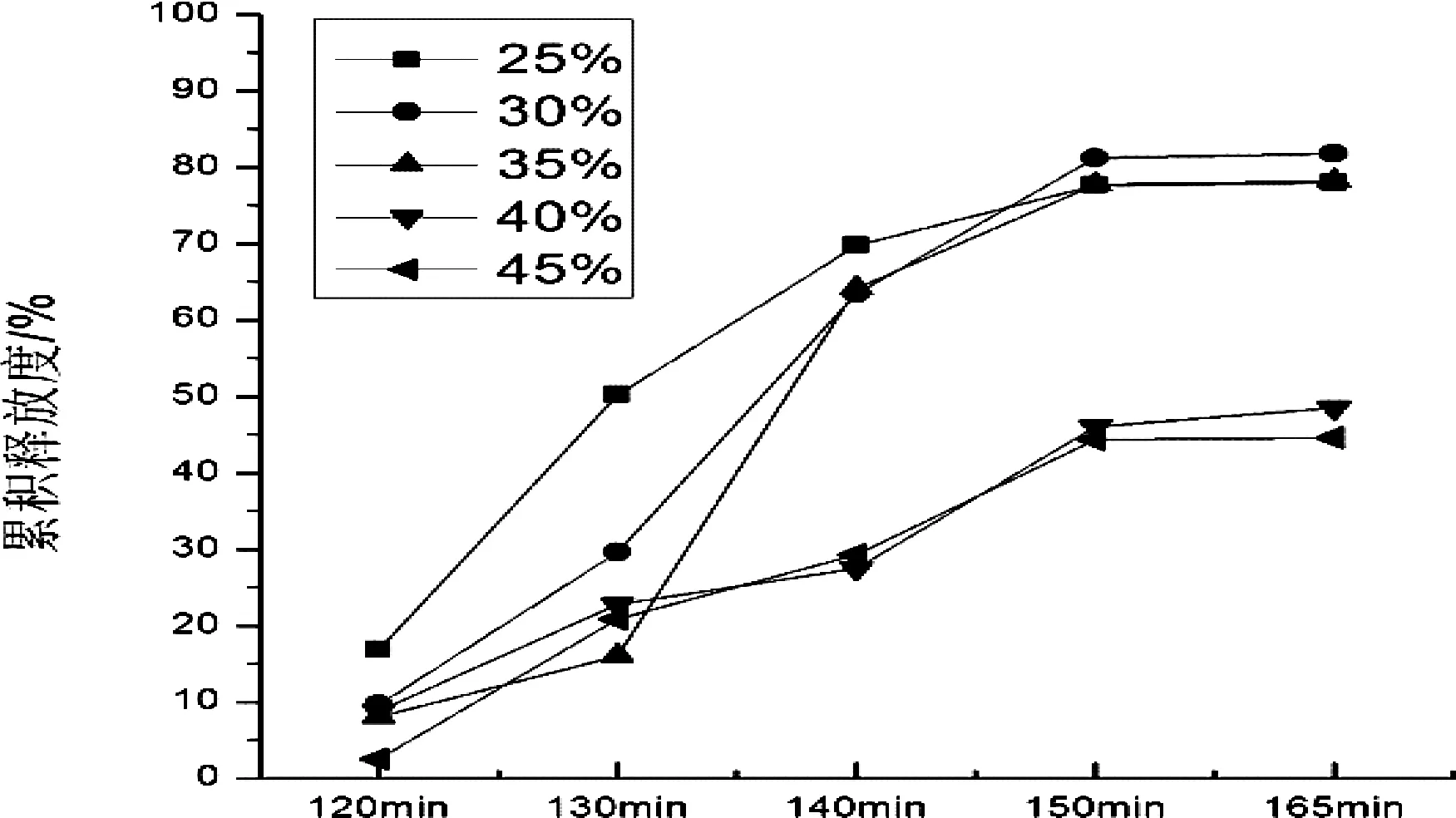
图2 包衣增重对胰酶释放度的影响
由图2可知,肠溶层包衣增重数值为25%时,胰酶在人工胃液中累计释放量>10%,不符合要求;包衣增重为40%和45%时,胰酶在人工肠液中累计释放量﹤70%,不符合要求;包衣增重为30%和35%时,胰酶累计释放度满足要求,考虑到成本和工艺,包衣增重定为30%。
增塑剂用量对胰酶累计释放度影响:配制柠檬酸三乙酯用量分别为12%、16%和20%的肠溶层包衣液进行包衣,保持其他条件不变,按照2.4.3.1项下方法分别测定不同增塑剂用量的胰酶肠溶微丸中胰酶累计释放度,见图3。
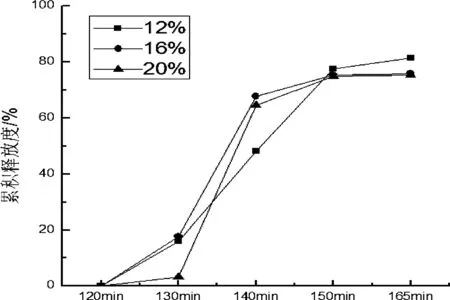
图3 不同增塑剂用量对胰酶累计释放度的影响
由图3可知,3种浓度的增塑剂都满足条件,考虑到成本,故选择增塑剂的用量为12%。
聚合物浓度对胰酶释放度影响:配制聚合物浓度分别为5%,7.5%,10%,在其它条件不变情况下进行包衣。按照2.4.3.1项下方法分别测定不同聚合物浓度的胰酶肠溶微丸中胰酶累计释放度,见图4。
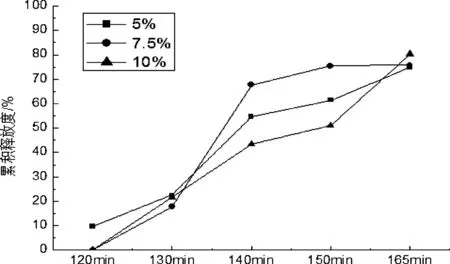
图4 聚合物浓度对溶出度的影响
由图4可知,聚合物浓度为5%时,胰酶在人工胃液中累计释放度>10%,不符合要求;聚合物浓度为10%时,包衣液粘度大,包衣时微丸容易粘连在一起难以分开,进而影响肠溶衣的成膜性,导致不成膜且多孔,药物释放速度加快;聚合物浓度为7.5%时满足要求,故选用聚合物浓度为7.5%。
肠溶层包衣液处方和工艺确定:通过肠溶层包衣液处方中各单因素考察,最后确定包衣处方和工艺为:聚合物浓度为7.5%,包衣增重为30%;柠檬酸三乙酯用量为12%;滑石粉适量。
处方和工艺验证试验:按上述肠溶层包衣液处方和工艺制备3批胰酶肠溶微丸,进行累计释放度测定,结果见表5。结果表明,3批胰酶肠溶微丸的释药速度无显著性差异,说明制备处方和工艺重现性良好。

表5 三批样品累计释放度测定
2.5 不同指标下的释放度考察
取140729批次的胰酶肠溶微丸,按照测定方法,用BCA蛋白浓度试剂盒、胰蛋白酶、胰脂肪酶和胰淀粉酶活力来计算累计释放度[2],见图5。

图5 不同的方法表示胰酶肠溶微丸中胰酶的累计释放度
由图5可知,用BCA蛋白浓度法表示胰酶肠溶微丸累计释放度时,数值要比胰脂肪酶活力表示的高一些,可能是制备过程中,机器产热引起少量胰酶失活所致。胰蛋白酶活力太小,没参考价值;胰脂肪酶活力和胰淀粉酶活力表示的溶出度基本一致,说明胰酶肠溶微丸中胰脂肪酶得到了抗酸保护。
3 讨论
为避免胰脂肪酶在胃酸中失去活性,保证胰酶在肠道中释药的目的,本实验选用Eudragit L30D-55聚合物水分散体作为肠衣材料使用[10]。该肠衣材料显酸性(pH值约为4),直接对胰酶微丸进行包衣时,会使部分胰脂肪酶活力失去,因此考虑在包肠衣之前,先对胰酶微丸进行包隔离层。HPMC是最常用的隔离衣材料,显中性,对胰酶活性无影响,与廉价的滑石粉配合使用,提高了包衣效率。
本实验结果表明,制得外观良好的胰酶微丸收率在90%左右,再进一步用含有滑石粉的HPMC混悬液进行包隔离液衣,当隔离衣厚度为10%时,有效地防止了肠衣对胰酶活力的破坏,最后用Eudragit L30 D-55聚合物水分散体包肠衣时,当肠衣增重为30%时,防止了胰酶肠溶微丸在胃中破坏,同时满足了在肠中迅速释放的要求,提高了胰酶肠溶微丸的稳定性,保证了产品的质量。
由于胰脂肪酶活力会受到胃酸的影响会失活,选用胰脂肪酶活力来计算胰酶肠溶微丸中胰酶的累计释放度,能更好地验证肠溶制剂制备是否成功。此外,本实验选用了BCA蛋白浓度法测定胰酶肠溶微丸中蛋白含量,可以判断胰酶肠溶微丸在制备过程中是否失活,实验结果表明,用离心式包衣制粒机在制备胰酶肠溶微丸时,胰酶有极少部分失活。原因是利用挤出滚圆制备微丸过程中,挤出筛孔与转筒之间摩擦产热,使得胰酶有一小部分失活,在后期工业化生产过程中,对机器工作产生的热量要及时排除,可以考虑进一步安装降温装置。

