废锂电池中钴锂浸出率影响因素的全因子实验
程 前,关世泽,李瑞霖,2,林赟达,徐 苏
(1.厦门理工学院环境科学与工程学院,福建 厦门 361024;2.福建省福海环保科技有限公司,福建 泉州 362000)
随着全球锂离子电池需求量不断增加,废锂电池产生量也日益增加。据估计,2015—2040年,全球会产生50~400万t的废锂电池[1]。废锂电池中含有大量的有价金属,以钴酸锂电池为例,根据电池本身结构的不同,其有价金属钴和锂的含量分别为5%~20%和5%~7%,若没有进行适当处理,不仅会污染环境,还会造成资源浪费[2-4]。目前,针对废锂电池正极材料中有价金属的回收主要有湿法冶金[5-6]、火法冶金[7-8]及机械物理生物[9-10]等处理技术,其中湿法冶金具有选择性好、金属回收率高、环境污染小、能耗低等优点,因而在工业上被广泛应用。
湿法冶金工艺通常是在常压条件下,利用无机酸[5,11]、有机酸[6,12-13]和碱[14]等溶液对有价金属离子进行浸出。由于无机酸和碱腐蚀性强,易污染环境,对实验设备损害较大,而有机酸因对设备损害小,绿色环保,工艺简单,回收率高,可工业化推广,因而被研究者们给予更多的关注。由于废锂电池在酸中的浸出效率会受到多种参数的影响,单因素实验常被用来获取金属离子的最大浸出率[15-17]。然而,单因素实验方法非常耗时,且忽略了参数之间的相互作用,会产生含有偏差的各参数的最优值。如Zeng等[18]利用正交试验设计来优化废锂电池正极活性材料中Co2+和Li+浸出率的提取参数,然而,正交试验是基于线性模型设计,在最佳试验条件区域往往是非线性变化,模型预测性差[19]。前期研究中,本课题组应用响应曲面法对三元系废锂电池正极活性材料中的各金属浸出提取参数进行了优化[20]。然而,响应曲面法通常适用于影响因素不大于3个的体系,且需要大量单因素试验来确定自变量数量及范围[21]。全因子实验是将每个因子的所有水平都参与实验设计,可准确估计所有主效应和各阶交互效应,是一种可以让实验技术与统计有效结合的综合处理方法。该方法采用多元二次回归方程来确定因素与响应值间的函数关系,可以筛选影响产品质量的关键过程参数。因此,本文以锂离子电池正极活性材料为原料,采用温和的NH2SO3H+H2O2体系进行浸出实验。对全因子进行实验设计,考察氨基磺酸浓度、过氧化氢质量分数、固液比、浸出温度对废锂电池中Co2+和Li+浸出率的影响,并分析其交互作用,从而找出最优的浸出条件,以获得快速、高效的浸出反应,实现废旧锂离子电池有价金属的绿色回收。
1 实验方法
1.1 试剂、材料和仪器
NH2SO3H,分析纯,阿拉丁生化科技(上海)股份有限公司;H2O2,分析纯,西陇化工股份有限公司;CoH4N2O6S2,分析纯,山东西亚化学工业有限公司;C5H9NO,分析纯,西陇化工股份有限公司。
废锂离子电池,福建某电池生产商提供。
7000DV型电感耦合等离子体光谱仪(ICP-OES),美国铂金埃尔默仪器有限公司;DF-101s型集热式恒温磁力搅拌器,杭州明远仪器有限公司。
1.2 全因子实验设计
正极活性材料的制备方法参考文献[22]。将正极活性材料溶于NH2SO3H+H2O2的混合体系中,按照实验条件进行钴锂金属离子的浸出。反应一定时间之后,对所得浸出液进行过滤,可得浸出液。正极影响活性材料中Co2+和Li+浸出率的因素包括氨基磺酸浓度、过氧化氢质量分数、固液比、浸出温度等。根据文献[22],固定浸出过程中影响较小的条件,如确定实验的搅拌速度为 300 r·min-1、浸出时间为90 min。选择4个影响Co2+和Li+浸出率的关键因素(氨基磺酸浓度、过氧化氢质量分数、固液比(S/L)、浸出温度(θ))为考察因素,以Co2+和Li+浸出率为评价指标,使用Minitab 17设计4因素2水平的全因子实验设计(24),加入3 个中心点以确认非线性响应,研究各因素的变化对Co2+和Li+浸出率的影响。因素水平见表1。
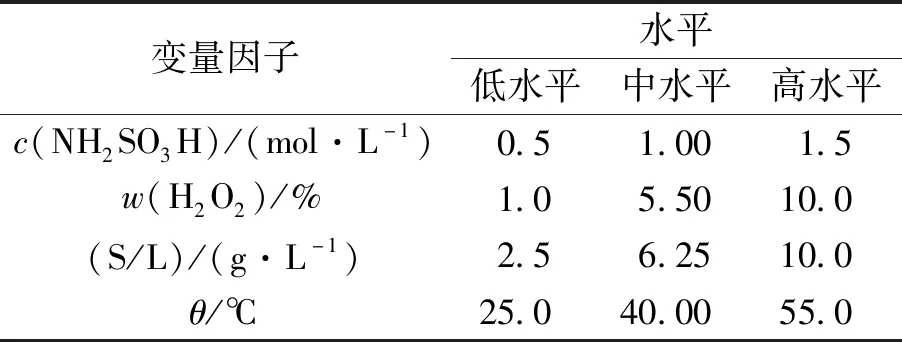
表1 4因素2水平因子全实验因素及水平Table 1 Full-factor experimental factors and levels with four factors and two levels
1.3 分析方法
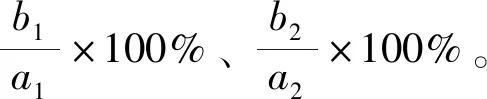
采用代码化的多元回归方程对所得实验结果进行多次二项式模型拟合,如式1所示:
(1)
式(1)中:Z是响应变量;x0、xi、xii和xij分别为截距、线性、平方项和交互项的回归系数;Xi和Xj为各因子的水平值。代码化后的回归方程中,自变量及交互效应项的各系数可以直接比较[23]。采用Minitab 17 软件得到二次多项式回归模型的系数。多元回归方程经过拟合之后可以用来说明响应值与实验变量之间的相关性。交互作用图用来表示变量之间的交互作用。在确定多因素方差分析和二阶模型预测合理的基础上,利用Minitab软件中的响应优化器来确定Co2+浸出率和Li+浸出率最大化的最佳浸出条件。
2 结果与讨论
2.1 全因子实验结果
实验实施的具体参数及数据见表2。组别3、11、16分别对应3个中心点,由表2可见,这3个中心点,Co2+浸出率分别为79.25%、81.56%、80.02%,Li+浸出率分别为73.32%、72.52%、72.34%,数值大致相同,说明实验体系在所设实验条件下是稳定的。
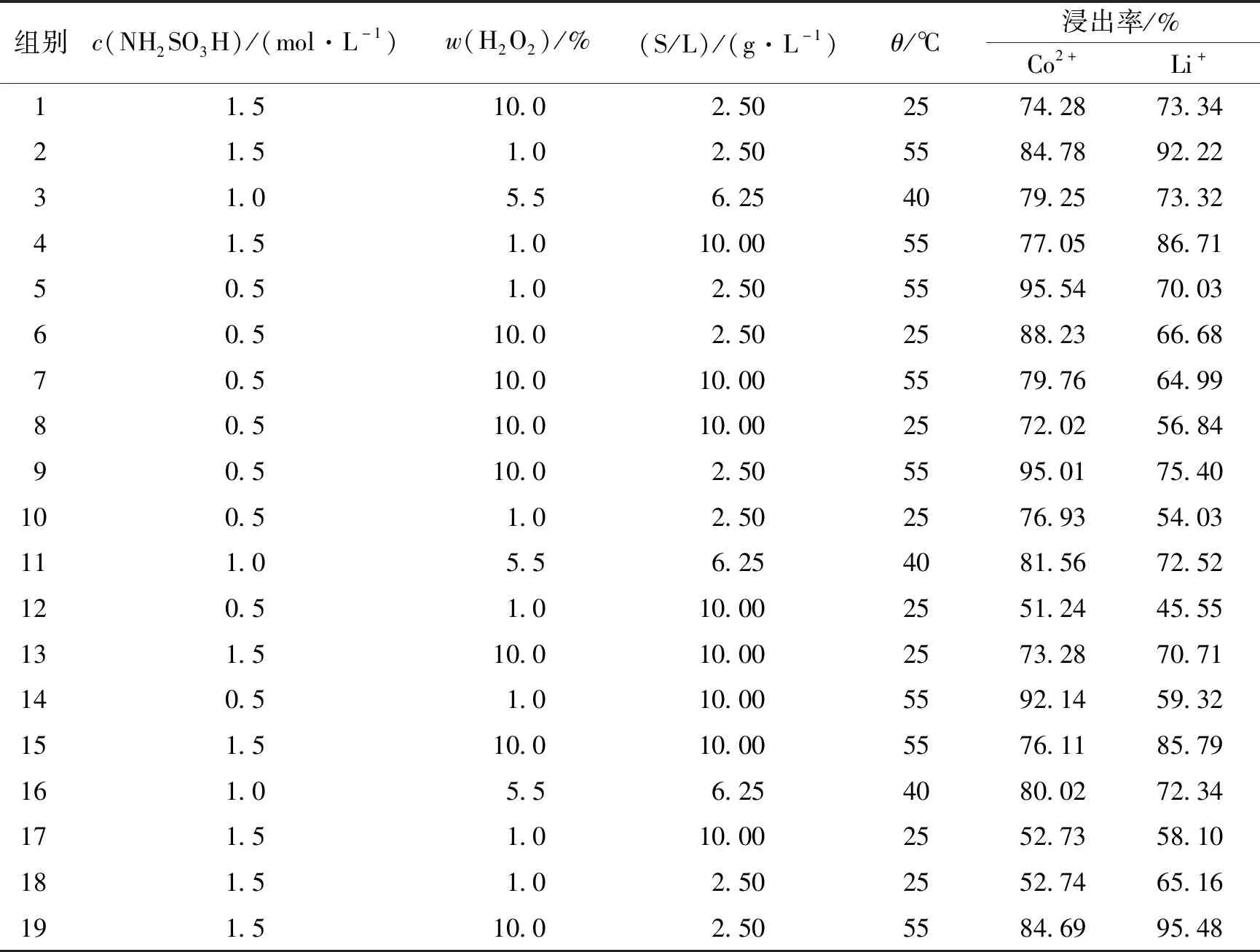
表2 全因子实验结果Table 2 Full-factor experimental results
2.2 实验结果分析
通过对实验数据的多元回归分析,根据软件计算结果提供的数值,可得代码化数据的回归方程式(2)和式(3),响应值和实验变量之间通过式(2)、式(3)进行关联。
Z1=0.331-0.267x1+0.050 7x2-0.038 5x3+0.016 46x4+0.008 24x1x2+
0.0213 9x1x3-0.0015 4x1x4-0.000 596x2x3-0.001 124x2x4+0.000 012x3x4,
(2)
Z2=0.124 2-0.055 2x1+0.027 56x2-0.006 26x3+0.004 40x4-0.002 66x1x2+
0.003 04x1x3+0.007 365x1x4-0.000 269x2x3-0.000 324x2x4-0.000 253x3x4。
(3)
式(2)和式(3)中:Z1和Z2分别由Co2+浸出率和Li+浸出率进行平方变换之后所得;x1、x2、x3和x4分别表示c(NH2SO3H)、w(H2O2)、S/L和θ。
对Z1和Z2的残差进行正态性检测,采用Minitab 17软件进行处理,所得残差结果如图1所示。由图1可得,Z1和Z2的残差所对应的检验统计量P值分别为0.432、0.897,均大于0.05,可认为该残差是正态性的,数据拟合得较好,说明该模型是可信的。

图1 正态概率图残差Fig.1 Normal probability diagram residual error
将主效应项和二因子交互效应项列入模型,得到Z1和Z2的方差分析,结果如表3所示。由表3可见,Z1和Z2回归项的P<0.05,认为回归效果显著,即所选定的模型总的效果是显著的、有效的。本文只分析主效应和二阶交互效应,失拟项的P>0.05,进而认为该回归方程并没有因为忽略高阶交互作用项而产生失拟现象。Z1和Z2弯曲项的P值分别为0.369和0.196,表明本模型中没有失拟现象。
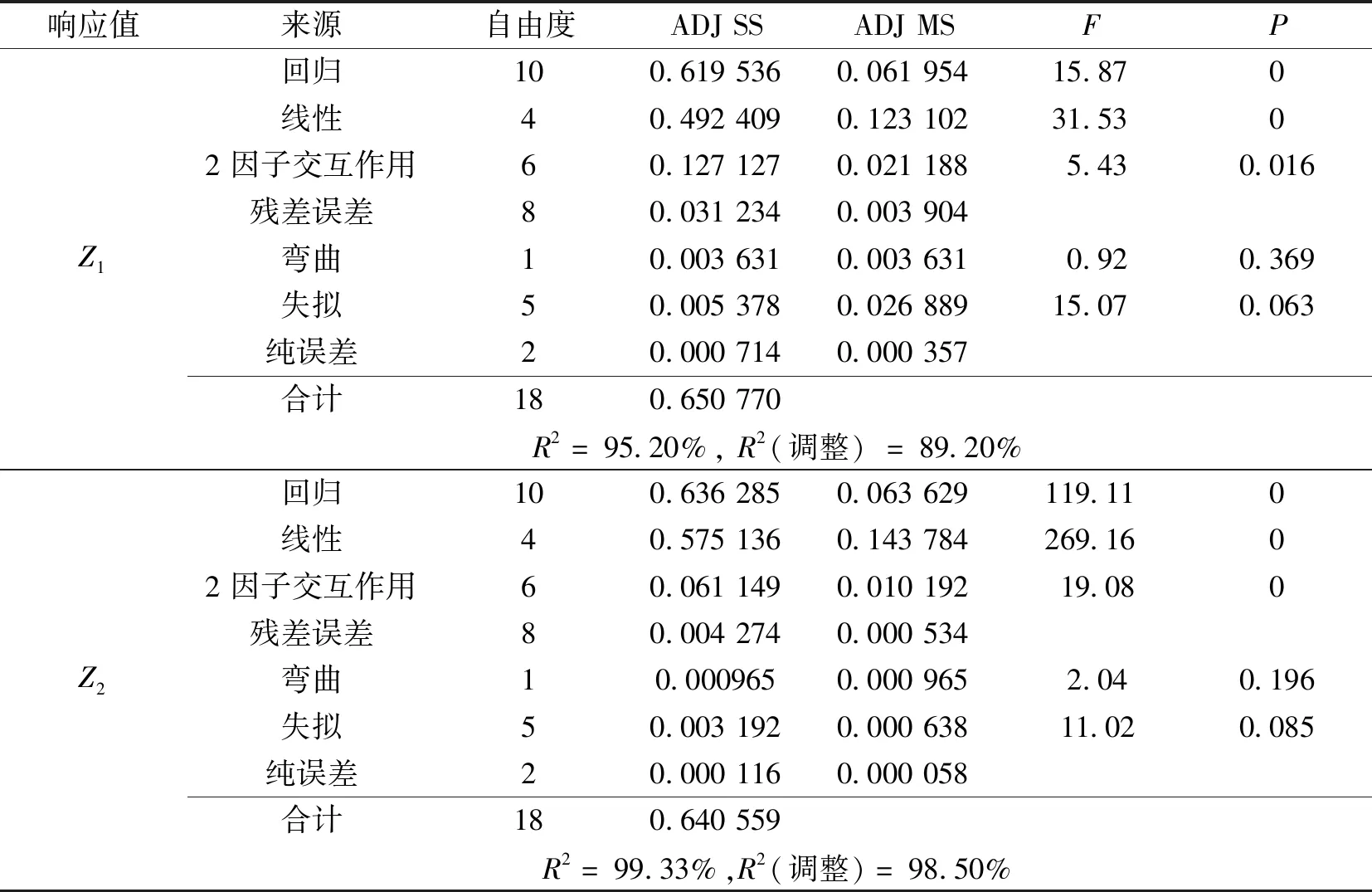
表3 Z1和Z2的方差分析结果Table 3 Analysis of variance table for Z1 and Z2
2.2.1 影响因素的主效应和交互效应
表4为Z1和Z2的估计回归系数。由表4可见,对于Z1,氨基磺酸浓度、过氧化氢质量分数、固液比、浸出温度、氨基磺酸浓度+固液比、过氧化氢质量分数+浸出温度这6项的影响较大;对于Z2,氨基磺酸浓度、过氧化氢质量分数、固液比、浸出温度、氨基磺酸浓度+浸出温度、过氧化氢质量分数+浸出温度、固液比+浸出温度这7项的影响显著。
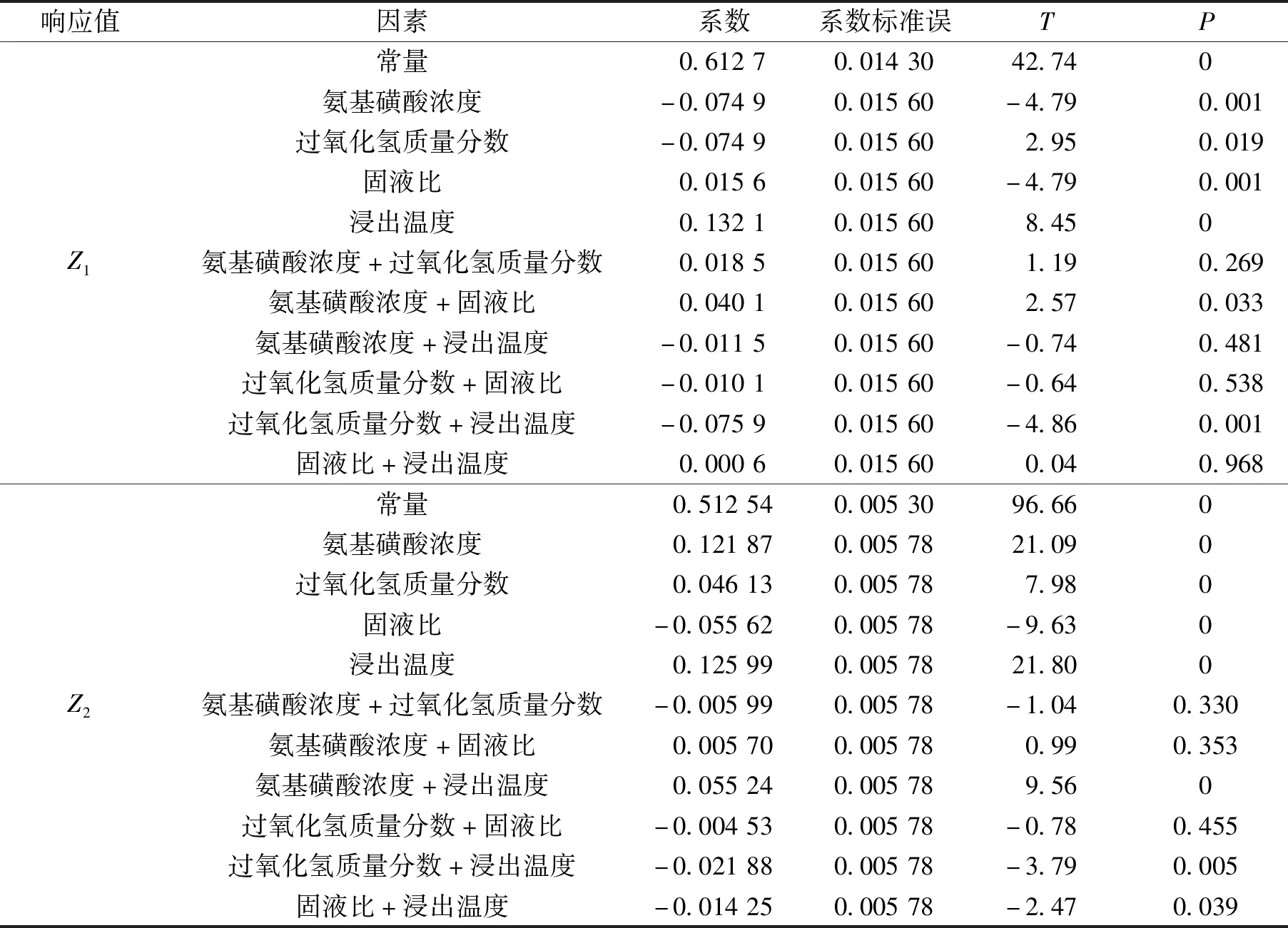
表4 Z1和Z2的估计回归系数Table 4 Estimated regression coefficients for Z1 and Z2
图2(a)、图2(c)为二因子交互效应氨基磺酸浓度+固液比、过氧化氢质量分数+浸出温度为参数对Z1有显著影响的交互作用图,图2(b)、图2(d)为二因子交互效应氨基磺酸浓度+固液比、过氧化氢质量分数+浸出温度对Z1有显著影响3D曲面图。
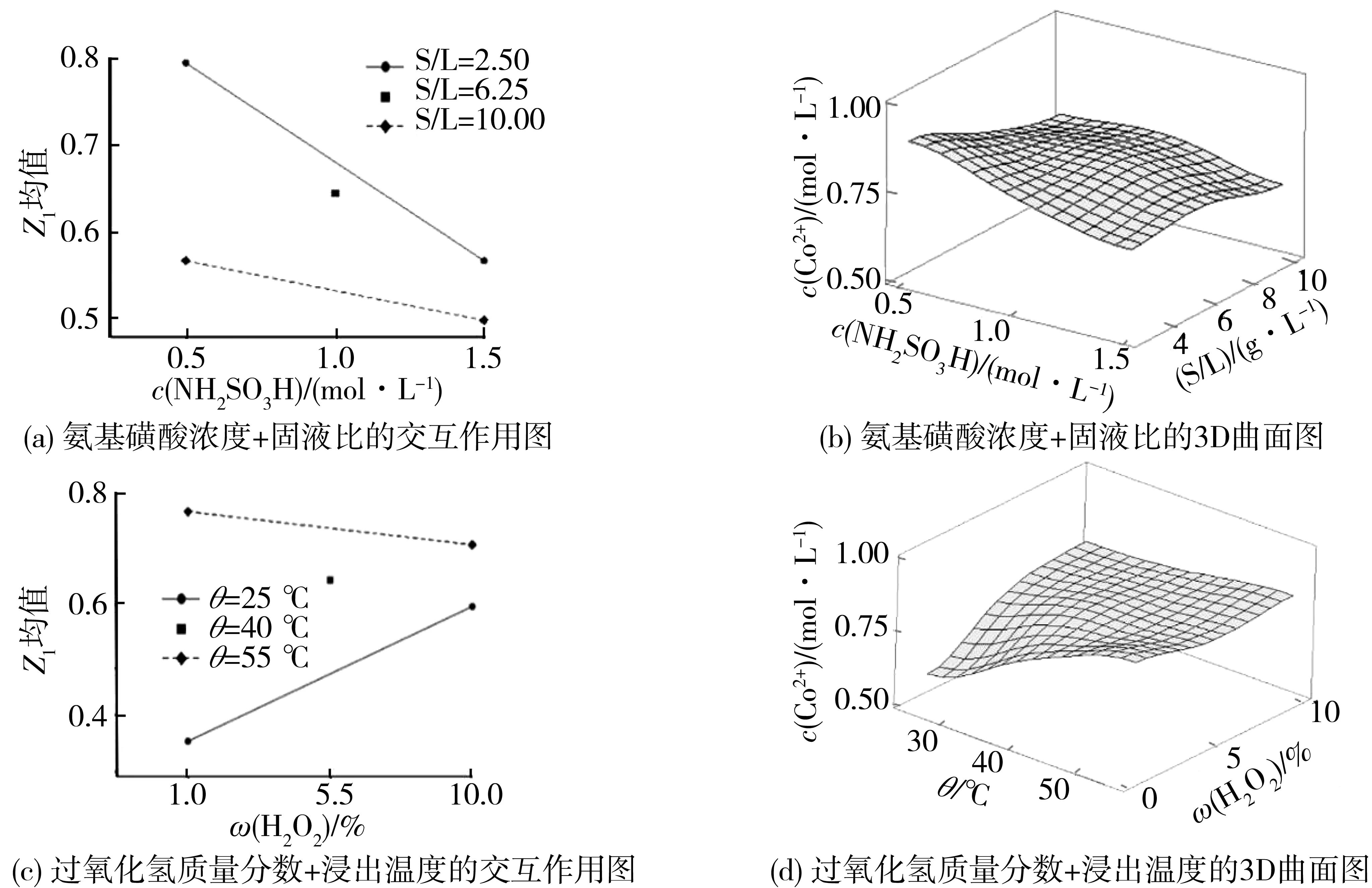
图2 Z1交互作用图和曲面图Fig.2 Interaction diagram and surface graph for Z1
由图2(a)可见,在氨基磺酸浓度和固液比保持中位值的情况下,过氧化氢质量分数和浸出温度对Co2+的浸出率的影响存在明显的交互作用。由图2(b)可见,在所选固液比范围内,Z1随着氨基磺酸浓度的增加均呈现先上升后下降的趋势,在低固液比时,氨基磺酸浓度能提高LiCoO2的溶解活化能,而过高的氨基磺酸浓度将造成反应生成的产物从LiCoO2表面向溶液主体的扩散速度减慢。在高固液比时,低的氨基磺酸浓度为反应提升的活化能不够,太高的浓度反而导致反应液过浓使LiCoO2中的Co3+扩散至溶液中的速度减慢。由图2(c)和图2(d)可见,在过氧化氢质量分数和浸出温度保持中位值的情况下,氨基磺酸浓度和固液比对Co2+的浸出率的影响存在相互作用。在25~40 ℃,Z1随着过氧化氢质量分数的增加出现先上升后下降的趋势,原因是,在反应过程中,H2O2起到还原作用,提高过氧化氢质量分数,能促进更多Co3+还原为Co2+溶解于酸中,从而提高Co2+浸出率[24]。而在40~60 ℃温度范围内,Z1随着过氧化氢质量分数的增加先小幅下降,而后基本维持不变,可能温度提高会促使H2O2发生分解,使得反应溶液与LiCoO2的接触面积变小,从而使得Z1的值小幅下降[25]。
二因子交互效应氨基磺酸浓度+浸出温度、过氧化氢质量分数+浸出温度、固液比+浸出温度为参数的对Z2有显著影响交互作用图分别见图3(a)、图3(c)、图3(e),二因子交互效应氨基磺酸浓度+浸出温度、过氧化氢质量分数+温度、固液比+浸出温度的对Z2有显著影响3D曲面图分别见图3(b)、图3(d)、图3(f)。
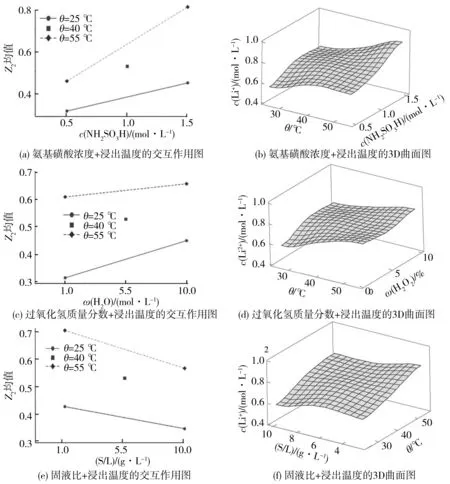
图3 Z2交互作用图和曲面图Fig.3 Interaction diagram and surface graph for Z2
由图3(a)可见,在氨基磺酸浓度和浸出温度保持中位值的情况下,氨基磺酸浓度和浸出温度对Li+的浸出率的影响存在相互作用。由图3(b)可见,随着氨基磺酸浓度和浸出温度的同时增加,Z2也出现增加的趋势。当c(NH2SO3H)=1.25~1.50 mol·L-1、θ=47~55 ℃的范围内,Z2处在曲面中的高水平。原因可能是因为:当氨基磺酸浓度提高时,LiCoO2正极活性材料的溶解活化能增大,而提高温度使得反应液与LiCoO2之间的接触反应更为剧烈,从而提高浸出率[26]。由图3(c)可见,在过氧化氢质量分数和浸出温度保持中位值的情况下,过氧化氢质量分数和浸出温度对Li2+的浸出率的影响存在相互作用。由图3(d)可见,Z2相比于其他曲面图只处于中水平,最高点的值只在0.6左右。主要原因是因为:H2O2作为还原剂主要是促进Co3+还原为Co2+,而对于Li+的影响相对较不明显。由图3(e)可见,在固液比和浸出温度保持中位值的情况下,固液比和浸出温度的交互作用对Li+的浸出率的影响不明显,与表4中固液比+浸出温度对应的2因子交互效应P=0.039相呼应。由图3(f)可见,当S/L=2.5~3 g·L-1、θ=53~55 ℃时,Z2达到曲面图中较高的水平。可能是因为:当固液比低时,LiCoO2与反应溶液接触的面积变大,而温度的提高进一步提高了反应的活化能,从而使得此时的Z2达到高水平。
2.2.2 Co2+浸出率和Li+浸出率最优浸出条件的确定及验证
Co2+浸出率和Li+浸出率的理想值均为100%,即当响应变量越接近目标值时,无标度性响应值D越接近于1。在Minitab 17的响应优化器中设置Z1和Z2为望目1.0000,对于各个变量进行区域约束,约束范围为全因子实验中各个变量所对应的范围,置信水平设置为95%,可得最佳的参数组合为:c(NH2SO3H)=1.44 mol·L-1,w(H2O2)=10%,S/L=2.5 g·L-1,θ=55 ℃。Z1和Z2的整体可取性D=0.714 3,整体优化效果合理。
对响应优化的结果进行验证实验,确保按响应优化所得的条件反应能获得预期效果。在最佳的参数组合下进行4次平行实验,平行实验结果如表5所示。由表5可见,平行实验所得Z1、Z2的均值都落在了95%置信区间内,进一步证明了该预估模型是可信的。

表5 平行实验结果Table 5 Results of parallel experiments
在c(NH2SO3H)=1.44 mol·L-1、w(H2O2)=10%、S/L=2.5 g·L-1、θ=55 ℃的条件下,以反应时间为变量,考察Co2+浸出率和Li+浸出率随着反应时间增加的变化情况,结果如图4所示。由图4可见,Co2+浸出率和Li+浸出率在该优化体系中反应时间为70 min时达到最大,其浸出率分别为95.31%和92.36%。
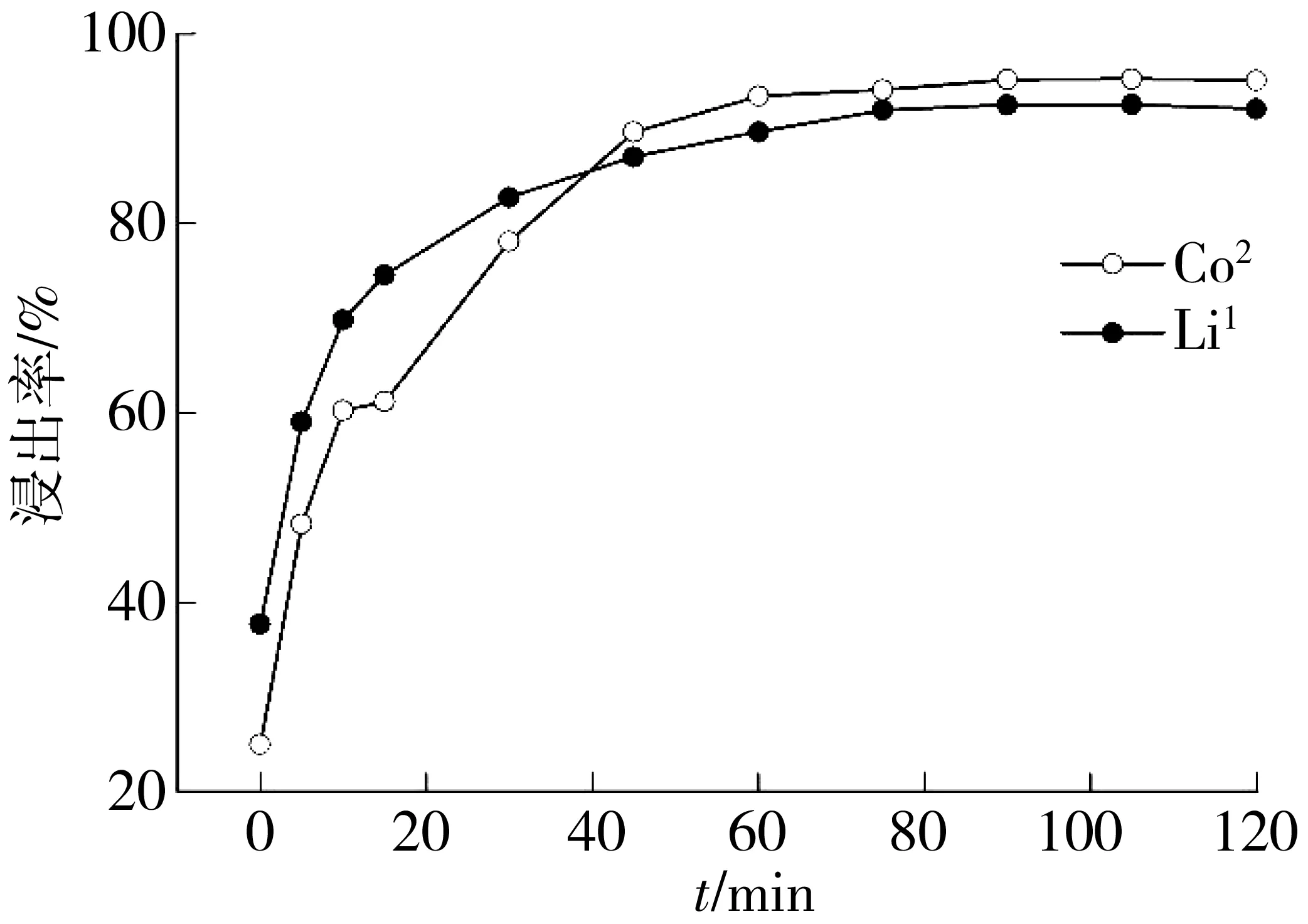
图4 最优浸出条件下Co2+、Li+浸出率与反应时间的关系Fig.4 The relationship between Co2+,Li+ leaching rate and reaction time under the optimal leaching conditions
3 结论
本文考察了锂离子电池正极活性材料在NH2SO3H+H2O2体系的浸出行为,并利用全因子实验研究了氨基磺酸浓度、过氧化氢质量分数、固液比、浸出温度对废锂电池中Co2+和Li+浸出率的影响。
1)全因子实验分析结果显示,氨基磺酸浓度、过氧化氢质量分数、固液比、浸出温度这4项主效应,以及氨基磺酸浓度+固液比、过氧化氢质量分数+浸出温度这2项交互效应对Co2+浸出率有显著影响,其余效应影响并不明显;氨基磺酸浓度、过氧化氢质量分数、固液比、浸出温度这4项主效应以及氨基磺酸浓度+浸出温度、过氧化氢质量分数+浸出温度、固液比+浸出温度这3项交互效应对Li+浸出率有显著影响,其余效应影响较小。
2)根据全因子实验结果,在使用响应优化器优化得到的最佳浸出条件下进行验证实验,得到的结果落在95%置信区间,表明该模型是有效的。
3)Co2+和Li+最优浸出条件为:c(NH2SO3H)=1.44 mol·L-1,w(H2O2)=10%,S/L=2.5 g·L-1,θ=55 ℃,t=70 min,在最优浸出条件下,Co2+和Li+浸出率同时达到最大,分别为95.31%和92.36%。

