肿瘤电场治疗仪治疗复发脑胶质母细胞瘤的前瞻性单中心单臂探索性研究*
周俊 罗承科 刘嘉霖 刘羽阳 贾牧原 李泽 陈凌 刘志雄
胶质瘤(glioma)是最常见的原发性颅内肿瘤,其中一半以上为恶性程度最高的胶质母细胞瘤(glioblastoma,GBM),属WHO Ⅳ级,年发病率约3.2/10万例,是目前世界上死亡率最高的三大肿瘤之一。近30 年来,脑胶质瘤发病率逐年递增,年增长率为1%~2%。脑胶质母细胞瘤从发现至死亡,虽然经过“手术、同步放化疗及辅助化疗”标准治疗,中位生存期仍仅13~16 个月[1]。而且,患者术后发生的神经功能障碍也给患者和家属带来较大负担。由于现有治疗手段的相对局限性,胶质瘤手术精准切除结合放化疗方案的治疗效果已达瓶颈,面临着患者整体生存时间短、肿瘤复发快、放化疗不良反应大等突出问题。随着医学科技探索的进步,一种创新的无创物理治疗手段“肿瘤电场治疗”技术应运而生。此手段已被国外大样本详实的循证医学Ⅲ期临床试验数据证实为有效[2-3],其对于延缓胶质母细胞瘤的复发、进展以及延长患者生存期具有重要意义。肿瘤治疗电场于2013 年起列入美国国家综合癌症网络(NCCN)中枢神经系统肿瘤治疗指南,并分别于2015 年和2018 年列入中国的《中国中枢神经系统胶质瘤诊断与治疗指南》和《脑胶质瘤诊疗规范》。肿瘤治疗电场作用的基本原理,不同于电流、射线或者磁场,是基于肿瘤细胞内极性分子受中频(100~300 kHz)、低强度(1~3 V/cm)的交变电场所牵拉,有丝分裂活动受阻,并最终使肿瘤细胞死亡[4-5]。然而,目前鲜见国产肿瘤电场治疗仪的安全性及疗效研究,本研究为截至目前国内首个使用国产肿瘤电场治疗仪的前瞻性、单中心、单臂探索性研究,主要目的是评价国产肿瘤电场治疗仪用于治疗复发胶质母细胞瘤患者的初步安全性和有效性。
1 材料与方法
1.1 临床资料
选取2020 年4 月至2020 年8 月中南大学湘雅医院和解放军总医院6 例复发胶质母细胞瘤受试者,均为男性,中位年龄53(48~68)岁,其中4 例经影像学诊断复发GBM,2 例经手术和病理诊断复发。所有患者入组时一般状态良好,KPS 评分≥70 分(表1)。本研究通过伦理委员会的批准(临床研究登记号NCT 04 417933;中南大学湘雅医院伦审科第 202001012号)。入组受试者或家属已签署知情同意书。

表1 6 例复发GBM 患者临床特征
入组标准:1)首次手术病理组织学确诊为脑胶质母细胞瘤者(WHO Ⅳ级,位于幕上)。2)年龄18~65 岁,男女不限。3)之前已完成放疗和至少2 个周期化疗。4)影像学或再次病理提示肿瘤复发。5)治疗前KPS 评分≥70 分。6)预期寿命≥3 个月。7)育龄妇女采取有效避孕措施。
排除标准:1)不愿意每天使用仪器设备≥18 h。2)依从性差或距离研究中心太远,不能亲自到院进行定期随访、调整治疗设备电极位置以及不接受随访至终末生存期。3)医师判断为头皮伤口愈合欠佳、头部皮肤状态欠佳、颅骨大面积缺损或其他不适合佩戴电极情况。4)距离放疗3 个月内;距离末次化疗4 周内;距离复发手术后4 周内;已参与其他临床试验。5)妊娠期妇女。6)癫痫症状未有效控制。7)血液及生化检查指标明显异常。8)患有严重感染性疾病者,如急性重症或HIV 感染。9)其他情况,如哺乳期、安装心脏起搏器和脑部刺激器;严重的颅内水肿、颅内压增高导致中线结构超过5 mm、视神经乳头水肿和意识障碍等;对导电耦合剂、凝胶过敏等,以及存在其他威胁生命的重大疾病。10)医师认为的不适合进行本治疗试验的其他情况。
1.2 方法
1.2.1 研究设计 本研究使用国产肿瘤电场治疗仪(湖南安泰康成生物科技有限公司,ASCLU 型)已通过中国食品药品检定研究院的检测,取得检测合格报告。临床前细胞实验和动物实验表明该设备具有良好的安全性,且对胶质母细胞瘤具有显著的抑制作用。
1.2.2 研究终点 主要终点为治疗安全性和患者耐受性。次要终点为肿瘤进展时间(time to progression,TTP)和总生存(overall survival,OS)时间。
1.2.3 治疗方式与要求 患者进行肿瘤电场治疗之前,需剃除头发,在医生的指导下将2 对无菌电极片无创性敷贴于头皮,电极片连接于主机,启动主机即开始治疗。医生将培训入组患者及其家属操作设备,患者可自行操作设备进行治疗。研究人员每天与受试者保持沟通,通过通讯工具或家访了解头皮不良事件的情况。受试者因肿瘤进展或不能耐受而中止/退出电场治疗临床研究后,医生根据患者病情予以最佳治疗方式。若患者要求延用电场治疗,经研究团队评估其获益/风险比,视情况决定是否继续使用电场治疗。推荐患者每天连续治疗时间≥18 h,可根据患者个人情况,如洗澡等适当间断。使用肿瘤电场治疗仪每28 天为1 个疗程。根据患者病情需要,允许联合指南推荐的药物治疗。
1.2.4 安全性评估 参考NCI-CTCAE5.0 评价不良事件的发生;通过不良事件和严重不良事件的发生频率对肿瘤电场治疗仪的安全性和受试者耐受性进行评估。
1.2.5 有效性评估 通过观察受试者的TTP 和OS获得肿瘤电场治疗仪的治疗有效性信息。采用神经肿瘤疗效评价(response assessment in neuro-oncology,RANO)标准,通过影像学结果、皮质激素应用和临床表现情况综合评估肿瘤进展状态,评估类型分为完全缓解(complete remission,CR)、部分缓解(partial remission,PR)、疾病稳定(stable disease,SD)和疾病进展(progression disease,PD)。
1.2.6 随访 受试者每个月进行血常规、血生化、凝血功能、尿常规和心电图检查;每2 个月进行头颅磁共振平扫及增加检查,停止电场治疗后进行2 个月的安全随访,后续通过电话进行生存随访。
1.3 统计学分析
采用SPSS 25.0 软件进行统计学分析。TTP 及OS 自入组开始计算,TTP 截至肿瘤进展或末次随访时间,OS 截至死亡或末次随访时间。生存分析采用Kaplan-Meier 法。以P<0.05 为差异具有统计学意义。
2 结果
2.1 治疗完成情况
6 例患者使用时间依从性良好,均达到18 h/d。1 例持续至2022 年1 月的末次随访时仍在使用,5 例使用至肿瘤进展后仍选择维持电场治疗。1 例受试者单用电场,5 例联合药物治疗,其中病例2 使用过替莫唑胺,病例3、5、6 使用过贝伐单抗。本研究允许使用指南推荐的药物治疗,病例3、5、6 使用过贝伐单抗,一定程度上缓解了神经症状,为患者争取到更多使用电场治疗的时间,为电场治疗发挥疗效提供更大的可能性。未进行特异靶点筛选,6 例患者中5 例已发生OS 事件。仍生存患者以及下一步研究中,将注意是否存在ZM 融合基因患者,以推荐进行伯瑞替尼靶向治疗。代表性病例治疗情况见图1。
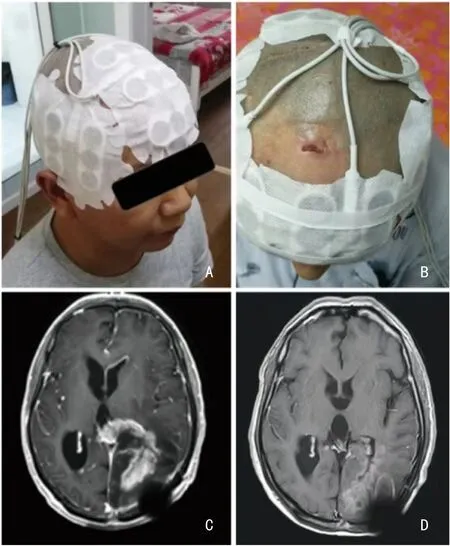
图1 代表性病例治疗情况及头颅影像
2.2 生存分析
6 例受试者中位随访时间10.9(8.4~22.7)个月。均发生肿瘤进展,5 例随访至死亡,1 例仍生存。中位肿瘤进展时间(median time to progression,mTTP)为4.7 个月(95%CI :3.62~5.78),中位无进展生存时间(median progression-free survival,mPFS)为4.7 个月(95%CI:3.62~5.78),中位总生存时间(median overall survival,mOS)为10.9 个月(95%CI:8.86~12.94)。
2.3 客观缓解率
1 例治疗2 个月后肿瘤缩小≥50%,达到PR 并持续1 个月以上,活动能力显著改善;1 例治疗1 个月肿瘤缩小≥50%,达到PR,活动能力和认知功能显著改善,并持续至治疗后6.6 个月;1 例接受治疗21.2 个月复查显示SD;1 例治疗2 个月后SD,并于治疗4.7 个月后进展;1 例治疗3 个月后呈SD,并于治疗4.9 个月后进展;1 例治疗2 个月时发生PD。总体上,2 例最佳治疗反应为PR,3 例为SD,1 例为PD,客观缓解率(CR+PR)33.3%,疾病控制率(SD+PR+CR)83.3%。
2.4 不良事件
不良事件见表2。治疗期间,受试者复查血常规、血生化、凝血功能、尿常规和心电图,均未出现严重不良事件,未见明显试验设备相关的全身系统性不良反应。未见Ⅲ~Ⅳ级不良事件。
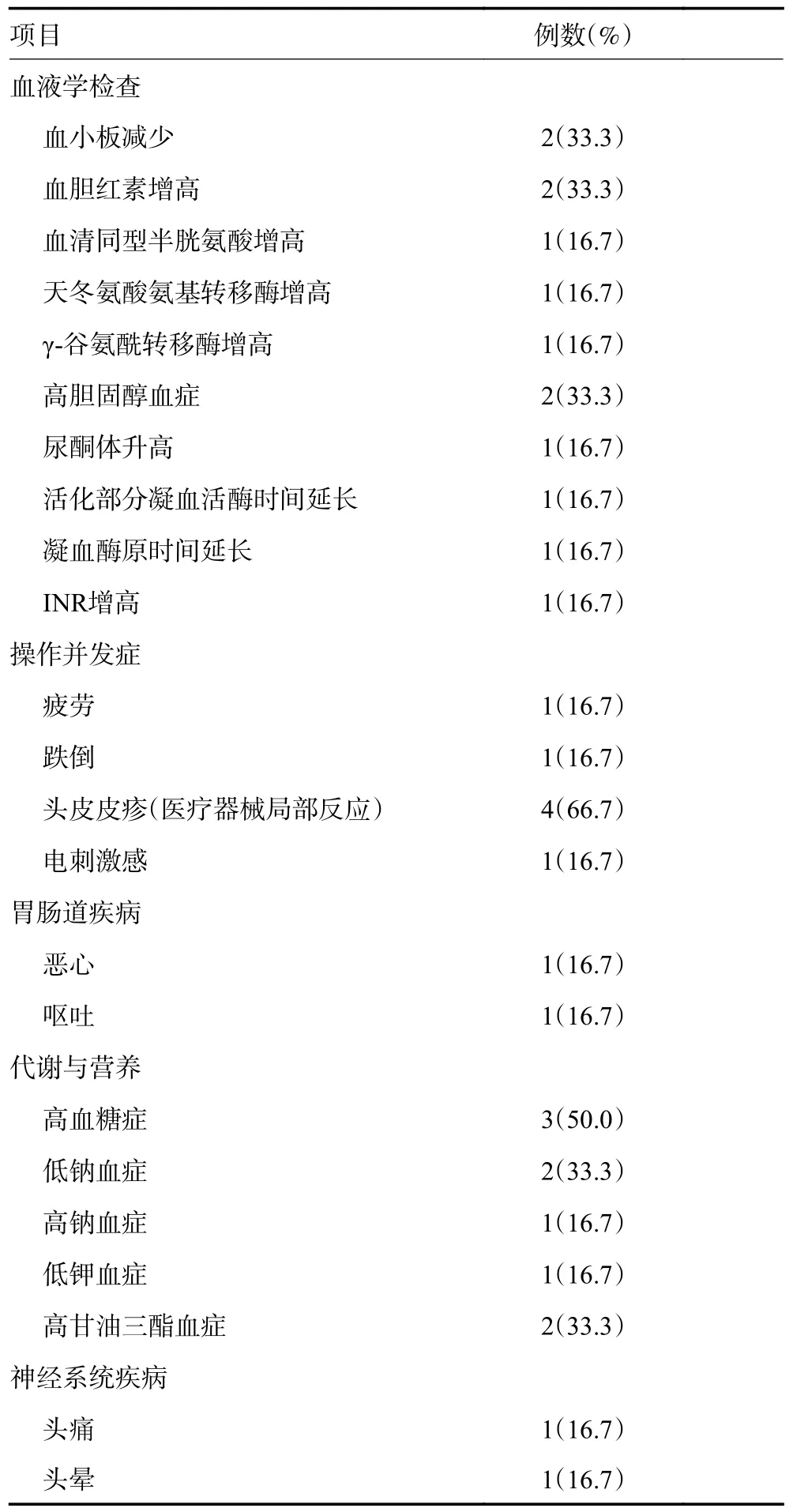
表2 不良事件发生情况
治疗相关的不良事件主要为Ⅰ~Ⅱ级头皮皮疹,发生率66.7%,属于医疗器械局部反应。其中1 例受试者出现轻度的头皮局部皮疹;2 例出现头皮皮疹后表皮破损,经调整电极片黏贴位置,保持创口干燥后恢复;1 例患者出现轻度的头皮局部水疱,经涂抹抗生素软膏及保持干燥后完全恢复。头皮局部皮炎经涂抹高效类固醇类和(或)抗生素软膏后均可有效缓解,未影响治疗依从性。其他不良事件有头晕、头痛、恶心呕吐、疲劳乏力、跌倒、电刺激感各1 例以及实验室医学检查异常等。此外,肌力下降、视物模糊、失语等与疾病发展直接相关的症状或体征,未视为不良事件。
3 讨论
目前,新诊断GBM 主要的治疗方式为经典的STUPP 方案,尚无针对复发性GBM 的标准治疗方法。国际上近10 年的研究发现,肿瘤电场治疗在新诊断GBM 患者的无进展和总体生存方面均有显著的改善,复发患者也可从电场治疗中获益。肿瘤治疗电场是低强度、中频交变电场,通过非侵入性传感器阵列(敷贴式电极片)传递至肿瘤区域周围。电场治疗作用于细胞有丝分裂过程中的大量极性大分子和细胞器。这些细胞成分的结构变化或错位可能改变其生理功能,并最终破坏正常的有丝分裂。
电场治疗对各种细胞过程的影响可以用两个基本的物理原理进行解释,即偶极子排列和介电泳[6]。偶极子是指分子中正电荷和负电荷的分离。在均匀的交变电场下,任何极性分子均将振荡,试图使其适当地平行于其所接触到的电矢量的方向[6]。负责有丝分裂和细胞分裂的关键大分子和细胞器是高度极性的,随机运动对其功能至关重要,可被局部电场破坏[7]。成功的有丝分裂需要在细胞分裂的不同阶段对可极化或带电结构进行精确的空间和时间对齐。在非均匀电场中,一种力施加在极性分子上,导致其迁移至一个高电场密度的区域,此过程称为介电泳[8]。基于多个参数,电场治疗在治疗区域内非均匀分布,这些参数包括治疗器官的几何形状、组织与体表电极的位置关系以及组织的介电特性[9]。电场并非随着与电极的距离而线性衰减,因此可用于深部肿瘤的治疗[10]。由于电场没有半衰期,电场治疗可以在治疗过程中持续发挥作用。
基于对作用机制的进一步研究,电场治疗已经被证明可通过消除中期细胞质内微管蛋白亚单位的正常随机运动,破坏形成有丝分裂纺锤体的微管的正常聚合过程[3,8,11],从而导致中期阻滞,延长有丝分裂,最终细胞死亡[12]。而在分裂中期逃脱了有丝分裂阻滞的细胞继续分裂,呈现沙漏状,导致非均匀电场的形成,并在卵裂沟区形成高强度电场。Septin 复合物负责收缩蛋白的生理定位,使细胞正常分裂为2 个子细胞,但电场的介电泳作用下可引起其脱位。这种作用发生在末期,可导致剧烈的细胞质起泡和细胞死亡[13-14],或异常的染色体分离导致子细胞非整倍体,并随后降低克隆基因的潜力[14]。电场治疗的上述作用最终导致细胞凋亡,并增加免疫原性细胞死亡标志物的细胞表达[6,14]。在正常分裂的组织中,鲜见因基因改变或其他有丝分裂效应而导致电场治疗相关不良事件的报道。
本研究团队基于国内外中频交变电场生物学效应研究结果,借鉴国际上已有类似领域产品特点,进行了电场参数及作用模式优化等多项创新,实现个体化电场治疗技术突破。在针对前期原理样机开展的大量细胞及动物实验研究结果基础上,成功研发出国产肿瘤电场治疗仪(ASCLU 系列)。本研究是截至目前国内首个关于国产肿瘤电场治疗仪的前瞻性单臂临床研究,评价国产肿瘤电场治疗仪治疗复发GBM 的初步安全性和有效性。安全性方面,国际文献报道电场治疗可出现电极覆盖部位的接触性皮炎、浅表破损/溃疡、感染/毛囊炎等,11%患者可出现电刺激感(tingling),这是电场治疗的正常现象[15]。本研究观察到的不良事件主要是头皮在电极敷贴部位下的Ⅰ~Ⅱ级皮疹,发生率为66.7%(4/6 例),经涂抹类固醇类/抗生素软膏可有效缓解,另外有1 例(16.7%)患者感受过轻微的电刺激感。根据观察,油性皮肤以及环境温度较高(研究开展时处于夏季)可促进头皮局部皮疹发生;及时清洗头皮、注意头皮卫生、剃头及更换电极片时轻柔操作则可降低头皮皮疹的发生。2 例受试者在长时间治疗过程中保持良好的头皮皮肤状态,可能与良好的头皮护理有关。总体而言,肿瘤电场治疗仪所引起的头皮不良事件,可通过头皮护理措施进行预防,并可通过涂抹外用药物进行缓解。其他不良事件如头痛、头晕、恶心呕吐、疲劳、跌倒,很可能与研究程序或疾病本身相关。医学检查中,血小板降低可能与受试者同时使用其他化疗药物有关,生化指标的轻-中度异常很可能与肿瘤患者系统功能变化及生活习惯相关。而电解质轻度紊乱是脑肿瘤患者的常见现象。这些异常指标的特异性较低,经处理和改善,未影响电场治疗。
有效性方面,本研究1 例受试者PFS/TTP 为2个月,其余均>2 个月,总体中位PFS 为4.7 个月,中位OS 为10.9 个月,客观缓解率为33.3%。EF-11 研究表明[15],国际同类设备用于治疗复发GBM 的临床疗效与最优化疗相近,PFS 为2 个月,OS 为6.6 个月,ORR 为14%(95%CI:7.9~22.4%)。EF-11 研究中纳入的一次复发患者占9%,二次复发占48%,其余为更多复发次数患者,受试者总体KPS 为80 分。EF-11 受试者的多次复发比例较高,可能是单用电场疗效未优于化疗的原因之一。另外,由于本研究允许联合临床常规药物治疗,部分患者使用了贝伐单抗或替莫唑胺,这为提高患者生存质量、延长电场使用时间以达到最优疗效提供了更多可能性。第4 届中国脑胶质瘤学术大会(2020 年)公布了一项评估肿瘤电场治疗(美国爱普盾)在中国GBM 患者中的前瞻性、单臂观察性研究结果,提示复发GBM 患者中位无进展生存期为4.5 个月,中位总生存期为8.6 个月,最常见的不良反应是轻度至中度皮肤刺激,发生率为66.7%,均为Ⅰ~Ⅱ级。因此,本研究中的生存数据及头皮不良事件与国际同类产品的临床研究数据结论相符,较高的OS 生存数据展现出良好的治疗前景,表明该肿瘤电场治疗仪具有良好的安全性和有效性。另外,本研究的2 号受试者,因2 个月进展时具备再次手术获取组织的可行性,本研究组对其术后原代细胞进行了敏感频率的体外探索,发现该受试者组织细胞对200 kHz不敏感,并调整其治疗频率为170 kHz 继续治疗,最终OS 为10.9 个月。因此,该受试者早期进展的原因可能是对200 kHz 不敏感,经调整至敏感频率后,仍获得较长的总生存时间,表明个体化敏感频率的应用可能是提高电场疗效的重要方向。
本研究的局限性:1)入组受试者数量较少,安全性和有效性还需要在更大样本中进一步评估。2)单臂研究存在一些系统性偏倚;虽然本研究是前瞻性研究,但缺乏严格的对照组,患者PFS 或OS 的延长尚需通过前瞻性、随机对照的大样本多中心临床试验进一步验证。3)敏感性亚组人群有待进一步研究目前中外指南均推荐电场治疗应用于新诊断和复发GBM,将来,更多的基础和临床研究将集中于揭示电场治疗的准确机制机理,以及电场治疗的个体敏感性或抵抗性。除治疗GBM 外,电场治疗临床研究未来可拓展至更多瘤种,探索电场与化疗、靶向或免疫治疗联合应用的可能性,为患者提供最佳治疗方案,以最大程度改善患者预后并提高生存质量。电场治疗设备将随着科技的进步,在体积和重量上进一步优化,给患者更好的体验。

