贝伐珠单抗治疗复发胶质母细胞瘤疗效和预后分析*
崔润 郭琤琤 郭颖 吕晓飞 胡婉明 陈忠平 牟永告 杨群英
胶质母细胞瘤(glioblastoma,GBM)是成人最常见且恶性程度最高的原发性脑肿瘤。采用最大安全范围手术切除、放疗和替莫唑胺化疗的标准治疗后,绝大多数患者出现肿瘤复发进展[1]。贝伐珠单抗(bevacizumab)作为复发后的治疗药物,为一种人源化单克隆抗体,靶向血管内皮生长因子(vascular endothelial growth factor,VEGF)来阻断肿瘤新血管生成。2009年美国食品药物管理局(FDA)基于两项Ⅱ期非随机对照临床试验结果[2]批准贝伐珠单抗用于复发GBM,临床广泛用于GBM 患者的挽救性治疗。2020 年9 月中国国家药品监督管理局(NMPA)批准贝伐珠单抗用于成人GBM 患者的治疗。
贝伐珠单抗是继替莫唑胺后GBM 治疗中最重要的药物之一。尽管现有的Ⅲ期随机对照临床试验(AVAglio,RTOG0825,EORTC26101)[3]结果显示贝伐珠单抗未能改善新诊断或复发GBM 患者的总生存期(overall survival,OS),但对无进展生存期(progression-free survival,PFS)有改善,同时可以改善健康相关生存质量评分和认知功能,并且可以减少患者对糖皮质激素的需求。因此,在目前复发GBM 缺乏有效挽救治疗手段的现状下,贝伐珠单抗在复发GBM 中的应用仍得到了国内外指南的一致推荐。国外文献报道了贝伐珠单抗在GBM 中的临床试验结果和应用经验[4]。但迄今为止,来自中国患者的数据较少。贝伐珠单抗的最佳治疗模式和预后影响因素仍不清楚,复发后早期使用还是延迟使用、高剂量使用还是低剂量使用、是否需要联合细胞毒药物化疗等临床问题尚无明确答案。本研究回顾性分析2011 年12 月至2020年7 月于中山大学肿瘤防治中心接受贝伐珠单抗单药或联合化疗治疗的81 例IDH 野生型成人复发GBM 患者的临床资料,评价真实世界临床实践中贝伐珠单抗的疗效和安全性,探讨其预后影响因素和最佳治疗模式。
1 材料与方法
1.1 临床资料
本研究纳入2011 年12 月至2020 年7 月于中山大学肿瘤防治中心接受治疗的81 例复发GBM 患者,其中男性54 例,女性27 例,年龄18~70 岁。入组标准:既往接受过手术、放疗和替莫唑胺辅助化疗后首次或多次(≥2 次)复发的GBM 患者;IDH 野生型;年龄≥18 岁;颅脑MRI 增强检查有可评价病灶;血常规、肝肾功能、心电图正常;止血、凝血功能正常,无明显出血倾向;签署知情同意书。排除标准:年龄<18 岁;IDH 突变型;4 周内接受过手术或预期接受手术治疗;存在愈合不良伤口;既往有脑出血和脑梗塞病史;对贝伐珠单抗过敏;存在严重的如心血管疾病、肝肾疾病或血液病等可能干扰治疗的基础疾病。
1.2 方法
治疗方法:贝伐珠单抗5~10 mg/kg,每2~3 周1 次。根据患者既往化疗的疗效及生存质量状况评分(KPS 评分)采用贝伐珠单抗单药或联合个体化的化疗。停药标准:贝伐珠单抗用至肿瘤进展或不良反应不可耐受,联合替莫唑胺化疗用至最多12 个周期或不良反应不可耐受,联合其他细胞毒化疗用至最多6 个周期或不良反应不可耐受。
疗效评价:治疗开始后每2 个周期进行颅脑MRI 平扫+增强+FLAIR 检查评价客观疗效。按照神经肿瘤疗效评价标准(RANO)评为完全缓解(complete remission,CR)、部分缓解(partial remission,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)。客观有效率(objective response rate,ORR)以CR+PR 所占的比例计算,疾病控制率(disease control rate,DCR)为CR+PR+SD 所占的比例。不良反应评价按CTC 5.0 版标准,分为1~5 级。PFS定义为开始贝伐珠单抗治疗至肿瘤进展或末次随访时间。OS 定义为开始贝伐珠单抗治疗至患者死亡或末次随访时间。本研究获得本院科研机构审查委员会或伦理委员会审查批准。
1.3 统计学分析
采用SPSS 26.0 软件进行统计学分析,Kaplan-Meier 法行生存分析,χ2检验和Fisher 精确概率法行不良事件的比较,Log-rank 检验行生存时间的比较,Cox 回归模型行多因素分析。以P<0.05 为差异具有统计学意义。
2 结果
2.1 患者特征
本研究纳入的81 例复发GBM 患者中,男性54例,女性27 例,年龄18~70 岁,中位年龄49 岁;KPS评分40~90 分,中位KPS 评分60 分;肿瘤Ki-67 指数3%~90%,中位Ki-67 指数25%。8 例患者入组前接受过再次手术但有可评价病灶。男性、年龄<60 岁、肿瘤未播撒、KPS评分≥60 分、MGMT 启动子非甲基化、多次复发(2~4 次)、贝伐珠单抗联合化疗、贝伐珠单抗低剂量(5 mg/kg)使用患者占多数(表1)。
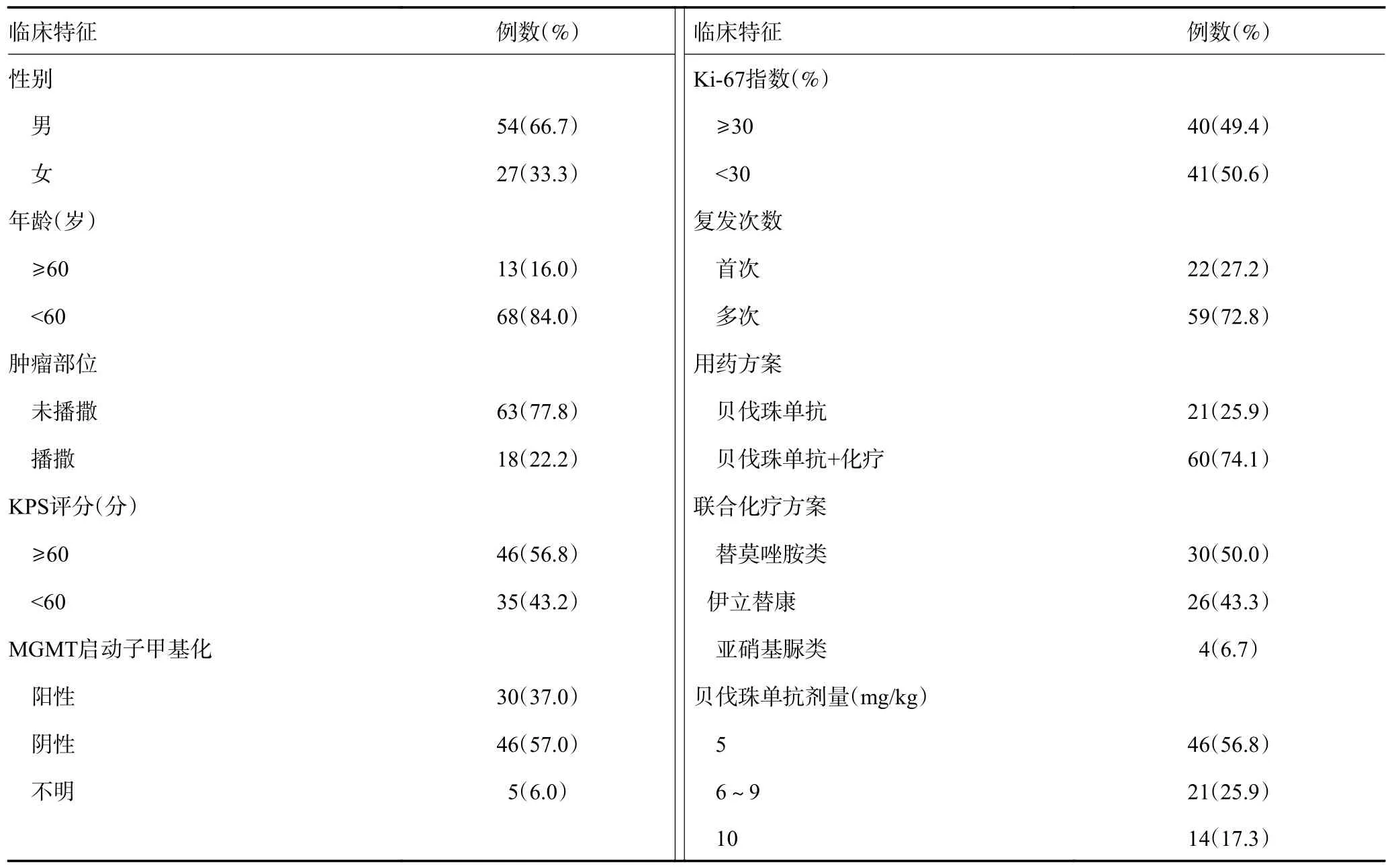
表1 81 例复发GBM 患者的临床资料
2.2 治疗情况
81 例患者共接受425 个周期的贝伐珠单抗治疗,中位周期4(1~18)个。21 例患者仅接受贝伐珠单抗单药治疗。60 例接受贝伐珠单抗联合化疗的患者中,11 例因KPS 评分差不能耐受化疗先单药1~2 个疗程,KPS 评分改善后再联合化疗。联合化疗方案包括替莫唑胺类(常规5 天方案、剂量-密集方案、替莫唑胺联合顺铂)、伊立替康或亚硝基脲类。
2.3 客观疗效
81 例患者中CR 2 例,PR 49 例,SD 14 例,PD 16例,客观有效率(CR+PR)62.9%,疾病控制率(CR+PR+SD)80.2%。90.1%(73/81)的患者在使用1~2 个周期贝伐珠单抗后KPS 评分和神经症状均有不同程度改善,激素和甘露醇用量减少(甘露醇从1 天使用2~3 次减少至1 周使用2~3 次或不需要,地塞米松从1 天总量5~20 mg 减少至不需要)。全组患者治疗后中位KPS 评分从60 分提高至70 分。
2.4 生存分析
随访截至2021 年12 月,81 例患者中79 例肿瘤进展(其中74 例死亡)。全组患者的mPFS 为4.4 个月(95%CI:4.0~4.8),mOS 为7.8 个月(95%CI:6.8~8.8),见图1。
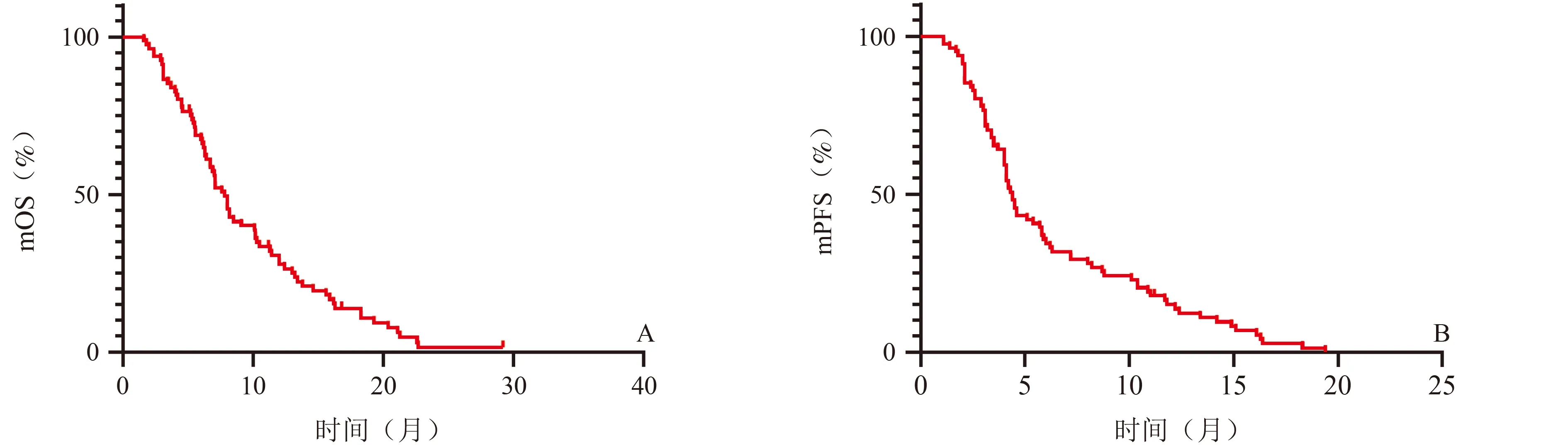
图1 81 例患者生存曲线
2.5 预后分析
单因素分析显示,性别、年龄、贝伐珠单抗使用时机(首次或≥2 次复发时使用)、是否联合化疗、剂量(5 mg/kg,6~9 mg/kg,10 mg/kg)对OS 无影响(均P>0.05);肿瘤未播撒、KPS 评分≥60 分、MGMT 启动子甲基化、Ki-67<30%的患者mOS 更长(均P<0.05,表2)。将影响患者预后的因素纳入Cox 回归多因素分析,结果显示,KPS 评分、MGMT 启动子甲基化状态是影响患者mOS 的独立预后因素(HR=0.452,P=0.003;HR=0.576,P=0.008;表3)。
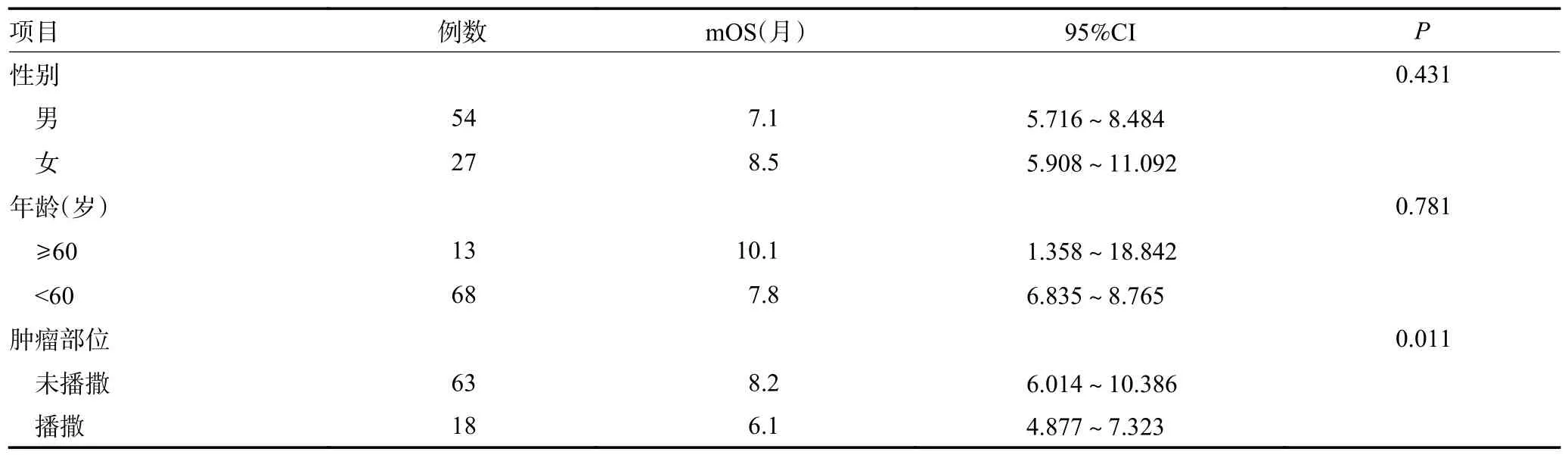
表2 影响81 例复发GBM 患者mOS 的单因素分析
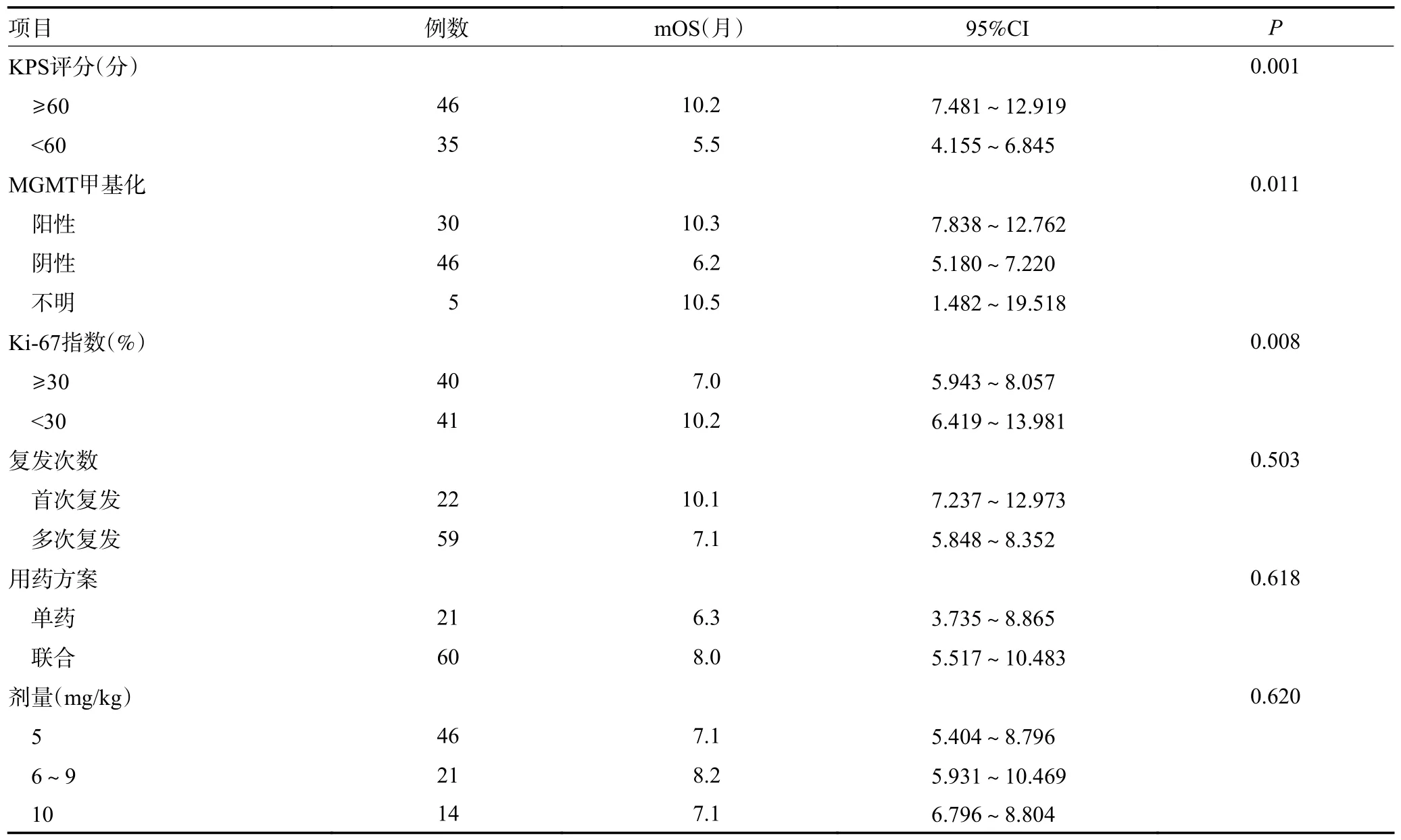
表2 影响81 例复发GBM 患者mOS 的单因素分析 (续表2)
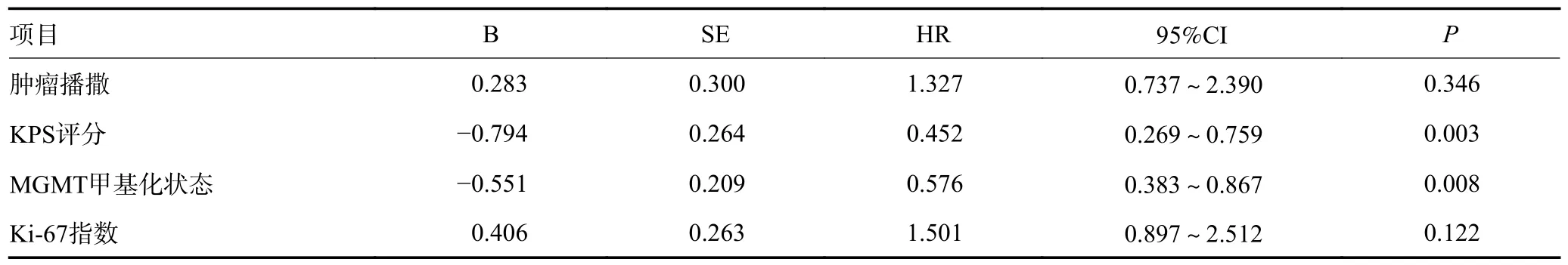
表3 影响81 例复发GBM 患者mOS 的多因素分析
2.6 不良反应
治疗相关不良事件主要为1~2 级的骨髓抑制、高血压、肝功能损害、胃肠道反应、蛋白尿和牙龈出血,3 级不良事件罕见,无4~5 级不良事件发生。贝伐珠单抗联合化疗组的骨髓抑制、胃肠道反应和肝功能损害发生率高于贝伐珠单抗单用组(P>0.05,表4)。
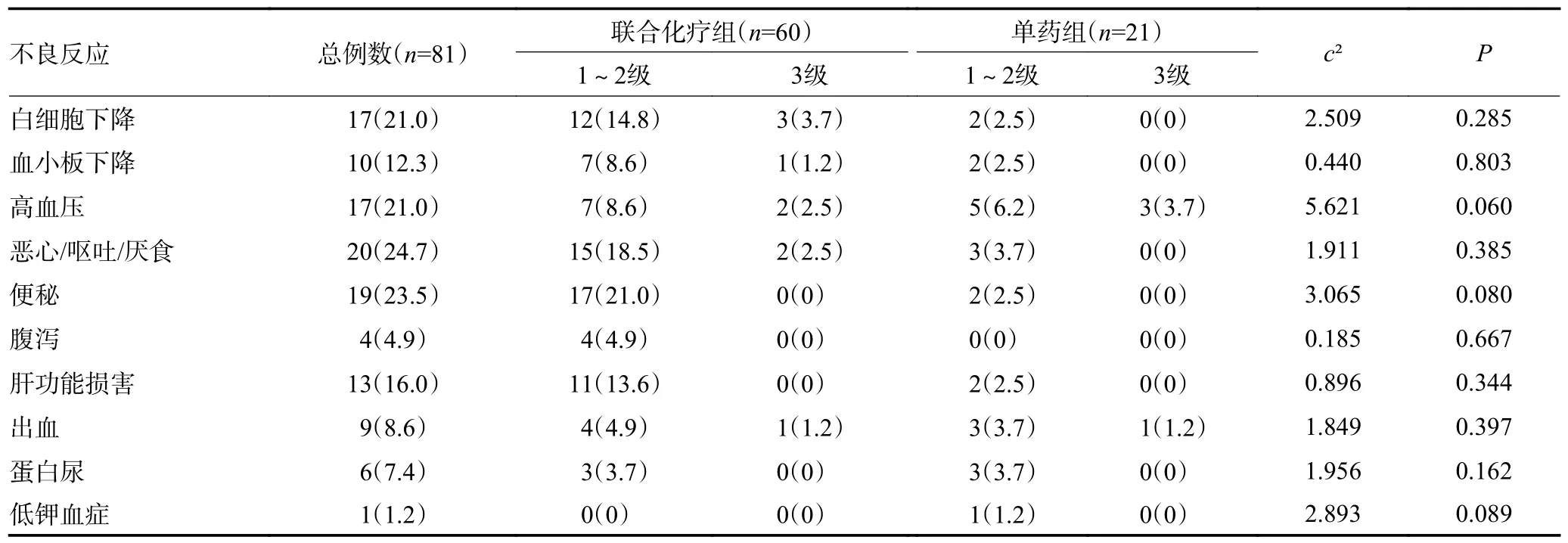
表4 不同治疗方案组间不良事件比较 例(%)
3 讨论
复发GBM 的治疗选择较少,二线化疗作用不大。尽管缺乏良好的对照试验,贝伐珠单抗仍被广泛用于治疗复发GBM。由于入组前瞻性临床试验的患者并不能完全反映真实世界中患者的状况,来自常规临床实践中真实世界的数据可以为治疗提供有价值的参考。本研究对中国人群真实世界单中心回顾性研究数据分析显示,贝伐珠单抗单用或联合化疗获得了62.9%的客观有效率,mPFS 和mOS 分别为4.4 个月和7.8 个月,与国外文献报道相当[4]。90.1%(73 例)的患者在使用贝伐珠单抗后KPS 评分和神经症状有不同程度改善,激素和甘露醇用量减少。72.8%患者(59 例)是在肿瘤多次复发进展后接受贝伐珠单抗治疗,在一定程度上延长了晚期患者的生存时间。
本研究入组的74.1%(60 例)患者接受了贝伐珠单抗联合细胞毒药物化疗。贝伐珠单抗是否应该与细胞毒化疗药联合使用,至今为止无Ⅲ期随机对照临床试验给出答案,Ⅱ期临床试验的结论也不一致[5]。BRAIN 研究是发表于2009 年的一项开放、多中心、非对照Ⅱ期临床试验[2],167 例复发GBM 患者随机分为单用贝伐珠单抗或联合伊立替康组。6 个月的PFS率分别为42.6%和50.3%,客观缓解率分别为28.2%和37.8%,mOS 分别为9.2 个月和8.7 个月,结果显示单用组与联合组比较无显著性差异。BELOB 研究是第1 个探索贝伐珠单抗在复发GBM 中作用的Ⅱ期随机对照临床试验,设立了不用贝伐珠单抗的对照组。试验数据表明,洛莫司汀和贝伐珠单抗联合治疗可能比单独使用洛莫司汀或贝伐珠单抗更有效,3 组患者在9 个月后的总OS 率分别为63%、43%和38%,联合治疗未对患者的健康相关生存质量产生负面影响。然而,在EORTC26101 临床Ⅲ期试验中并未证实贝伐珠单抗和洛莫司汀联合治疗有获益,但该试验证实了MGMT 启动子甲基化的预后作用[6]。本组患者大多数联合了替莫唑胺和伊立替康等细胞毒药物化疗,获得了8.0 个月的mOS。贝伐珠单抗单用组患者的mOS为6.3 个月,低于联合化疗组患者,但差异无统计学意义(P=0.618)。提示贝伐珠单抗无论是单用还是联合其他细胞毒药物使用可能均为合理的选择。本研究认为,对于KPS 评分差不能耐受细胞毒化疗药物的患者,可以先单用贝伐珠单抗治疗1~2 个周期,KPS 评分改善后再联合化疗。目前NCCN 指南推荐贝伐珠单抗单药或联合多种细胞毒药物化疗均可用于治疗复发GBM。
贝伐珠单抗治疗复发GBM 的最佳时机目前尚不清楚。本研究中72.8%(59 例)患者是在≥2 次复发时使用贝伐珠单抗,mOS 为7.1 个月,而首次复发患者的mOS 为10.1 个月,比多次复发患者长,但差异无统计学意义(P=0.503)。在临床试验中,贝伐珠单抗多在首次复发时使用。而在日常临床实践中,多数医疗中心常在第2 次或第3 次复发时使用贝伐珠单抗作为最后一线治疗。Gonnelli 等[7]报道了早期(首次复发后)和延迟(≥2 次复发后)使用贝伐珠单抗治疗复发GBM 的单中心经验。129 例患者的mPFS 在早期组和延迟组分别是3.45 个月和2.92 个月(P=0.504),mOS 分别是6.18 个月和6.47 个月(P=0.318)。Piccioni 等[8]的研究中,468 例复发GBM 患者接受贝伐珠单抗为基础的治疗,首次、2 次或≥3 次复发患者的PFS 相似(中位数4.1 个月),3 组的OS 无显著性差异(中位数9.8 个月)。结论是推迟使用贝伐珠单抗与疗效下降无关,延迟使用贝伐珠单抗治疗对大多数患者更可取。Franceschi 等[9]回顾性分析168 例接受三线治疗的复发GBM 患者的临床资料,三线治疗分为贝伐珠单抗组或化疗(亚硝脲类、替莫唑胺或卡铂+依托泊苷)组。与三线化疗比较,三线贝伐珠单抗治疗显著提高了mPFS(4.7 个月vs.2.6 个月,P=0.02)和mOS(8.0 个月vs.6.0 个月,P=0.014)。3 级以上不良反应发生率为13.7%。多变量分析显示,三线治疗的生存率取决于MGMT 甲基化状态(P=0.006)和是否接受贝伐珠单抗治疗(P=0.011)。该研究结论认为在经过选择的复发GBM 患者中三线使用贝伐珠单抗治疗是可行的,且耐受性良好。Schaub 等[10]研究同样也发现,在MGMT 启动子非甲基化的复发GBM 患者中,贝伐珠单抗作为三线治疗时,mPFS 和二线治疗比较差异无统计学意义(117 dvs.107 d)。贝伐珠单抗治疗失败后肿瘤的浸润性增强,更容易发生颅内远处播撒转移。由于贝伐珠单抗进展后的挽救治疗十分困难,本研究认为,在一线替莫唑胺化疗失败后先尝试其他挽救化疗方案,后线用贝伐珠单抗。
近期发表的荟萃分析[11-12]纳入了15 项研究共548 例接受过贝伐珠单抗挽救治疗的复发GBM 患者,发现贝伐珠单抗10~15 mg/kg 剂量组患者的6 个月PFS 率(P=0.223)、OS 率(P=0.145)、CR(P=0.997)、PR(P=0.639)和SD(P=0.428)比例均未超过5 mg/kg剂量组。有研究甚至设立了更低剂量组(1~5 mg/kg)和对照组(10 mg/kg)比较,在53 例复发GBM 患者中,低剂量组和对照组患者的mOS 分别为73 周和62 周(P=0.086),低剂量组患者的OS 甚至有更长的趋势[13]。Weathers 等[14]研究中,71 例复发性GBM 患者随机接受高剂量贝伐珠单抗(10 mg/kg)单用或低剂量贝伐珠单抗(5 mg/kg)联合洛莫司汀。在首次复发的患者中,低剂量贝伐珠单抗联合洛莫司汀组的mPFS 为4.96个月,较贝伐珠单抗单用组(3.22 个月,P=0.08)有获益趋势。贝伐珠单抗具有21~27 d 的较长的半衰期,允许给药间隔3~4 周或更长时间。因此结合上述研究结论,本研究中贝伐珠单抗的剂量是每次5~10 mg/kg,频率为每2~3 周使用1 次。仅17.3%(14 例)患者接受了高剂量(10 mg/kg)贝伐珠单抗治疗,56.8%(46 例)患者为低剂量(5 mg/kg),其余患者的剂量在5~10 mg/kg 之间。因为在早年贝伐珠单抗价格昂贵且医保不覆盖,减少剂量也有医学经济学上的利益考虑。本研究中3 个剂量组患者的mOS 无显著性差异,分别是7.1 个月(10 mg/kg 组)、8.2 个月(6~9 mg/kg 组)和7.1 个月(5 mg/kg 组)。
本研究主要的治疗相关不良事件为1~2 级骨髓抑制、肝功能损伤、高血压、肝功能损害、胃肠道反应、蛋白尿和牙龈出血。有2 例患者出现肿瘤内少量出血,经对症处理后出血吸收,继续用贝伐珠单抗可耐受。3 级不良事件发生率低,无4~5 级不良事件发生,治疗耐受性好。联合化疗组的骨髓抑制、胃肠道反应和肝功能损害发生率高于单用贝伐珠单抗组。不良事件发生率低可能与本组患者贝伐单抗使用剂量较低有关。
从临床角度来看,一些患者似乎更受益于贝伐珠单抗治疗,但目前还没有明确的预后指标。一项对贝伐珠单抗临床试验的回顾性基因表达谱分析表明[15],IDH 野生型前神经元型GBM 患者有可能从一线贝伐珠单抗治疗中生存获益。但在临床试验之外,影响贝伐珠单抗疗效的临床预后因素研究报道较少。本研究的单因素分析显示肿瘤未播撒、KPS 评分≥60 分、MGMT 启动子甲基化、Ki-67<30% 的患者具有更长的mOS。但多因素分析结果显示只有KPS 评分、MGMT 启动子甲基化状态是影响患者mOS 的独立预后因素。
综上所述,贝伐珠单抗治疗可以改善IDH 野生型成人复发GBM 患者的生存质量,治疗耐受性好。贝伐珠单抗在复发后的使用时机、剂量、是否联合化疗对患者的mOS 无影响。KPS 评分、MGMT 甲基化状态是影响mOS 的独立预后因素。

