转移因子口服液结合阿奇霉素序贯疗法治疗小儿肺炎支原体肺炎的效果分析
安 娜,项红霞,吕贞燕
(无锡市儿童医院儿童感染性疾病科,江苏 无锡 214023)
肺炎支原体是儿科最为常见的一类肺炎致病病原体,是广泛存在于自然界中的一种原核生物(电镜下观察支原体无细胞壁结构)[1-2],其主要传播途径是通过空气飞沫传播[3]。此种病原体的传播无明显季节特点,可在全年传播引起疾病。相关的传染病学研究显示,肺炎支原体肺炎占小儿肺炎总发病率的20%[4],近年来随着空气污染的持续加重,越来越多小儿出现支原体肺炎感染的表现,患儿感染肺炎支原体肺炎的典型临床表现通常包括高热、头痛、呼吸困难、胸痛、肺部啰音等[5-7]。本文对2019 年3 月至2022 年3 月在无锡市儿童医院就诊的102 例肺炎支原体肺炎患儿进行研究,旨在探讨对肺炎支原体肺炎患儿采用转移因子口服液结合阿奇霉素序贯疗法进行治疗的效果。
1 资料和方法
1.1 临床资料选取2019 年3 月至2022 年3 月在无锡市儿童医院就诊的102 例肺炎支原体肺炎患儿,采用随机数表法将其分为对照组和观察组。对照组患儿中男性共34例,女性共17 例;年龄范围在4 ~10 岁,平均年龄为(6.31±2.81)岁;体温范围在28 ~41℃,平均体温为(39.22±0.25)℃;病程范围在5 ~21 d,平均病程为(7.84±0.88)d。观察组患儿中男性共25例,女性共26 例;年龄范围在4 ~11 岁,平均年龄为(6.57±2.46)岁;体温范围在28 ~41℃,平均体温为(39.45±0.41)℃;病程范围在5 ~22 d,平均病程为(7.55±0.97)d。两组患儿的各项资料相比,差异无统计学意义(P>0.05)。
1.2 纳入标准及排除标准
纳入标准:所选患儿经临床检查符合肺炎支原体肺炎的诊断标准;患儿及患儿家属均知情并同意参加本次试验。排除标准:排除对阿奇霉素过敏的患儿;排除存在呼吸道畸形的患儿;排除合并严重肝肾功能障碍的患儿;排除在本次试验开始前采用其他抗生素类药物进行治疗的患儿;排除临床资料不全的患儿;排除存在意识障碍的患儿。
1.3 治疗方法
两组患儿均接受退热、止咳、雾化吸入等临床常规治疗。对照组患儿进行常规治疗联合阿奇霉素序贯治疗,其中将阿奇霉素注射液(生产厂家:辰欣药业股份有限公司;批准文号:国药准字H20060041 ;规格:2 mL:0.1 g/ 支)10 mg/kg 与5% 葡萄糖注射液进行混合后,对患儿进行静脉注射治疗,每日1 次,持续用药5 d(单日阿奇霉素使用剂量<0.5 g)后停药4 d,给予阿奇霉素分散片(生产厂家:南京易亨制药有限公司;批准文号:国药准字H20093302;规格:0.25 g×12 片)10 mg/(kg·d), 随水冲服,每日1次。持续用药3 d 后停药4 d。根据患儿病情的改善程度再次给予相应剂量的阿奇霉素进行序贯治疗。患儿共需治疗30 d。观察组患儿在对照组患儿采用常规治疗联合阿奇霉素序贯治疗的基础上加以转移因子口服液联合治疗。转移因子口服液〔生产厂家:金花企业( 集团) 股份有限公司西安金花制药厂;批准文号:
国药准字H20013288;规格:10 mL×6 支〕的用法是:口服,每日2 次,每次10 mg,共治疗30 d。
1.4 观察指标
观察两组患儿治疗前后高热、咳嗽、肺部啰音等相关临床肺炎表现消失的时间;观察两组患儿治疗前及治疗后30 d 血清免疫球蛋白A、免疫球蛋白G、免疫球蛋白M 水平的变化情况;观察两组患儿治疗前及治疗后30 d 血清白介素-6、肿瘤坏死因子-α、C反应蛋白等炎症因子水平的变化情况;观察两组患儿治疗前及治疗后30 d 肺泡灌洗液MPO 及GM-CSF 水平的变化情况。
1.5 疗效评定
患儿的临床疗效按照《诸福棠实用儿科学》中的相关标准进行判定。痊愈:患儿各类症状及肺部啰音等表现完全消失,高热表现消失且未复发,影像学检查显示患儿肺部病灶完全吸收消失;有效:患儿各类症状及肺部啰音等表现基本消失,高热表现消失且未复发,影像学检查显示患儿肺部病灶大部分被吸收;无效:患儿各项症状及肺部啰音未出现改善甚至加重,高热表现未出现缓解,影像学检查显示患儿肺部病灶未出现缩小迹象甚至增大。治疗总有效率=(痊愈例数+有效例数)/ 总例数×100%。
1.6 统计方法
数据用SPSS 20.0 软件进行统计分析,计量资料用均数± 标准差(±s)表示,采用t检验,计数资料用百分比(%)表示,采用χ² 检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患儿治疗后临床症状消失时间对比
进行阿奇霉素序贯治疗联合转移因子口服液治疗后,观察组患儿高热、咳嗽、肺部啰音等症状消失的时间分别为(2.21±0.25)d、(3.12±0.16)d、(4.15±0.35)d。进行阿奇霉素序贯治疗后,对照组患儿高热、咳嗽、肺部啰音等症状消失的时间分别为(2.81±0.28)d、(3.88±0.45)d、(4.81±0.48)d。观察组患儿进行阿奇霉素序贯治疗联合转移因子口服液治疗后其高热、咳嗽、肺部啰音等症状消失的时间均短于对照组患儿,差异显著(P<0.05)。见表1。
表1 两组患儿治疗后临床症状消失时间对比(d,± s)

表1 两组患儿治疗后临床症状消失时间对比(d,± s)
组别 例数 高热 咳嗽 肺部啰音对照组 51 2.81±0.28 3.88±0.45 4.81±0.48观察组 51 2.21±0.25 3.12±0.16 4.15±0.35 t 值 3.515 3.815 2.815 P 值 0.0001 0.0002 0.0001
2.2 两组患儿治疗前及治疗后30d 血清免疫球蛋白A、免疫球蛋白G、免疫球蛋白M 水平变化的对比
治疗前,两组患儿血清免疫球蛋白A、免疫球蛋白G、免疫球蛋白M 的水平相比,无明显差异(P>0.05)。观察组患儿进行阿奇霉素序贯治疗联合转移因子口服液治疗后30 d 其血清免疫球蛋 白A 的 水 平〔(1.98±0.25)g/L〕、 免 疫 球 蛋 白G 的 水 平〔(11.65±1.25)g/L〕、免 疫 球 蛋 白M 的水 平〔(1.99±0.23)g/L〕 均 高 于 对 照 组 患 儿 进行阿奇霉素序贯治疗后30 d 血清免疫球蛋白A 的水 平〔(1.81±0.21)g/L〕、 免 疫 球 蛋 白G 的 水平〔(11.51±1.28)g/L〕、 免 疫 球 蛋 白M 的 水 平〔(1.85±0.16)g/L〕,差异显著(P<0.05)。见表2。
表2 两组患儿治疗前及治疗后30 d 血清免疫球蛋白A、免疫球蛋白G、免疫球蛋白M 水平变化的对比(g/L,± s)
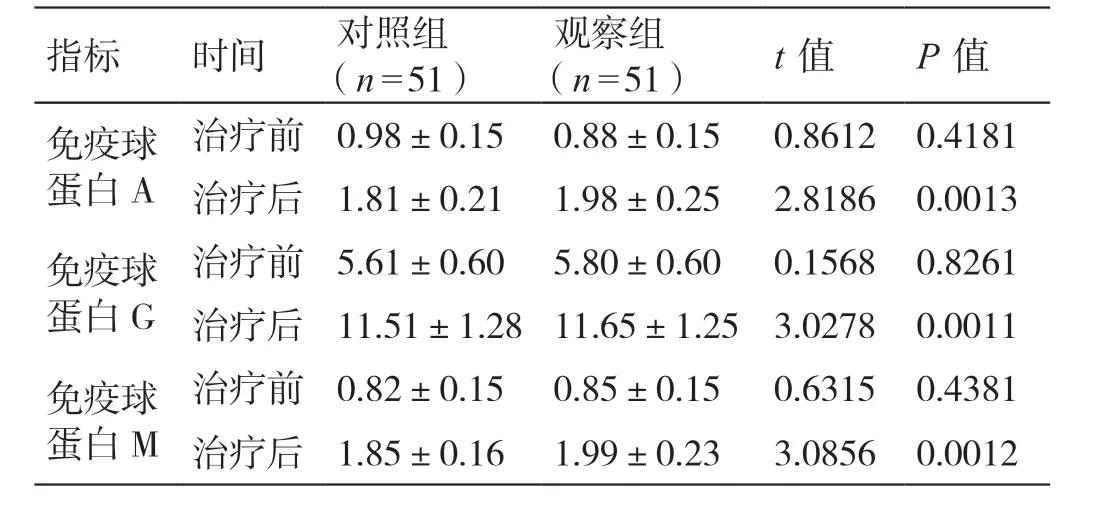
表2 两组患儿治疗前及治疗后30 d 血清免疫球蛋白A、免疫球蛋白G、免疫球蛋白M 水平变化的对比(g/L,± s)
指标 时间 对照组(n=51)观察组(n=51) t 值 P 值治疗前 0.98±0.15 0.88±0.15 0.8612 0.4181治疗后 1.81±0.21 1.98±0.25 2.8186 0.0013免疫球蛋白G免疫球蛋白A治疗前 5.61±0.60 5.80±0.60 0.1568 0.8261治疗后 11.51±1.28 11.65±1.25 3.0278 0.0011免疫球蛋白M治疗前 0.82±0.15 0.85±0.15 0.6315 0.4381治疗后 1.85±0.16 1.99±0.23 3.0856 0.0012
2.3 两组患儿治疗前及治疗后30d 血清白介素-6、肿瘤坏死因子-α、C 反应蛋白等炎症因子水平变化的对比
治疗前,两组患儿血清白介素-6、肿瘤坏死因子-α、C 反应蛋白的水平相比,无明显差异(P>0.05)。观察组患儿进行阿奇霉素序贯治疗联合转移因子口服液治疗后30 d 其血清白介素-6 的水 平〔(18.17±2.51)pg/mL〕、肿 瘤 坏 死 因 子-α的 水 平〔(17.78±2.04)pg/mL〕、C 反 应 蛋 白 的水平〔(9.51±1.01)mg/L〕均低于对照组患儿进行阿奇霉素序贯治疗后30 d 血清白介素-6 的水平〔(22.81±2.65)pg/mL〕、肿 瘤 坏 死 因 子-α 的水平〔(19.58±2.12)pg/mL〕、C 反应蛋白的水平〔(11.18±1.15)mg/L〕,差异显著(P<0.05)。见表3。
表3 两组患儿治疗前及治疗后30 d 血清白介素-6、肿瘤坏死因子-α、C 反应蛋白等炎症因子水平变化的对比(± s)

表3 两组患儿治疗前及治疗后30 d 血清白介素-6、肿瘤坏死因子-α、C 反应蛋白等炎症因子水平变化的对比(± s)
指标 时间 对照组(n=51) 观察组(n=51) t 值 P 值白介素-6(pg/mL) 治疗前 148.16±15.38 149.88±15.84 0.6851 0.4816治疗后 22.81±2.65 18.17±2.51 2.5181 0.0001肿瘤坏死因子-α(pg/mL) 治疗前 56.18±6.15 57.69±6.15 0.6817 0.4815治疗后 19.58±2.12 17.78±2.04 3.3561 0.0001 C 反应蛋白(mg/L) 治疗前 55.81±5.56 54.91±5.56 0.0815 0.8915治疗后 11.18±1.15 9.51±1.01 3.2641 0.0013
2.4 两组患儿治疗前及治疗后30d 肺泡灌洗液MPO 及GM-CSF 水平变化的对比
治疗前,两组患儿肺泡灌洗液MPO 及GM-CSF的水平相比,无明显差异(P>0.05)。观察组患儿进行阿奇霉素序贯治疗联合转移因子口服液治疗后30 d其肺泡灌洗液MPO 的水平〔(15.31±1.63)ng/mL〕、GM-CSF 的水平〔(128.76±14.74)ng/L〕均低于对照组患儿进行阿奇霉素序贯治疗后30 d 肺泡灌洗液MPO 的水平〔(16.41±1.85)ng/mL〕、GM-CSF 的水平〔(137.51±15.26)ng/L〕,差异显著(P<0.05)。见表4。
表4 两组患儿治疗前及治疗后30 d 肺泡灌洗液MPO 及GM-CSF 水平变化的对比(± s)
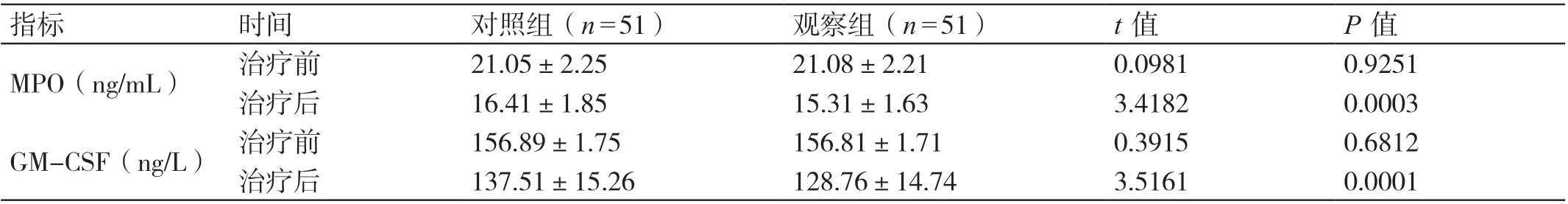
表4 两组患儿治疗前及治疗后30 d 肺泡灌洗液MPO 及GM-CSF 水平变化的对比(± s)
指标 时间 对照组(n=51) 观察组(n=51) t 值 P 值MPO(ng/mL) 治疗前 21.05±2.25 21.08±2.21 0.0981 0.9251治疗后 16.41±1.85 15.31±1.63 3.4182 0.0003 GM-CSF(ng/L) 治疗前 156.89±1.75 156.81±1.71 0.3915 0.6812治疗后 137.51±15.26 128.76±14.74 3.5161 0.0001
2.5 两组患儿治疗后临床治疗总有效率的对比
观察组患儿进行阿奇霉素序贯治疗联合转移因子口服液治疗后其中临床疗效为痊愈者有22 例(43.14%),为有效者有25 例(49.02%),其治疗的总有效率为92.16%。对照组患儿进行阿奇霉素序贯治疗后其中临床疗效为痊愈者有12 例(23.53%),为有效者有18 例(35.29%),其治疗的总有效率为58.82%。观察组患儿治疗的总有效率高于对照组患儿,差异显著(P<0.05)。
3 讨论
小儿由于其机体免疫功能尚未发育完全,因此极易受到外在病原体的入侵。小儿肺炎在临床上较为常见,其中小儿支原体肺炎是小儿肺炎的一大常见类型[8]。此类疾病没有典型症状,在临床就诊时仅表现为常见的肺炎症状(如高热、咳嗽、呼吸困难、肺部啰音等症状),患儿一旦感染肺炎支原体,会引起其机体免疫系统出现过度反应,导致患儿机体持续分泌炎性因子与趋化因子等[9-10],导致患儿自身正常免疫功能出现失衡表现,从而加重患儿的各类症状[11-12]。以往临床上对于支原体肺炎,主要是采用红霉素进行治疗,虽然红霉素可以有效杀灭患儿体内的支原体,但长期应用会导致患儿肠道内的菌群出现紊乱,从而导致患儿出现不同程度的消化道症状。近年来,随着对于小儿支原体肺炎的不断深入研究,临床试验结果证实阿奇霉素序贯治疗其临床治疗效果可以与红霉素的治疗效果相媲美,且减轻了患儿肠道正常菌群受损的情况,当阿奇霉素进入患儿体内后可以在肺脏局部形成特殊的高浓度药物区域,从而定点对患儿肺部的支原体进行有效杀灭[13]。临床资料显示,阿奇霉素在帮助患儿转归过程中虽然可以有效控制支原体的增殖,但无法有效减少患儿各项症状的持续时间。针对此类现象,本次研究在阿奇霉素序贯治疗的基础上加以转移因子口服液联合治疗。转移因子主要由正常机体免疫系统的淋巴细胞分泌,其本质为核苷酸与小分子多肽(对于机体免疫具有调节功能),与阿奇霉素联合应用可以发挥最大效应,在最短时间内控制支原体肺炎的症状,改善患儿的免疫功能[14]。本研究的结果显示,观察组患儿进行阿奇霉素序贯治疗联合转移因子口服液治疗后其高热、咳嗽、肺部啰音等症状消失的时间均短于对照组患儿,差异显著(P<0.05)。观察组患儿治疗的总有效率为92.16%。对照组患儿治疗的总有效率为58.82%。观察组患儿治疗的总有效率高于对照组患儿,差异显著(P<0.05)。治疗后,观察组患儿血清免疫球蛋白A、免疫球蛋白G、免疫球蛋白M、白介素-6、肿瘤坏死因子-α、C 反应蛋白的水平均优于对照组患儿,差异显著(P<0.05)。这表明,进行阿奇霉素序贯治疗联合转移因子口服液治疗可有效改善患儿受损的免疫功能,抑制患儿体内的炎症反应,改善患儿的肺功能,帮助患儿快速恢复。研究发现,小儿肺炎发生过程中出现氧化应激是造成患儿肺功能受损的重要因素之一,而MPO 作为氧化应激分子通常由巨噬细胞所分泌,是炎症反应的重要标志物。GM-CSF 则是促进MPO 生成的关键引物。本研究的结果显示,治疗后,观察组患儿肺泡灌洗液MPO 及GM-CSF 的水平均优于对照组患儿,差异显著(P<0.05)。这说明,进行阿奇霉素序贯治疗联合转移因子口服液治疗可有效减轻患儿机体的氧化应激损伤,保护患儿正在发育的肺脏。
综上所述,对肺炎支原体肺炎患儿进行阿奇霉素序贯治疗联合转移因子口服液治疗可在有效控制其体内炎症反应、改善其各类肺炎症状的同时,减轻氧化应激对其肺功能的损害。此法值得在临床上推广应用。

