磺酰氨基氯磺隆的合成、除草活性、作物安全性及其土壤降解研究
武 磊, 李永红, 周 莎, 李正名 , 王忠文
(南开大学 化学学院 元素有机化学国家重点实验室,天津 300071)
0 引言
磺酰脲类除草剂具有活性强、毒性低、用量少、对哺乳动物安全等优点而被广泛应用[1]。其通过抑制乙酰乳酸合成酶 (ALS) 而影响植物体内支链氨基酸生成途径中的第1 个反应,从而抑制杂草生长,并最终导致杂草死亡[2]。
磺酰脲类除草剂对不同作物的敏感性差异很大,在其应用过程中有关杂草对其产生耐药性的问题[3-6]以及其在土壤中的残留药害问题[7-8]已十分突出。1985 年,Anderson 在研究氯磺隆在土壤中的降解时发现,尽管氯磺隆可以选择性地控制冬小麦和大麦田中的阔叶杂草生长,但在其施用3 年后,土壤中残留的氯磺隆仍对玉米和向日葵等下茬作物产生药害[7]。Thirunarayanan 等报道,在20 ℃的条件下,氯磺隆在pH 8.1 的土壤中的降解半衰期为144 d[8];Fredrickson 等发现在pH 7.5 的土壤中,氯磺隆的降解半衰期为70 d 左右[9]。1989年,Walker 等发现,氯磺隆、甲磺隆和醚苯磺隆等磺酰脲类除草剂在土壤中的残留会对下茬作物(玉米、油菜等) 产生长达一年以上的药害[10]。在中国,氯磺隆、甲磺隆和胺苯磺隆等磺酰脲类除草剂主要用于小麦田,但因其在土壤中的残留已严重影响到下茬作物幼苗的正常生长,故中国农业部从2014 年起已禁止其在田间应用[11]。
本课题组在前期工作中发现,在氯磺隆的苯环5 位引入给电子取代基可以加快其在土壤中的降解速率,其中二甲氨基 (ZSA-IIa) 和二乙氨基(ZSA-IIb) 取代的氯磺隆 (图式1) 保持了较好的除草活性,其在碱性 (pH 8.46) 土壤中的降解半衰期(half-life of degradation,DT50) 分别为3.36 d 和6.25 d,降解速率比氯磺隆 (DT5084.53 d) 大为增加[12-13];然而,该结构化合物对小麦的安全性较差,会显著抑制小麦的正常生长,其中,ZSA-IIa经苗前处理对小麦的安全性略优于ZSA-IIb[14-15]。
2002 年,拜尔公司研发出了主要用于谷物田的甲酰胺磺隆 (foramsulfuron) 和甲磺胺磺隆(mesosulfuron-methyl) (图式2),对谷物展现较好的安全性[16-17]。由其结构可以看出,在其苯环均含有5 位取代基团。鉴于此,笔者推测在氯磺隆苯环的5 位引入磺酰氨基可能会提高氯磺隆对作物的安全性。本文选择在碱性土壤环境中降解速率较快的ZSA-IIa 为基础,在其苯环5 位引入不同的磺酰基团,设计合成4 个目标化合物 (设计思想见图式1,合成路线见图式3),对其结构进行表征,并初步研究其除草活性、在土壤中的降解及其对作物的安全性,以期发现绿色安全的新型磺酰脲除草先导化合物。
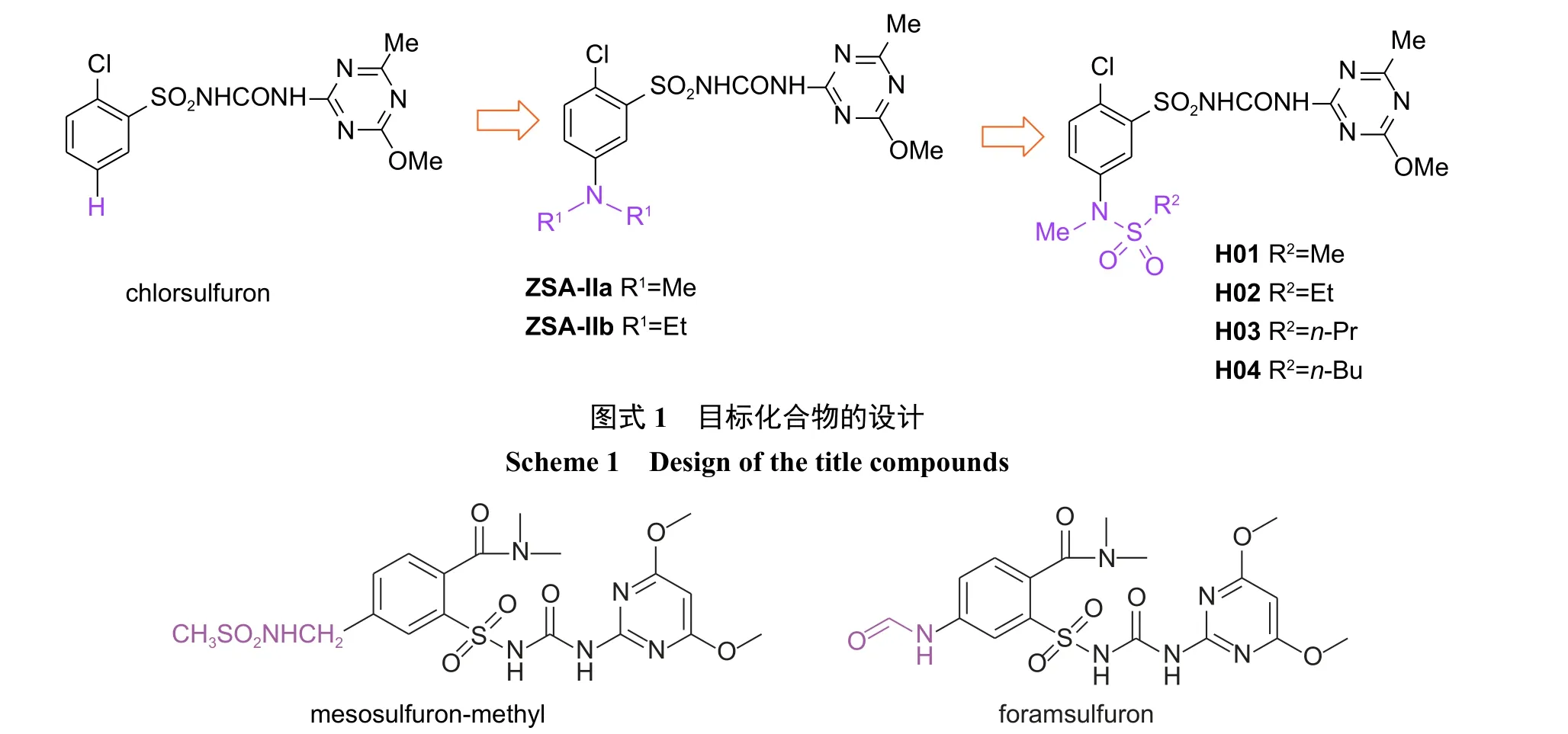
图式2 甲酰胺磺隆和甲磺胺磺隆的化学结构式Scheme 2 Structural formula of mesosulfuron-methyl and foramsulfuron

图式3 目标化合物H01~H04 的合成路线Scheme 3 Synthetic route of the title compounds H01-H04
1 材料与方法
1.1 仪器与试剂
X-4 型数字显示显微熔点仪 (温度计未校正,北京泰克仪器有限公司);Bruker Avance 400 型核磁共振仪 (以TMS 为内标,瑞士Bruker);Bruker solariX XR 型傅立叶变换高分辨质谱仪 (美国Agilent公司)。合成所用试剂为分析纯,色谱分析所用试剂为色谱纯。TU-1810 紫外-可见光谱仪 (北京普析通用仪器有限公司);SHIMADZU LC-20AT 高效液相色谱仪 (日本SHIMADZU 公司);Thermo-Scientific Legend Mach 1.6 R 高速离心机 (美国Thermo Fisher);SPX-150B-Z 系列生化培养箱 (上海博迅实业有限公司医疗设备厂)。
杂草种子采集自天津农耕田中,包括双子叶植物油菜Brassica napus和反枝苋Amaranthusretroflexus以及单子叶植物稗草Echinochloa crusgalli和马唐Digitaria sanguinalis。
小麦 (济麦22) 和玉米 (新单66) 种子购自天津市华农种子有限公司。
1.2 化合物的合成
1.2.1 中间体7、8、9 和12 的合成 按前期报道方法[18]方法合成中间体7 和12,参考文献方法[18-19]合成中间体8 和9。
1.2.2 目标化合物H01~H04 的合成 向25 mL圆底烧瓶中加入中间体9 (1.90 mmol)、12 (2.00 mmol)、1,8-二氮杂双环[5.4.0]十一碳-7-烯 (DBU)(2.85 mmol) 和15 mL 乙腈,室温下磁力搅拌过夜。薄层层析(TLC,展开剂为V(甲醇) :V(二氯甲烷) = 1 : 10) 监测至反应完全。减压浓缩,添加10 mL 蒸馏水,超声1 min 后,通过硅藻土抽滤,滤液用稀盐酸调节pH = 4,添加20 mL 二氯甲烷萃取,有机相用无水硫酸钠干燥后浓缩,经柱层析 (V(甲醇) :V(二氯甲烷) = 1 : 40) 纯化,干燥后得目标化合物H01~H04。
1-(4-甲基-6-甲氧基-1,3,5-三嗪-2-基)-3-[2-氯-5-(N-甲基-甲磺酰氨基)苯基磺酰基]脲 (H01):白色固体,收率90%,熔点175~177oC.1H NMR (400 MHz, chloroform-d),δ: 12.86 (s, 1H, NH), 8.18 (s, 1H, Ph-H), 7.72 (d,J= 8.5 Hz,1H, Ph-H), 7.52 (d,J= 8.4 Hz, 1H, Ph-H), 4.06 (s, 3H, OCH3),3.39 (s, 3H, NCH3), 2.89 (s, 3H, SO2CH3), 2.59 (s, 3H, CH3).13C NMR (101 MHz, chloroform-d),δ: 179.24, 170.63, 163.42,148.16, 140.53, 136.51, 134.09, 132.50, 130.32, 128.12, 55.79,37.79, 35.38, 25.49. HRMS (ESI): C14H18ClN6O6S2[M + H]+, 计算值465.041 2, 测试值465.041 1.
1-(4-甲基-6-甲氧基-1,3,5-三嗪-2-基)-3-[2-氯-5-(N-甲基-乙磺酰氨基)苯基磺酰基]脲 (H02):白色固体,收率87%,熔点98~100oC.1H NMR (400 MHz, chloroform-d),δ:12.82 (s, 1H, NH), 8.18 (s, 1H, Ph-H), 7.73 (d,J= 7.9 Hz, 1H,Ph-H), 7.51 (d,J= 7.9 Hz, 1H, Ph-H), 4.06 (s, 3H, OCH3),3.41 (s, 3H, NCH3), 3.09 (q,J= 7.1 Hz, 2H, CH2CH3), 2.58 (s,3H, CH3), 1.35 (t,J= 6.7 Hz, 3H, CH2CH3).13C NMR (101 MHz, chloroform-d),δ: 179.31, 170.71, 163.40, 148.02,140.77, 136.48, 133.37, 132.41, 129.77, 128.06, 55.77, 44.42,38.08, 25.47, 7.79. HRMS (ESI): C15H20ClN6O6S2[M + H]+,计算值479.056 9, 测试值479.056 5.
1-(4-甲基-6-甲氧基-1,3,5-三嗪-2-基)-3-[2-氯-5-(N-甲基-丙磺酰氨基)苯基磺酰基]脲 (H03):白色固体,收率90%,熔点86~88oC.1H NMR (400 MHz, chloroform-d),δ:12.81 (s, 1H, NH), 8.17 (d,J= 2.3 Hz, 1H, Ph-H), 7.74 (dd,J= 8.6, 2.3 Hz, 1H, Ph-H), 7.50 (d,J= 8.6 Hz, 1H, Ph-H),4.06 (s, 3H, OCH3), 3.40 (s, 3H, NCH3), 3.00 (t, 2H,CH2CH2CH3), 2.59 (s, 3H, CH3), 1.79-1.89 (m, 2H,CH2CH2CH3), 1.04 (t,J= 7.4 Hz, 3H, CH2CH2CH3).13C NMR(101 MHz, chloroform-d),δ: 179.43, 170.56, 163.45, 148.11,140.72, 136.42, 133.36, 132.41, 129.73, 128.01, 55.80, 51.25,37.91, 25.49, 16.84, 13.00. HRMS (ESI): C16H22ClN6O6S2[M + H]+, 计算值493.072 5, 测试值493.072 1.
1-(4-甲基-6-甲氧基-1,3,5-三嗪-2-基)-3-[2-氯-5-(N-甲基-丁磺酰氨基)苯基磺酰基]脲 (H04):白色固体,收率84.3%,熔点85~87oC.1H NMR (400 MHz, chloroform-d),δ:12.84 (s, 1H, NH), 8.18 (s, 1H, Ph-H), 7.74 (d,J= 8.3 Hz, 1H,Ph-H), 7.50 (d,J= 8.3 Hz, 1H, Ph-H), 4.06 (s, 3H, OCH3),3.40 (s, 3H, NCH3), 3.02 (t,J= 7.9 Hz, 2H, CH2CH2CH2CH3),2.59 (s, 3H, CH3), 1.78 (t, 2H, CH2CH2CH2CH3), 1.43 (q,J=7.4 Hz, 2H, CH2CH2CH2CH3), 0.93 (t,J= 7.2 Hz, 3H,CH2CH2CH2CH3).13C NMR (101 MHz, chloroform-d),δ:179.37, 170.93, 163.51, 148.08, 140.84, 136.54, 133.57,132.54, 129.87, 128.11, 55.92, 49.46, 38.08, 25.61, 25.05,21.69, 13.64. HRMS (ESI): C17H24ClN6O6S2[M + H]+, 计算值507.088 2, 测试值507.088 0.
1.3 除草活性测试
供试药液的配制:称量1.0 g 乳化剂 (吐温-80)于烧杯中,用20 mL 蒸馏水充分溶解后,再用蒸馏水定容至1 000 mL,制得质量分数为1‰的乳化水溶液,备用。将10.0 mg 供试化合物溶于1 mL的N,N-二甲基甲酰胺 (DMF) 中,制得10.0 mg/mL的测试母液,随后用质量分数为1‰的乳化水溶液稀释至所需浓度,待测。
采用盆栽法[14,18]测定。处理方式为苗前处理和苗后处理,化合物的测试浓度为有效成分15 和150 g/hm2。以氯磺隆作为对照药剂。
1.4 目标化合物对作物安全性测试
采用盆栽法测试目标化合物对小麦和玉米的安全性[14,18]。处理方式为为苗前处理和苗后处理,测试浓度为有效成分30 和60 g/hm2。分别设置目标化合物测试组、空白对照组及氯磺隆对照组。
1.5 目标化合物在土壤中的降解试验
参考文献方法[12-14,18]进行。包括土壤选择、高效液相色谱(HPLC)条件的确定、标准曲线的绘制、添加回收率测定以及目标化合物在土壤中的降解试验。详见本文所附辅助材料。
根据GB/T 31270.1—2014《化学农药环境安全评价试验准则》[20],试验用土选择河北省沧州市的pH 8.39 的碱性土壤,土壤性质见表1。

表1 土壤分析数据Table 1 Analysis data of soils
2 结果与讨论
2.1 化合物的合成
如图式3 所示的合成路线,化合物1 先经过重氮化反应制成重氮盐,再与亚硫酸氢钠和氯化铜反应,生成磺酰氯。此法制得化合物2 的收率依赖于重氮盐的稳定性,由于温度升高会加快重氮盐分解,故反应过程中要控制在低温环境 (0 ℃以下) 进行。同时,体系中需要保持盐酸过量,盐酸与芳胺投料质量比为3 : 1;否则,在酸不足的情况下,制得的重氮盐易与未反应的芳胺反应,生成偶氮化合物,影响收率。
2.2 化合物的波谱分析
以化合物H03 为例,1H NMR 中,δ12.81 为磺酰脲桥上活泼氢的特征吸收峰 (SO2NHCONH),δ8.17、7.74 和7.50 为苯环上的3 个氢 (Ph-H),三嗪杂环上的甲氧基和甲基的氢以单峰形式分别位于δ4.06 和2.59,甲氨基的甲基氢位于δ3.40(NCH3),δ3.00 为与磺酰基相连的第一个乙基的氢 (CH2CH2CH3),裂分为三重峰,δ1.79~1.89 处的多重峰为与甲基相连的乙基上的氢 (CH2CH2CH3),δ1.04 处为甲基氢 (CH2CH2CH3),裂分为三重峰。
13C NMR 中,一共有16 个碳峰。其中,脂肪族碳峰包括:三嗪环上的甲氧基碳峰 (δ55.80) 与甲基上的碳峰 (δ25.49),与氨基相连的甲基碳峰(δ37.91) 以及丙磺酰氨基上的3 个丙基碳峰δ51.25 (CH2CHCH3)、16.84 (CH2CHCH3) 和13.00(CH2CHCH3);芳香族包括苯环上的6 个碳峰和三嗪杂环上的3 个碳峰 (δ170.56, 163.45, 148.11,140.72, 136.42, 133.36, 132.41, 129.73, 128.01);此外还有1 个脲桥上的羰基碳峰 (δ179.43)。
2.3 化合物的除草活性
除草活性测试结果 (表2) 表明:在15 g/hm2剂量下,苗前处理时,H01 和H02 对油菜的抑制率分别为90.3%和83.5%,与氯磺隆 (94.8%) 相比,保持了一定的除草活性;在150 g/hm2剂量下,苗前处理时,化合物H01、H02 及H04 对油菜的抑制率分别为94.8%、89.5%和85.8%,与氯磺隆 (100%) 相比,保持了一定的除草活性,而相同条件下H01 和H02 对反枝苋的抑制率分别为100%和89.4%,高于对照药剂氯磺隆 (68.8%)。在150 g/hm2的施药剂量下苗后处理时,H04 对油菜和苋菜的抑制率与氯磺隆相当,均达100%,H03和H04 对稗草的抑制率分别为90.7%和85.2%,优于对照药氯磺隆 (68.8%)。
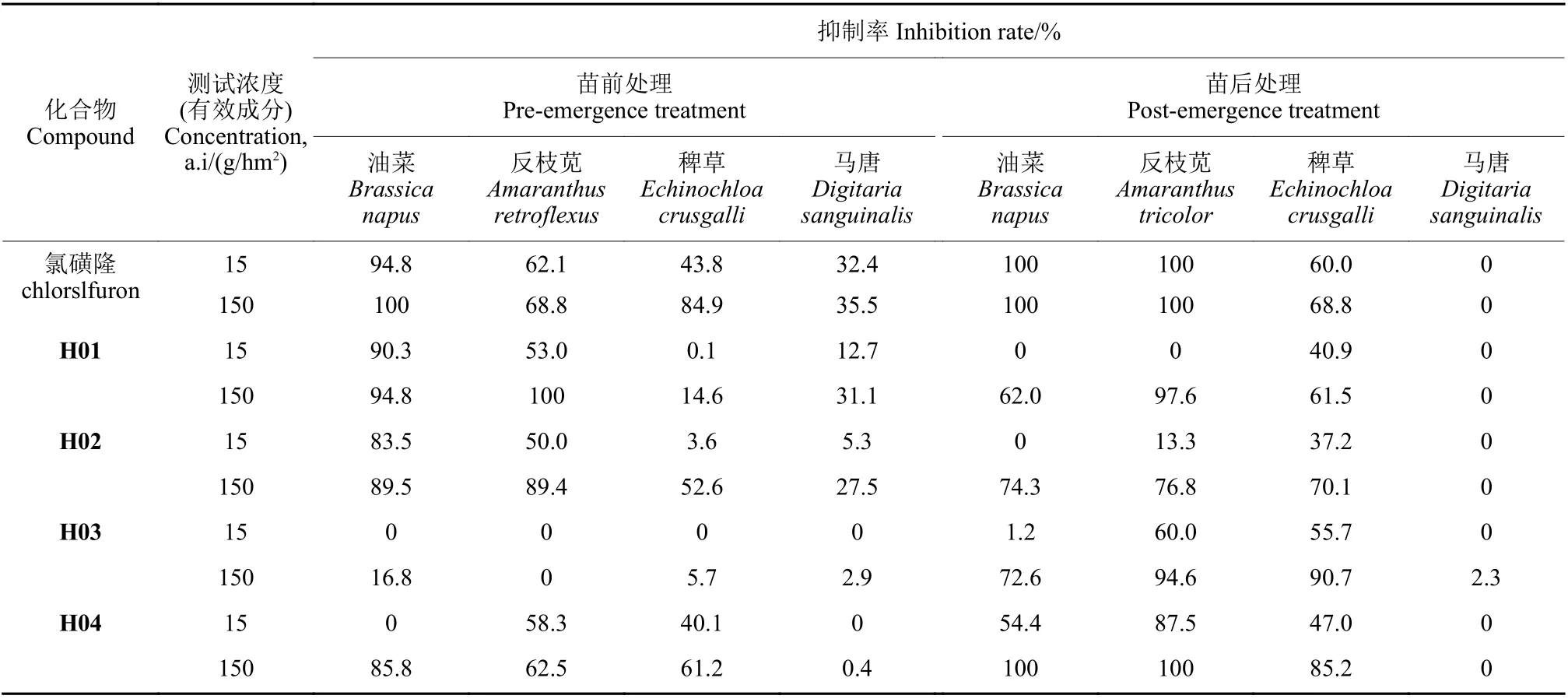
表2 不同处理方式下目标化合物H 在15 g/hm2 和150 g/hm2 测试浓度下的除草活性Table 2 Herbicidal activities of the target compounds H at concentration of 15 g/hm2 and 150 g/hm2 through different treatments
2.4 化合物对作物的安全性
在盆栽条件下,目标化合物对小麦和玉米的安全性测试结果见表3 和表4。由表3 可知,在30 g/hm2的测试浓度下,H01、H03 和H04 通过苗前处理对小麦的抑制率均为0;而苗后处理时,H01、H02 及H04 对小麦的抑制率均为0。在60 g/hm2的测试浓度下,H03 和H04 通过苗前处理对小麦的抑制率均为0;而苗后处理时,H01和H04 对小麦的抑制率均为0,对小麦无抑制作用。综合来看,目标化合物对小麦保持了与对照药剂一致的安全性。
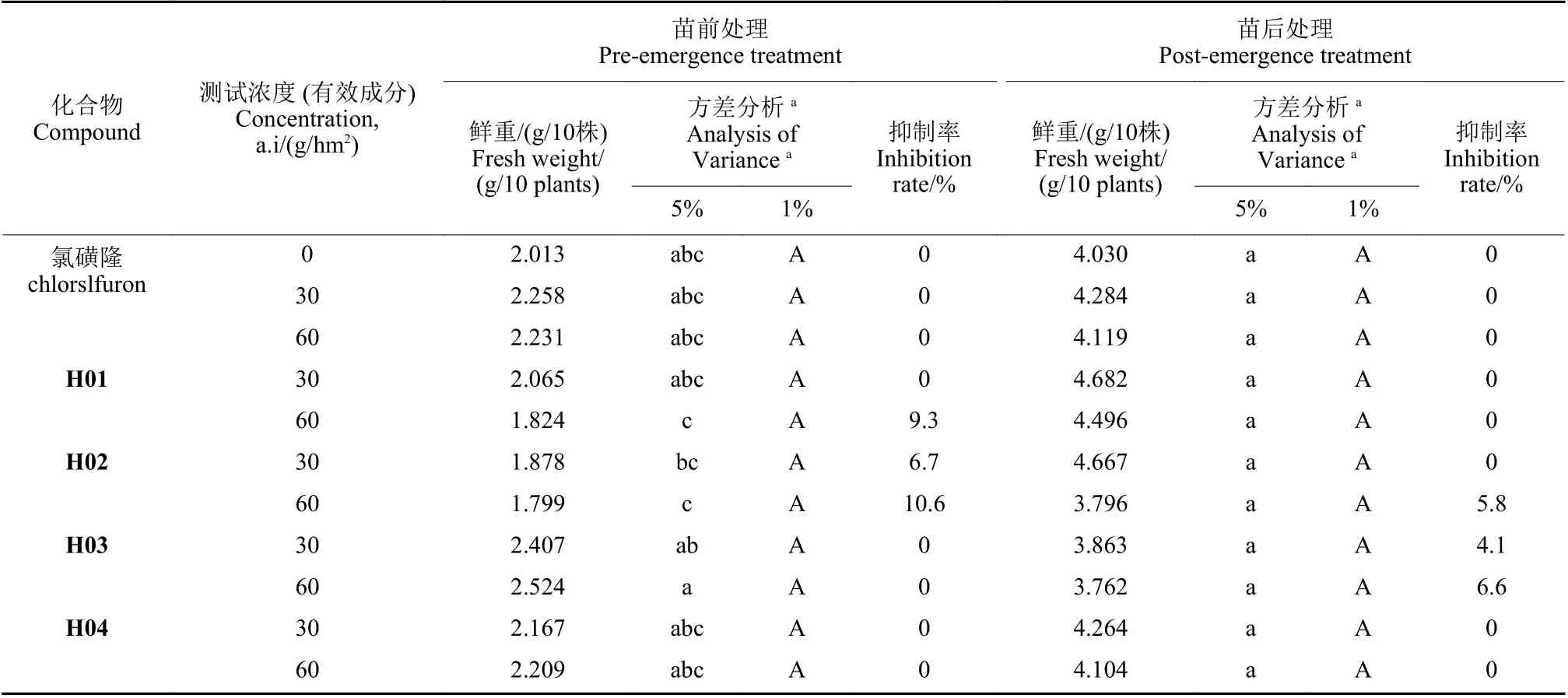
表3 不同处理方式下目标化合物H 在30 g/hm2 和60 g/hm2 测试浓度下对小麦 (济麦22) 的安全性Table 3 Crop safety of the target compounds H at concentration of 30 g/hm2 and 60 g/hm2 on wheat (Jimai 22) through different treatments

表4 不同处理方式下目标化合物H 在30 g/hm2 和60 g/hm2 测试浓度下对玉米 (新单66) 的安全性Table 4 Crop safety of the target compounds H at concentration of 30 g/hm2 and 60 g/hm2 on corn (Xindan 66) through different treatments
由表4 可知,在30 g/hm2的测试浓度下,H01~H04 通过苗前处理对玉米生长的抑制率分别为3.3%、23.1%、4.8% 及2.6%,优于氯磺隆(39.2%);苗后处理的结果表明,H01~H04 对玉米的抑制率均为0。在60 g/hm2的测试浓度下,H01~H04 通过苗前处理对玉米的抑制率分别为13.4%、25.7%、19.2% 和4.6%,优于氯磺隆(60.7%);苗后处理的结果表明,H01~H04 对玉米的抑制率均分别为0、2.8%、0 和0.8%,优于氯磺隆 (55.4%)。综合来看,目标化合物对玉米展现较好的安全性。
2.5 化合物在碱性土壤中的降解
目标化合物的HPLC 分析条件及其在土壤中添加回收率测定结果见表5。
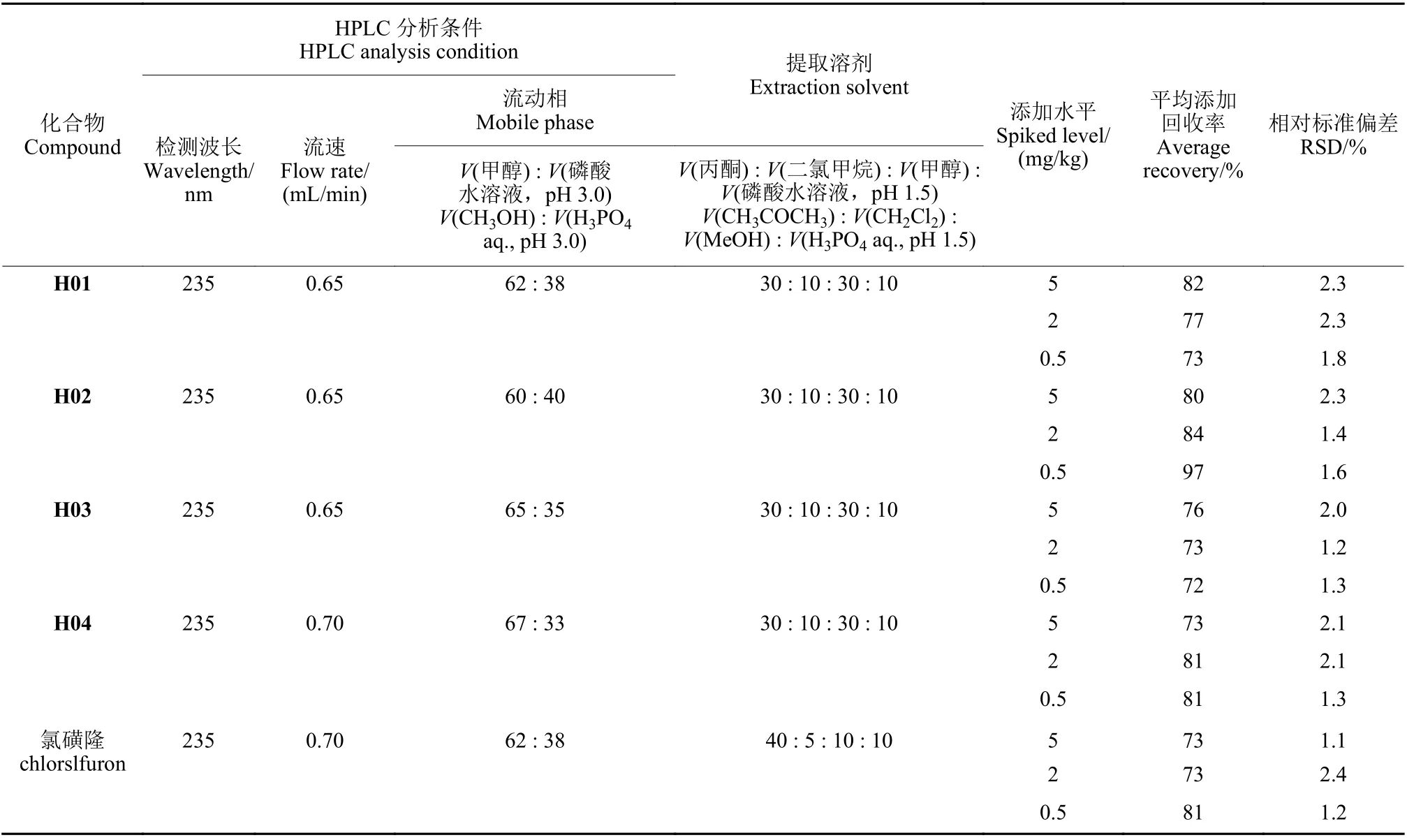
表5 目标化合物的HPLC 分析条件及其在土壤中的添加回收率Table 5 HPLC analysis condition and recovery rate of taeget compounds
目标化合物在碱性土壤 (pH=8.39) 中的降解结果见表6。
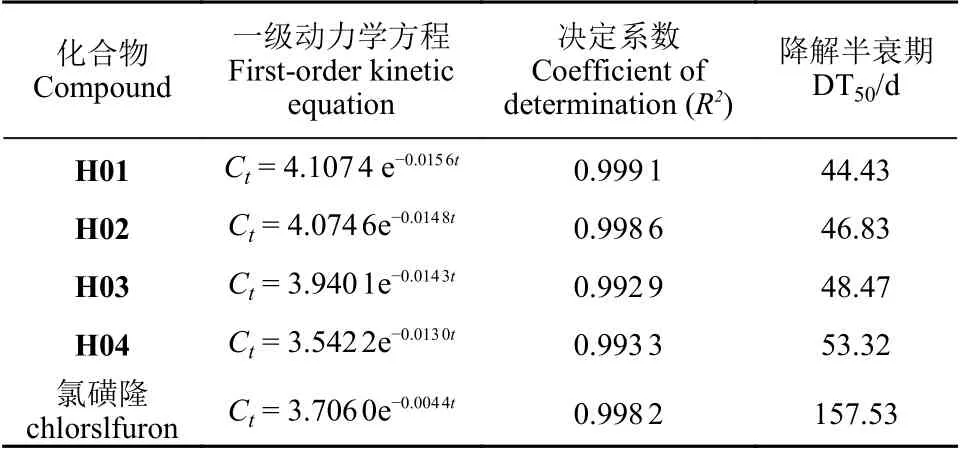
表6 目标化合物在碱性土壤中的降解Table 6 Degradation results of the target compounds in alkaline soil
化合物H01~H04 在pH 8.39 的土壤中的降解半衰期分别为44.43、46.83、48.47 和53.32 d,与氯磺隆 (157.53 d) 相比明显缩短。根据化合物的结构初步推测,H 系列化合物的降解半衰期受取代磺酰基上碳原子个数的影响,碳原子数越多 (基团体积越大),降解半衰期越长。
3 结论
本文以氯磺隆分子中苯环5 位的二甲氨基取代结构为基础,在氨基上引入不同磺酰基,设计合成了4 个苯环5 位磺酰氨基取代的氯磺隆衍生物 (H01~H04),并通过1H NMR、13C NMR 和HRMS 确证了新化合物的结构。初步的除草活性测试结果显示,目标化合物基本保持了较好的除草活性,其中,在150 g/hm2测试浓度下,通过苗前处理,H01 和H02 对苋菜的抑制率优于氯磺隆,而苗后处理时,H03 和H04 对稗草的抑制率超越了氯磺隆。作物安全性测试结果表明,H01~H04在保持对小麦安全性的同时,显著改善了对照药剂氯磺隆对玉米的药害。降解试验结果表明,在碱性土壤中,H01~H04 的降解半衰期相较于氯磺隆明显缩短。综合试验结果,H01 和H04 结构具有较好的除草活性、较快的碱性土壤降解速率以及对小麦和玉米较好的作物安全性,可作为潜在的除草剂候选药物。本文为进一步设计具有高效除草活性、降解速率快以及高作物安全性的新型磺酰脲类除草剂提供了参考。

