α-萜品烯酰基农用杀菌活性物的合成及活性研究
李 璇, 潘婷敏, 耿媛霄, 周海玉, 李 健, 高艳清,3*
(1.西北农林科技大学 植物保护学院;陕西省生物农药工程技术研究中心,陕西 杨凌 712100; 2.西北农林科技大学 林学院,陕西 杨凌 712100;3.广西民族大学;广西林产化学与工程重点实验室;广西林产化学与工程协同创新中心,广西 南宁 530006)
随着现代农业的高速发展,人们对农产品的要求不断提高,数量足的同时,质量也要高。农药的使用,稳定了粮食产量的同时,其弊病随着时间的流逝也日益突出,众所周知的“3R”(即:残留、抗性、再猖獗)问题便是其中一个典型的代表[1]。以天然产物为先导,通过结构修饰或者亚结构拼接将潜在药效基团引入天然特性结构中,有望开发出低毒、高效的新型农药[2-3]。松节油是一种经济、易得的天然可再生资源,主要成分为α-蒎烯和β-蒎烯。近年来,松节油被用于医药、调香及香料生产,也合成了许多具有生物活性的农用化学产品,比如具有农药增效作用、驱虫或引诱活性、除草活性、抗菌杀菌活性的产品等[4]。β-蒎烯是典型的双环单萜类化合物,可以提供C10或C5分子骨架,分子结构中还有四元环、六元环、环外双键以及2个手性中心[5],化学性质活泼,具有改造为农用化学品的潜力[6]。卤素取代物在现代农药研发中应用广泛,在已知的农药中,约有三分之二的药品含有卤素取代的芳基或杂芳基[7]。卤素原子或者卤取代基因其独特的电负性,作为氢键受体,能显著改变分子的物理化学性质,从而影响化合物的生物活性,在当今农药领域得以成功应用[8]。松节油作为林源可再生资源,通过对其特有结构进行改性修饰,可促进松节油的提质增效利用[9-12]。本研究通过活性亚甲基拼接原理,将卤素、酰胺、肟酯、酰腙等具有潜在活性的单元引入β-蒎烯中合成蒎烯基衍生物,并研究化合物在农用抑菌剂方面的开发潜力,以期为松节油在现代有机农业领域的高附加值利用提供思路。
1 实 验
1.1 主要仪器与试剂
AVANCE Ⅲ 核磁共振波谱仪、microTOF-Q Ⅲ电喷雾质谱仪,瑞士Bruker公司;Nicolet iS10傅里叶变换红外光谱仪,美国Thermo公司;SGW X- 4B显微熔点仪,上海仪电物理光学仪器有限公司。
β-蒎烯,上海麦克林生化科技有限公司;其他试剂均为国产分析纯。苹果腐烂病菌(Valsamali)、辣椒疫霉(Phytophthoracapsici)和番茄灰霉病菌(Botrytiscinerea),3种真菌均来自西北农林科技大学陕西省生物农药工程技术研究中心。
1.2 蒎烯基酰胺类化合物的合成
将根据参考文献[9]制备的50 mmol二氢枯茗酸(化合物3)溶解于二氯甲烷中,滴加15 mL二氯亚砜,40 ℃保温回流8 h,反应完毕,减压旋蒸除去过量的二氯甲烷和二氯亚砜溶液,得到二氢枯茗酸酰氯(化合物4)[13]。将50 mmol含卤素的苯胺溶解于二氯甲烷溶液中,60 mmol吡啶为缚酸剂,冰浴下滴加前期制备的50 mmol二氢枯茗酸酰氯,室温反应3 h,采用薄层色谱(TLC)监测反应进程。所得反应产物经酸洗、碱洗、水洗至中性后,柱层析(V(乙酸乙酯) ∶V(石油醚)=1 ∶15~1 ∶5)纯化,干燥制得蒎烯基酰胺类化合物5a~5g(见图1)。
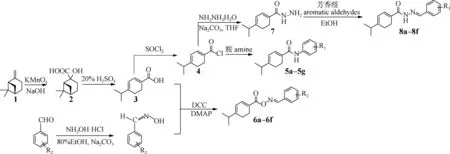
5a.R1=4-F; 5b.R1=2,6-F; 5c.R1=4-CF3;5d.R1=2-Br; 5e.R1=3-Br; 5f.R1=4-CH3O; 5g.R1=4-NO2; 6a.R2=2-F; 6b.R2=3-F; 6c.R2=4-F; 6d.R2=2-Cl; 6e.R2=2-Br; 6f.R2=3,5-F; 8a.R3=H; 8b.R3=2-Br; 8c.R3=2-F; 8d.R3=4-Br; 8e.R3=4-NO2; 8f.R3=4-CN图1 蒎烯基衍生物的合成路线Fig.1 The synthetic routes of β-pinene derivatives
1.3 蒎烯基肟酯类化合物的合成
在50 mL 80%乙醇溶液中,加入50 mmol含卤素的苯甲醛和盐酸羟胺,搅拌溶解,分批加入15 g的无水碳酸钠,将反应液的pH值调至中性,采用TLC监测反应进程。过滤除去反应生成的氯化钠后,将滤液倾倒入冰水中,即生成大量白色絮状固体。用无水乙醇重结晶,即可得到所需的含卤素苯甲醛肟(化合物10)[14-15]。取48 mmol上述合成的肟,加入25 mL的二氯甲烷溶解后,加入2 g无水硫酸镁,静置,过滤除去硫酸镁固体。用同样的方法除去二氢枯茗酸中的水,将二氢枯茗酸倒入单口圆底烧瓶中,滴加1 g的二环己基碳二亚胺,0.4 g的4-二甲胺基吡啶,将除过水的含卤素苯甲醛肟用滴液漏斗逐滴滴入反应液中,采用TLC监测反应4 h。柱层析(V(乙酸乙酯) ∶V(石油醚)=1 ∶15)提纯,干燥制得蒎烯基肟酯类化合物6a~6f(见图1)。
1.4 蒎烯基酰腙类化合物的合成
将62.5 mmol水合肼和50 mmol碳酸钠在50 mL四氢呋喃中搅拌溶解后,缓慢滴加前期制备的50 mmol二氢枯茗酸酰氯,室温反应12 h,反应完毕后,旋蒸出溶剂,50%乙醇和水80 ℃重结晶,过滤,干燥得白色粉末二氢枯茗酸酰肼(化合物7)。将20 mmol二氢枯茗酸酰肼和20 mmol醛溶于无水乙醇中,80 ℃回流,采用TLC追踪反应进程[16-18]。反应完毕后,冷却至室温,析出大量固体,抽滤收集产物,乙醇重结晶,得二氢枯茗酸酰腙类化合物8a~8f(见图1)。
1.5 结构表征
使用KBr压片法在傅里叶变换红外光谱仪上进行红外光谱测定;使用核磁共振波谱仪在400/500 MHz 下测定化合物的1H HMR,试剂为DMSO-d6,以TMS为内标;使用电喷雾质谱进行化合物相对分子质量测定;固体化合物熔点的测定在显微熔点仪上进行。
1.6 抑菌活性测试
1.6.1含毒培养基的配制 将化合物用二甲基亚砜溶解,配制成质量浓度为10 g/L的药液。根据参考文献[9]制成马铃薯葡萄糖琼脂(PDA)培养基,将100 mL培养基,倒入锥形瓶,再加1 mL药液,混匀。最后,将含毒培养基倒入直径为 9 cm的培养皿中,待其凝固。
1.6.2真菌的培养 用直径为4 mm的打孔器取活化的苹果腐烂病菌、番茄灰霉病菌和辣椒疫霉,沿着菌落外围打一圈菌饼。将菌饼菌丝面朝下依次接种在含毒培养基中央,设置3个重复,空白对照和阳性对照分别为二甲基亚砜和多菌灵,将接好菌的培养皿放置于培养室中28 ℃恒温培养。
1.6.3初筛与复筛 采用菌丝生长速率抑制法测试化合物的抑菌活性[19]。观察菌落大小,若菌落生长至培养皿的2/3大小,则可采用十字交叉法测量,按下式计算抑制率(η):
η=(dCK-dT)/(dCK-4)×100%
式中:dCK,dT—分别表示空白对照和处理的菌落直径,mm。
在初筛结果的基础上,进行更为精密的毒力测定,将药液进行梯度稀释为100、 50、 25、 12.5和6.25 mg/L的一系列含毒培养基,等量的二甲基亚砜溶液为空白对照。每组测3次,计算平均值,采用SPSS软件计算出半数有效质量浓度(EC50),并作出毒力回归曲线。
1.7 蒎烯基化合物的结构优化
采用量子化学计算软件Gaussian 16对化合物的分子结构进行了几何优化,并计算化合物的最低能量。针对活性较高的化合物8f进行了最低未占用分子轨道(LUMO)、最高未占用分子轨道(HOMO)、电子密度和电荷分布以及静电势能的研究,进一步探讨卤素、氰基和硝基等电负性官能团的引入对化合物活性的影响。
2 结果与讨论
2.1 蒎烯基衍生物的结构表征









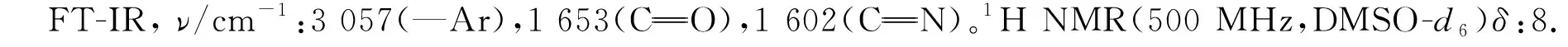









2.2 抑菌活性研究
3个系列蒎烯基衍生物的抑菌活性初筛结果列于表1,以广谱商品杀菌剂多菌灵为阳性对照。在100 mg/L质量浓度下,19个化合物对苹果腐烂病菌、番茄灰霉病菌、辣椒疫霉均有一定抑菌活性,对苹果腐烂病菌抑制活性最好。其中,8个化合物对苹果腐烂病菌的抑制率超过80%,活性最高的化合物5a、5b和8c的抑制率分别为90.6%、 90.3%和90.6%;其次是化合物8a、8b、8d、8e和8f,抑制率分别为88.8%、 85.9%、 87.6%、 82.4%和88.9%。从3个系列化合物对苹果腐烂病菌的抑菌活性来看,酰腙类化合物(8a~8f)均表现较高的抑菌活性,肟酯类化合物(6a~6f)抑菌活性较低,推测在蒎烯基衍生物的骨架中增加氮原子个数,可能有利于提高化合物的抑菌活性。此外,含氟原子的化合物,如5a、5b、8c对苹果腐烂病菌的抑制率都在90%以上,表明在苯环上引入氟原子能显著提高化合物的活性。

表1 β-蒎烯衍生物对3种农业真菌的抑菌活性(100 mg/L)Table 1 Antifungal activities of β-pinene derivatives on three agricultural fungi(100 mg/L)
在此基础上,选取8个对苹果腐烂病菌抑制率在80%以上的化合物进行复筛,结果发现:蒎烯基酰胺类衍生物5a、5b,蒎烯基酰腙类衍生物8a~8f对苹果腐烂病菌具有较好的抑制活性,化合物5a、5b和8b~8f的EC50值范围在10~20 mg/L之间,其中酰胺类和酰腙类活性较高的化合物5a、5b、8c和8f的抑菌效果见图2,EC50数据见表2。
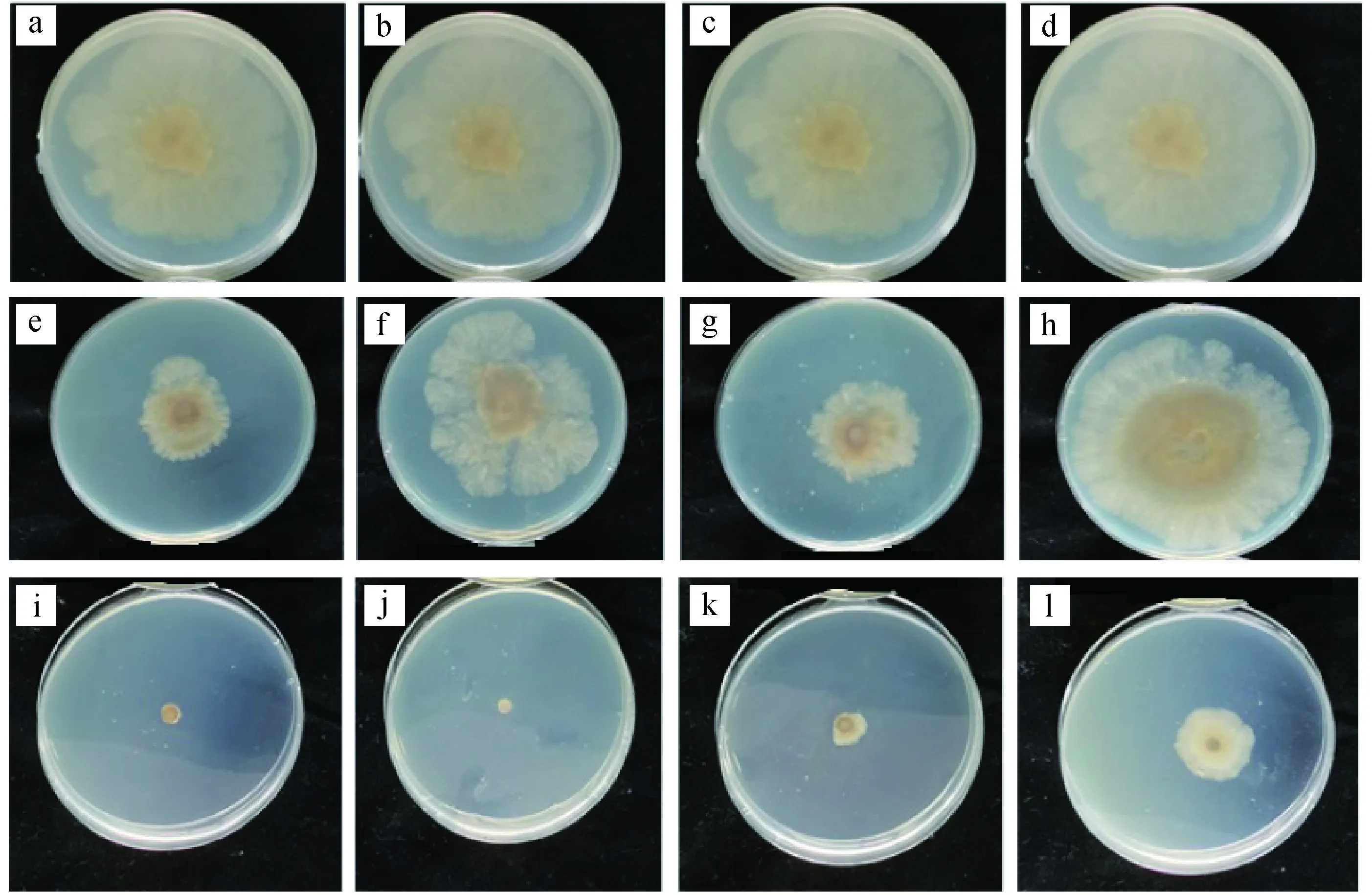
a.5a,空白对照control(CK); b.5b,CK; c.8c,CK; d.8f,CK; e.5a,25 mg/L; f.5b,25 mg/L; g.8c,25 mg/L; h.8f,25 mg/L; i.5a,100 mg/L; j.5b,100 mg/L; k.8c,100 mg/L; l.8f,100 mg/L图2 蒎烯基衍生物5a、 5b、 8c和8f对苹果腐烂病菌的抑菌效果Fig.2 The antifungal effects of β-pinene derivatives 5a,5b,8c and 8f on Valsa mali
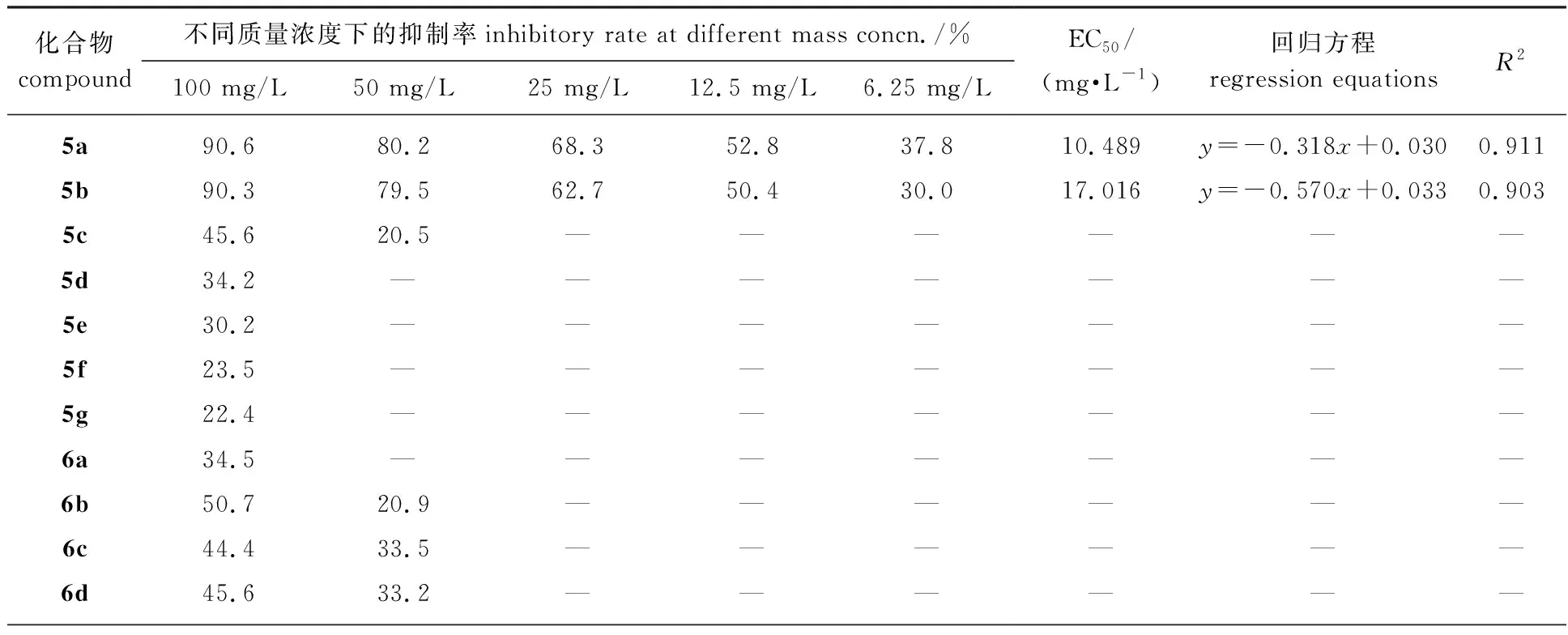
表2 蒎烯基衍生物对苹果腐烂病菌的抑制活性Table 2 Inhibitory activity of β-pinene derivatives on Valsa mali

续表2
2.3 化合物8f的能量优化
选择对苹果腐烂病菌抑制活性较高的化合物8f为代表,通过分析化合物的未占用轨道、电子密度和电荷分布以及静电势能图等量子化学描述符,如图3所示。

a.LUMO; b.HOMO; c.电子密度和电荷分布electronic density plot; d.静电势能图electrostatic potential energy plot图3 化合物8f最低能量结构的理论计算Fig.3 Theoretical calculation of the lowest energy structure of compound 8f
初步构建出化合物的结构特性与抑菌活性之间的相互关系。由于卤素、氰基和硝基等电负性官能团的引入,有利于化合物共轭键的稳定,能够提高化合物的电子云密度,并增大极性相互作用,有利于化合物与作用靶标之间的相互作用,因而显著提高了化合物的活性。
3 结 论
以β-蒎烯为原料,制备了3系列19种蒎烯基衍生物。通过菌丝生长速率抑制法研究目标化合物对3种常见的农业病原菌的抑制活性,筛选出8种对苹果腐烂病菌有较好抑菌活性的化合物, EC50值范围为10~20 mg/L,其中化合物5a和8e的EC50值分别为10.489和10.810 mg/L。通过进一步研究化合物结构与抑菌活性的关系,发现在蒎烯基衍生物中引入氮原子和氟原子有利于提高化合物的抑菌活性。通过对化合物8f的最低能量结构进行理论计算,发现引入电负性较大的官能团有利于化合物与作用靶标相结合,从而显著提高化合物活性。因此,在后续研究中可选取化合物5a和8e作为先导化合物,引入更多电负性较大的基团,获得活性更高的化合物,以期为林业可再生资源松节油在现代农业领域的高值化利用提供理论参考。

