两种国产荧光定量PCR试剂与Roche定量试剂的比较*
杨鑫城,单幼兰
重庆医科大学附属第二医院感染病科,重庆400010
乙型肝炎(下称乙肝)病毒(HBV)感染是一个全球性的公共健康问题,据世界卫生组织估计,2019年全世界约有2.96 亿慢性乙肝患者[1]。我国是全球HBV感染率最高的国家,大约有9 000万HBV感染者[2]。HBV具有高度传染性,可以通过血液、性接触或者母婴传播,感染后可导致急或慢性肝炎、肝硬化甚至肝癌。还有研究表明HBV感染不仅可以增加肝癌风险,还可以增加其他癌症的发生率,例如胃癌、胰腺癌等[3]。乙肝核酸(HBV-DNA)定量测定在乙肝患者的临床治疗过程中有着极为重要的参考价值,准确定量血清中的HBV-DNA对医生的诊断和用药非常重要[4-5]。HBV-DNA还是直接反映HBV复制状态及传染性的最佳指标[6],HBV-DNA的含量能直接反映病毒在体内存在的数量、是否传染,传染性有多强。此外,国外报道称,较高浓度的HBV-DNA与肝细胞癌的发病率和快速进展高度相关[7]。近年来,高灵敏度HBV-DNA技术因其检测下限低和线性范围广等优势,越来越受到临床医生的关注,许多专家和指南也将高灵敏度HBV-DNA检测结果作为HBV核苷酸药物治疗终点的重要指标[8]。国内有很多不同厂家生产的HBV-DNA荧光定量聚合酶链反应(RT-qPCR)试剂盒,不同试剂盒的性能存在一定差异,导致不同医院之间的结果难以进行比较[9]。因此,本文选用国内两种HBV-DNA RT-qPCR试剂盒及目前国际广泛应用的Roche试剂对71例临床乙肝患者血清进行检测,并对两种试剂的一些性能参数进行验证,比较检测结果之间的差异性和相关性,探讨各方法之间临床应用价值,以选择更适合本实验室的试剂,现报道如下。
1 资料与方法
1.1一般资料 收集2019年10月至2020年3月在本院感染科实验室做高灵敏度HBV-DNA定量检测的门诊及住院乙肝患者标本71例,标本以4 000 r/min的速度离心5 min,将血清分装至无菌EP管中,于-20 ℃冰箱冷冻保存,最长保存时间不超过6个月。HBV-DNA标准品(1.0×108IU/mL,批号300022-201601)购自中国食品药品检定研究院,使用阴性血清10倍梯度稀释至相应浓度值备用。
1.2仪器与试剂 核酸扩增仪为Applied Biosystem 公司提供的ABI-7500荧光定量分析仪和罗氏公司的Cobas AmpliPrep/Cobas Taqman 48系统;A试剂由上海复星医学有限公司提供,采用台湾圆点奈米技术股份有限公司提供的FD-SLA-32型全核酸自动提取仪提取核酸;B试剂由北京纳捷诊断试剂有限公司提供,采用静态核酸制备技术对核酸进行提取。
1.3方法 取用Roche定量试剂检测过的71例血清标本,分别用A、B两种试剂进行平行检测,测定标本的HBV-DNA载量,所有操作均严格按照试剂盒和仪器说明书进行。
1.3.1A试剂检测方法 在96孔预装板第一列中加入300 μL标本,放入核酸提取仪进行提取,35 min后取提取结束的HBV-DNA 20 μL加入含有30 μL反应液的反应管中,低速离心后置RT-qPCR仪上进行检测。其扩增条件为50 ℃反应2 min,94 ℃保温5 min,94 ℃ 10 s、60 ℃ 45 s,5个循环,再按94 ℃ 10 s、60 ℃ 45 s,循环40次,扩增总时间约为80 min。
1.3.2B试剂检测方法 将100 μL待测标本加入分装有裂解液的PCR反应管中,轻轻吹打混匀,静置 5 min,移至磁力架静置3 min,吸弃上清液,加入250 μL漂洗液,静置2 min,吸弃上清液。加入45 μL PCR反应液即可上机检测。扩增条件为50 ℃反应2 min,95 ℃保温5 min,再按95 ℃ 15 s、62 ℃ 45 s,循环50次,扩增过程需要90 min。
1.3.3Roche定量试剂检测方法 取750 μL待测标本加入样品管,移至Cobas AmpliPrep仪进行核酸提取,一个标本大概需要45 min可以提取完成,提取结束后转移至Cobas Taqman 48仪进行扩增,扩增过程需要150 min。
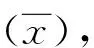
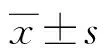
2 结 果
2.13种试剂检出率及病毒载量分析 在检测的71例血清标本中,A试剂检出阳性标本49例,检出率为69.01%;B试剂检出阳性标本60例,检出率为84.51%;Roche试剂检出阳性标本44例,检出率为61.97%,三者比较差异有统计学意义(χ2=9.327,P<0.05)。A试剂HBV-DNA病毒载量检测结果为(2.73±0.82)Log10IU/mL,B试剂HBV-DNA病毒载量检测结果为(3.38±0.84)Log10IU/mL,Roche试剂HBV-DNA病毒载量检测结果为(3.10±0.88)Log10IU/mL。A、B试剂分别与Roche试剂定量结果比较,差异均无统计学意义(P=0.282、0.611)。而A试剂与B试剂定量结果比较,差异有统计学意义(P=0.039)。见表1。
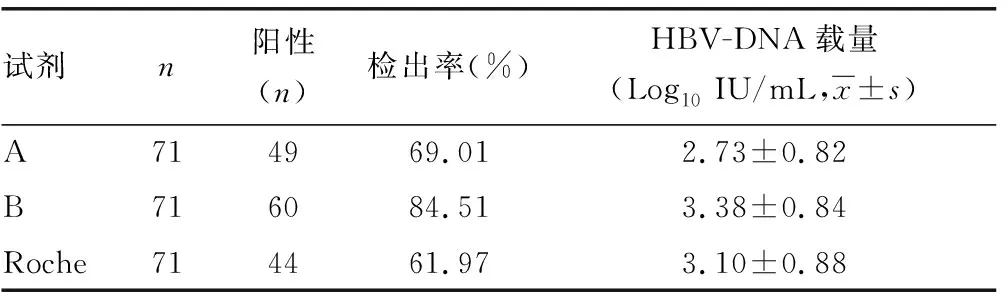
表1 三种试剂检出率及病毒载量结果比较
2.2两种试剂与Roche试剂检测结果的阴阳性符合率比较 71例标本中,A试剂与Roche试剂的阳性符合率为90.91%(40/44),阴性符合率为66.67%(18/27),总符合率为81.69%;B试剂与Roche试剂的阳性符合率为97.72%(43/44),阴性符合率为37.04%(10/27),总符合率为74.65%。根据检测结果,A试剂与Roche试剂的Kappa值为0.597,但差异无统计学意义(P=0.267),两种试剂一致性中等;B试剂与Roche试剂的Kappa值为0.393,两种试剂一致性一般,差异有统计学意义(P<0.05)。见表2。
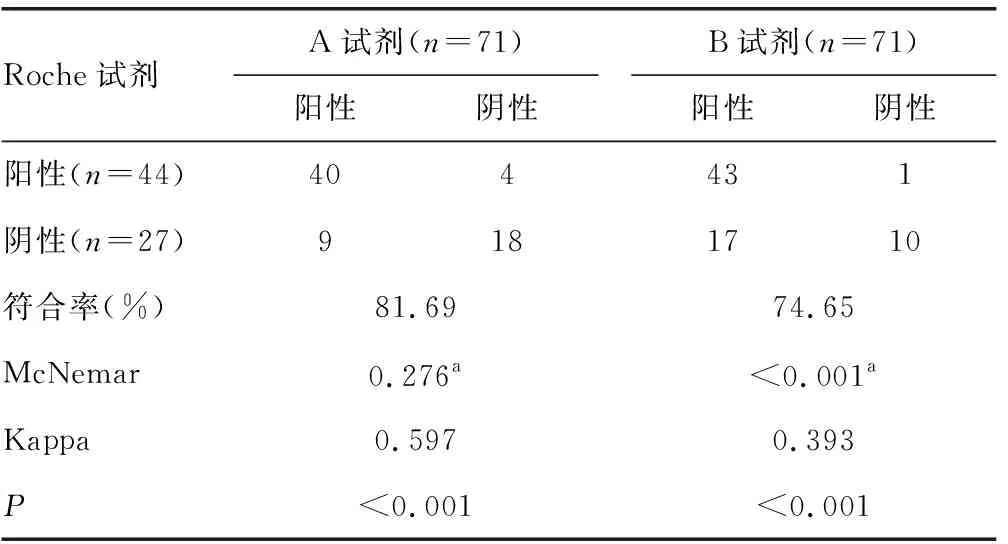
表2 A、B两种试剂与Roche试剂检测结果阴阳性符合率检验
2.3两种试剂与Roche试剂检测结果的相关性分析 3种试剂对71例血清标本进行检测,其中32例标本的3种试剂检测结果均有数值,其余至少有一种试剂未检测出具体数值。对A、B试剂和Roche试剂检测有数值的结果取对数值后进行相关性分析。A试剂与Roche、B试剂与Roche的分别为0.896、0.908(均P<0.05),A试剂与Roche、B试剂与Roche的相关线性回归方程分别为Y=0.763X+0.590(R2=0.803)、Y=0.760X+1.100(R2=0.825)。见表3。

表3 A、B两种试剂与Roche试剂的相关性分析
2.4A、B试剂的性能验证
2.4.1最低检测限及最低定量限 A试剂重复检测8次浓度为20 IU/mL的标本,检出率为100.00%,提示该试剂的最低检测限为20 IU/mL,重复检测8次浓度为100 IU/mL的标本,检出率为100.00%且对数值结果偏差均在±0.4范围内,提示该试剂的最低定量限为100 IU/mL;B试剂重复检测8次浓度为20 IU/mL的标本,检出率为100.00%且87.50%的对数值结果偏差在±0.4范围内,提示该试剂的最低检测限和最低定量限均为 20 IU/mL。
2.4.2线性范围 A试剂数据处理后得到的回归方程为:Y=-0.996X+8.925,R2=0.999。见图1。通过最低定量限实验及此实验验证可知,A试剂在1.0×102~1.0×108IU/mL浓度范围内线性良好。

图1 A试剂线性回归直线
B试剂数据处理后得到的回归方程为:Y=-0.985X+8.575,R2=0.999。见图2。通过最低定量限实验及此实验验证可知,B试剂在2.0×101~1.0×108IU/mL浓度范围内线性良好。

图2 B试剂线性回归直线
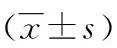
2.4.4正确度评价 根据偏倚=(实验方法结果-参比方法结果)/参比方法结果×100.00%,A、B两种试剂检测均有数值的结果剔除离群值后计算偏倚分别为-6.69%,6.08%。两种试剂偏倚均在±7.50%内,正确度良好,但B试剂与Roche试剂之间的偏倚绝对值更小,可比性更高。
3 讨 论
尽管现在有很多有效的抗病毒药物和疫苗,但是HBV感染仍然是世界范围内一个重大的公共卫生挑战。为了判断HBV感染的阶段或者HBV感染者肝脏炎性疾病的发生进展,需要进行HBV-DNA定量检测。HBV-DNA定量检测在判断疾病活动性、制订抗病毒治疗方案、治疗监测以及判断治疗终点中均起到重要作用[14]。目前,定量检测HBV-DNA的方法有很多种,其中,荧光定量PCR是常用的检测手段[15]。Roche试剂具有较高的灵敏度、精密度、重复性,被国际公认为是HBV-DNA定量的参比试剂[16],其最低检测限为20 IU/mL,但价格昂贵,难以在基层医院广泛使用。A试剂核酸提取采用的是目前国内常用的磁珠分离技术,最低检出限为20 IU/mL,虽然其最低检测限与Roche试剂的一致,但其最低定量限为100 IU/mL,高于Roche试剂的最低定量限20 IU/mL,这意味着使用A试剂进行检测时,100 IU/mL以下的病毒载量无法准确定量,甚至有无法检出的可能性。而B试剂所采用的是一种简称“静态核酸制备技术”的方法,标本处理和检验在一个PCR反应管中完成,其最低检测限和最低定量限均为20 IU/mL,可以达到和Roche试剂同一个灵敏水平。在此次研究中,有2例标本A试剂的检测结果偏低,比B试剂和Roche试剂低了3个数量级以上,原因可能与不同基因型病毒株感染或病毒发生变异造成的引物探针不能有效结合有关。因此,对于实验室检测结果与临床症状严重不符的标本,有必要采用不同的试剂盒进行复核,以保证结果的准确性。
研究结果显示,A、B试剂的检出率均高于Roche试剂。不同试剂间检测结果的差异考虑可能与试剂引物扩增序列,或者某些乙肝病毒发生前区变异有关[9],也可能与试剂的质量或操作误差等有关[17]。此次结果与既往的部分报道[18-19]不一致,这些实验发现国产试剂的阳性率低于进口试剂,而此次实验发现,此两种国产试剂的检出率均高于Roche试剂。但此种差异是否是由于准确度或灵敏度所导致的还需要更进一步的研究。近年来国内也有不少针对国产高灵敏度HBV-DNA定量的方法学研究报道[20-21]。本实验还将A、B试剂与Roche试剂病毒载量的结果进行了比较,发现A、B试剂与Roche试剂定量结果之间差异无统计学意义,说明两种试剂定量结果与Roche试剂无显著差别。这与周美美等[19]报道有所不同,说明近年来一些国产HBV-DNA试剂定量性能方面逐渐优化,可以和Roche试剂相媲美。而且本研究结果发现B试剂的定量结果稍高,这可能与其核酸提取的方式有关,其核酸提取和扩增过程均在一个反应管中进行,减少了HBV-DNA提取过程的各种损耗。本研究将两种国产试剂与Roche试剂的检测结果在阴阳性符合率方面做了比较,结果显示,A、B试剂与Roche试剂的符合率分别为81.69%、74.65%。相比之下,B试剂与Roche试剂的符合率偏低,这是因为在Roche试剂44例阳性标本中,B试剂检出了43例,仅有1例未检出,而Roche试剂27例阴性标本中,B试剂检出了17例阳性,阳性符合率达到了97.72%,阴性符合率仅有37.04%。分析认为可能是近年来一些国产荧光定量PCR试剂的灵敏度逐渐提高,可以检测到Roche试剂无法检测到的低浓度值,导致阴阳性符合率有较大的差异,期待后续补充完善相关实验。在定量方面,A试剂与Roche试剂的r为0.896,B试剂与Roche试剂的r为0.908。说明两种试剂的检测结果与Roche都有良好的相关性,B试剂相对更好一些。此外,本研究结果表明,A、B试剂的最低检测限均不大于30 IU/mL,符合《乙型肝炎病毒脱氧核糖核酸定量检测试剂注册技术审查指导原则》中限定HBV-DNA注册试剂的最低检测限[10]。极低水平的HBV-DNA在部分人群中有着重要的临床意义[8],行HBV-DNA 检测能从HBV表面抗原无反应性标本中有效发现低病毒载量的乙肝患者,特别是能有效检出OBI和HBeAg(-)慢性乙型肝炎患者,防止血清学漏检[22]。此外,本研究发现,A、B试剂检测值与理论值之间线性良好,分别在1.0×102~1.0×108IU/mL和2.0×101~1.0×108IU/mL浓度范围内成线性,r2≥0.995,符合要求。A、B试剂说明书所述的最高定量限分别1.0×109IU/mL和2.0×109IU/mL,但是本次实验未取得浓度高于1.0×109IU/mL的标本,故仅验证108IU/mL以下的线性。验证的低、高浓度标本重复性、精密度、CV均符合要求,验证通过,具有良好的重复性。本文还以Roche试剂为参比试剂,A、B试剂为实验试剂,分别验证了A、B试剂的正确度,平均偏倚均小于±7.5%,可以满足临床应用的要求。
通过比较可以发现B试剂的性能相对A试剂更加优越,B试剂核酸提取率较高,灵敏度和准确度也较高,重复性更好,且具有更宽的线性范围,但是自动化程度相对较低。总体来说,近年来我国国产的乙肝定量试剂性能逐渐优化,定量结果方面与进口试剂有良好的相关性,可以满足临床患者治疗监测的要求。各实验室应综合考虑,在保证检验质量的前提下,选择符合自己实验室的试剂。通过进行A、B试剂的性能验证实验及与Roche试剂对临床标本的检测结果比较可知,B试剂更适合本实验室,选择B试剂将可以检测到更低水平的HBV-DNA,核酸获取率也更高,能为临床提供更准确的报告。

