基于教材解读与真实情境模拟的催化剂教学实践


摘 要:在教学中创设有效情境是调动学生学习兴趣的最好动力,这样能够激发学生的好奇心和灵感。各种高效、经济、选择性强的催化剂的研制是重大课题,高中化学教学也要重视催化剂的研究。教师应对教材文本中催化剂的表述进行深刻解读,并以真实情境下催化反应的工业或实验模拟图辅助教学,帮助学生建构催化剂认知模型,使其能够建立解决复杂化学问题的思维框架。对此,文章阐述了催化剂的相关研究、催化剂教学的现状以及相关教材解读,并列举了模拟真实情境的催化剂教学实践,以供参考。
关键词:催化剂;教材文本;真实情境;教学启示;思维框架
作者简介:刘现林(1976—),男,浙江省杭州第十四中学。
催化剂是化学研究中永恒的主题。催化剂在生产和生活中有广泛的应用,有关催化剂的教学也需要与时俱进。高中生已从定性思维进入定量思维阶段,可以对催化剂进行较为严格、真实的学习[1]。
一、催化剂相关研究
文献中与“催化剂”匹配的大多是新型、高效催化剂的研究进展,基于高中学生认知水平且与教材文本相关的催化剂反应机理和选择应用有关的文章较少[2]。新课程改革以来,模拟化工生产真实情境的催化剂应用评价主要从自发反应、反应历程、活化能、反应速率、平衡移动、催化剂选择等角度入手[3]。
二、催化剂教学现状及相关教材解读
学生通过《化学反应原理》的学习可了解到,催化剂之所以能够促使反应的速率加快,最主要的原因是其能够降低化学反应的活化能。催化剂的催化效果受环境的影响比较大,比如温度、pH、比表面积等,但催化剂不改变化学平衡转化率。当前,与催化剂相关的教学仅仅停留在简单动手做实验、表层理解的阶段,导致学生尚未能够依据催化反应及其变化的信息建构模型,建立解决复杂化学问题的思维框架,也没有从催化剂知识学习的初级思维上升到高阶思维。这就需要教师对教材文本中催化剂的表述作深刻解读与研究。
(一)新课标对催化剂的教学要求
(二)催化反应的两种理论解释
碰撞理论和过渡态理论是用于解释催化作用的两个理论。碰撞理论指出,唯有活化分子之间的碰撞才有可能引起反应,又称有效碰撞理论。
Eyring和Pzer基于碰撞理论提出过渡态理论,指出化学反应并不是通过简单的碰撞就能完成的,反应物到生成物的过程中必须经过一个高能量的过渡态。基态是分子比较稳定的初始状态;过渡态是分子极其不稳定的状态,分子在此状态极易重新组合形成新物质。活化能指的是将1mol反应物中的所有分子由基态转化为过渡态所需要的能量,而降低化学反应当中的活化能就是催化劑所具备的重要作用。
吸热反应的正反应和逆反应的活化能都会受到催化剂的影响。放热反应的活化能会受到催化剂的影响。实验证明,催化剂与反应历程、活化能的关系都可以归结到催化剂能有效降低活化能,提高活化分子百分数,增大有效碰撞的频率。显然,催化反应正是碰撞理论和过渡态理论的综合体现。
三、模拟真实情境的催化剂教学实践
情境模拟具有以下四个特点:第一,实践性。情境模拟与传统的教学模式不同,其是利用情境仿真出复杂的情况,然后引导学生利用知识解决问题,从而实现从实践到理论再回归实践的要求。第二,综合性。情境模拟通过设置,使情境具有一定的开放性和包容性,学生可以将学到的东西运用到具体的问题情境中,利用联系、发展的眼光来看待并分析问题。第三,参与性。真正将学生作为课堂的主体,教师起到组织和引导的作用,锻炼学生的观察能力、分析能力与交流能力,这与单向的讲解完全不同。第四,实效性。情境模拟的方式更加形象直观,便于学生理解,有助于学生解决一些比较抽象、难以理解的问题。
科学理解可以分为描述性理解、定性式理解、定量式理解、符号式理解等若干阶段,化学课程的设计者需要据此作通盘考虑[4]。
首先,在对催化剂的相关内容进行教学设计时,教师需要选取一些能够对学生思维形成挑战而且具有化学反应应用价值的素材。其次,在开展模拟工业真实情境的教学活动中,教师要注重发展学生的演绎推理、系统假设等思维能力。最后,教师带领学生开展相关的研究活动时,要注重培养学生分析图像和解释实验现象的能力,并结合一些具体的生产实例,引导学生对反应条件的选择以及优化进行合作讨论,进而帮助学生形成从各个角度调控化学反应的基本思路,促使学生在化学学习的过程中形成“绿色化学”的观念,并能运用辩证的思维看待问题。下面,笔者从三例模拟工业真实情境的图像和数据解读催化剂教学。
(一)催化剂与转化率(或产率)的关系
[例1]已知反应:NH4Cl(s)+CH3OH(g)NH3(g)+CH3Cl(g)+H2O(g)。图1是在反应的过程中运用了几种不同的催化剂而得到的关系图,在实验的过程中反应时间以及催化剂的用量等条件都相同,且n(甲醇)/n(氯化铵)=1/2。
[问题1]图1表明:当其他条件相同时,多孔球型γ-Al2O3催化活性明显高于分子筛催化剂,试解释其原因。
[参考答案1]当其他条件相同时,多孔球型γ-Al2O3能更大程度地降低该反应的活化能,增大单位体积内活化分子百分数,从而提高CH3Cl生成速率。
[变式1]请在图2中分别画出无催化剂、分子筛催化剂、多孔球型γ-Al2O3三种情况下“反应过程—能量”示意图。与标准答案对照,学生答案中有催化剂参与的反应普遍只有一个峰。显然,学生对催化反应并不理解。普通的一级反应一般只有一个峰。但有催化剂参与的反应是先与反应物形成一个不稳定的中间物,此反应在能量进程图中显示一个峰,不稳定的中间物分解或继续与反应物作用形成生成物与等量性质不变的催化剂,图中出现第二个峰。
[问题2]分析图3中a、b、c三条曲线中的点,思考哪些可能是CH3Cl的平衡产率,哪些不是CH3Cl的平衡产率。
[参考答案2]催化剂不能改变平衡转化率(或产率)。但在平衡前,加入催化效率高的催化剂,相同时间内反应物的转化率更高,所以工业上往往寻找高效催化剂。产率高者更可能达到平衡,因此c曲线可能为平衡产率,a、b曲线肯定不是平衡产率。
[变式2]当其他条件都相同,温度为370℃且使用三种不同类型的催化剂时,请在图3当中绘制出CH3Cl的产率随时间变化而发生变化的曲线,分别运用a、b、c对相应的曲线进行标注。学生答案与标准答案基本一致。显然,学生对于催化剂的表观作用掌握到位。
教师在课堂教学中通过实例层层递进,引导学生对预测、方案、结论进行完整论证,才能培养学生的系统思维能力,并帮助学生建立系统思维框架,提高学生分析、解决问题的能力,学生才能轻松作答变式1和变式2。
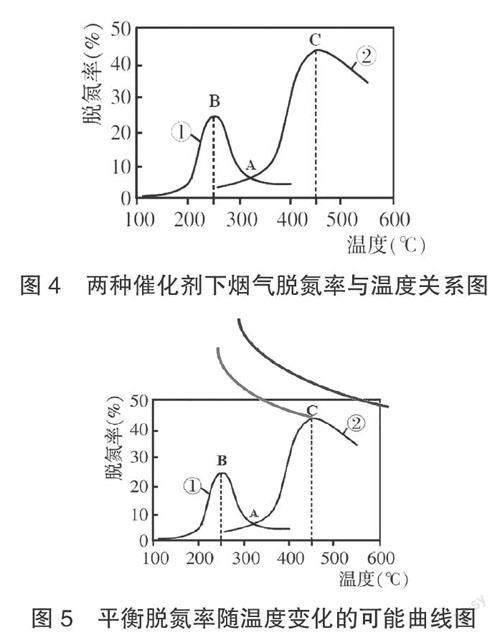
[例2]已知反应:NO(g)+NO2(g)+2NH2(g)2N2(g)+3H2O(g)ΔH<0。如果采用的还原剂为NH3,烟气以一定的速率通过两种不同的催化剂时,对产生气体当中的氮氧化物含量进行测量,最终得到烟气脱氮率,结果如图4所示:
[问题1]由图4可知,在催化剂①的作用下,烟气脱氮率先增大后减小,请指出100~250℃脱氮率增大的可能原因。
[参考答案1]100~250℃脱氮率增大可以用两种理论解释。a.碰撞理论——温度升高,单位体积内活化分子百分数增加,反应速率增大;b.过渡态理论——催化剂活性随温度升高而增大,从而加快速率。而速率的加快使相同时间内的脱氮率增大。
[问题2]在图4交叉点A处,使用催化剂①或②,上述反应 (肯定/可能/肯定没有)达到平衡,并说明理由。
[参考答案2]肯定没有达到平衡。若A点是平衡点,则温度升高,平衡逆向移动,脱氮率下降,这与催化剂②所呈现的图像相矛盾。
[问题3]在图4催化剂①的作用下,请指出250~400℃脱氮率下降的可能原因。
[参考答案3]反应尚未达到平衡,催化剂活性下降造成脱氮率下降。
[问题4]由图4可知,在催化剂②的作用下,烟气脱氮率先增大后减小,请指出450~500℃脱氮率下降的可能原因。
[参考答案4]a.反应已达平衡,温度升高,平衡逆向移动;b.温度升高,催化剂活性下降。
[变式3]请在图5中绘制出平衡脱氮率随温度变化的可能曲线图。学生的答案中只給出C点之前已经达到平衡的曲线,但未画出存在平衡点更高的曲线。显然,学生没能完全领会图5中最高点的含义。
教师在课堂实例中要有意识地说明建构思维模型的重要作用,只有这样,学生才能够更好地把握模型建立与论证证据之间的关系,才能更完整地回答变式3。
(二)催化剂与反应选择性之间存在的关系
[例3]当存在Cu/ZnO催化剂时,CO2和H2之间可以发生两个不同的反应,相对应地,会形成CH3OH和CO两种产物。具体会发生如下反应:
[问题]根据表2中的数据可以看出,在温度相同的情况下,种类不同的催化剂往往会对CO2转化成CH3OH反应的选择性产生非常大的影响,试分析其中的原因。
[教师过渡]a.有很多的化学反应往往不止产生一种产物,但是通过对催化剂的控制可以实现对反应方向的控制。因此,在工业生产时要优先考虑对目标产物选择性高的催化剂。选择性是指所消耗的原料中转化成目的产物的百分率,即选择性=转化成目标产物的指定反应物的量/已转化的指定反应物的量×100%。b.化学平衡是由热力学决定的,ΔGθ=-RT㏑Kp,其中Kp为反应的平衡常数,ΔGθ是状态函数,表示产物与反应物的标准吉布斯自由能之差,只决定于过程的始终态,而与过程无关。催化剂的存在不影响ΔGθ值,它只能缩短到达平衡所需的时间,而不能移动平衡点。
[参考答案]这时并没有达到反应的平衡点,采用不同的催化剂往往会对反应Ⅰ产生不同的催化能力,在这一刻,对甲醇的选择性会受到影响。可见,反应未达平衡,催化剂才能体现选择性。
催化剂与转化率、反应选择性的关系,催化剂的效率与反应条件的关系等教学的开展依托真实情境的工业或实验模拟图,教师的启发与过渡可帮助学生搭建解决催化剂相关问题的思维模型和框架,使学生的学习有事半功倍的效果。调查显示,学生对此节课内容的掌握程度达到90%以上。
“催化剂教学”是将学习化学知识和技能的过程转变为联系社会生产、生活实际进行科学研究并形成科学素养的典型代表。情境模拟为教学提供了很大的便利,它是理论联系实际的桥梁,开辟了一条从课堂走向社会的道路,还能调动学生的积极性,让他们从被动学变为主动学,提高了学生的实践能力和认知能力,在实际生活中应用也十分广泛,能够科学分析问题,使学生愿意主动去学习。通过教师的积极引导,这样的教学会有事半功倍的效果,对学生以后的工作和学习都有帮助,能为他们步入社会打下基础。
[参考文献]
张映明.化学教材中与催化剂有关的几个问题[J].化学教育,2013,34(2):10-13.
吴晗清,李豆豆.“催化剂”认知困境与教学对策[J].化学教学,2018(3):87-91.
尹沧浪.基于真实情境下催化剂考查形式的多维分析[J].中学化学教学参考,2018(10):65-66.
钟启泉,崔允漷,张华.《基础教育课程改革纲要(试行)》解读[M].上海:华东师范大学出版社,2001.

