促进氨燃料转化的预裂解器反应动力学分析*
路 广,王君雷,李世龙,梁兴雨,王 昆
促进氨燃料转化的预裂解器反应动力学分析*
路 广,王君雷,李世龙,梁兴雨,王 昆†
(天津大学 先进内燃动力全国重点实验室,天津 300354)
在国家双碳背景和节能减排要求下,以氨为燃料的微型燃气轮机是氨利用的热门方向。但其火焰稳定性差和NO排放等问题亟待解决。设计燃烧器底部燃料喷射和旋流方式,加入旁通管路,利用燃烧器外壁热量使部分氨预裂解为氢气和氮气以强化燃烧。优化氨热解反应动力学模型并利用Ansys Chemkin-Pro软件模拟温度和流速对旁路氨转化率的影响。结果表明,当温度达到1 500 K时,氨开始出现明显裂解行为;在1 500 ~ 1 800 K之间,氨转化率随温度升高迅速升高;当温度高于1 800 K后,氨转化率超过85%。流速的变化也会影响转化率,但明显小于温度的影响。同时,对不同温度下氨裂解反应路径开展敏感性分析,结果表明氨裂解反应路径受温度影响,在1 700 K温度下,反应NH3+ NH2⇋N2H3+ H2对氨裂解促进效果最显著。结论验证了使用部分预裂解氨稳定燃烧的可行性,可为下一步研究氨单一燃料在微型燃气轮机的稳定燃烧和降低排放提供理论支持。
氨气;微型燃气轮机;燃烧室;预裂解
0 引 言
燃烧是人类活动的主要能量转换方法,自工业革命以来人类的运输、生产、发电等各类活动都离不开燃烧。虽然人们已经在努力减少温室气体排放,例如通过提高燃烧效率等方法,但这些努力还不足以实现低温室气体排放的目标[1]。工业发电及其他能源方向原动机的脱碳对克服这一问题和履行温室气体排放方面的目标法规至关重要。然而,无碳发电的未来主要取决于可再生、低碳或无碳燃料的利用,以解决能源需求的增加,同时将能源生产过程中的环境影响降至最低[2]。
氨(NH3)作为一种无碳燃料,其在全球范围内的储存和分配都有完善、可靠的基础设施。因此,氨作为化学储能材料替代化石燃料的应用吸引了很多学者的兴趣,并成为某些研究团队的主要研究目标,尤其是在燃气轮机方面。但是,氨燃烧的现状并没有理想中的完美,其燃烧速度低和点火能量高等特点使其难以像其他碳氢燃料一样在燃烧器中稳定地燃烧。表1列举了氨与其他碳氢燃料燃烧特性的对比。氨不完全燃烧会产生其他氮氧化物如NO等,加剧对空气的污染。因此,若要实现对氨气高效低污染的应用,其火焰的稳定燃烧以及排放物浓度的降低是需要解决的问题。

表1 NH3、H2及碳氢燃料的燃烧特性比较[3]
有研究显示,旋流燃烧器可以使氨气燃烧的稳定性得到一定程度的提高[4],并且可在一定程度上降低有害气体的排放。目前已有的关于开发氨气旋流燃烧的研究比较成熟,且在某些领域已经得到应用。HAYAKAWA等[5]对旋流稳定氨/空气预混火焰的火焰稳定性和排放特性进行了实验研究,结果表明,在无任何添加剂的旋流燃烧器中,即使氨的层流燃烧速度很慢,在不同当量比和入口流速条件下,氨/空气预混火焰仍能保持稳定。OKAFOR等[6]提出了氨旋流燃烧器高效燃烧和低NO排放的燃烧技术及燃烧器设计,模拟了两段式燃烧室对排放产物浓度优化的影响。数值计算和实验结果表明,与沿燃烧室中心轴垂直喷射相比,倾斜燃油喷射可提高火焰稳定性,降低NH3和NO排放。
除单纯使用旋流燃烧器稳定氨气火焰外,研究者还考察了掺混其他碳氢燃料以改善氨气燃烧特性。如掺混氢气、甲烷等火焰燃烧速度更快的燃料以稳定燃烧。卫旭涛等[7]基于半封闭空间旋流燃烧器,对氨气掺混氢气火焰的流场和火焰结构进行测量。结果表明,在特定条件下总会存在一个最佳当量比使得各个尾气组分处于较低水平。VALERA-MEDINA等[8]通过实验和燃烧诊断检测方法,使用摩尔分数为70%的NH3和30%的H2混合气作为燃料气进行燃烧实验。结果表明,氨气可以用作燃气轮机的燃料,并具有稳定的燃烧作用。掺混其他气体固然可以提高氨气层流火焰燃烧速度,但实验条件下的掺混往往难以进行工程上的应用,而将部分氨气进行裂解后产生的氢气同样可以达到稳定燃烧的目的,并且省去了额外添加其他气体的麻烦。20世纪60年代,美国陆军资助了一系列研究工作,以测试氨作为替代燃料来源的可行性。STARKMAN等[9]测试了一台火花点火、混合燃料研究发动机。氨从储存在热水浴中的高压瓶中提取。结果表明,为了在发动机中燃烧无水氨,氨必须以蒸气的形式引入,并部分裂解为氢和氮,最小氨分解量为氨重量的4% ~ 5%。VERKAMP等[10]研究了使用添加剂(C2H2、NO、NO2、N2O、CO)或者部分预解离氨稳定燃烧。实验结果表明,在添加剂含量为5%的体积浓度下,所有添加剂均未能将火焰稳定性提高到所需的程度。结果还验证了28%的游离氨可以作为替代燃料用于最适合烃类燃料的燃气轮机燃烧系统。另外,多数学者在进行此类研究时采用了预裂解后的产物浓度进行实验。KHATEEB等[11]研究了预混氨/氢/氮/空气旋流火焰的稳定性极限和NO排放,指出将氨分解为氢气和氮气并使用稀薄燃烧的氨/氢/氮/空气混合物有望为旋流燃烧器提供燃料,因无需二次燃烧阶段即可实现稳定的火焰和低废气NO的排放。
综上可知,目前在氨燃烧领域的研究主要集中在通过旋流燃烧器和掺混其他气体稳定火焰的方法,以及模拟部分氨预裂解再进行掺混的研究,但并没有进行真实的部分预裂解氨稳定燃烧的实验。本研究以新设计的微型燃气轮机燃烧室为基础,引出旁路通入氨气,利用燃烧器外壁热量达到预裂解,以实现纯氨燃料稳定燃烧的目的。使用化学机理模型模拟了不同壁温及流速条件下氨气的转化率,分析温度及旁路流速对转化率的影响,以目前已有研究氨气火焰温度为基础,确定裂解气旁路的流量及其他因素。探究在不额外添加其他气体的条件下,仅利用余热预裂解氨气达到稳定火焰燃烧及降低排放的可行性。
1 燃烧器设计和裂解反应实验模拟
1.1 燃烧器设计
目前已有的微型燃气轮机燃烧室结构大同小异,基本都包含旋流器、燃料喷射口、二次掺混孔等传统设计。与传统燃气轮机燃烧室相比,微型燃气轮机结构更加紧凑,性能上更具有优势,如减少尾气排放、稳定火焰燃烧等。本文对燃烧室的设计以已有的微型燃气轮机燃烧室结构及尺寸为基础,参考了文献[12],增加了可预裂解部分氨气的螺旋旁路管道,利用燃烧室外壁回收热量,将其用于氨气预裂解。取消了传统二次掺混孔。整体结构采用分体式和模块化设计,即燃烧室的各个组成均可根据后期实验和工程要求进行更换调整。根据后期实验进度和需求,本设计的单筒燃烧器主要有燃料喷射方式、盘管盘旋和管路设置、旋流器设置三个关键点。
1.1.1 燃烧器头部设计
研究涉及氨气裂解产物的掺混,即氢气的参与,将燃烧室设计为非预混燃烧型,因氨气的参与使得回火和爆炸的可能性增加,出于安全考虑不适用预混燃烧。如图1所示,喷嘴采用多孔式燃烧喷射。燃料喷孔与水平面存在夹角,角度本身不可改变,但可通过更换喷嘴进行角度调整,默认角度为45°,喷嘴本身不产生旋流,旋流由旁边旋流叶片生成;喷嘴旁边的旋流器可以使空气流经时产生旋流气流,旋流气流可使燃料气和空气更好地混合,使火焰产生旋流以达到稳定燃烧、延长停留时间的目的。同时燃料与空气的充分混合可以避免回火,降低有害尾气排放。

图1 燃烧器头部结构示意图
旋流器的叶片和旋流度本身是固定的,但同样可以进行更换以满足实验需求,本设计使用叶片数为12片,旋流度为0.8。
1.1.2 燃烧器盘管设计
燃烧器外壁在内部火焰的加热下会达到一个比较高的温度,而这些热量往往难以回收利用,本设计为了充分利用外壁的热量,将其热量传递给氨气使其热裂解。由于氨气热裂解需要较长停留时间,因此将管路设计为盘旋方式增加其长度。如图2,为了让管路能够接受更多来自燃烧器外壁的热量,将管路设置为矩形界面管,长度设置为10 mm,宽为6 mm(内管不包括厚度)。

图2 盘管结构示意图
1.1.3 气体通路设计
设计预期通入气体仅为氨气和空气,因此保留两个气体入口,具体如图3。氨气在进入燃烧室前被分为两股,一股直接通入燃料喷嘴的管路中;另一股通入燃烧器外部的盘旋管路中。盘管中的氨气随着盘管流动,同时被来自燃烧器外壁的热量加热裂解,当其流到出口处时,已经裂解为氢气和氮气。再将裂解后的气体通过管路和燃料喷射管路相连,中间设置单向阀防止氨气回流。

图3 气体通路示意图
1.2 氨气预裂解实验模拟
模拟以已设计好的燃烧器为几何基础,部分氨气通过其周围盘管,盘管热量来自燃烧器外壁传热。管路温度通过传热模拟发现其在极短时间内即可达到与外壁同温,因此将管道温度视作常温,温度设置参考文献[5,13],其基础模拟参数见表2。

表2 模拟参数设置
氨气预裂解实验采用的软件为Ansys Chemkin-Pro,模型选取平推流模型。如图4所示,模型流程图包括一个入口(氨气)、一个平推流反应器、一个出口。在流程图中,氨气从入口进入,在反应器中进行裂解,产物从出口排出。

图4 动力学仿真流程图
1.3 氨气热解反应动力学模型
选取合适的氨气热解反应动力学模型前,对比了已有的氨气模型,如KONNOV[14]、DAVIDSON[15]、GLARBORG[16]、SHRESTHA[17]、KLIPPENSTEIN[18]等提出的模型,但这些模型的使用目标仅针对其论文中的实验工况进行优化,在进行其他工况预测时会出现偏差。因此本文建立一个能够对多种工况进行预测的氨气反应动力学模型,该模型基于GLARBORG等[16]的模型进行了优化,使其在进行氨气热解模拟时能够更加接近真实结果。表3列出了与氨热解相关的11个反应,其速率常数已针对不同反应进行了验证。

表3 氨热解关键基元反应
注:反应速率系数采用修正的阿伦尼乌斯表达式,即=AT∙exp[−/()],其中:为指前因子,单位为1/s(一级反应)或cm3/(mol∙s)(二级反应);为温度依赖系数,无量纲;为修正的反应能垒,单位为cal/mol,1 cal = 4.187 J。
2 模拟结果与反应动力学分析
模型对氨宏观燃烧特性预测的准确性结果见图5[19]、图6。预测结果显示本模型能够对氨气层流火焰燃烧速度和点火延迟时间等宏观燃烧特性进行良好预测。
氨的热解实验数据来自BENÉS等[21]在流动管内进行的氨气热解实验数据,以用于与模拟使用机理进行比较,验证机理的准确性。实验条件设置如下,流动管长度为100 cm,直径为4 cm,管内压力为0.1 MPa,氨气摩尔分数为0.001,反应温度为900 ~ 1 475 K,管内载气为N2,气体流速为2 L/min。模拟条件与实验条件相同。结果如图7所示。图中可见,本模型在预测氨气热解方面与文献[21]的实验结果吻合较好,当温度高于1 400 K后氨气均出现明显裂解行为,证明了本模型机理的可行性以及模拟结果的可靠性。

图5 本模型与文献模型对层流火焰燃烧速率的模拟对比[19]

图6 本模型与文献[20]模型对点火延迟时间的模拟对比

图7 氨热裂解模拟结果与文献[21]实验结果对比
2.1 气体流速对转化率的影响
参考文献通常以实际燃烧工况下的流速为模拟条件进行模拟。文献[5-7]提到当来流速度约为3 m/s时,氨在旋流燃烧器下可稳定燃烧,为保证旁路裂解气与主路燃料气可以均匀混合,因此将流速范围设置列于表4。HAYAKAWA[5]、VALERA-MEDINA[13]等提到在化学当量比下,氨在其模型燃烧室中的火焰温度可达2 060 K,仅比甲烷火焰温度低160 K,但在贫燃条件下,其火焰温度会有所降低。参考文献[5,13]中实验结果表明,当量比在0.5附近且稳定燃烧状态下,氨气火焰温度为1 500 ~ 1 700 K。考虑到传热效率等问题,具体参数设置见表4。

表4 动力学仿真:流速与温度设置
模拟结果关注管道末端氨气转化率,如图8所示。随着气体流速的增加,未裂解的氨气含量逐渐增加,即气体在管路内的停留时间对氨气转化率有影响。但是在1 500 K条件下,氨气转化率非常低,当气体流速为280 cm/s、停留时间约为0.7 s,约6%的氨气被裂解;当流速增加至380 cm/s后,气体停留时间约为0.5 s,约5%的氨气被裂解。而当温度升至1 700 K、气体流速为280 cm/s时,约65%的氨气被裂解;当流速增加至380 cm/s后,约60%的氨气被裂解。由此可见,虽然气体在管内停留时间会对转化率产生影响,但影响幅度不大。同时,在1 500 K条件下远不能达到裂解气稳定燃烧。

图8 不同流速下氨气转化率
2.2 管路温度对转化率的影响
热解模拟以温度作为变量,根据参考文献[21]实验所得数据,氨气在平推流反应器中约1 200 K时开始出现裂解行为,但实际工况下对气体流速要求较高,因此将模拟温度范围设为1 400 ~ 1 900 K,流速根据参考文献取300 cm/s。具体实验设置见表5。
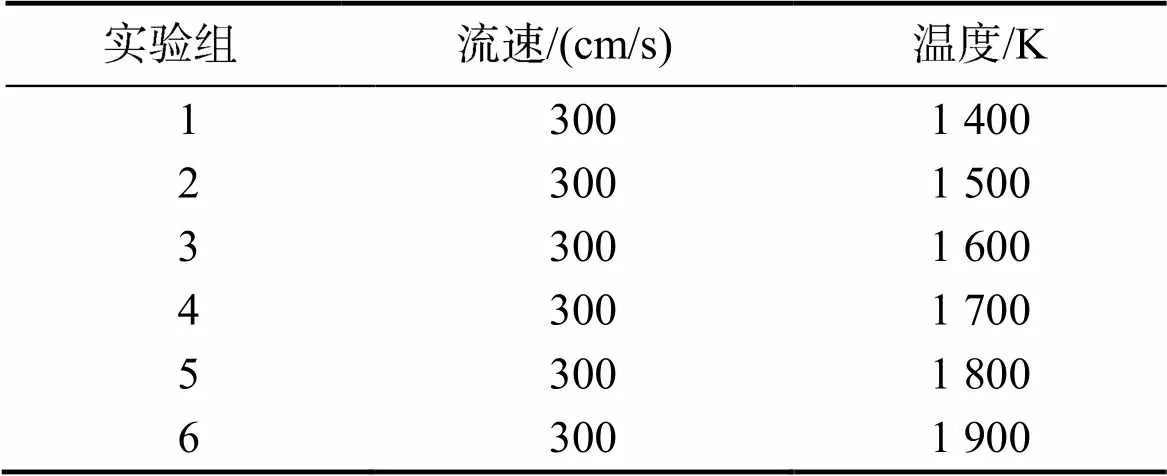
表5 动力学仿真:温度设置
模拟结果见图9。从模拟结果可见,氨气流速为300 cm/s时,在温度约为1 400 K以后开始有明显裂解行为出现;在1 500 ~ 1 800 K之间,氨气转化率随温度升高迅速升高,即在此温度区间内,氨气反应活性因温度升高而升高。当温度高于1 900 K后,氨气转化率达99%以上,即基本全部被裂解。由此也可看出,在该流速下,存在一个最佳温度范围使得氨气转化率在70%以上。在实际工况下,可以根据壁温进行流速的实时调整以满足掺混需求。

图9 不同温度下氨转化率
在实际工况下,需要根据掺混需求对氨气预裂解量进行调整,如参考文献[3,22]中提到,掺混氢气量不能过高也不能过低,当氢气在燃料气中含量约为30% ~ 40%时,其燃烧速度基本与小分子碳氢燃料相当,能够在旋流器下稳定燃烧。而当量比又是决定燃烧稳定性和污染物排放浓度的重要因素。稀薄燃烧作为燃气轮机潜在的减排燃烧方式之一,是未来的研究重点方向。
2.3 管路温度和流速共同影响
由2.1节和2.2节可知,氨气在盘管中的转化率与气体在管中停留时间和管路温度有关,温度越高、流速越慢,转化率越高。温度和流速对氨气转化率的影响结果见图10。

图10 不同流速下的氨气转化率
由图10可以看出,温度对氨气转化率的影响更加明显。流速虽然也对转化率产生影响,但影响幅度较小。温度从1 600 K升高至1 700 K后,氨气转化率约提高了40%;但流速从300 cm/s增加至400 cm/s后,氨气转化率下降不超过10%。并且,在流速较大条件下,1 500 ~ 1 800 K是氨气主要开始裂解及基本完全裂解的温度区间,该结果与参考文献[21]的结论基本一致。温度低于1 400 K时,无论何种流速,氨气基本未裂解或仅裂解了1%;高于1 800 K后各个流速下氨气转化率均高于85%。
图11展示了温度对氨气转化率的影响。当温度不超过1 500 K时,无论何种流速下氨气都没有明显裂解的现象;而当温度达到1 800 K及以上后,流速虽然会对转化率产生影响,但总体来看大部分氨都已经裂解。

图11 不同温度下的氨转化率
图11中,若火焰温度只能达到1 500 ~ 1 600 K,氨气最高转化率只能达到30%,若要使得掺混氢气量达到30%,需要将裂解旁路流量增加,即增加裂解旁路通入气体的比例。例如,若要达到掺混30%氢气的目的,在1 600 K温度条件下需要将约65%的氨气通入旁路进行裂解,余下的35%氨气通过燃料喷口直接通入燃烧即可。在富燃条件下,火焰温度较高,可达2 000 K以上,此时旁路氨气基本完全裂解,只需20%的氨气进入旁路裂解即可达到掺混需求。综上所述,在实验时需要根据当量比和掺混比例来动态调节预裂解氢气的通入量,贫燃时应使更多的氨气进入旁路裂解,而富燃时可降低该比例。
2.4 不同温度下的氨气热解反应路径分析
由2.3节可知,温度是影响氨气裂解的主要因素,本节主要在1 500 K和1 700 K下,对氨气裂解的反应路径进行分析,图12展示了具体的反应路径。图中可见,1 500 K时,氨气的裂解反应从脱氢开始,而脱氢反应主要由NH3与H反应生成NH2,即反应NH3+ H ⇋NH2+ H2(R3),随后NH2又与NH3结合再次脱氢生成N2H3,即反应NH3+ NH2⇋ N2H3+ H2(R4)。这两种反应通道对氨气裂解的贡献几乎相同。两个通道产物即NH2和N2H3接下来都进一步脱氢生成N2H2,但主要以N2H3通道为主。产生的N2H2一部分继续脱氢生成NNH,即反应N2H2+ H ⇋NNH + H2(R6),另一部分异构化生成H2NN。最终两个通道产物均分解生成N2,链终止。

图12 1 500 K和1 700 K温度下氨气裂解反应路径
由图12可知,在1 500 K和1 700 K两个不同温度下,氨气裂解路径基本一致,在反应前期各通道占比也几乎一致,而二者差别主要发生在N2H2产物的去向。在1 500 K时,两个通道几乎各占一半,即反应R6和反应H2NN ⇋ N2H2(R8),而当温度升高至1 700 K时,反应R8占比明显高于反应R6,即有更多的N2H2脱氢生成了NNH。反应R6相较于R8在温度升高时有更大的活性,因此生成了更多的NNH,在脱氢时,NNH相较于H2NN仅脱去一个H就可达到链终止,因此其反应阻力更小,这也是在1 700 K温度下氨气转化率更高的主要原因。
图13为1 700 K和1 500 K时氨裂解的敏感性分析,正值表示抑制,负值表示促进。可以看到,不同温度下影响氨裂解的反应种类大致相同,但对各个反应影响程度不同。在1 700 K时,反应NH3+ NH2⇋ N2H3+ H2(R4)对氨气裂解的促进效果最为明显,而在1 500 K时,反应N2H2+ H ⇋ N2H3(R11)对氨气裂解的促进效果更为明显。同时也可以看到,在1 700 K时,反应NH3(+M) ⇋ NH2+ H (+M)(R1)对氨气裂解的促进相较于1 500 K时更为重要,从图12也可以看出,虽然产率上该反应占比不大,仅为4%(1 700 K),但其对氨气裂解的促进作用明显。

3 结 论
基于微型燃气轮机燃烧室结构,设计了带有氨气预裂解功能的以氨为单一燃料的燃烧室。使用优化后的氨气反应动力学模型模拟了在不同温度和流速下氨气预裂解的效率,验证了增加预裂解旁路燃烧室可以稳定氨气火焰的可行性。对氨气裂解在不同温度下的反应路径和敏感性进行了分析,为下一步研究氨气火焰在不同当量比或其他工况下稳定燃烧及降低NO排放提供理论支持。主要结论如下:
(1)通过对已有微型燃气轮机燃烧室结构进行改进设计,加入带有旁路盘管的氨气预裂解通路,使部分氨气裂解为氢气和氮气,以达到仅使用单一氨燃料稳定燃烧的预期效果。
(2)使用Ansys Chemkin-Pro软件对旁通管路不同温度和流速下氨气预裂解效率进行模拟。在不同流速下,当温度达到1 500 K后,氨气开始有明显裂解行为出现;在1 500 ~ 1 800 K温度区间,氨气转化率随温度升高迅速升高。当温度高于1 800 K后,氨气转化率大于85%。温度是影响其转化率的主要因素,其影响幅度明显大于流速。
(3)温度的改变会影响氨气裂解的反应路径,主要表现在中间产物的产率大小。氨的裂解反应从脱氢开始,主要从两个反应路径进行,即NH3+ H ⇋ NH2+ H2(R3)和NH3+ NH2⇋ N2H3+ H2(R4)。1 700 K时,R4对氨气裂解的促进效果相较于1 500 K时更为明显。
[1] KOBAYASHI H, HAYAKAWA A, SOMARATHNE K D K A, et al. Science and technology of ammonia combustion[J]. Proceedings of the combustion institute, 2019, 37(1): 109-133. DOI: 1016/j.proci.2018.09.029.
[2] MORLANÉS N,KATIKANENI S P, PAGLIERI S N, et al. A technological roadmap to the ammonia energy economy: current state and missing technologies[J]. Chemical engineering journal, 2021, 408: 127310. DOI: 10.1016/j.cej.2020.127310.
[3] ELBAZ A M, WANG S X, GUIBERTI T F, et al. Review on the recent advances on ammonia combustion from the fundamentals to the applications[J]. Fuel communications, 2022, 10: 100053. DOI: 10.1016/j.jfueco.2022.100053.
[4] 刘镇剑. 旋流燃烧特性的数值计算与分析[D]. 北京: 清华大学, 2015.
[5] HAYAKAWA A, ARAKAWA Y, MIMOTO R, et al. Experimental investigation of stabilization and emission characteristics of ammonia/air premixed flames in a swirl combustor[J]. International journal of hydrogen energy, 2017, 42(19): 14010-14018. DOI: 10.1016/J.IJHYDENE. 2017.01.046.
[6] OKAFOR E C, SOMARATHNE K D K A, HAYAKAWA A, et al. Towards the development of an efficient low-NOammonia combustor for a micro gas turbine[J]. Proceedings of the combustion institute, 2019, 37(4): 4597-4606. DOI: 10.1016/J.PROCI.2018.07.083.
[7] 卫旭涛, 王金华, 张猛, 等. 氨气/甲烷旋流火焰结构及NO排放规律研究[J]. 工程热物理学报, 2022, 43(4): 1108-1115.
[8] VALERA-MEDINA A, GUTESA M, XIAO H, et al. Premixed ammonia/hydrogen swirl combustion under rich fuel conditions for gas turbines operation[J]. International journal of hydrogen energy, 2019, 44(16): 8615-8626. DOI: 10.1016/J.IJHYDENE.2019.02.041.
[9] STARKMAN E S, NEWHALL H K, SUTTON R, et al. Ammonia as a spark ignition engine fuel: theory and application[C]//1966 Automotive engineering congress and exposition. Berkeley: University of California, 1966. DOI: 10.4271/660155.
[10] VERKAMP F J, HARDIN M C, WILLIAMS J R. Ammonia combustion properties and performance in gas-turbine burners[J]. Symposium (international) on combustion, 1967, 11(1): 985-992. DOI: 10.1016/S0082-0784.
[11] KHATEEB A A, GUIBERTI T F, ZHU X R, et al. Stability limits and NO emissions of technically-premixed ammonia-hydrogen-nitrogen-air swirl flames[J]. International journal of hydrogen energy, 2020, 45(41): 22008-22018. DOI: 10.1016/j.ijhydene.2020.05.236.
[12] OKAFOR E C, SOMARATHNE K D K A, RATTHANAN R, et al. Control of NOand other emissions in micro gas turbine combustors fuelled with mixtures of methane and ammonia[J]. Combustion and flame, 2020, 211: 406-416. DOI: 10.1016/j.combustflame.2019.10.012.
[13] VALERA-MEDINA A, PUGH D G, MARSHA P, et al. Preliminary study on lean premixed combustion of ammonia-hydrogen for swirling gas turbine combustors[J]. International journal of hydrogen energy, 2017, 42(38): 24495-24503. DOI: 10.1016/j.ijhydene.2017.08.028.
[14] KONNOV A A. Implementation of the NCN pathway of prompt-NO formation in the detailed reaction mechanism[J]. Combustion and flame, 2009, 156(11): 2093-2105. DOI: 10.1016/j.combustflame.2009.03.016.
[15] DAVIDSON D F, KOHSE-HÖINGHAUS K, CHANG A Y, et al. A pyrolysis mechanism for ammonia[J]. International journal of chemical kinetics, 1990, 22(5): 513-535. DOI: 10.1002/KIN.550220508.
[16] GLARBORG P, MILLER J A, RUSCIC B, et al. Modeling nitrogen chemistry in combustion[J]. Progress in energy and combustion science, 2018, 67: 31-68. DOI: 10.1016/J.PECS.2018.01.002.
[17] SHRESTHA K P, SEIDEL L, ZEUCH T, et al. Detailed kinetic mechanism for the oxidation of ammonia including the formation and reduction of nitrogen oxides[J]. Energy & fuel, 2018, 32(10): 10202-10217. DOI: 10.1021/acs.energyfuels.8b01056.
[18] KLIPPENSTEIN S J, HARDING L B, GLARBORG P, et al. The role of NNH in NO formation and control[J], Combustion and flame, 2011, 158(4): 774-789. DOI: 10.1016/j.combustflame.2010.12.013.
[19] MEI B , ZHANG X , MA S ,et al.Experimental and kinetic modeling investigation on the laminar flame propagation of ammonia under oxygen enrichment and elevated pressure conditions[J]. Combustion and flame, 2019,210(Dec.): 236-246. DOI: 10.1016/j.combustflame.2019. 08.033.
[20] SHU B, VALLABHUNI S K, HE X,et al.A shock tube and modeling study on the autoignition properties of ammonia at intermediate temperatures ScienceDirect[J]. Proceedings of the combustion institute, 2019, 37(1): 205-211.DOI:10.1016/j.proci.2018.07.074.
[21] BENÉS M, POZO G, ABIÁN M, et al. Experimental study of the pyrolysis of NH3under flow reactor conditions[J]. Energy & fuels, 2021, 35(9): 7193-7200. DOI: 10.1021/acs.energyfuels.0c03387.
[22] ZHU X R, KHATEEB A A, GUIBERTI T F, et al. NO and OH* emission characteristics of very-lean to stoichiometric ammonia-hydrogen-air swirl flames[J]. Proceedings of the combustion institute, 2020, 38(4): 5155-5162. DOI: 10.1016/j.proci.2020.06.275.
Ammonia Fuel Pre-Pyrolyzer Design and Reaction Kinetic Analysis
LU Guang, WANG Junlei, LI Shilong, LIANG Xingyu, WANG Kun†
(State Key Laboratory of Engines, Tianjin University, Tianjin 300354, China)
Under the national background of carbon neutrality and the requirements for energy conservation and emission reduction, the use of ammonia as fuel in micro gas turbines is a popular direction for ammonia utilization. However, issues such as poor flame stability and NOemissions need to be addressed. In this study, a combustion chamber with fuel injection at the bottom and swirling flow was designed, and a bypass pipe was added to utilize the heat on the outer wall of the combustion chamber to partially pre-pyrolysis ammonia into hydrogen and nitrogen to enhance combustion. The effects of temperature and flow rate on the efficiency of bypass ammonia cracking were simulated by using Ansys Chemkin-Pro. The simulation results showed that when the temperature reached 1 500 K, there was significant cracking of ammonia. Within the temperature range of 1 500 ~ 1 800 K, the efficiency of ammonia cracking increased rapidly with increasing temperature. When the temperature exceeded 1 800 K, the efficiency of ammonia cracking exceeded 85%. Changes in flow rate also affect cracking efficiency, but the effect was significantly less than that of temperature. At the same time, the reaction pathways and sensitivity of ammonia cracking at different temperatures were analyzed. The results showed that the reaction pathway of ammonia cracking was influenced by temperature, and the reaction NH3+ NH2⇋N2H3+ H2was most sensitive to promoting ammonia cracking at 1 700 K. The conclusion verifies the theoretical feasibility of using partially pre-cracked ammonia to stabilize combustion and may provide theoretical support for further research on stable combustion and emission reduction of ammonia as a single fuel in micro gas turbines.
ammonia; micro gas turbines; combustion chamber; pre-pyrolysis
2095-560X(2023)04-0311-09
TK16
A
10.3969/j.issn.2095-560X.2023.04.003
2023-03-24
2023-04-10
国家自然科学基金项目(52176124)
王 昆,E-mail:kwang5@tju.edu.cn
路广, 王君雷, 李世龙, 等. 促进氨燃料转化的预裂解器反应动力学分析[J]. 新能源进展, 2023, 11(4): 311-319.
: LU Guang, WANG Junlei, LI Shilong, et al. Ammonia fuel pre-pyrolyzer design and reaction kinetic analysis[J]. Advances in new and renewable energy, 2023, 11(4): 311-319.
路 广(1998-),男,硕士研究生,主要从事零碳、可再生燃料与燃烧反应动力学研究。
王 昆(1982-),男,博士,教授,博士生导师,主要从事新能源转化与高效利用、发动机燃烧与排放、高能量密度燃料与含能材料、动力电池设计与优化等研究。

