超导材料YBCO的制备及其催化降解有机污染物性能的研究
张立东,郝文明,张洪丽,范雅琪
(1.青岛科技大学 山东化工研究院,山东 济南 250014;2.舜合科技(山东)有限公司,山东 济南 250014;3.山东师范大学 化学化工与材料科学学院,山东 济南 250014)
化工染料是造成环境污染的主要污染物之一,工业上每年生产超过10万种有机染料,总产量超过7×105t,这些染料毒性很高,因此它们的降解受到很多关注[1-3]。虽然传统的物理技术,例如活性炭上的吸附和化学试剂的凝聚通常是有一定效果,但它们只是将有机化合物从水相转移到另一相,易造成二次污染。现代染料所含有机化合物具有稳定性,使生物处理对其脱色降解难有成效,很难在自然界中自然降解[4-5]。当这些有机染料进入水循环系统时,可能对环境和人类健康构成潜在危害。因此,开发有效的技术来降解废水中的有机染料已被认为是实现可持续的重要任务。因为高效、简单、可再生性好、易于处理,高级氧化工艺(AOPs)在降解有机染料方面表现出良好的前景[6-8]。在各种AOP中,可见光诱导的非均相Fenton样光催化过程被认为是将一系列有机染料降解为易降解化合物的有效方法[6-7,9-11]。在此过程中,高活性的羟基自由基(·OH)对降解起着关键作用[12],其降解是通过铁离子(如Fe2+、Fe3+)激发H2O2产生羟基自由基(·OH),能够快速且非选择性地氧化多种污染物[13-14]。可见,·OH的浓度及产生速率,对污染物的降解速率有很大影响。因此,促进H2O2的分解,将有助于污染物降解效率的提高。
除了上述Fenton反应中Fe2+能够促进H2O2的分解,MnO2也是典型的分解H2O2的催化剂,在H2O2存在时,不需要光照,便能迅速将H2O2分解成羟基自由基(·OH),故具有降解亚甲基蓝的性能[14],而超导材料YBCO同样可以在室温下无需光照催化分解H2O2[15]。亚甲基蓝(MB)是一种常见的染料,特别耐生物降解[16]。尽管已有大量有关TiO2光催化剂光催化MB降解的报道,但大多数研究都是在紫外光照射下进行的[17-18]。最近,Zhao等人报道,在可见光照射下,一些染料可通过自感光过程TiO2上发生降解,但亚甲基蓝不包括在内[18]。到目前为止,只有少数研究报道了在可见光照射下成功降解亚甲基蓝染料[18-19]。此外,催化效率受到TiO2基光催化剂光吸收特性的限制。因此选用YBCO作为降解亚甲基蓝的催化剂,在H2O2存在的条件下,探究其催化性能。
1 实验所用试剂及仪器设备
1.1 实验所用原料及试剂
碳酸钡,分析纯,上海麦克林生化科技有限公司;氧化钇,分析纯,上海麦克林生化科技有限公司;纳米氧化铜,75~150 μm(100~200目),上海麦克林生化科技有限公司;亚甲基蓝(MB),分析纯,国药集团化学试剂有限公司;30%过氧化氢,分析纯,国药集团化学试剂有限公司;二次去离子水,杭州娃哈哈集团有限公司。
1.2 实验所用的仪器设备
恒温磁力搅拌器,90-2型,上海巨荣生化仪器厂;高速离心机,Sigam 3K15,Sigma;低速离心机,TDL-40B,上海飞鸽;超声清洗仪,KQ3200B,昆山市超声仪器有限公司;电子分析天平,CP64,美国OHAUS;高温管式炉,OTF-1500X,郑州科晶电炉有限公司;X射线粉末衍射仪,Bruker D8,Bruker;扫描电子显微镜,SU8010,日本日立;高分辨透射电子显微镜,JEM-2010,日本日立;紫外可见分光光度计,TU-1900,北京普析通用仪器;X射线光电子能谱仪,ESCALAB 250,ThermoFisher SCIENTIFIC。
2 催化剂的制备
目前最常用的合成YBCO超导体等固态物质的制备方法主要分为三大类:固态烧结法、溶液合成法和熔化法。固态烧结法通常是将氧化物和碳酸盐等原料,直接研磨混合进行烧结,操作较为简单,能够大量合成,基本满足普通的实验需求,故是目前较为广泛运用的一种典型合成方法。溶液合成法以柠檬酸盐合成法和溶胶-凝胶法为例,柠檬酸盐法是以相应硝酸盐与过量柠檬酸盐混合溶解,水热合成后再进行煅烧处理。该法制备的样品,纯度较高,且煅烧时的温度相对较低,可制备出形貌较好的粒子。溶胶-凝胶法可以产生高反应性的均匀粉末,操作技术简单,且具有高度均匀混合、良好的化学计量控制以及在较低温度下和相对较短的处理时间内即可生产活性亚微米尺寸的颗粒等优点。熔融法对温度和设备的要求较高,操作复杂,在实验室操作中,相对前两种方法较为不常用。本实验中采用反复烧结的固态烧结法制备催化剂超导材料YBCO,化学反应方程式为:
Y2O3+ BaCO3+ CuO → YBa2Cu3O7-δ+CO2↑
称取0.20 g氧化钇(Y2O3,99.99%)、0.40 g纳米氧化铜(CuO,75~150 μm(100~200目),99.5%)于玛瑙研钵中,手动研磨30 min,使其混合均匀。再加入0.69 g碳酸钡(BaCO3,99.95%),继续手动研磨30 min,使混合均匀。然后将混合后的样品装入坩埚中,高温管式炉空气氛围下980 ℃煅烧24 h,升温速率5 ℃/min。自然冷却至室温后,将样品取出,重新研磨至混合均匀,再将研磨好的样品放入高温管式炉中,空气氛围下980 ℃煅烧24 h,升温速率5 ℃/min。自然冷却至室温后,收集备用。
3 结果与讨论
3.1 催化剂的表征
3.1.1 X射线粉末衍射(XRD)
为了确定催化剂的组成,对催化剂进行了X射线粉末衍射表征,所得结果如图1所示。X射线粉末衍射,是通过对比样品衍射峰与标准衍射卡片的位置和强度关系,确定样品晶相,并对样品进行定性相分析的一种方法。本实验采用的测试仪器为德国Bruker D8型X射线粉末衍射仪。通过与标准卡片比对,实验所制备的YBCO材料与标准卡片中YBa2Cu3O6.8的特征峰(PDF 39-0487)相对应,表明已成功制备出了所需要的超导材料。

图1 超导材料YBCO的XRD图
3.1.2 扫描电镜表征(SEM)
为研究超导材料YBCO表面状态,对其进行了扫描电镜表征,如图2所示,图中为倍率依次进行放大的YBCO扫描电镜图像。可以看出,材料形貌为聚集态不规则大颗粒,材料表面呈现出一种不规则的片状结构,分布较为均匀。进一步对材料表面的元素分布情况进行EDS mapping测试,如图2(b)所示,Y、Ba、Cu、O四种元素在材料表面分布范围一致,呈现为均匀分布状态。进一步证明合成的样品是YBCO。

图2 超导材料YBCO的SEM图及EDS-mapping图
3.1.3 EDS能谱表征
为确定材料中四种元素的含量,对材料做了EDS能谱表征分析,如图3所示。
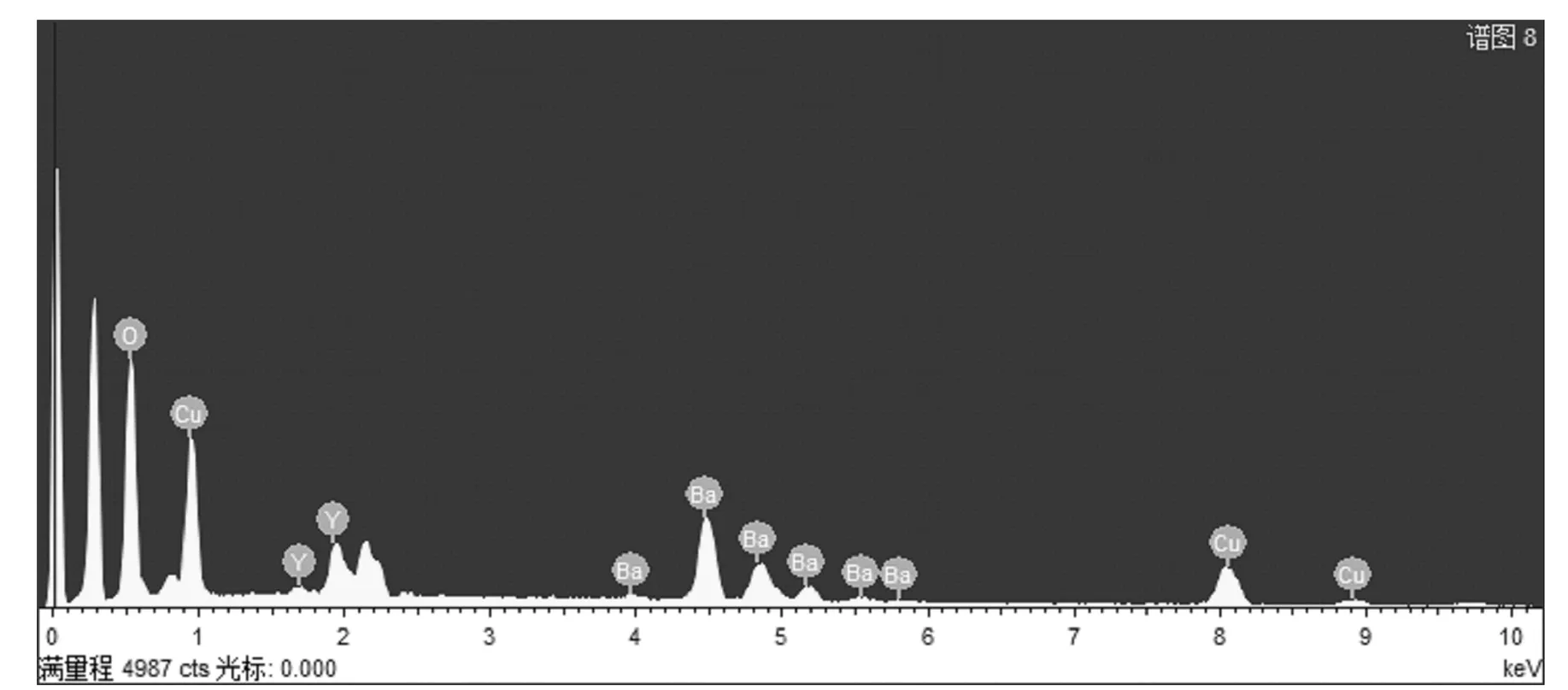
图3 超导材料YBCO的EDS能谱图
由图3发现了Y、Ba、Cu、O四种元素的元素峰,并且通过质量比计算得到,Y、Ba、Cu、O四种元素的物质的量比为1∶1.9∶3.3∶12,数值基本与目标材料YBa2Cu3O6.8中元素物质的量比相一致。证明确实成功合成了超导材料YBCO。
3.1.4 透射电镜表征(TEM)
在扫描电镜结果图中,YBCO材料呈现片状堆积结构。透射电镜测得尺寸更小的样品颗粒,如图4(a)所示,样品呈现片状堆积结构,与扫描电镜结果一致。又对材料进行了高分辨透射电镜测试,结果如图4(b)所示,样品的晶格条纹间距为0.247 nm,与YBCO的XRD标准卡片(PDF#39-0486)中(1 1 2)晶面的晶格条纹间距相对应,与XRD谱图的衍射峰对应一致,表明本研究成功合成了YBCO材料。

图4 超导材料YBCO的TEM及HRTEM图像
3.2 超导材料YBCO催化降解有机污染物性能测试
3.2.1 催化降解有机污染物性能测试
选用亚甲基蓝作为有机污染物,进行降解性能测试。室温下,配制10 mg/L的亚甲基蓝溶液,搅拌均匀,加入一定量的催化剂,避光条件下搅拌30 min,使催化剂达到吸附平衡。再加入一定量H2O2溶液(30%),每隔30 min取一次样,高速离心后取上清液,使用紫外可见分光光度计测其吸光度,根据吸光度的变化分析材料降解性能。典型样品重复上述步骤,循环进行测试。全部反应均在避光条件下进行。
3.2.2 结果与讨论
3.2.2.1 催化剂用量对降解能力的影响
配制10 mg/L 的亚甲基蓝溶液500 mL,取7个100 mL烧杯,编号1~7,分别加入50 mL已配制好的亚甲基蓝溶液。在7个烧杯中,按编号顺序由小到大分别加入一定量催化剂,使催化剂质量浓度分别为0.2,0.4,0.6,0.8,1.0,1.2 g/L,最后在7号烧杯中不加入催化剂作为空白对照。避光搅拌30 min,使催化剂达到吸附平衡。再加入2.5 mL H2O2水溶液(30%),每隔30 min取样,测其吸光度。
实验结果如图5所示。从图5(a)中可以看到,不加入催化剂仅是加入H2O2水溶液时,亚甲基蓝依然会被降解,因为H2O2自身便会分解产生羟基自由基(·OH),但其降解率较低,仅能降解至80%左右。加入催化剂后,催化剂YBCO迅速将H2O2分解为具有高活性的·OH,在180 min内,基本可将亚甲基蓝降解至20%以下,表明催化剂YBCO具有较好的降解能力,且其降解速率与时间呈现良好的线性关系,如图5(b)所示。当催化剂质量浓度为0.4 g/L时,其催化效果最好。
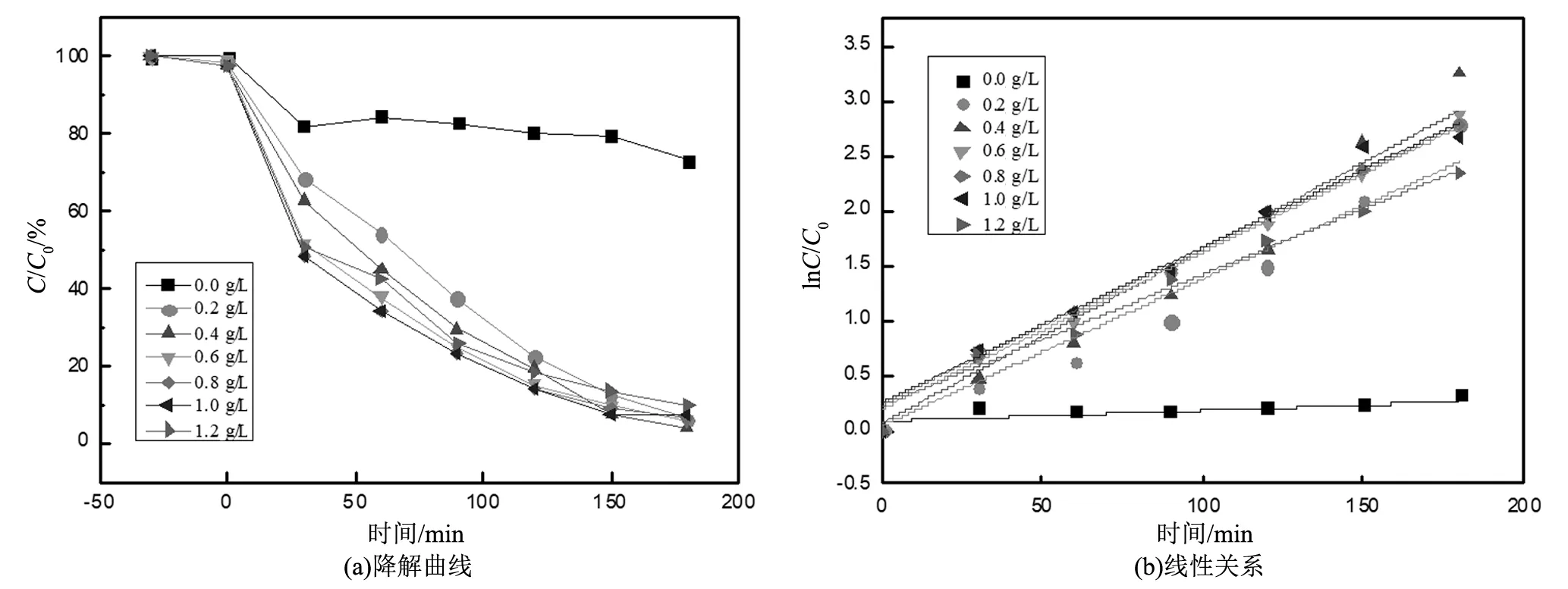
图5 不同催化剂浓度下降解曲线及线性关系图
3.2.2.2 H2O2水溶液(30%)对降解能力的影响
配制10 mg/L的亚甲基蓝溶液500 mL,取5个100 mL烧杯,分别加入50 mL亚甲基蓝溶液。各加入0.4 g/L催化剂,避光搅拌30 min,分别加入1.0,2.0,2.5,3.0 mL H2O2水溶液(30%),5号烧杯不加H2O2水溶液作为空白对照。每隔30 min取样,测其吸光度。
结果如图6所示,不加H2O2水溶液只加催化剂时,不能降解亚甲基蓝。当加入H2O2水溶液(30%)后,催化剂均可在180 min内将亚甲基蓝溶液降解至20%以下,且呈现良好的线性关系,如图6(b)所示。从图6(a)中发现当H2O2水溶液(30%)含量为2.5 mL时,其催化效果最好。

图6 不同H2O2水溶液(30%)含量降解曲线及线性关系图
3.2.2.3 光照对降解能力的影响
因为H2O2水溶液在受热或光照下自身即可缓慢分解,为了研究光照对降解反应是否产生影响,在亚甲基蓝质量浓度10 mg/L、催化剂质量浓度0.4 g/L、H2O2水溶液(30%)含量2.5 mL条件下,仅改变光照因素,对比了催化剂的催化能力,如图7所示。从图中可以看到,光照对催化剂降解能力的影响不大,相比之下,避光条件降解能力更强一些,这可能是由于在强光照射下,H2O2水溶液发生了缓慢分解的缘故。

图7 光照下和避光条件下降解曲线及线性关系图
3.2.2.4 催化剂寿命测试
在亚甲基蓝质量浓度10 mg/L、催化剂质量浓度0.4 g/L、H2O2水溶液(30%)含量2.5 mL、避光条件下,对催化剂寿命进行了测试,如图8所示。从图8(a)中可以看出,经过六次循环测试后,催化剂仍具有较好的催化性能,并且从图中看到,催化速率随着循环次数的增加也有所升高。这可能是由于经过长时间的催化降解,催化剂颗粒相对变小,分散更均匀的缘故。从图8(b)中也可以看出,每次催化剂的降解度均能达到20%以下,证明所制备的催化剂具有较好的稳定性。

图8 催化剂寿命测试
4 总结
通过固态烧结法成功制备了催化剂超导材料YBCO,并成功利用其分解H2O2将其用于催化降解亚甲基蓝。研究发现,当亚甲基蓝质量浓度是10 mg/L时,催化剂质量浓度为0.4 g/L,H2O2水溶液(30%)加入量为2.5 mL时获得了最优的催化效果。催化剂浓度较低或H2O2加入量不足,会导致产生的·OH不足,而催化剂浓度过高或H2O2过量会则产生过量的·OH,两者均会影响降解能力,使降解能力降低。且催化剂寿命试验,六次循环后依然具有较好的催化降解能力。本实验首次将超导材料引入催化降解领域,为降解废水中的有机污染物催化剂的选择提供了一个新的思路。

