1 株猪4 型细小病毒的分子鉴定与全基因组分析
尹 苗,扶星星,董鹏宇,王 聪,陈俊巧,陈希文
( 1. 四川百诺吉科技有限公司,四川 绵阳 621000 ;2. 四川生猪重大疫病监测与防控工程研究中心,四川 绵阳 621000 )
猪细小病毒(PPV)是引起猪繁殖障碍的常见病毒之一,目前包括猪细小病毒1 型~7 型(PPV1~PPV7)。1965年,德国科学家在细胞污染物中首先分离到PPV1,该病毒主要引起猪不育、胚胎和胎儿死亡、木乃伊化胎儿和死产等[1],造成猪的繁殖障碍,影响猪群健康以及猪的生产性能。之后PPV2~PPV7 也陆续被发现并报道[2-4],给猪群健康及养猪业发展造成了严重威胁[5-8]。PPV4属细小病毒科、细小病毒亚科、博卡病毒属[9],是美国科学家于2009年在2005年暴发圆环病毒2型(PCV2)的病死猪病料中检测到的新病毒[10]。2012 年,黄律等[11]首次在我国发现了PPV4。PPV4 具有快速感染性,对猪肺脏以及肠道器官组织的嗜性最强,主要引起猪呼吸道疾病和繁殖障碍等,严重影响猪群的生产性能和经济效益[9]。我国目前在PPV4方面的研究报道不多,本研究通过采集发病猪场的猪肺脏、淋巴结、血液等病料,经PCR扩增和全基因组测序成功鉴定到1株新型PPV4,综合运用生物信息学软件对分离株进行遗传变异和全基因组分析,为丰富我国PPV4 基因数据并为其遗传变异、疫苗研究、疫病防控等提供参考。
1 材料与方法
1.1 病料来源
病料为四川地区某发病猪场有呼吸道症状和繁殖障碍症状的猪肺脏、淋巴结、血液等,由四川生猪重大疫病监测与防控工程研究中心保存。
1.2 试剂与仪器
FineMag 快速磁珠法病毒DNA/RNA 提取试剂盒(济凡生物科技(北京)有限公司);琼脂糖(上海必德生物技术有限公司);2×Taq PCR 预混试剂Ⅱ、ddH2O、DL 2000 DNA Marker(天根生化科技(北京)有限公司);GoldView I型核酸染色剂(北京索莱宝科技有限公司)。T100 PCR仪、凝胶成像仪(美国Bio-logic公司);EL204-IC电子分析天平(梅特勒-托利多仪器(上海)有限公司)。
1.3 生物信息学软件
运用Primer Premier 5软件进行引物设计,对比选择条件适合的引物,将设计好的引物使用Primer-BLAST 工具进行引物特异性检查(网址为https://www.ncbi.nlm.nih.gov/tools/primer-blast/);应用DNAMAN 软件进行测序结果拼接。应用ORFfinder工具对全基因进行开放阅读框的预测(网址:https://www.ncbi.nlm.nih.gov/orffinder/);应用DNAMAN 软件进行DNA 多序列比对以及氨基酸对比分析;使用MEGA-X软件构建系统发育树。
1.4 引物设计
根据相关报道[12]合成特异性检测引物(PPV4-F:5'-TGATGAACATTGGCAGGGCA-3'、PPV4-R:5'-ATGGACCTGTGTAGCGATGA-3',目的片段大小180 bp。根据GenBank公布的PPV4全基因序列合成全基因分段扩增引物,送至宝生物工程(大连)有限公司合成。PPV4 全基因分段扩增引物信息见表1。

表1 PPV4全基因分段扩增引物信息Tab.1 Primers imformation for PPV4 whole gene segmentation amplification
1.5 核酸提取
使用FineMag快速磁珠法病毒DNA/RNA提取试剂盒提取样品核酸,-80 ℃冰箱保存。
1.6 PCR扩增与测序
PPV4 PCR 扩增体系(25μL):2×Taq PCR Master Mix 12.5 μL、10 μmol/L 的上下游引物各1 μL、ddH2O 8.5 μL、DNA 模板2 μL。PCR反应程序:94 ℃预变性5 min;94 ℃变性30 s,57 ℃退火30 s,72 ℃延伸30 s,共35 个循环;72 ℃延伸7 min。反应程序:95 ℃预变性5 min,95 ℃变性30 s,57 ℃退火30 s,72 ℃延伸1 min。
取5 μL PCR 产物进行1.5%琼脂糖凝胶电泳,将符合预期目的条带的PCR产物送华大基因进行测序。
1.7 序列拼接与全基因组分析
将测序结果进行BLAST比对,应用DNAMAN软件中Sequence-Sequence Assembly 工具进行PPV4 全基因分段扩增测序结果拼接。运用ORFfinder、DNAMAN、MEGAX等生物信息学软件进行全基因分析。
2 结果与分析
2.1 PPV4的分子鉴定结果(图1)

图1 PPV4鉴定结果Fig.1 PPV4 identification results
由图1可知,提取的DNA用检测引物进行PCR扩增和电泳,在约180 bp处出现了目的条带,与预期大小一致。
2.2 PPV4的全基因组扩增结果(见图2)
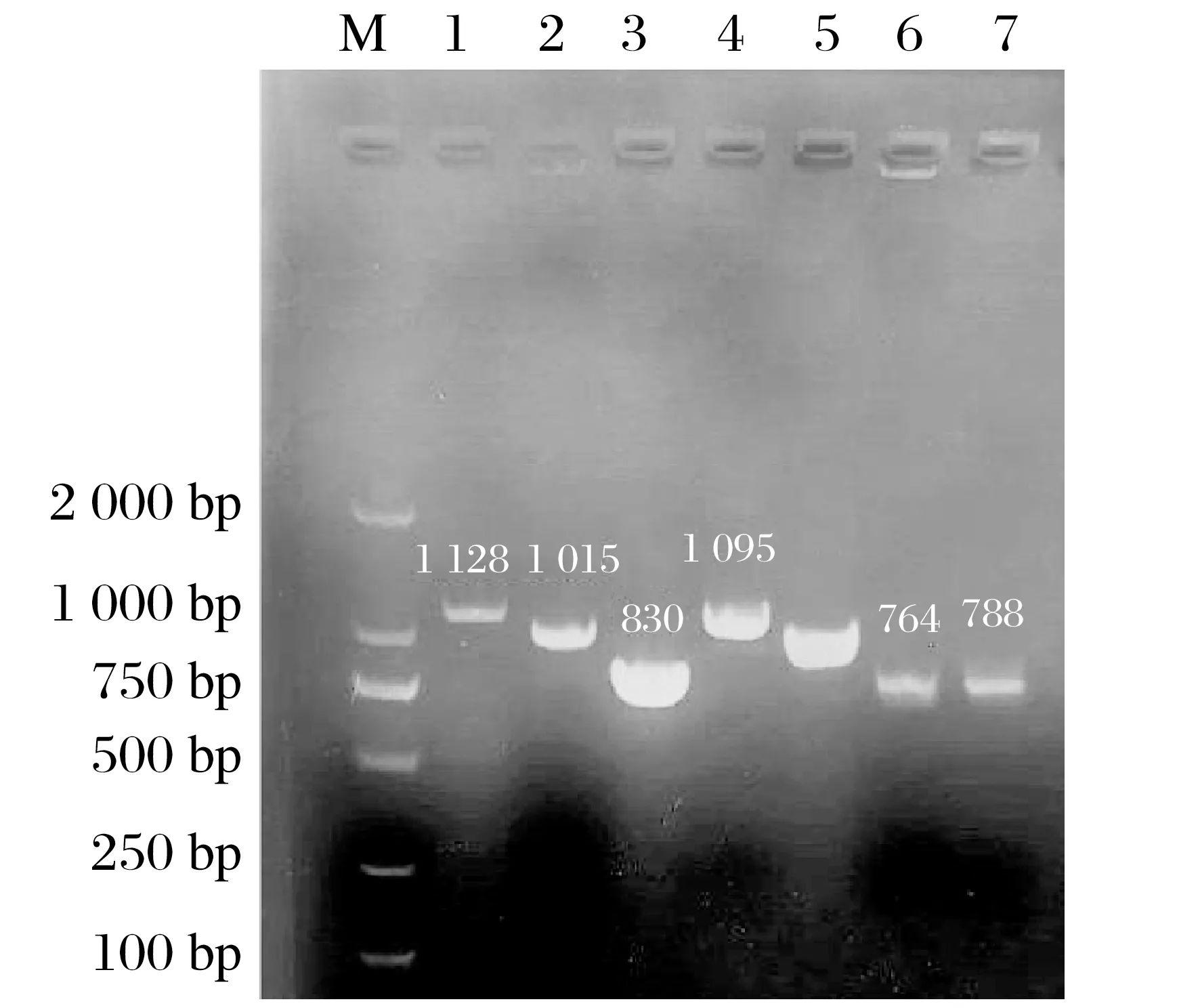
图2 PPV4全基因分段扩增结果Fig.2 Results of whole gene segment amplification of PPV4
由图2 可知,将提取的DNA 用全基因扩增引物进行PCR扩增和电泳,分别在1 128、1 015、830、1 095、983、764和788 bp位置出现目的条带,与预期条带大小相符。
2.3 PPV4-MY全基因组分析结果
选取其中1株PPV4阳性样品(命名为PPV4-MY),使用DNAMAN将PPV4-MY株与本地参考序列进行多序列比对,全基因核苷酸一致性为98.8%~99.2%,与2017 年山东的SDWF20170530-68 毒株(MZ577035.1)一致性最高,与2006 年美国PPV4(NC_014665.1)一致性最低,结果见图3~图5。
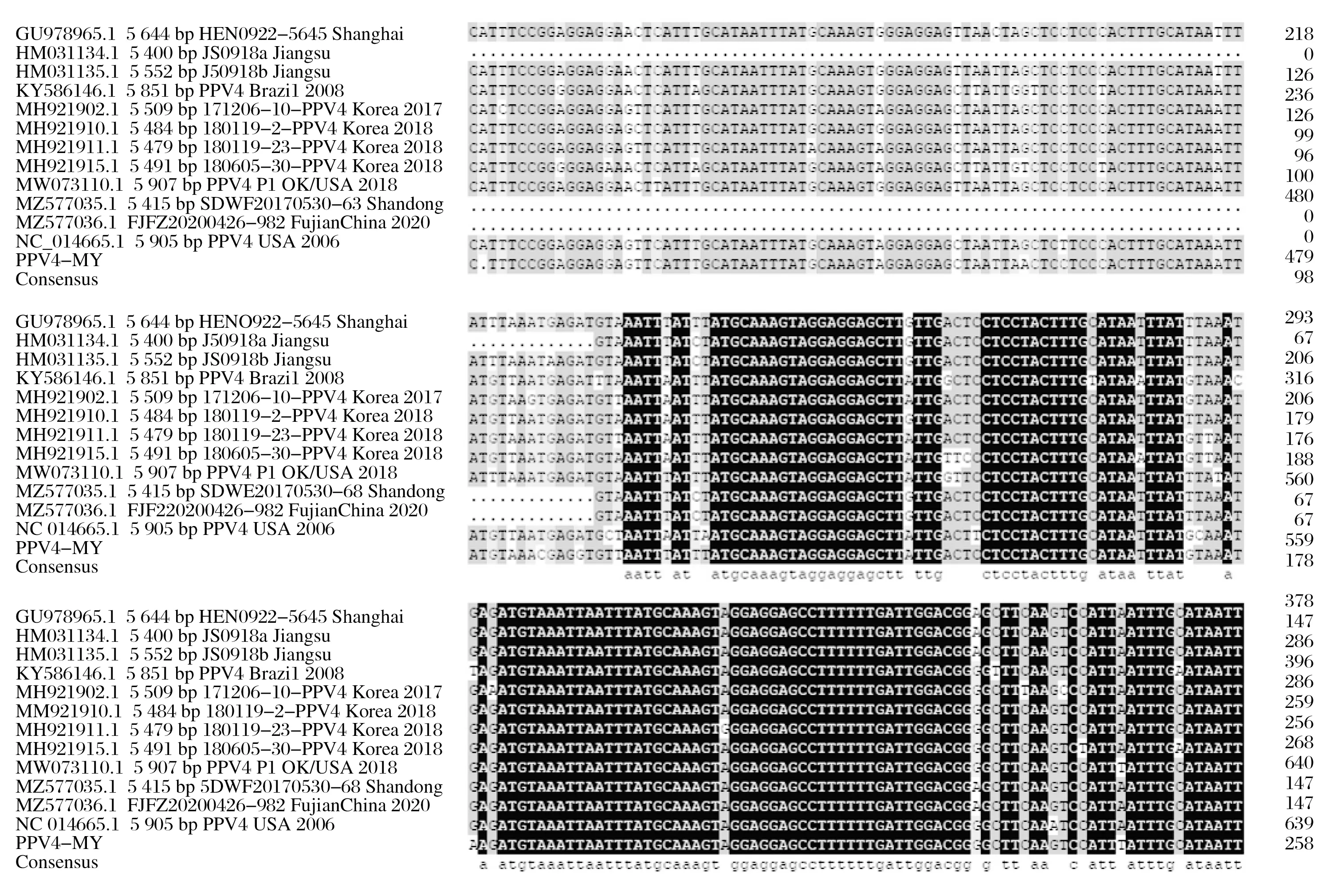
图3 PPV4全基因多序列比对前端Fig.3 PPV4 whole gene multiple sequence alignment front-end

图5 PPV4全基因多序列比对后端Fig.5 Back end of PPV4 whole gene multiple sequence alignment
由图3~图5 可知,PPV4 全基因开始与末端各序列间具有较大差异,在全基因中间各序列差异较小,序列一致性高。2006 年美国PPV4(NC_014665.1)与2018 年PPV4 P1 OK/USA分离株(MW073110.1)比其他本地参考序列前端多出250~490 bp,比PPV4-MY 前端多出380 bp;在PPV4 多序列比对末端,PPV4-MY 与2008 年巴西(KY586146.1)检出的PPV4比其他本地序列长约200 bp。
对PPV4-MY 与其他本地PPV4 全基因构建系统发育树(Neighbor-Joining建树),见图6。
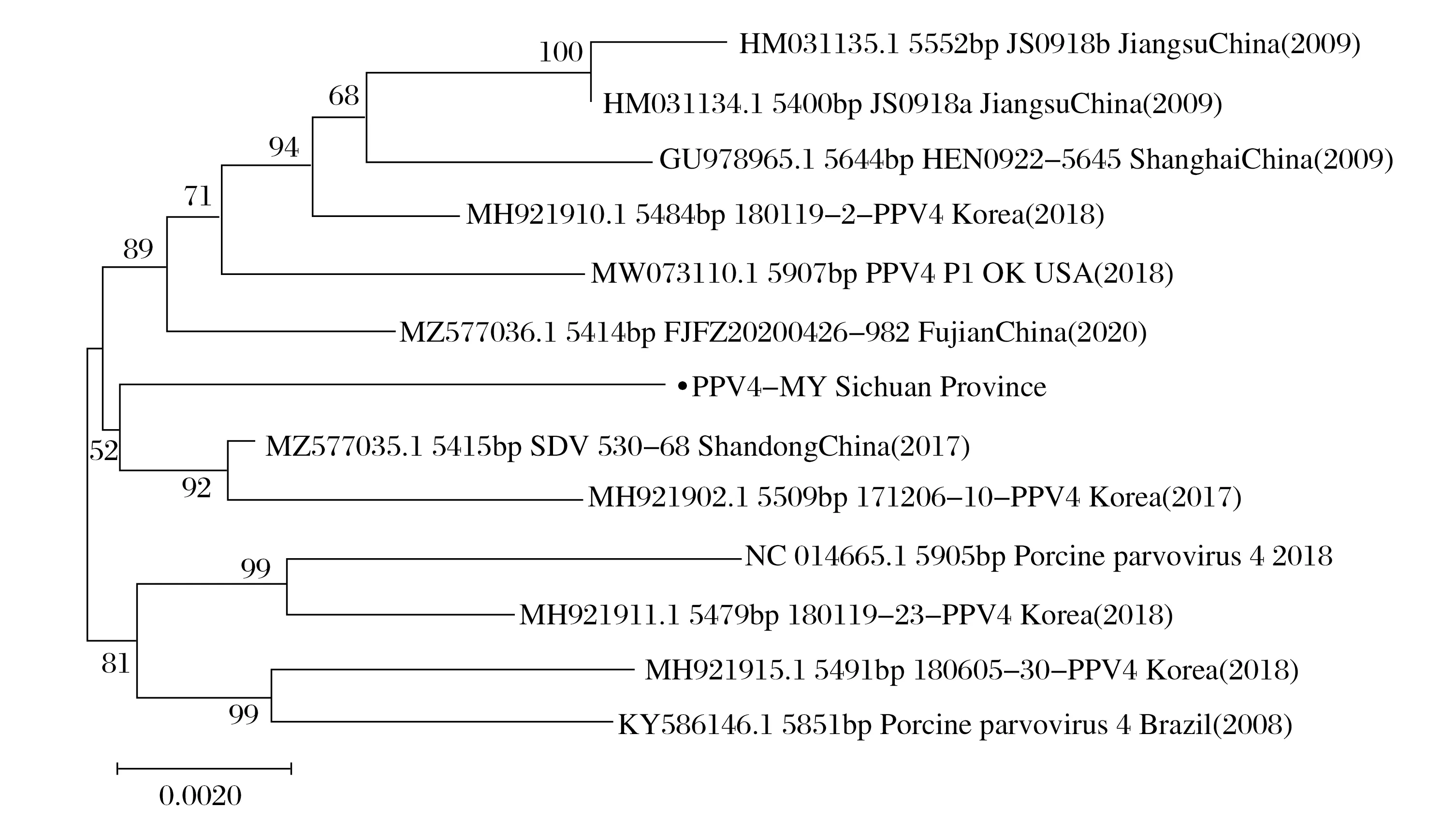
图6 PPV4-MY全基因建树Fig.6 PPV4-MY whole gene establishment
由图6 可知,PPV4-MY 与2017 年国内发现的山东SDWF20170530-68 毒株(MZ577035.1)、2017 年韩国171206-10-PPV4 毒株(MH921902.1)处于同一小分支,亲缘性较近,共同特征较多。与江苏(HM031134.1、HM031135.1)、巴西(KY586146.1)、韩国另外3 株毒株(MH921910.1、MH921911.1、MH921915.1)亲缘性较远。
3 讨论
PPV 会引起猪的繁殖障碍,降低仔猪的出生率,特别是新型PPV发现以来。虽然目前有疫苗可对PPV1进行防控,但PPV2~PPV7尚无有效疫苗。因此,为防控猪细小病毒病应从源头控制,定期检测PPV抗体,严格防控传染病,提高猪群质量,减少经济损失。PPV4感染范围广,传播途径多,具有很强的组织嗜性,尤其是肠道,严重影响猪的生长性能。自2012年PPV4在我国首次发现起,各地相继出现疫情相关报道。2012 年,黄律等[9]对我国部分地区2006—2011 年的样品开展流行病学调查,总阳性率为14.07%;2023年,李吉祥[12]研究了我国PPV1~PPV7流行演化,指出其实早在1996 年我国猪群已存在PPV4 的感染。2020 年,张鑫杰等[13]在福建省进行PPV4 的分子流行病学调查,PPV4 阳性率为9.09%。2021 年,Li 等[14]对2016—2020年部分地区样品进行调查,PPV4检出率为4.37%。
本研究对测序拼接的PPV4 全基因进行序列分析,发现PPV4-MY全基因前端和后端与其他本地序列具有较大差异,中间差异很小。美国毒株普遍比其他地区毒株前端多250~490 bp 左右,而PPV4-MY 与巴西毒株的后端比其他全基因序列长,提示了PPV4 可能在适应宿主或传播时发生了一定的变异,使前端或后端部分基因发生了缺失;也可能是由于当初技术不成熟,导致PPV4 测出的全基因比实际的短。此前有研究发现,PPV4 基因组结构为首尾相连环状结构,并且此结构对PPV4 持久宿主感染可能具有一定作用[15]。夏娜等[16]报道称,PPV 感染过程中,其非结构蛋白可与自噬相关蛋白、RAB2A 互作。这种缺失曾在腺病毒(AAV)中发现,并且不影响其感染性[17-18]。但目前关于PPV4 的缺失无相关研究,提示还需要进一步研究PPV4 的全基因长度以及发现相应缺失增添对PPV4 的表达等有无相应影响。对PPV4-MY构建系统发育树分析发现,其与2017 年国内发现的山东SDWF20170530-68 毒株、2017 年韩国171206-10-PPV4 毒株亲缘性近,在同一分支,共同特征较多。
综上所述,本研究从发病猪场病料中成功鉴定到1 株新型PPV4(PPV4-MY),运用生物信息学软件对PPV4-MY 进行遗传变异和全基因组分析,系统进化树构建结果表明其与2017 年山东株(SDWF20170530-68)、2017 年韩国株(171206-10-PPV4)亲缘关系最近。本研究结果丰富了我国PPV4的基因数据,为PPV4的遗传变异、疫苗研究、疫病防控等提供了理论依据。
4 结论
本研究结果显示,PPV4-MY 全基因组存在一定程度的突变,全基因组前端和末端各序列存在较大差异,中段序列基本一致,差异较小;系统发育树分析发现,分离株PPV4-MY与山东、韩国检出的毒株亲缘性最近。

