毛囊微型化发生的机制与最新研究进展
李 潇,雷铁池
武汉大学人民医院皮肤科,湖北 武汉 430060
雄激素性脱发(androgenetic alopecia,AGA)是临床上最常见的脱发类型,通常起病于青春期。近年来该病有年轻化趋势,越来越多的儿童被发现患有AGA[1-2]。在AGA 发生发展过程中,携带AGA 易感基因的成年人雄激素敏感区(如男性前额和头顶、女性头顶部位)的毛囊在局部高浓度双氢睾酮(dihydrotestosterone,DHT)的刺激下,逐渐完成了终毛(毛干直径≥0.03 mm)向毳毛(毛干直径<0.03 mm)的转换,这一过程称为毛囊微型化,目前通过皮肤镜确诊。毛囊干细胞(hair follicle stem cell,HFSC)[3-4]和真皮乳头 细胞(dermal papilla cell,DPC)[5-6]作为毛囊中最重要的两种细胞参与了毛囊周期循环。真皮乳头位于毛囊的基底部,在毛发周期性更新过程中提供指令性信号,启动毛囊再生,真皮乳头主要由DPC构成,它的数量多少决定着毛发直径和毛囊的周期循环,当DPC数量低于某一个阈值时,毛囊将不会进入生长期[7]。HFSC位于毛囊外毛根鞘的隆突区,被认为是具有多谱系分化潜力和强大增殖能力的慢循环细胞[8]。本文具体阐述毛囊微型化发生的相关机制,并简要综述最新发现的可逆转毛囊微型化的相关治疗手段。
1 DPC分泌毛囊抑制因子
毛囊DPC 通过WNT(wingless-type MMTV integration site family)蛋白、骨形态发生蛋白(bone morphogenetic protein,BMP)、音猬因子(sonic hedgehog,SHH)、分泌型卷曲相关蛋白1(secreted frizzled related protein-1,sFRP1)等途径来调节隆突区HFSC 的活化、增殖与分化,进一步启动毛囊下一个循环周期的发生[4,9-10]。AGA 患者通过分泌DHT 来抑制或促进毛发生长因子调控毛囊周期、影响毛发直径从而促使小型化的发生(表1)[11-15]。Ceruti 等[16]分析了雄激素对人毛囊DPC增殖影响后发现,DHT可显著下调DPC 球状体中BMP2 和BMP4 的分子表达,并影响HFSC向毛囊祖细胞的分化,但当添加BMP2后真皮乳头恢复了毛发诱导因子碱性磷酸酶(alkaline phosphatase,ALP)活性及HFSC 向祖细胞的分化。Wnt/β-连环蛋白信号是维持毛囊正常发育的一个重要通路,与DPC 的聚集功能紧密相关[17]。Shin 等[18]发现多花虎杖提取物下调了退行蛋白Dickkopf相关蛋白1(Dikkopf-related protein 1,DKK1)的表达来激活DPC并延长毛囊生长期。Premanand等[19]向毛发生长初期的小鼠皮下注射人重组DKK1(rhDKK1)后导致小鼠毛发生长中期提前出现,而中和性DKK1 抗体延缓了小鼠毛发向生长中期转换的进展。DKK1 作为Wnt 蛋白的抑制剂,可诱导β-连环蛋白在细胞内的累积,并抑制毛囊周期迅速完成生长期向退行期的转换[20]。除此之外,miRNA-181a-5p[21]、miR-195-5p[22]、人参提取物[23]、香草酸[24]通过抑制Wnt/β-连环蛋白信号来促进毛囊的生长发育,从而逆转毛囊微型化。这些研究说明或许恢复Wnt/β-连环蛋白这一信号通路即可恢复毛囊周期的正常转换。

表1 人/鼠毛囊DPC来源的毛发调节因子Table 1 Hair factors derived from DPC in human/mouse hair follicles
2 DPC凋亡与自噬
DPC 数量多少决定毛囊的大小。许多证据显示DHT 诱导DPC 发生凋亡促使了毛囊微型化的发生。Inui 等[38]研究表明DHT 刺激DPC 表面的转化生长因子β(transforming growth factor β,TGF-β)表达增加并进一步以自分泌和旁分泌的方式诱导DPC 凋亡,抑制毛囊上皮细胞生长,从而导致毛囊逐渐变小、毛发变细。Winiarska等[39]对比用DHT刺激健康志愿者和AGA患者的DPC后发现,DHT以剂量依赖和时间依赖的方式诱导DPC 凋亡,通过诱导含半胱氨酸的天冬氨酸蛋白水解酶8(cysteine aspartate specific proteinase 8,Caspase-8)的裂解,降低了B 细胞淋巴瘤/白血病-2(B-cell lymphoma-2,BCL2)蛋白的表达,这进一步说明DHT 可增加凋亡蛋白的表达并降低抗凋亡蛋白表达,致使毛囊微型化。一项研究提取正常头皮中DPC 与外毛根鞘中的角质形成细胞并共培养后发现,当给予DPC DHT刺激后,可诱导DPC 分泌DKK1 蛋白并促进角质形成细胞发生凋亡[40]。可见想要逆转微型化,必须尽可能减少DHT 对DPC 的破坏。除了美国食品与药品监督管理局(Food and Drug Administration,FDA)批准的非那雄胺外,目前研究已发现多种药物可以通过抑制毛囊抑制因子分泌或表达来抑制DPC 凋亡,从而逆转微型化的发生。Wisuitiprot 等[41]发现毛蕊花糖苷可预防睾酮诱导的DPC凋亡,不仅促进DPC 增殖且极大降低了DPC 促炎因子的释放。Ma等[42]发现山茶籽饼提取物呈现出有效的抗雄激素作用,可逆转DPC中雄激素受体(androgen receptor,AR)和5α-还原酶表达的增加,降低DHT刺激DPC中BCL2 相关X 蛋白(BCL2-associated X protein,BAX)和细胞肿瘤抗原p53的表达,进而呈现出有效的抗凋亡作用。KY19382是一种新型的Wnt/β-连环蛋白激活剂,通过增加小鼠触须和人头皮毛囊DPC中的碱性磷酸酶活性和增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)的表达来诱导毛发再生[9]。
此外,细胞自噬通过消除错误折叠或受损的蛋白质和受损的细胞器来适应营养缺乏和其他不利的环境条件,这对于维持体外毛囊生长至关重要[43-45]。Liu 等[46]发现相比正常的生长期毛囊,AGA 毛囊自噬受损,自噬基因与蛋白的表达降低,透射电镜显示早期自噬小体数量减少,晚期自噬小体增加,表明自噬和凋亡都参与了AGA 期间的毛囊微型化。此外,还证明了早期退行期样AGA毛囊通过调节自噬相关基因beclin1(BECN)与BCL2 蛋白的结合导致自噬障碍,促进凋亡,从而导致AGA患者的毛囊过早进入休止期而致使毛囊微型化。Chai等[47]发现毛囊休止期可以通过激活自噬的小分子刺激启动生长期和头发生长,包括代谢物α-酮戊二酸(α-ketoglutaric acid,α-KG)、α-酮丁酸(α-ketobutyric acid,α-KB)以及处方药雷帕霉素和二甲双胍,这些药物对毛发生长的刺激能被特定的自噬抑制剂阻断。Kang 等[30]利用5-溴-3,4-二羟基苯甲醛增加自噬囊泡和自噬调节蛋白家族(Atg7、Atg5、Atg16L、LC3B)的水平,从而诱导了大鼠触须DPC 的增殖,触发了毛囊生长期的激活。
3 毛囊周围血管生成障碍
在毛囊生长期早期,微血管包绕在真皮乳头周围为其提供营养物质,这些微血管在毛囊的生长发育过程中起重要作用。Chew 等[48]发现相比健康头皮,秃顶患者的头皮血管形成基因下调,可能更有助于AGA的进展。Deng等[49]通过对AGA患者脱发区毛囊DPC 和正常患者头皮DPC 行转录组学分析对比后发现,AGA患者真皮乳头周围的微血管发生异常。进一步发现在AGA患者毛囊微型化的早期,AGA 真皮乳头周的血管会发生消退。因此,导致AGA 发生毛囊微型化的重要原因与真皮乳头周围血管形成障碍有关。Zhu等[50]发现雄激素可通过结合毛囊血管内皮细胞的AR来诱导毛囊周围的血管钙化,从而导致毛囊微型化。而当消除AR 时,DHT 刺激血管平滑肌钙化的作用消失。证明DHT或许通过AR 来诱导毛周血管发生钙化来影响相应的血供。除此以外,雄激素可以刺激血管内皮细胞发生氧化应激,并促进血管内皮平滑肌的凋亡和迁移,过量的活性氧和毛囊周围微环境中血管形成不足引起的毛囊生态位失调是AGA的主要原因[51]。有研究者设计出一种氧化铈纳米酶集成的微针贴剂,可以同时缓解氧化应激并促进血管生成以重塑AGA的毛囊周围微环境,减少毛囊微环境的进一步破坏从而缓解毛囊微型化的发展[10,52]。
4 HFSC耗竭
位于毛囊隆突的HFSC 具有较强的体外增殖与分化能力,通过HFSC 的静止和激活调控毛囊周期[53]。HFSC的耗竭和自噬功能障碍会直接影响毛干直径,加速毛囊微型化的发生,而毛干损失或直径缩小同时也会缩小毛囊的物理生态位尺寸,这导致HFSC进一步发生机械压缩及凋亡[54]。导致HFSC耗竭的因素众多,目前发现原因有肥胖、转录因子叉头盒C 家族(forkhead box C,FOXC)缺乏及衰老等。Morinaga等[55]发现,当连续4 d给予年轻小鼠高脂饮食后会导致小鼠体内产生过量的活性氧,进而促使HFSC 过早角化,最终导致小鼠毛囊微型化加速发生。FOXC1 和FOXC4 具有维持HFSC 生态位及控制干细胞静止的作用,以保证毛囊在长期的周期循环中有足够的干细胞储备。FOXC1与FOXC4的缺乏会加速毛囊周期循环,使休止期明显缩短,导致HFSC在静止状态下的时间更少,进一步加速了HFSC 消耗,这些因素都加快了毛囊微型化的发生发展[56-57]。Matsumura等[58]在衰老的小鼠毛囊中进行免疫荧光定位发现,组织中累积的DNA损伤可以导致型胶原(collagen type,COL17A1/BP180)蛋白水解,引发HFSC过早发生终末表皮分化,使HFSC周期性地从皮肤中消除导致毛囊微型化。
5 真皮鞘细胞(dermal sheath cell,DSC)的丢失与纤维化
毛囊微型化的发生并不是一种迅速和即时的的毛囊变小,而是患病毛囊生长期逐渐缩短而休止期逐渐延长的毛囊周期转换障碍,这一过程通常发生在退行期早期。有研究推测真皮鞘在毛囊周期转换过程中扮演了重要角色。正常毛囊的退行期中,毛囊DSC 高表达α-平滑肌肌动蛋白(α-smooth muscle actin,α-SMA)等后产生向心收缩力挤压真皮乳头向上移动并接近毛囊隆突区,从而促进毛囊由休止期向生长期转换[7,59]。衰老可能对真皮鞘产生影响,Ahlers 等[60]提取不同年龄供体的活检皮肤,分析了72 048个细胞样本,行单细胞RNA测序并检测相关的干细胞因子含量后,发现具有干细胞特征的DSC丢失。由此可以推测,当衰老发生后,DSC丢失便会影响生长周期真皮乳头位置的移动,从而影响毛囊由生长期向退行期的顺利转换。另一方面,Williams等[61]在AGA患者头皮病理中发现了真皮鞘的增厚和纤维化,这一病理变化被认为是AGA发生毛囊微型化的重要原因。English等[62]推测DHT或衰老或许参与了真皮鞘的增厚与纤维化的过程。目前仍未有研究证实真皮鞘纤维化后是否影响α-SMA的表达从而影响其向心收缩力,但AGA患者毛囊休止期提前并延长或许可以通过这个现象进行解释。
6 结语
毛囊微型化作为AGA重要的病理临床特征,一直以来备受关注。DPC和HFSC在维持毛囊大小和毛囊循环稳定时发挥了重要作用。参考并总结近年来的最新研究后发现:一方面通过DSC分泌抑制因子、DHT 等诱导DPC 凋亡及自噬障碍,最终致使毛囊生长周期紊乱从而发生毛囊微型化;另一方面通过毛周微循环障碍、HFSC 的过度耗竭和自噬障碍及DSC 的丢失与纤维化进一步加剧AGA 的发生发展(图1)。进一步认识毛囊微型化可以加强对临床治疗的指导,从而进一步治疗秃发类疾病。目前,FDA批准的可逆转毛囊微型化的药物仅有非那雄胺。已有多篇文献报道了非那雄胺存在抑制性欲、诱发抑郁症和精神障碍等不良反应[63-64],逆转毛囊微型化的治疗措施可有效替代非那雄胺以减少患者的不良反应,本文列举了最新的逆转毛囊微型化的相关治疗措施(表2),未来仍需研发更多具有临床价值的治疗方法。
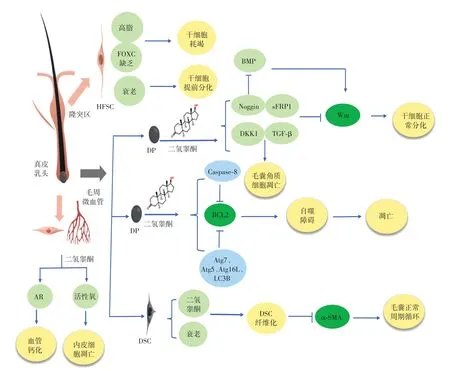
图1 毛囊微型化发生机制概要Figure 1 Mechanism of hair follicle miniaturization

表2 逆转毛囊微型化的方法及相关治疗Table 2 Methods and related treatments for reversing hair follicle miniaturization

