液化残渣气化过程钠/铁协同催化作用及对焦结构演化的影响规律*
李 佩 王冬生 李雯瑜 张文健 李 晓
(中国矿业大学煤炭加工与高效洁净利用教育部重点实验室,221116 江苏徐州)
0 引 言
2022年我国原油进口量为5.08亿t,原油过度依赖进口严重制约我国经济快速协调发展。在众多煤转化技术中,煤直接液化通过在适宜的温度和压力条件下将煤大分子结构裂解加氢,转化成汽油、柴油和航空煤油等油品[1],是缓解目前原油供需矛盾的有效手段。作为煤直接液化工艺伴生的有机固体废弃物——液化残渣是直接液化产物的重要组成部分,产率约占原煤量的30%[2],其成分复杂、环境危害大且处理成本高,但含有重质油和沥青烯等高附加值组分,有潜在的二次利用价值。液化残渣主要利用途径有气化、焦化和燃烧[3-4],还有一些非燃料类利用方式,如作为道路沥青添加剂和制备炭材料等[5-6],其中残渣气化因技术成熟、有机质热转化效率高等优点备受关注,以液化残渣代替部分原煤作为气化制氢原料向直接液化加氢段供H2,还可实现残渣气化和直接液化有机耦合,破解煤直接液化发展瓶颈。
我国新疆地区煤炭储量丰富,煤中碱金属钠含量相对其他产煤区偏高,属于典型的高钠煤种[7]。研究表明该地区煤反应性强、挥发分高、杂原子含量低,是煤直接液化工艺理想原料[8-10]。高钠煤直接液化后固有钠富集于液化残渣中,相比原煤,液化残渣钠含量升高4~10倍,约占残渣总质量的1%~3%。如前所述,残渣气化是液化残渣高效转化的适宜方法,但采用常规气化方式处理高碱液化残渣因反应温度过高,致使钠挥发、沉积,造成气化装置结渣、腐蚀和积灰等[11];另一方面,碱金属钠是煤炭气化催化剂,能够加快有机质与气化剂反应速率,缩短反应时间并降低气化温度。关于碱金属催化机理的主流学说有:1) CnM型络合物学说,认为在热处理过程中,碱金属与碳基质反应生成的CnM型络合物具有优秀的转移电子能力,可以更好地吸附气化介质;2) 氧化还原学说,认为碱金属催化作用主要来源于碱金属的氧化态中间体和还原态中间体相间的氧传递作用。因此,充分发挥高碱液化残渣钠含量较高的特点,借助固有钠的催化作用对液化残渣进行催化气化处理,不仅能降低反应温度实现节能降耗,还可缓解钠在高温下的挥发沉积,是高碱液化残渣提质利用的理想途径。
高温过程碱金属易挥发是制约含碱原料高效气化利用的主要原因,针对气化过程碱金属钠易挥发导致气化炉结渣、腐蚀和积灰的问题,贺冲等[12]通过添加黏土类矿物质促使钠转化为高熔点的硅铝酸盐,有效降低了钠离子的挥发量,但钠以硅铝酸盐形式存在时对煤炭气化催化的活性相对偏低。MEI et al[13]对比了不同碱金属盐的催化和释放特性,发现Na2CO3在700 ℃时与矿物质反应生成含钠硅铝酸盐,但NaAlO2直至900 ℃以上才会反生类似反应,且NaAlO2高温时不易挥发析出。此外,通过在碱金属中添加其他元素,利用组分间协同效应获得更高催化活性的同时,抑制钠的挥发也引起研究者的关注[14-15]。在煤的直接液化过程中,为提高反应转化率及油收率会添加一定比例的催化剂,铁基催化剂由于反应活性好、廉价易得、无需回收等优点已实现工业应用[16],高钠煤添加铁基催化剂后,所得液化残渣会同时富含钠、铁两种金属元素,研究表明含铁矿物对液化残渣同样具有催化气化作用效果[21]。然而,采用气化方式处理的高钠煤液化残渣中含有的钠、铁双金属是否存在协同催化效应鲜见相关报道,在气化过程中铁基催化剂与钠的相互作用规律也尚不明晰,液化残渣在反应过程中钠赋存形态变迁和高温挥发特征等同样需进一步深入研究。
围绕高钠煤液化残渣有机固废的资源化利用,本实验首先通过煤直接液化实验制取了钠含量较高的高碱液化残渣,为定量研究添加铁基催化剂对钠高温释放特征及赋存形态迁移规律的影响,在高碱液化残渣中加入了不同比例的铁基催化剂,探究了钠/铁催化气化过程相互作用规律。液化残渣等温气化实验在热重分析仪和固定床反应器中进行,分别研究了含有不同钠铁摩尔比(0.5和2)液化残渣在900 ℃,1 000 ℃和1 100 ℃下的气化反应性及钠高温释放率以及气化焦结构演化特征等,建立了反应模型对气化过程的动力学分析,以为煤直接液化残渣的资源化、减量化和无害化利用提供参考。
1 实验部分
1.1 液化残渣的制备
实验所用原煤为采自五彩湾矿区的准东高钠煤(ZD),原煤经研磨、筛分至粒径小于74 μm后放入干燥器中备用。煤直接液化实验在100 mL微型高压反应釜内进行,具体实验流程为:准确称量5.0 g原煤和10 mL四氢萘溶剂置于微型高压反应釜内,通过调节进气阀和出气阀使得釜内H2初始压力保持在3.0 MPa,液化反应温度设置为430 ℃,反应釜达到预设温度后恒温60 min,反应结束后釜内固液混合产物通过索氏萃取法分离,其中四氢呋喃不可溶物即为液化残渣(DCLR),经电感耦合等离子发射光谱(ICP-AES)检测原煤及液化残渣中钠的质量分数分别为0.34%和0.97%(空干基),原煤和液化残渣的工业分析、元素分析及灰成分分析见表1和表2。
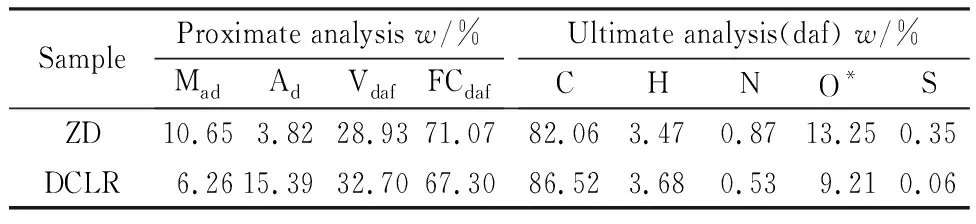
表1 原煤及液化残渣的工业分析和元素分析Table 1 Proximate and ultimate analyses of ZD and DCLR

表2 原煤及液化残渣的灰成分分析(%*)Table 2 Chemical compositions of ashes of ZD and DCLR(%*)
1.2 铁基催化剂负载
为定量研究铁基催化剂在气化过程中对钠催化活性及其高温挥发率的影响,采用浸渍法将铁基催化剂负载于原煤液化残渣中,其中n(Na)∶n(Fe)分别为1∶2(此时液化残渣标记为0.5-DCLR,0.5代表n(Na)∶n(Fe)=0.5,依此类推)和2∶1(液化残渣标记为2-DCLR)。以n(Na)∶n(Fe)=1∶2为例,准确称取1.500 g原煤液化残渣和0.048 g硫酸亚铁置于烧杯中,使用玻璃棒搅拌并缓慢滴入30滴丙酮以辅助液化残渣快速溶解在水中,持续搅拌直至溶液呈糊状,随后边搅拌边加入100 mL去离子水,搅拌均匀后将烧杯放置在磁力搅拌器中继续搅拌12 h,最后放入烘箱中于105 ℃干燥后备用。
1.3 气化实验及反应性评价指标
利用STA449F5型热重分析仪(德国,耐驰公司)进行等温气化实验。称取10.0 mg液化残渣均匀放置在氧化铝坩埚内,在N2气氛下(200 mL/min)以20 ℃/min升温速率升至设定温度(900 ℃,1 000 ℃,1 100 ℃),恒温10 min后切换为CO2气氛(120 mL/min),继续在设定温度下保持60 min后降至室温。采用KD-2型固定床反应器(太原兴盛恒科技有限公司)进行气化实验,实验条件与等温气化实验相同,每次液化残渣用量为1.0 g(见图1)。

图1 固定床反应器Fig.1 Diagram of fixed-bed reactor 1—Control panel;2—Balance;3—Heating furnace; 4—Quartz tube;5—Condenser;6—Tar collector
气化碳转化率(x)的计算见式(1)。
(1)
式中:x为碳转化率,%;m0为气化阶段开始时液化残渣的初始质量,mg;mt为气化反应t时刻液化残渣质量,mg;m∞为气化反应结束后残渣质量,mg。
采用反应性指数R0.5表示气化反应性强弱(见式(2))。
(2)
式中:τ0.5为碳转化率达到50%时所需反应时间,min;R0.5越大,气化反应性越强。
气化反应速率计算式见式(3)。
(3)
式中:v为气化反应速率,%/min;x为碳转化率,%;t为气化反应时间,min。
1.4 气化反应动力学
1.4.1 动力学模型选取
1) 均相模型
该模型假设气化反应在反应环境的内外表面是均相发生的,且内外扩散作用非常快,模型表达式为:

(4)
积分速率表达式为:
-ln (1-x)=kt
(5)
式中:k为气化反应速率常数,s-1。
2) 收缩核模型
该模型假设气固两相反应只在固体颗粒外表面进行,反应作用面随时间推移逐渐由外向内迁移,未反应核逐渐减小直至完全消失,模型表达式为:

(6)
积分形式为:
3[1-(1-x)1/3]=kt
(7)
1.4.2 动力学参数计算
对气化反应进行动力学计算及数据拟合,分析对比不同模型的适用性。阿伦尼乌斯方程计算求解动力学参数见式(8)。
kT=Ae-Ea/RT
(8)
对阿伦尼乌斯方程等式两边取自然对数,得到公式:
(9)
式中:kT为温度T时对应的速率常数;Rg为摩尔气体常数,8.314 J/(mol·K);Ea为反应活化能,J/mol或kJ/mol;T为绝对温度,K;A为指前因子。以lnk对1/T作图,并对图进行线性拟合,所得拟合直线斜率为-Ea/Rg,截距为lnA,从而求得活化能Ea及指前因子A。
1.5 样品表征
采用VERTEX 80 V型傅立叶变换红外光谱仪(德国,Bruker公司)测定样品官能团种类,准确称量样品(1±0.01) mg和KBr粉末(50±0.01) mg,将样品与KBr粉末混合均匀研磨,在10 MPa~15 MPa压力下压片1 min,光谱波数范围为400 cm-1~4 000 cm-1,分辨率为4 cm-1,扣除背景进行基线校正后得到各样品的红外光谱。使用D8 ADVANCE型X射线衍射仪(德国,Bruker公司)研究气化过程中矿物质赋存形态迁移演化规律,采用铜靶产生的K α射线对样品进行扫描,光谱扫描范围为10°~80°,扫描时间为10 min,通过Jade软件分析获得样品物相组成。
2 结果与讨论
2.1 钠/铁协同催化气化反应性
不同反应温度对钠/铁协同催化气化反应性的影响如图2所示。由图2可知,0.5-DCLR在900 ℃时气化反应性较差,完全气化所需时间约为40 min,随反应温度升高气化时间明显缩短,1 000 ℃和1 100 ℃气化用时约为10.0 min和4.0 min。与0.5-DCLR在不同温度下的热失重曲线类似,2-DCLR在900 ℃时气化反应性最差,完全气化时间约为30 min,随温度升高气化反应性逐渐增强,在1 000 ℃和1 100 ℃时气化反应时间约为9.5 min和4.0 min。2-DCLR在900 ℃完全气化较0.5-DCLR完全气化缩短了10 min,其余温度下二者无明显差异,该现象与液化残渣碳转化率曲线趋势一致。900 ℃相同反应时间下2-DCLR的碳转化率明显高于0.5-DCLR的碳转化率,1 000 ℃和1 100 ℃时两种液化残渣碳转化率曲线高度重合,达到相同碳转化率基本同步。上述实验结果表明,钠/铁协同催化气化的液化残渣反应性受温度影响较大,温度升高增大了气化反应速率常数,有效提高了液化残渣的气化反应性,因而削弱了Fe元素含量不同造成的反应性差异。与高碱液化残渣单独气化实验[18]结果相比,添加铁基催化剂后相同实验条件下,液化残渣气化反应性皆有所提高,证实铁基催化剂进一步提升了液化残渣气化活性,其添加比例对高碱液化残渣气化反应性也有一定影响,铁含量较高时反应过程易形成无催化活性的铁/碱金属化合物,从而降低了钠催化活性。
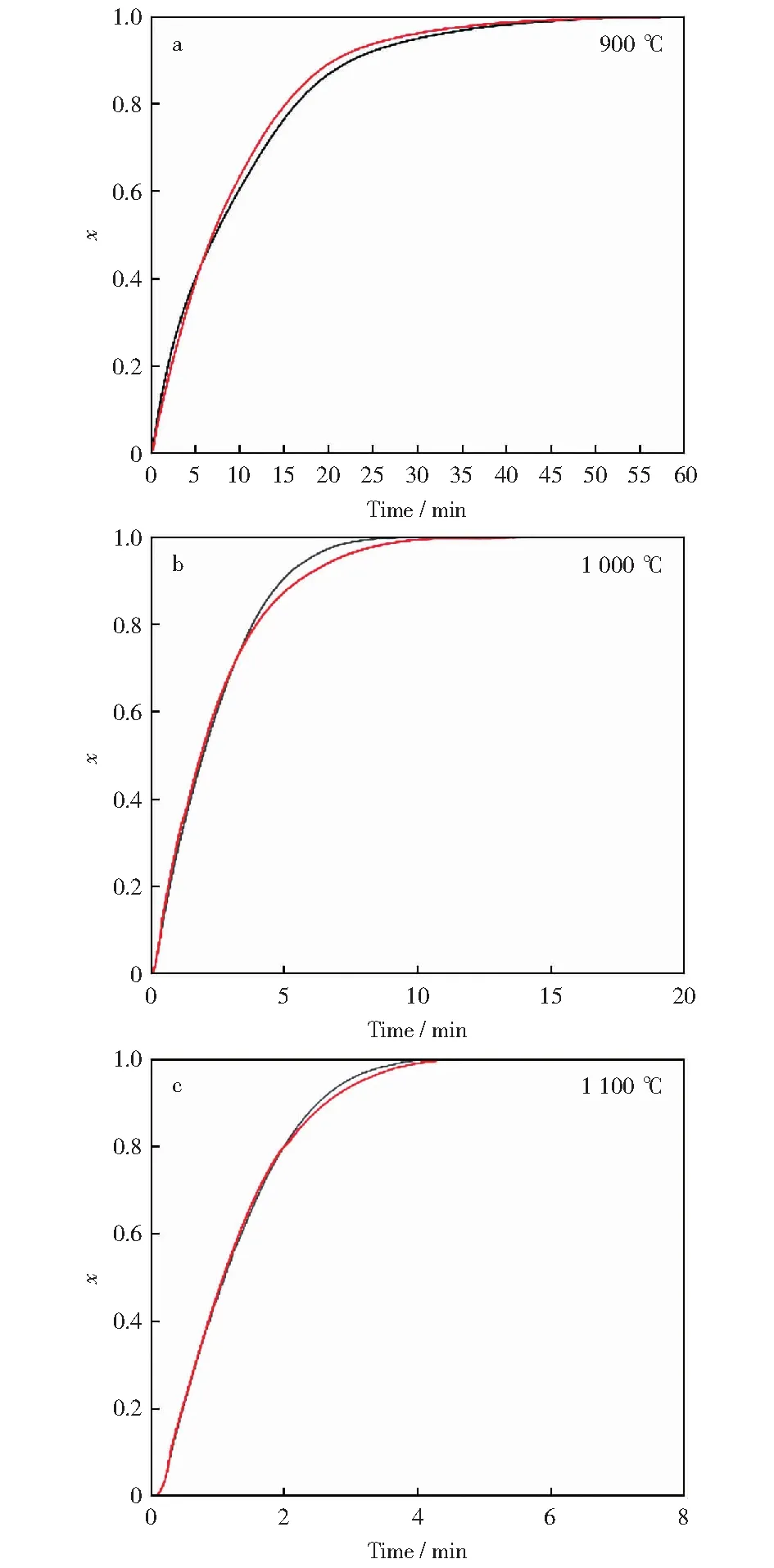
图2 0.5-DCLR与2-DCLR在不同气化温度下的碳转化率Fig.2 Carbon conversion of 0.5-DCLR and 2-DCLR at different gasification temperatures
为定量研究钠/铁添加比例对高碱液化残渣气化反应性的影响,本研究分析了两种液化残渣在不同温度下的气化反应速率曲线,并计算了残渣气化反应性指数,如图3所示。由图3可知,液化残渣气化反应速率在反应初期变化较大,速率曲线呈尖峰状,到达峰值时间在2 min以内,随气化温度升高,液化残渣气化反应速率最高值也相应增大。高碱液化残渣单独气化时最大反应速率分别为6%/min(900 ℃),15%/min(1 000 ℃)和28%/min(1 100 ℃)[18],而相同温度下0.5-DCLR的最大反应速率分别为13%/min,35%/min和60%/min,比单独气化分别增大了1.17倍、1.33倍和1.14倍。在完整的气化反应过程中,2-DCLR的总体气化反应性要强于0.5-DCLR的总体气体反应性,即添加少量的Fe可以与高碱液化残渣中固有钠产生协同催化作用,碱金属的存在促进了铁基催化剂的分散和还原,进一步提高了催化剂反应活性,加速了气化反应进行。
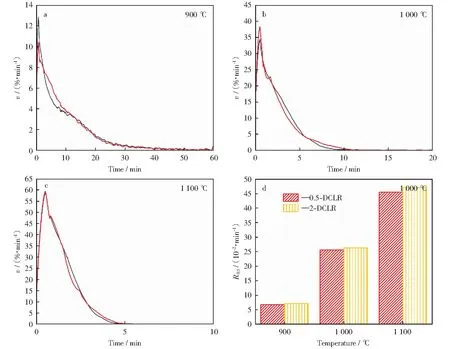
图3 在不同气化温度下液化残渣反应速率曲线及反应性指数Fig.3 Reaction rate curve and reactivity index of DCLR at different gasification temperatures
2.2 气化反应过程动力学分析
不同温度下0.5-DCLR和2-DCLR的均相反应模型数据拟合曲线及收缩核模型数据拟合曲线如图4所示。图5所示为利用不同模型进行数据拟合的结果。由图5可知,温度影响不同模型拟合结果的相关性系数。均相模型适合描述900 ℃时的气化反应过程,相关性系数均在0.99以上,而1 000 ℃和1 100 ℃的气化反应过程更适用于收缩核模型,其相关性系数同样在0.99以上。
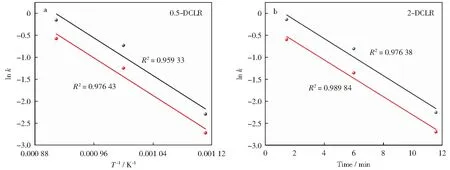
图5 ln k与1/T间关系Fig.5 Relationship between ln k and 1/T
利用阿伦尼乌斯方程计算反应活化能和指前因子等动力学参数,计算结果见表3。由表3可知,铁基催化剂添加比例对反应活化能及指前因子的影响不大,利用不同拟合模型得出的实验结果较为相近,钠/铁协同催化的活化能为66 kJ/mol~69 kJ/mol。相对于高碱液化残渣单独气化过程,添加铁基催化剂后残渣气化反应活化能均有所降低,说明复合催化剂在相同条件下催化性能优于碱金属催化剂,钠/铁间存在协同催化作用。
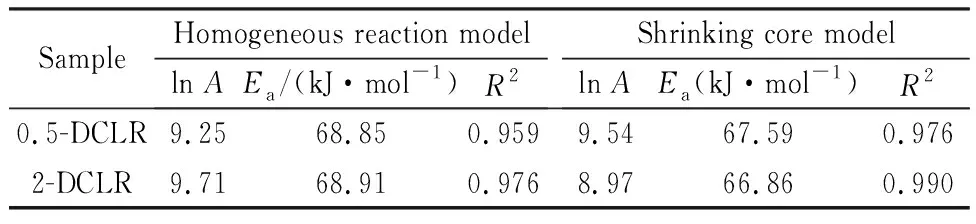
表3 在气化过程中的反应活化能和指前因子Table 3 Reaction activation energy and pre-exponential factor in gasification process
2.3 气化过程钠/铁相互作用规律


图6 0.5-DCLR和2-DCLR及其不同温度下气化焦的红外光谱Fig.6 FTIR spectra of 0.5-DCLR and gasification residues obtained at different temperaturesa—0.5-DCLR;b—2-DCLR
为探究铁基催化剂添加量对液化残渣气化后晶相矿物质组成的影响规律,对液化残渣及不同温度下的气化焦进行了XRD分析(见图7)。由图7可以看出,0.5-DCLR和2-DCLR在气化前的出峰位置与峰形相似,并未检测到明显的结晶化合物,25°至28°的衍射角为无定形碳的衍射峰。液化残渣在900 ℃下气化1 h后,负载的铁基催化剂主要以Fe2O3
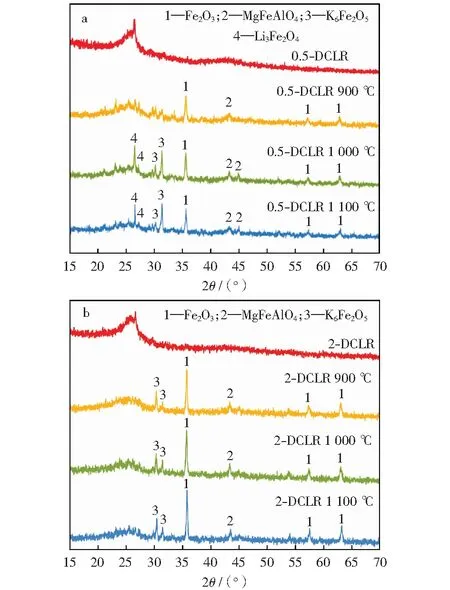
图7 0.5-DCLR和2-DCLR及其不同温度下气化焦的XRD谱Fig.7 XRD patterns of 0.5-DCLR and 2-DCLR and gasification residues obtained at different temperaturea—0.5-DCLR;b—2-DCLR
的形式存在。随气化反应温度升高,两种添加比例的液化残渣出现了K-Fe和Li-Fe等碱金属/铁复合化合物物相,说明温度升高有利于Fe与碱金属间的相互作用。铁基催化剂添加量较高时(0.5-DCLR),反应过程更易形成无催化活性的铁/碱金属化合物。钠/铁间协同作用的原因可能是,铁以低价态存在时催化活性较强,碱金属钠将电子转移给过渡金属铁,抑制了过渡金属铁的氧化,因而表现出较高的协同反应活性;同时,铁系催化剂使得碱金属钠在气化过程中生成了更多的活性中间体,并减少了钠离子挥发损失。钠在升温阶段便与铁催化剂发生了作用,使得铁催化剂更好参与氧化还原循环。钠盐的熔点较低,在气化过程中铁系催化剂在钠的参与下能够均匀分散至煤焦颗粒表面,进一步提高铁系催化剂的催化活性。XRD谱中并没有检测到含钠化合物的衍射峰,但有Fe/Al化合物衍射峰的存在,上述结果表明在气化反应过程中,添加适量的铁基催化剂有效阻止了碱金属钠与Si和Al之间反应生成无催化活性的不溶物[20],更好地保证了碱金属钠的催化活性。
2.4 钠高温释放特征
钠的高温释放率通过式(10)进行计算。
(10)
式中:RNa为钠离子释放率,%;M0为气化残渣中钠离子的质量,mg;M1为液化残渣中钠离子的质量,mg;所有钠离子含量均通过电感耦合等离子发射光谱法测定,结果为两次及以上平均值。
原煤液化残渣及添加铁基催化剂液化残渣的钠高温释放率如图8所示。由图8可知,原煤液化残渣中钠释放率较高,900 ℃时即高达85.2%,随气化温度升高,钠释放率进一步提升,1 100 ℃时91.6%的钠从液化残渣中析出至气相。添加铁基催化剂后,液化残渣的钠高温挥发量明显降低,尤其是在900 ℃和1 000 ℃的气化过程。相比原煤液化残渣,相同气化温度下0.5-DCLR的钠释放率分别减少26.7%,23.9%,15.8%,2-DCLR的钠释放率分别减少17.9%,15.5%,9.6%。上述结果表明,液化残渣中含铁矿物对钠高温释放过程具有显著的抑制作用,能够降低气化过程钠的析出量,进而缓解因钠挥发引起的设备沾污和腐蚀等问题。

图8 液化残渣在不同温度下的钠高温释放率Fig.8 Release ratio of sodium species at different temperatures
3 结 论
1) 铁基催化剂提高了液化残渣的气化反应性,残渣最高气化反应性指数超过0.45°/min,相同温度下0.5-DCLR的最大反应速率比单独气化分别增大了1.17倍(900 ℃),1.33倍(1 000 ℃)和1.14倍(1 100 ℃)。
2) 均相模型适合描述900 ℃气化反应过程,更高温度的气化反应过程则适用收缩核模型。添加铁基催化剂后残渣气化反应活化能均降低,表明复合催化剂间存在协同催化作用。
3) 气化温度升高有利于Fe与碱金属间的相互作用,铁基催化剂添加量较高时,气化焦中出现了K-Fe,Li-Fe,Na-Fe等弱催化活性的碱金属/铁复合化合物,从而降低了钠催化活性。
4) 液化残渣中含铁矿物对钠高温释放过程具有显著的抑制作用,能够降低气化过程钠的析出量,添加铁基催化剂后钠挥发量减少了9.6%~26.7%,有助于缓解因钠挥发引起的设备沾污和腐蚀等问题。
致谢:国家重点研发计划(2022YFC2905900)和中国矿业大学优秀青年骨干教师项目资助,感谢中国矿业大学现代分析测试中心路遥博士在红外测试分析上的协助。

