酶法催化合成乙二醇硬脂酸酯工艺优化
姚新卯 黄振波 粟晖

摘 要:以硬脂酸和乙二醇为原料,探索得到脂肪酶作催化剂、反应条件温和、合成绿色的乙二醇硬脂酸酯合成方法。采用红外光谱表征、拉曼光谱结合独立分量分析(independent component analysis,ICA)分离算法对合成产物快速定性分析,判断合成产物含有目标产物的结构特征,并测定产物的酸值,结果表明脂肪酶催化合成乙二醇单硬脂酸酯的方法可行。通过单因素及正交实验设计对酶法催化合成乙二醇硬脂酸酯的工艺进行优化,得到最优的工艺条件为:反应温度为70 ℃,反应时间为3 h,酸醇摩尔比为2∶1,催化剂质量分数为4%,分子筛质量分数为5%;在优化条件下平行3次实验,平均酯化率达93.68%;脂肪酶催化合成乙二醇硬脂酸酯效果较好,为乙二醇硬脂酸酯的绿色合成提供了新方法。
关键词:酶催化;乙二醇硬脂酸酯;光谱定性;酯化率;工艺优化
中图分类号:TQ 658 DOI:10.16375/j.cnki.cn45-1395/t.2023.04.018
0 引言
乙二醇硬脂酸酯是一种常用的珠光剂,是以硬脂酸和乙二醇为原料,在催化剂作用下发生酯化反应合成的,在纺织、涂料、造纸、化妆等[1]领域中有广泛应用。目前常用的催化剂主要有磷酸、硫酸、对甲苯磺酸[2]、磷钨酸[3]和氧化锌[4]等,转化率较高,但存在反应温度高、副产物较多[5]、产品易被碳化[6]等缺点,且产生的废液污染环境。因此,探索一种反应条件温和、工艺简单、绿色节能的乙二醇硬脂酸酯合成方法具有重要意义。脂肪酶作为水解、酯化等反应的高效生物催化剂,具有对环境友好、反应条件温和、无毒无刺激等优点[7-8],在聚乙二醇硬脂酸酯[9]、乙酸芳樟酯[10]、柠檬酸三乙酯[11]、衣康酸酯[12]等合成中得到应用,但脂肪酶催化合成乙二醇硬脂酸酯的研究尚未见报道。
本文选用脂肪酶作催化剂合成乙二醇硬脂酸酯,采用红外光谱、拉曼光谱结合独立分量分析(independent component analysis,ICA)方法分析合成产物,探索脂肪酶催化合成乙二醇硬脂酸酯的可行性。通过单因素及正交实验设计,探讨反应温度、反应时间、酸醇摩尔比、分子筛质量分数等因素对酯化率的影响,对酶法催化合成乙二醇硬脂酸酯的工艺进行了优化。
1 实验部分
1.1 实验仪器
广域透射拉曼光谱仪(PERT1000,西派特(北京)有限公司),傅里叶变换红外光谱仪(Frontier,美国PE公司),电子分析天平(CP214,奥豪斯仪器有限公司),智能磁力搅拌器(DF-101S,河南爱博特科技发展有限公司)。
1.2 实验试剂
乙二醇(AR,西陇化工股份有限公司),硬脂酸(AR,上海麦克林生化科技有限公司),脂肪酶(Novozym 435,杭州创科生物科技有限公司),乙二醇单硬脂酸酯(单酯)(AR,上海麦克林生化科技有限公司),乙二醇双硬脂酸酯(双酯)(AR,山东优索化工科技有限公司),5A分子筛(AR,上海麦克林生化科技有限公司),氢氧化钾(AR),无水乙醇(AR),邻苯二甲酸氢钾(AR)。
1.3 脂肪酶催化合成乙二醇硬脂酸酯的可行性实验
以0.01 mol(摩尔质量为284.48 g/mol)的硬脂酸为基准,在50 mL三口烧瓶中,依次加入硬脂酸2.50 g、乙二醇3.90 mL及分子筛0.30 g;71 ℃水浴加热,待物料完全熔化后,加入0.02 g的脂肪酶。150 r/min磁力搅拌,反应3 h。反应结束后,用蒸馏水清洗合成产物3次以上,去除未反应的乙二醇、硬脂酸、分子筛和脂肪酶,干燥后得到6.12 g乳白色蜡状固体,熔点为59~62 ℃,将合成产物记为M1。
采用KBr压片法采集对照品(硬脂酸、单酯、双酯)、M1的红外光谱(扫描范围450~4 000 cm-1,扫描3次,分辨率4 cm-1,数据间隔0.1 cm-1),对M1进行表征 [13]。
采集对照品与M1拉曼光谱(积分时间500 ms,平滑点数0,中心波长532 nm,功率等级5,拉曼位移为200~3 442 cm-1,每个样本采集10次),通过拉曼光谱结合独立分量分析(ICA)分离算法 [14-15]求出分量(ICs),判断M1是否含有目标产物。根据《化妆品用原料 乙二醇二硬脂酸酯》(GB/T 34820—2017)[16]测定M1酸值,验证脂肪酶催化合成乙二醇硬脂酸酯的可行性。
1.4 脂肪酶催化合成乙二醇硬脂酸酯的單因素实验
在酶法催化合成乙二醇硬脂酸酯方法可行基础上,通过单因素实验,探索不同反应时间、反应温度、酸醇摩尔比、催化剂质量分数、分子筛质量分数等因素对酯化率的影响,得到各因素的较优水平。合成步骤同1.3。
1.5 正交实验设计优化合成工艺条件
采用[L9(34)]正交实验设计,以酯化率为指标,选取反应时间、酸醇摩尔比、催化剂质量分数、分子筛质量分数等单因素实验结果的最佳条件与2个邻近点,考察不同水平因素对酶法催化合成乙二醇硬脂酸酯的影响,因素水平表如表1所示。按1.3的合成步骤,固定硬脂酸的用量,依照表1的条件进行实验,得出优化工艺条件,并对其进行验证,平行3次。
2 结果与讨论
2.1 酶催化合成乙二醇硬脂酸酯的可行性实验结果分析
2.1.1 产物红外光谱表征
将对照品与M1的红外谱图进行对比,结果如图1(a)所示,发现在870 cm-1和1 110 cm-1处出现了很强的C—O—C基团特征吸收峰,1 704 cm-1处出现了羧基峰,2 920 cm-1和2 848 cm-1处出现了羟基伸缩振动吸收峰,1 739 cm-1处出现了酯基峰[17-18],说明M1主要为乙二醇单硬脂酸酯,并截取4阶导数谱的特征峰波段1 730~1 740 cm-1做图,结果如图1(b)所示。
从图1(a)可发现在1 739 cm-1处M1出现了明显的酯羰基伸缩振动吸收峰,含有目标产物结构特征。从图1(b)可看出目标产物及M1有显著的特征吸收峰,而硬脂酸未出现吸收峰,说明M1含有目标产物,表明酶法催化合成乙二醇单硬脂酸酯可行。
2.1.2 ICA判断合成产物
各对照品和M1样本光谱图如图2所示,从图2可发现在波数为1 369 cm-1处M1有显著的目标产物特征峰。
ICA 能够从复杂的组分体系中获得输出分量与源信号一致的分离结果[19],从未知多元混合体系中确定待测组分,实现快速定性分析。截取在181~2 200 cm-1與2 300~3 230 cm-1间的特征峰数据,采用自编算法,求取样本光谱的4阶导数后,再分离得到M1的ICs,从而求出ICA分离算法解出的合成产物M1各分量与源光谱的相关系数,其中IC1与单酯相关系数r=0.994 6,IC3与双酯的相关系数达到0.960 4,说明酶法催化合成了目标产物。
原料硬脂酸酸值为207.69 mgKOH/g,测定M1的酸值为63.68 mgKOH/g。M1的酸值较大,说明酯化不够成功,但M1酸值降低了近3倍,表明酶法催化合成乙二醇单硬脂酸酯是可行的。
2.2 单因素实验结果分析
2.2.1 反应时间对酯化率的影响
将酸醇摩尔比为1∶4、催化剂质量分数为1%、分子筛质量分数为1%等因素条件放大4倍的样品,在搅拌转速为150 r/min、温度为75 ℃的水浴锅中反应5 h,每隔1 h取约0.6 g样品测定酸值,得出酯化率,酯化率随时间变化如图3所示。
随着反应时间的增加,酯化率先增加后降低,可能与酶的活性和反应逆向移动有关,反应时间越长,脂肪酶的活性渐渐降低,反应逐渐逆向进行,当反应酯化率趋缓时,应停止反应,或添加酶用量促进反应正向移动,可抑制反应逆向进行,反应3 h的酯化率达80.04%,为最佳。
2.2.2 反应温度对酯化率的影响
将酸醇摩尔比为1∶4、催化剂质量分数为1%、分子筛质量分数为1%等因素条件的样品,在搅拌转速为150 r/min,温度分别为60 、65、70、75、80 ℃的反应体系中反应3 h,反应结束清洗合成产物,测定样品酸值,得出酯化率。但反应温度为80 ℃的样品酸值接近原始酸值,未发生酯化。酯化率随反应温度变化如图4所示。
温度是影响酶活性和稳定性的重要因素,脂肪酶活性温度在25~80 ℃,超出最佳范围,酶将失去活性。选择60~80 ℃的温度进行试验,酯化率先增加后降低,反应温度为80 ℃的样品无酯化率,说明脂肪酶已失去活性。应控制反应温度在硬脂酸熔点与脂肪酶活性范围内,则有利于反应正向进行,从而可提高合成产物的酯化率。在70 ℃下,酯化率达87.19%,为最佳。
2.2.3 酸醇摩尔比对酯化率的影响
将酸醇摩尔比分别为3∶1、2∶1、1∶1、1∶2、1∶4,催化剂质量分数为1%、分子筛质量分数为1%的各样品,在搅拌转速为150 r/min、温度为70 ℃的水浴锅中反应3 h,反应结束后,清洗合成产物,测定样品酸值,得出酯化率,酯化率随酸醇摩尔比的变化如图5所示。
随着酸醇摩尔比中醇的比例增加,酯化率逐渐降低,可能是过量的乙二醇会使pH值变大,从而影响酶的活性,导致酯化率降低。酸醇摩尔比为2∶1时,酯化率为87.32%,达到最佳。
2.2.4 催化剂质量分数对酯化率的影响
将酸醇摩尔比为2∶1,催化剂质量分数分别为1%、2%、3%、4%、5%和6%,分子筛质量分数为1%的各样品,在搅拌转速为150 r/min、温度为70 ℃的水浴锅中反应3 h,反应结束后,清洗合成产物,测定样品酸值,得出酯化率,酯化率随催化剂质量分数的变化如图6所示。
脂肪酶是促进反应的关键因素,脂肪酶质量分数增加,酯化率呈现上升趋势,当酶质量分数为5%时,酯化率增加平缓,可能是酶质量分数的持续增加会限制体系中反应底物的接触,导致酯化率增加趋缓。添加适量脂肪酶能有效促进合成反应,脂肪酶质量分数过低不利于反应正向进行,过高则增加生产成本,且对酯化率影响有限。脂肪酶质量分数为5%和6%时的酯化率分别为89.61%和89.72%,差值较小,考虑到生产成本,选取质量分数为5%的脂肪酶进行后续优化实验。
2.2.5 分子筛质量分数对酯化率的影响
将酸醇摩尔比为2∶1,催化剂质量分数为5%,分子筛质量分数分别为0、1%、2%、3%和4%等因素条件的样品,在搅拌转速为150 r/min、温度为70 ℃的水浴锅中反应3 h,反应结束后,清洗合成产物,测定样品酸值,得出酯化率,酯化率随分子筛质量分数的变化如图7所示。
加分子筛有助于去除酯化反应中生成的水分。从图7中看出,随着分子筛质量分数升高,酯化率呈现上升趋势,说明质量分数升高会促进反应物充分接触,使酯化率升高。但随着质量分数的升高,酯化率逐渐缓慢升高,说明反应生成的水分较少,质量分数升高对合成产物酯化率影响较小。分子筛质量分数为4%时,酯化率最佳,达到了86.42%。
2.3 工艺优化结果与分析
通过单因素实验得到各因素的较优水平,为提高酯化率,采用正交法进行工艺优化。由于硬脂酸熔点及脂肪酶活性温度在70 ℃附近,通过单因素实验得到最佳反应温度为70 ℃,确认该点为最优反应温度,又因邻近反应温度较难控制,不将其列为正交考察。测定各条件下合成产物的酸值,进而求得酯化率,正交实验结果如表2所示。
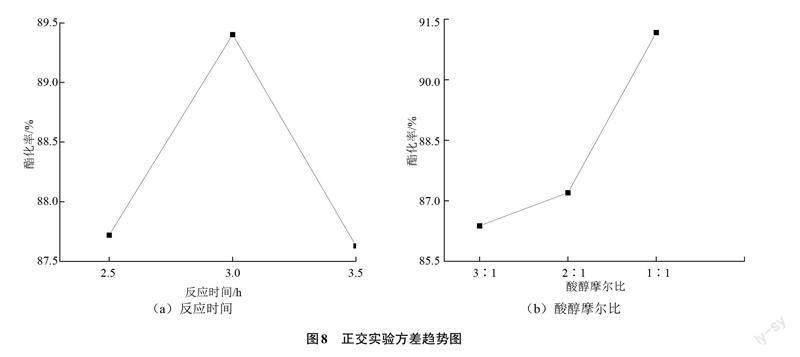
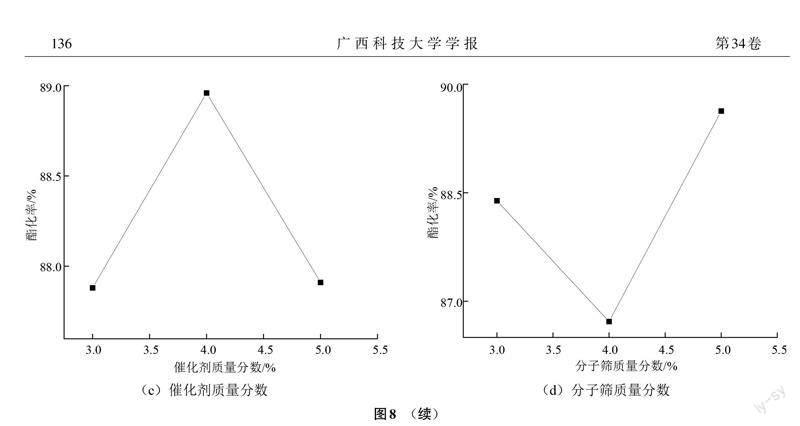
根据正交实验方差分析结果做趋势图如图8所示。
通过正交实验设计优化得到最佳工艺条件为反应时间3 h、酸醇摩尔比1∶1、催化剂质量分数4%、分子筛质量分数5%。从表2及图8结合单因素实验结果,得到正交工艺优化的反应时间、催化剂质量分数最优条件与单因素结果相符,而分子筛质量分数与酸醇摩尔比的结果有偏差,可能是样品杂质未彻底去除所导致的,需进一步做酸醇摩尔比实验。分子筛质量分数达3%后酯化率增加平缓,正交分子筛质量分数为4%和5%的酯化率极差较小,继续增加分子筛质量分数对提高酯化率可能影响较小,因此确定最佳分子筛质量分数为5%。
在正交优化条件基础上,进一步在酸醇摩尔比分别为3∶1、5∶2、2∶1、3∶2、1∶1、2∶3和1∶2的条件下做单因素实验,酸醇摩尔比与酯化率的关系如图9所示,酸醇摩尔比为2∶1时的酯化率达93.57%,为最佳,优于正交实验酸醇摩尔比1∶1的酯化率,因此,确认酸醇摩尔比的最优工艺条件为2∶1。
2.4 验证实验
通过单因素及正交实验得到了最优工艺条件:反应温度70 ℃、反应时间3 h、催化剂质量分数4%、分子筛质量分数5%。在该工艺条件下进行3次平行实验,得到的酯化率(表3)分别为93.89%、93.40%、93.75%,均值为93.68%,3组实验均高于单因素及正交实验各条件的酯化率。验证了通过单因素及正交实验探索得到的酶法催化合成乙二醇硬脂酸酯的工艺条件为优化条件。
3 结论
首先采用红外光谱表征、拉曼光谱结合ICA分离快速定性方法,判定了酶法催化合成产物含有目标产物乙二醇单硬脂酸酯,产物酸值测定结果表明酶法催化合成乙二醇單硬脂酸酯可行。并通过单因素实验及正交实验设计优化得到了最优工艺条件,平均酯化率达93.68%。探索得到的工艺路线反应条件温和、简单、环保,为乙二醇硬脂酸酯的催化合成提供了更加绿色的方法。后续可进行酶法催化合成反应的过程分析,跟踪过程产物的组成变化,实现单酯和双酯可控合成,得到珠光效果较佳的乙二醇硬脂酸酯的合成工艺条件。
参考文献
[1] 孟丽丰.增效型乙二醇硬脂酸酯合成工艺研究[D].昆明:昆明理工大学,2010.
[2] 杜运平,朱兵.乙二醇硬脂酸双酯的合成工艺研究[J].轻工科技,2020,36(6):26-27.
[3] 文婕英,白林,朱彦荣,等.TiO2负载磷钨酸催化剂的制备及其催化乙二醇与硬脂酸双酯化反应研究[J].甘肃高师学报,2017,22(6):13-16.
[4] 解田,段永华.乙二醇硬脂酸酯的合成新工艺研究[J].广西轻工业,2008(5):12-13.
[5] 徐光年,谢红璐.乙二醇硬脂酸酯的合成新方法[J].安徽化工,2005,31(4):34-35.
[6] 白林,陈洁,王代莲.负载型对甲苯磺酸催化剂的制备及其催化双酯化反应研究[J].甘肃高师学报,2017,22(3):16-19.
[7] 陈潇.脂肪酶催化非专一性在氧化反应及多组分反应中的应用研究[D].长春:吉林大学,2019.
[8] 申卫家,郦金龙,黎金鑫,等.微生物脂肪酶的研究进展及其在食品工业中的应用[J].粮食与油脂,2017,30(4):5-7.
[9] NHIVEKAR G S,RATHOD V K. Optimization of lipase-catalyzed synthesis of polyethylene glycol stearate in a solvent-free system[J].Green Processing and Synthesis, 2019,8(1):30-37.
[10] 胡坤,代斌,胡建国,等.有机相中脂肪酶催化合成乙酸芳樟酯的研究[J].安徽农业科学,2016,44(7):1-3.
[11] 胡媛,李士桥,孙建华,等.酶催化法合成柠檬酸三乙酯[J].蚌埠学院学报,2015,4(1):15-18.
[12] 王世臻.脂肪酶催化衣康酸酯合成工艺研究[D].北京:北京化工大学,2019.
[13] 潘彦伶,任奕,阎磊,等.固体酸催化制备珠光剂乙二醇硬脂酸酯的研究[J].山东化工,2021,50(2):26-27,30.
[14] YAO Z X,SU H,YAO J. Improve the performance of independent component analysis by mapping the spectrum to an orthogonal space[J].Spectrochimica Acta-Part A:Molecular and Biomolecular Spectroscopy,2021,251:119467.
[15] 宁荣华,粟晖,周丹丹,等.基于DSCS-ICA的布洛芬胶囊混合拉曼光谱定性分析[J].光散射学报,2022,34(1):15-21.
[16] 全国香料香精化妆品标准化技术委员会.化妆品用原料 乙二醇二硬脂酸酯:GB/T 34820—2017 [S].北京:中国标准出版社,2017.
[17] 史修启,孙永强,张 勇,等.乙二醇双硬脂酸酯乙氧基化物的合成与性能研究[J].日用化学工业,2013,43(3):184-187.
[18] 吴其辉,刘晓磊,姚思远,等.乙二醇单硬脂酸酯-十六醇复合相变材料的热性能[J].安徽工业大学学报(自然科学版),2020,37(2):132-136.
[19] 姚志湘,刘焕彬,粟晖,等.盲信号分离输出与源信号的一致性判断[J].华南理工大学学报(自然科学版),2007,35(5):50-53.
Optimization of enzymatic synthesis of ethylene glycol stearate
YAO Xinmao, HUANG Zhenbo, SU Hui*
(School of Biological and Chemical Engineering, Guangxi University of Science and Technology, Liuzhou 545006, China)
Abstract: A green synthesis method of ethylene glycol stearate was developed by reacting stearic acid and ethylene glycol catalyzed with lipase under mild reaction conditions. Infrared spectroscopy, Raman spectroscopy and independent component analysis (ICA) separation algorithm were utilized for rapid qualitative analysis of the synthesized products to judge their possession of the structural feature of the target products and gauge their acid value. The results showed that the method of catalytic synthesis of ethylene glycol monostearate by lipase was feasible. Through single factor and orthogonal experimental design, the enzymatic synthesis process of ethylene glycol stearate was optimized. The optimal process conditions were reaction temperature of 70 ℃, reaction time of 3 h, acid-alcohol molar ratio of 2∶1, catalyst mass fraction of 4%, and molecular sieve mass fraction of 5%. The average esterification rate was 93.68% through three parallel confirmation experiments under the optimized condition. The process of lipase catalyzed synthesis of ethylene glycol stearate has good esterification effect, which provides a new method for the green synthesis of ethylene glycol stearate.
Key words: enzyme catalysis; ethylene glycol stearate; qualitative spectrometric analysis; esterification rate; optimization of process
(责任编辑:于艳霞)
收稿日期:2023-01-03
基金项目:广西自然科学基金项目(2015GXNSFAA139038);广西高等教育本科教学改革工程项目(2021JGB232)资助
第一作者:姚新卯,在读硕士研究生
*通信作者:粟晖,硕士,教授,研究方向:化工过程分析技术及精细化学品开发,E-mail:suhui@gxust.edu.cn

