地中海贫血儿童非亲缘造血干细胞移植后BK病毒相关出血性膀胱炎临床特征分析
庄燕红, 洪秀理, 陈 洁, 陆婧媛, 鹿全意
目前,异基因造血干细胞移植(allogeneic hematopoietic stem cell transplantation,allo-HSCT)是治愈儿童输血依赖型地中海贫血(简称地贫)的最主要手段,接受干细胞移植的患儿长期生存率达到80%~90%,但仍有5%~10%的地贫患儿接受干细胞移植后死于移植相关的并发症,其中移植后病毒感染性疾病[如巨细胞病毒(cytomegalovirus,CMV)、EB病毒(Epstein-Barr virus,EBV)和BK病毒(BK polyomavirus,BKV)感染]是导致患者死亡的重要原因[1-2]。出血性膀胱炎(hemorrhagic cystitis,HC)是干细胞移植后常见的并发症之一,在儿童干细胞移植中并不少见,可导致患儿死亡[3-6]。患儿通常表现为尿急、尿痛和肉眼血尿,严重者导致肾功能衰竭。多数情况下,HC发生与病毒感染密切相关[7-8]。BKV属于多瘤病毒科,多潜伏于泌尿道上皮细胞、淋巴细胞和可能的其他细胞中。原发性BKV感染大多无症状,病毒呈潜伏状态。allo-HSCT后的骨髓空虚和免疫抑制剂的应用常使BKV发生再激活,BKV感染可导致患者免疫功能重建延迟,合并重症感染或死亡,目前尚无有效的治疗方法。本文探讨了输血依赖型地贫儿童非亲缘干细胞移植后BKV相关HC的临床特征和影响因素,为地贫儿童造血干细胞移植后并发症的防治提供参考。
1 资料与方法
1.1临床资料 回顾性分析2018年2月至2021年2月厦门大学附属中山医院62例输血依赖型地贫儿童接受非亲缘造血干细胞移植后的临床资料。纳入标准:(1)造血干细胞移植前供受者经血清学和尿液检测均无BKV感染;(2)受体术后1年内每月检测有无BKV感染;(3)年龄≤14岁。排除标准:(1)术前供者或受者确诊BKV感染;(2)受体术后1年内未规律检测有无BKV感染;(3)年龄>14岁。62例患儿中男30例,女32例,移植年龄(5.18±2.29)岁,均确诊为输血依赖型地贫,非亲缘供者来源于中华骨髓库,供受者人类白细胞抗原(human leukocyte antigen,HLA)配型10/10一致者47例,HLA 1~2位点不合者15例。62例患儿临床资料见表1。本研究经厦门大学附属中山医院伦理委员会批准(伦理批件号:XMZSYYKY2021-228)。

表1 62例患儿临床资料
1.2预处理和干细胞移植 全部患儿统一应用由氟达拉滨、环磷酰胺、白消安和兔抗人胸腺细胞球蛋白(antithymocyte globulin,ATG)组成的预处理方案[9]。预处理完成后输注非亲缘供者干细胞悬液,CD34+细胞数量为(5~10)×106/kg。常规采用普通肝素5 000~10 000单位24 h泵入联合前列地尔预防肝静脉闭塞病(hepatic veno-occlusive disease,VOD),在粒细胞缺乏阶段给予泊沙康唑悬液口服预防真菌感染。移植物抗宿主病(graft-versus-host disease,GVHD)预防方法采用半量后置环磷酰胺(25 mg/kg,+3~+4 d)联合环孢素(cyclosporine,CsA)/吗替麦考酚酯(mycophenolate mofetil,MMF)方案,CsA浓度维持在100~300 μg/L。
1.3BKV感染、HC的诊断和治疗 干细胞移植前供受者均进行血清、尿样本的CMV、EBV和BKV抗原、抗体筛查,阳性者接受2周以上阿昔洛韦抗病毒治疗,干细胞输注完成后给予静脉输注丙种球蛋白(5 g,3次/周)预防感染。采用定量PCR每周对受者进行血清CMV-DNA、EBV-DNA和BKV检测一次。当患者出现尿急、尿痛、肉眼血尿等典型临床表现,尿液和血液中BKV-DNA拷贝数≥103copies/ml,则确认为BKV感染[10],立即给予丙种球蛋白输注(5 g,1次/d),免疫抑制剂减量,阿昔洛韦抗病毒,来氟米特口服和碱化尿液,利尿止血等治疗措施。直至患儿症状消失,BKV-DNA连续3次以上检测阴性。HC:多见于造血干细胞移植后,常与病毒感染及GVHD相关。典型临床表现为尿频、尿急、尿痛和血尿[11]。
2 结果
2.1BKV相关HC的发生率 62例患儿干细胞植入成功,干细胞植入率达100.00%,植入成功后至少随访12个月以上,无移植相关的死亡病例。62例接受干细胞移植儿童中发生HC 14例,发生率为22.58%(14/62)。14例患儿尿液中均检出BKV,BKV copies最高达107/ml,HC与BKV感染符合率为100.00%。
2.2BKV相关HC的临床特征 诊断BKV感染的HC儿童14例。其中12例患儿表现为尿频、尿痛和肉眼血尿;2例患儿初始表现为会阴区剧烈疼痛,尿常规检查发现血尿并逐渐加重。1例出现发热,未合并严重咳嗽、呕吐和腹泻症状。出现BKV感染的HC最早时间为+27 d,最迟时间为+50 d,泌尿系症状持续时间为7~16 d,未出现BKV感染相关的死亡病例。以尿标本检出一定量BKV病毒拷贝数为诊断标准,确诊后立即启动治疗,主要治疗措施是停用MMF,改用来氟米特,减低CsA浓度,水化、碱化和利尿止痛。治疗1~2周后患儿症状消失,复查血清学和尿液BKV阴性,临床治愈率为100.00%。
2.3BKV相关HC影响因素分析 在单因素分析中,BKV相关HC组与非BKV相关HC组的配型结果及Ⅱ~Ⅳ度aGVHD、广泛型cGVHD发生率比较差异有统计学意义(P<0.05)。见表2。以患儿HLA配型、aGVHD及cGVHD发生情况为自变量,以干细胞移植后是否发生BKV相关HC为因变量,多因素logistic回归分析结果显示,非亲缘全相合及aGVHD、cGVHD是地贫儿童干细胞移植后发生BKV相关HC的影响因素(P<0.05)。见表3。
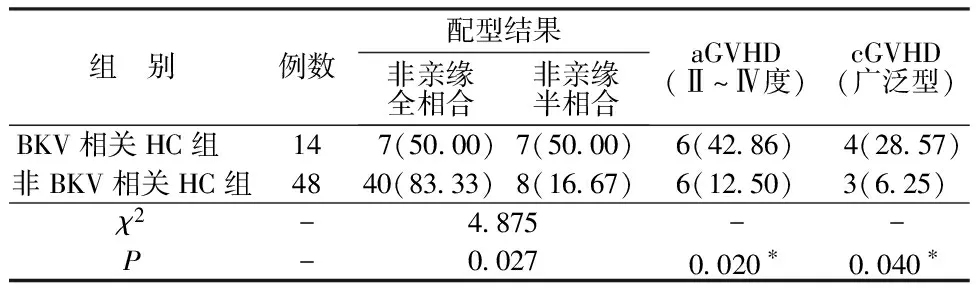
表2 BKV相关HC组和非BKV相关HC组配型结果及GVHD发生率比较[n(%)]

表3 地贫儿童干细胞移植后发生BKV相关HC影响因素的多因素logistic回归分析结果
3 讨论
3.1有研究结果显示,BKV感染是干细胞移植后HC发生的最主要原因,大剂量的化疗药物预处理和免疫抑制剂的使用是BKV感染的诱因,由于化疗药物和免疫抑制剂的使用,潜伏在泌尿系统上皮的BKV被激活,导致了HC的发生[12],严重影响了移植受者的生存质量。虽然通过移植前的病毒筛查可以明确血液、泌尿系统BKV的存在,但目前没有证据显示提前的抗病毒治疗可以减少BKV相关膀胱炎发生,某些药物和预防性措施疗效有限,特别是对于儿童患者资料有限[13],有必要对BKV感染相关因素进行分析,为本病的预防提供参考。
3.2据文献报道,儿童干细胞移植后HC发生率约为20%[14-15]。但国内儿童移植,特别是非恶性疾病(如地贫)儿童干细胞移植后BKV相关HC的发生率鲜见报道。文献报道儿童年龄与HC发生有关,与性别关联性不显著[16-17]。本文研究结果初步证实,地贫儿童接受非亲缘移植后HC发生率为22.58%,均存在泌尿系统BKV感染,由于没有同时监测患儿血清BKV感染的情况,其是否同时存在血清BKV阳性无法证实。经过转换免疫抑制剂、碱化、水化和利尿止痛治疗1~2周后,全部患儿尿BKV检测阴性,同时血清学检测阴性,治愈率为100.00%。因此,BKV活化是儿童干细胞移植后HC的最主要原因,通过一般性治疗、转换免疫抑制和对症处理能够安全度过感染期,无死亡病例发生。
3.3本研究结果显示,在预处理方案相同情况下,非亲缘移植儿童BKV相关HC的发生与GVHD发生具有关联性,aGVHD和cGVHD均是诱发BKV感染的危险因素。大样本的研究结果显示,82.8%的Ⅱ~Ⅳ度GVHD的移植受者儿童合并有BKV相关HC[18-19]。其原因可能是强烈的免疫抑制疗法促进了CMV和BKV的激活、复制,导致了BKV相关HC发生。本研究结果也验证了这一点。虽然已经有BKV相关HC患者的死亡报告,但本文结果与大部分临床研究结果一致,多数儿童预后良好[20-21]。因此,虽然对于本病的预防仍缺乏有效的措施,但是基于临床症状的早期识别和及时的免疫抑制剂调整、转换,碱化和强迫利尿等治疗,患儿均能获得治愈,没有再次发作的病例。所以,减轻预处理强度和减少免疫抑制剂的使用,控制GVHD的发生时间是减少BKV感染,预防HC发生的有效措施。对于儿童非恶性疾病的移植,非清髓性预处理和新的GVHD预防措施的使用有利于改善儿童患者移植后生存。
本研究结果初步证实,BKV相关HC是儿童干细胞移植后常见的并发症之一,典型的临床表现和血、尿标本的BKV抗原检测可作出明确诊断。移植后GVHD是BKV相关HC发生的危险因素。经过调整免疫抑制剂以及积极对症治疗,患者可获得良好预后。降低化疗预处理强度,积极防控GVHD可以减少BKV相关HC发生。由于本研究属于回顾性研究,收集病例数有限,需要大样本的临床研究进一步验证,提出有效的防治策略。

