内脏型肥胖男性患者血清25羟维生素D与早期颈动脉粥样硬化的相关性研究
朱 晶,郭峻臣,毕 兵,吴礼贤,申利平,刘 韬,潘贤翠,郭久畅
(1.四川省自贡市第一人民医院健康管理中心,四川 自贡 643000;2.四川省富顺县人民医院骨二科,四川 自贡 643000)
长期以来,以动脉粥样硬化(atherosclerosis,AS)为主要病理基础的心脑血管疾病发病率及死亡率居高不下,严重威胁着人们的生命。颈动脉粥样硬化(carotid atherosclerosis,CAS)一般较冠状动脉粥样硬化更早出现,同时也是脑卒中、心血管事件强有力的预测因子[1],因此早期诊治尤为重要。研究证实脂肪分布的差异对心血管产生不同程度的影响,与皮下脂肪相比,内脏脂肪堆积更易导致心血管疾病的发生[2];过量的内脏脂肪还可能会导致维生素D缺乏[3],而维生素D受体广泛分布于心、脑、血管、脂肪细胞等器官或组织,低水平的维生素D可能通过调节脂代谢、影响血管张力及血管平滑肌细胞增殖等多种机制参与AS及心脑血管病的发生发展[4],由此可见,维生素D、脂肪代谢、AS互相调节,彼此影响。目前内脏型肥胖状态下血清维生素D水平是否对颈动脉仍存在影响鲜有报道,颈动脉内中膜增厚和粥样硬化斑块形成被认为是CAS的早期标志[5,6],故本研究通过观察男性内脏型肥胖合并早期颈动脉粥样硬化(Early carotid atherosclerosis,ECAS)患者血清25羟维生素D[25(OH)D]水平,分析该类人群血清25(OH)D与ECAS的相关性,以期为ECAS的防治提供参考。
1 资料与方法
1.1 一般资料2021年1月至2022年12月自贡市第一人民医院健康体检的男性内脏型肥胖人群264例。纳入标准:年龄40~70岁,男性,符合内脏型肥胖的诊断标准[7]。排除标准:既往有高血压、糖尿病及心脑血管疾病者;合并自身免疫系统疾病、其他内分泌疾病及恶性肿瘤者;合并急、慢性感染者;妊娠、哺乳期者;3个月内使用过钙剂、维生素D及类似物等者;吸烟及长期大量饮酒者。内脏型肥胖的诊断标准符合2021年《超重或肥胖人群体重管理流程的专家共识》的诊断及评价标准:人体成分检查提示内脏脂肪面积(visceral fat area,VFA)>100 cm2为内脏型肥胖[7];ECAS定义为颈动脉内中膜的增厚或动脉粥样硬化斑块形成,测量颈总动脉、颈动脉分叉处及颈内动脉起始处动脉内膜中层厚度(intima-media thickness,IMT)<1.0 mm为正常,IMT≥1.0 mm为增厚,局限性IMT≥1.5 mm并超过周围IMT的50%定义为斑块形成[4~6]。根据内脏脂肪面积(VFA)及CIMT将所有受检者分为:单纯内脏型肥胖组(VO组)及内脏型肥胖合并早期动脉硬化组(VO-ECAS组);根据中华医学会骨质疏松和骨矿盐疾病分会提出的标准将维生素D水平分为充足[25(OH)D≥30 ng/ml],不足[20 ng/ml≤25(OH)D<30 ng/ml]、缺乏[25(OH)D<20 ng/ml]及严重缺乏[25(OH)D<10 ng/ml][8]。根据血25(OH)D的四分位数进行维生素D水平分级,将受检者分为Q1组[25(OH)D ≥24.70 ng/ml]、Q2组[19.70 ng/ml≤25(OH)D<24.70 ng/ml]、Q3组[16.10 ng/ml≤25(OH)D<19.70 ng/ml],Q4 组[25(OH)D<16.10 ng/ml]。本研究经本院伦理委员会批准,研究对象均签署知情同意书。
1.2 方法采集受试者身高、体重、收缩压、舒张压数据,计算BMI。全部受试者禁食至少8 h,于次日晨8点,空腹状态采集肘静脉血测空腹血糖、总胆固醇、甘油三酯、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low density lipoprotein cholesterin,LDL-C)、尿酸、25(OH)D;采用已糖激酶法测定空腹血糖,采用Olympus (AU2700)全自动分析仪分析生化指标,采用质谱法测定血清25(OH)D。内脏脂肪面积(VFA)测量:由同一名专业医师完成检测。受检者于空腹状态下排空大小便,仰卧位,暴露手腕、腹部及脚踝处皮肤,安装手腕和脚踝电极夹及腹部腰带,于平静呼气末屏气采用内脏脂肪测定仪测量VFA(生物电阻法,欧姆龙,型号HDS-2000)。CIMT测量:由同一彩超医师采用彩色多普勒超声仪(飞利浦,型号EPIQ5c,探头频率:10.0 MHz)测量颈总动脉、颈动脉分叉处及颈内动脉起始处IMT,分别测量3次取平均值。
1.3 统计学方法使用SPSS 22.0软件进行统计学分析。正态分布计量资料以均数±标准差表示,两组间比较采用独立样本t检验;采用卡方检验进行率的比较,双变量采用Pearson相关分析;二元Logistic回归分析男性内脏型肥胖患者发生ECAS的相关因素。P<0.05为差异有统计学意义。
2 结果
2.1 一般情况入组人群年龄(54.20±8.30)岁,维生素D水平为(20.93±6.91)ng/ml,其中维生素D充足者23例(8.71%),不足者104例(39.39%),缺乏者127例(48.11%),严重缺乏者10例(3.79%)。
2.2 VO组及VO-CAS组临床资料和实验室指标比较两组间年龄、BMI、舒张压、总胆固醇、LDL-C、尿酸及VFA差异均无统计学意义(P>0.05);与VO组相比,VO-ECAS组收缩压、空腹血糖、甘油三酯水平明显增高,血清25(OH)D、HDL-C水平明显降低(P<0.05)。见表1。
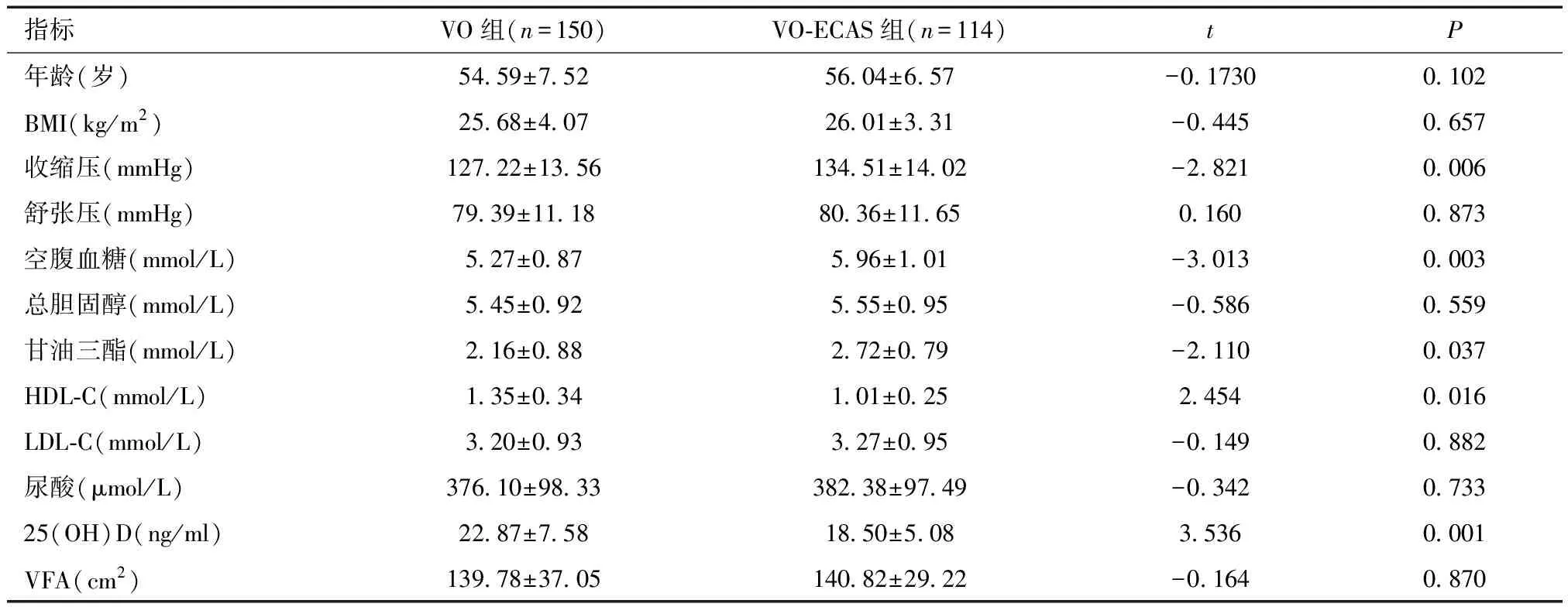
表1 两组间临床资料和实验室指标比较
2.3 Q1、Q2、Q3、Q4组ECAS患病率比较Q1、Q2、Q3和Q4组ECAS患病率分别为24.24%、46.97%、51.52%和65.15%,组间差异有统计学意义(P<0.05)。
2.4 男性内脏型肥胖患者血清25(OH)D与各指标的相关性Person相关分析显示,内脏型肥胖患者血清25(OH)D与SBP、FPG、TG、VFA及BMI呈负相关(P<0.05)。见表2。

表2 男性内脏型肥胖患者血清25(OH)D与其他指标的相关性分析
2.5 男性内脏型肥胖患者发生ECAS相关因素的Logistic回归分析以男性内脏型肥胖患者是否合并ECAS为因变量,以25(OH)D水平(Q1、Q2、Q3、Q4=0、1、2、3)、收缩压、BMI、空腹血糖、甘油三酯为自变量,进行Logistic回归分析。结果显示:BMI、收缩压、空腹血糖、甘油三酯及低水平的维生素D[25(OH)D<24.70 ng/ml]是发生ECAS的独立影响因素。校正年龄后,BMI、收缩压、空腹血糖、甘油三酯及低水平的维生素D仍是内脏型肥胖的患者发生CAS的影响因素(P<0.05),与Q1组相比,Q2、Q3、Q4组发生CAS的可能性分别是Q1组的4.038、5.883、12.248倍。见表3。

表3 男性内脏型肥胖患者发生CAS相关因素的Logistic回归分析
3 讨论
心脑血管疾病是全球范围内死亡率最高的疾病,且已呈现出年轻化趋势[9],有效扼制早期AS的发生发展具有重大意义。过量蓄积的内脏脂肪是AS的不容忽视的危险因素[10],与皮下脂肪相比,内脏脂肪的分解过程更为活跃,大量的游离脂肪酸分解释放入血,将加剧血管壁脂质沉积与内皮氧化[11];此外,内脏脂肪会分泌大量的促炎因子,使得血管内皮遭受更严重的氧化应激和炎症反应,故较均一性肥胖而言,内脏型肥胖者有着更高的AS罹患风险[12]。既往研究报道,内脏型肥胖者广泛存在维生素D缺乏或不足[13],本研究结果与之一致,同时低水平的维生素D也是CAS的独立危险因素,而目前内脏型肥胖患者血清25(OH)D水平与ECAS关系的研究较少。
本研究发现,内脏型肥胖患者合并ECAS者血25(OH)D水平较未合并者明显降低,且随25(OH)D下降程度加重,ECAS患病率逐渐上升,提示低水平的25(OH)D与ECAS的发生发展可能存在关系。Person相关分析显示:内脏型肥胖者血清25(OH)D与BMI、收缩压、空腹血糖、甘油三酰、VFA呈负相关,提示在内脏型肥胖的患者中,低水平25(OH)D可能加重内脏型肥胖,促使血压上升及糖脂代谢紊乱,与文献报道一致[14];而血流动力学紊乱、脂毒性、糖毒性及肥胖导致的低度炎症反应等危险因素都可能触发血管内皮细胞内质网应激,对AS的进展产生关键影响,从而促进ECAS的发生发展[15]。另有研究发现,受损的血管内皮高度表达维生素D受体(VDR),活化的维生素D与之结合后可调节血管内皮生长因子启动子中的元件来修复受损血管[16];而内脏型肥胖患者由于内脏脂肪过量蓄积及脂肪细胞肥大,维生素D的血清浓度和生物利用度均明显降低[17],我们推测这将导致血管修复能力明显下降。此外,循环25(OH)D浓度降低会导致血管平滑肌细胞钙离子通道关闭,导致钙离子在平滑肌细胞中沉积[18];较高浓度的血清维生素D不仅可以直接参与血管修复,还可明显降低细胞因子和粘附分子的表达,减少脂质及过氧化物沉积[19,20],从而有效保护血管。本研究回归分析也显示,血压、血糖和血脂的上升和25(OH)D水平的下降可能是内脏型肥胖患者患ECAS的独立影响因素,同时本研究对25(OH)D水平分级还发现,25(OH)D水平下降到一定程度(<24.70 ng/ml)是ECAS的独立影响因素,越低水平的25(OH)D对ECAS的影响可能更大。
综上,本研究显示男性内脏型肥胖者血清25(OH)D水平较低,较低水平25(OH)D可能是该类患者罹患ECAS的影响因素。由于内脏脂肪堆积导致维生素D受体分布和细胞内酶活性等改变,补充维生素D是否能使ECAS结局逆转尚待更深入的探索,维生素D在ECAS中扮演的角色是预防性还是兼有治疗性的尚未明朗。此外,本研究为减少混杂因素的影响,仅研究了男性患者,针对不同年龄段的内脏型肥胖女性维生素D水平与ECAS的相关性还需进一步探索。

