纳米片状CuCo2O4的合成及析氧性能研究
高志永,胡战强
(河南师范大学 化学化工学院,河南 新乡 453007)
氢燃料是一种高能量密度、零污染能源载体,可用于太阳能、风能等间歇能源的储存、转化和开发利用[1-2],实现低碳生活.规模化产氢对未来重型车辆[3]、机械,以及炼钢[4]、合成氨工业[5]的发展也能提供有力支撑.根据来源,氢燃料可分为灰氢和绿氢,灰氢主要是通过化石燃料的蒸汽再造,会伴随碳排放[6],而绿氢主要通过水的裂解产生,完全规避碳排放[7].很显然,绿氢更符合工业化应用的需求,已成为支撑地方经济长远发展,特别是资源型城市转型重点规划的发展方向之一,受到普遍关注.电解水具有电能利用率高和可控等特点,是绿氢生产的重要技术[8],其整个过程包括析氢和析氧(OER)两个半反应,其中OER涉及四电子四步反应,反应动力学较慢,直接制约电能利用率和产氢效率[9],开发廉价高效OER催化剂是领域内的研发重点.
RuO2和IrO2是OER的经典催化剂,但其规模化应用受制于贵金属资源和成本.铁系过渡金属元素与贵金属价层电子排布近似,其氧化物有望用作替代催化剂,应用于OER[10].一系列铁系金属氧化物[11]、氢氧化物[12]、硫化物[13]、磷化物[14]被广泛尝试用于非贵金属OER催化剂,并通过电子结构调控[15]、元素协同[16]、缺陷工程[16]等策略提高催化活性和稳定性,获得了预期效果.其中,双金属氧化物可通过金属元素之间的电荷偏移调节表观价态和价电子排布[17],优化电解质离子和各步中间体物种在金属位点的吸附能和界面电荷迁移动力学,降低OER活化能及过电位(η),从而有效提高电解水产氢性能.尖晶石相过渡金属氧化物是一类高活性、高稳定性OER催化剂,其结构由+2价金属与4个晶格氧形成的四面体几何位和+3价金属与6个晶格氧配位的八面体几何位共同组成,其中八面体[MO6]n-位点中心金属d轨道在晶体场作用下发生能级分裂,当eg轨道电子占据接近1.2时[18-19],含氧反应物及中间体在该位点具有最合适电子云重叠程度和吸附强度,有助于多步反应的进行,从而提供最佳OER性能.通过+2价金属元素掺杂取代四面体位点,可以有效调控八面体位点中心金属eg轨道电子占位率、金属-氧键的共价性和晶格畸变演化,促进决速步中间体的形成,有效提高OER催化活性.Co3O4是一种典型的尖晶石相氧化物,具有良好OER催化性能;Cu元素在化合物中一般呈现+2价态,将Cu掺入Co3O4晶格形成双金属氧化物(CuCo2O4),有望优化活性八面体Co位点的电子构型,获得良好OER催化活性.进一步通过催化剂形貌调控,优化可接触表面积和传质速率,可更大幅度提高OER催化性能和总体电解水效率.
本文通过水热反应和高温热解,合成了CuCo2O4纳米片催化剂,用于OER催化.得益于其片层结构及丰富的表面O缺陷,该催化剂能提供较高电化学活性面积和良好电解质传质速率,降低η并加快反应速率,同时能保持良好催化稳定性,可用作高活性和耐用OER催化电极.本工作可为高性能OER催化剂的设计提供可行方案,有望在电解水绿氢制备方面获得良好性能.
1 实验部分
1.1 催化剂的制备
称取15 mmol Co(NO3)3·6H2O(4.36 g)及15 mmol Cu(NO3)2·3H2O(3.62 g),溶解于30 mL去离子水中,形成溶液A.同时,称取7.7 mmol Na2CO3(4 g)溶于30 mL去离子水中形成溶液B.在搅拌条件下将溶液A缓慢加至溶液B中,形成均匀混合溶液.将该混合溶液转移至聚四氟乙烯内衬的反应釜中,置于100 ℃烘箱中水热处理24 h.冷却后将沉淀物分别用水和乙醇洗涤,60 ℃干燥过夜,获得CuCo LDH前驱体.最后将该前驱体置于马弗炉中,350 ℃下空气气氛煅烧2 h将其转化为CuCo2O4,标记为:CuCo2O4-1.将溶液A中Cu(NO3)2·3H2O的剂量分别改为7.5 mmol(1.81 g)和5 mmol(1.21 g),采取同样方法分别合成CuCo2O4-2和CuCo2O4-3样品.
1.2 材料表征
采用扫描电镜(SEM,Hitachi SU-8000)和能谱仪(EDS)表征样品的微观形貌和元素组成.采用X射线粉末衍射(XRD,Cu Kα radiation Bruker D8衍射仪)确认样品的物相,通过激光共聚焦Raman光谱(LabRAM,激光波长:532 nm)表征样品的化学键信息,以及X射线光电子能谱(XPS,Kratos Amicus Mg Kα radiation)分析样品表面元素组成及价态.将样品用浓硝酸溶解并用去离子水稀释,通过电感耦合等离子体质谱(ICP-MS)测试样品中Cu、Co元素比例.
1.3 电化学测试
电极的制备:称取10 mg催化剂,2 mg科琴黑,研磨成均匀的粉末,然后和40 μL Nafion溶液通过超声处理,将其分散在2 mL乙醇溶液中形成均匀催化剂墨水.然后将该墨水(约100 μL)滴涂在清洁的泡沫镍表面,控制催化剂的负载量为1 mg·cm-2.
使用CHI 660E电化学工作站(上海辰华),在标准的三电极体系中测试电极的OER性能,电解液为1 mol·L-1KOH,AgCl/Ag(内置饱和KCl电解质)为参比电极,碳棒为对电极,负载有催化剂的泡沫镍为工作电极.通过线性扫描伏安(LSV,电位扫速:5 mV·s-1,所有电位均用90%的内阻电位(IR)进行补偿)测试了电极在不同电位下的OER电流响应,所有电位(E)均采用可逆氢电极(RHE)进行校正:E(vs RHE)=E(vs AgCl/Ag)+0.197+0.059pH[20].在0.01~105Hz频率范围内,测试电极在1.5 V电位的Nyquist电化学阻抗.测试非法拉第电位区间(1.02~1.12 V)不同扫速循环伏安曲线(CV),固定电位下的半电流密度差(ΔJ/2=(J正扫-J反扫)/2)与电位扫速曲线的斜率即为双电层电容(Cdl)[20],以其作为指标衡量电极的电化学活性表面积.
2 结果与讨论
本文通过Cu、Co盐在碱性介质中的水热水解,形成CuCo LDH,并经高温热解处理转化形成CuCo2O4.借助SEM表征了不同剂量条件所制备催化剂的形貌,如图1(a-c)所示,不同Cu含量的CuCo2O4催化剂主要呈现纳米片形貌,这类形貌基本符合层状双氢氧化物热解所形成氧化物的特征.其中,CuCo2O4-1由初级纳米片交叉连接构筑(图1(a)),其片层间隙的丰富孔洞有助于电解质的充分填充渗透,可以提高传质速率;同时初级纳米片表面粗糙,有助于提供充裕的表面位点,促进界面充分反应.CuCo2O4-2展示出微米级片层结构(图1(b)),其表面较为光滑,部分片层交叉连接;CuCo2O4-3由初级纳米片单元堆叠而成(图1(c)),相对于CuCo2O4-1,其余两个样品的形貌特性可能降低可接触表面积和电子、离子传质速率,其表面催化性能可能逊于前者.图1(d)为CuCo2O4-1的EDS,该样品仅含Cu、Co、O 3种元素,表明通过水热水解及热解处理可以形成CuCo2O4.

通过XRD分析了3个样品的物相,如图2(a)所示,3个样品在18.9°、31.1°、36.6°、44.5°、59.0°和64.8°的衍射峰分别对应于尖晶石型CuCo2O4(JCPDS:80-1536)的(111)、(220)、(311)、(400)、(511)和(440)晶面,表明三者具有相同物相[21].CuCo2O4-1的(311)晶面衍射主峰较宽,表明其初级晶粒尺寸更小,有助于提供更丰富表面位点及更高催化性能.图2(b)为3个样品的Raman光谱,样品在200~900 cm-1区间出现一系列振动信号,其中276 cm-1处的宽峰归属于O-Co-O键的Eg模式伸缩振动[22];461和503 cm-1处的弱峰是由Cu空位、间充型O原子以及O缺陷引起的[22];663 cm-1处的峰归属于Co-O键的A1g模式伸缩振动[22],这些数据表明所合成样品为双金属氧化物,其结构中存在的配位不饱和金属位点及O缺陷位点有助于吸附反应物,对OER可能提供一定贡献.



图3(c)为3个样品的Cu 2pXPS图谱,位于933.6和953.5 eV附近的峰分别对应于Cu2+的2p3/2和2p1/2自旋轨道[21,24],941.5和961.5 eV处的峰为两个轨道的卫星峰,表明3个样品中Cu元素主要以+2价形式存在.其中CuCo2O4-1的2p3/2和2p1/2轨道结合能更低,这可能与氧化物表面更丰富的O缺陷有关.图3(d)为3个样品的O 1sXPS图谱,其中位于529.2 eV处的峰可归属于晶格Cu(Co)-O键,530.7 eV处的峰归属于氧化物表面的O缺陷位点,而532.2 eV处的峰归属为材料表面的吸附水[24].可以看出,样品氧化物晶格表面存在O缺陷,其不仅能降低其周围金属位点价态,尤其是Co元素价态,优化含氧反应物及中间体物种的吸附,促进界面反应,而且能提高氧化物自身导电性,对OER发挥积极作用.
鉴于这类片层交叉连接CuCo2O4的多孔结构,Co元素双重价态以及表面O缺陷带来的导电性,此类双金属氧化物有望用作高性能OER催化剂,提高电解水产氢的能量效率.因此,采用三电极体系探讨了这类CuCo2O4催化电极在碱性电解质中的OER性能.图4(a)比较了3个电极在1 mol·L-1KOH电解质体系中5 mV·s-1扫速的LSV曲线,所有电极在1.45 V附近出现一个弱的氧化峰,这主要来源于Co、Cu元素的氧化反应,随后更高电位下的强电流响应归因于OER,其中CuCo2O4-1电极的OER响应更早,表明其更低的OER过电位.当J=10 mA· cm-2时,CuCo2O4-1电极的η(标记为η10)为243 mV,体现出良好OER活性,其η10值优于或接近于已报道的Co、Cu基催化电极(表1)[25-30],显示出其在OER催化方面的竞争力.在更高OER电流密度情况下,J=100 mA·cm-2时,CuCo2O4-1电极的η为362 mV,优于CuCo2O4-2电极的376 mV及CuCo2O4-3电极的368 mV,可以看出,CuCo2O4-1具有最佳OER催化效率,其最低η值可以降低电解水产氢电压.以η与OER响应电流密度对数(lgJ)作图可以获得塔菲尔曲线(图4(b)),塔菲尔曲线斜率值反映电流增大或者减小10倍时所需过电位的变化,亦即催化动力学;塔菲尔斜率越小,则反应动力越快.由图4(b)可知,CuCo2O4-1、CuCo2O4-2和CuCo2O4-3电极的塔菲尔斜率分别为112.2、148.8及160.6 mV·dec-1.CuCo2O4-1电极的最小塔菲尔斜率表明其拥有最快的OER反应动力学[20],有利于高电位下更充分快速反应.
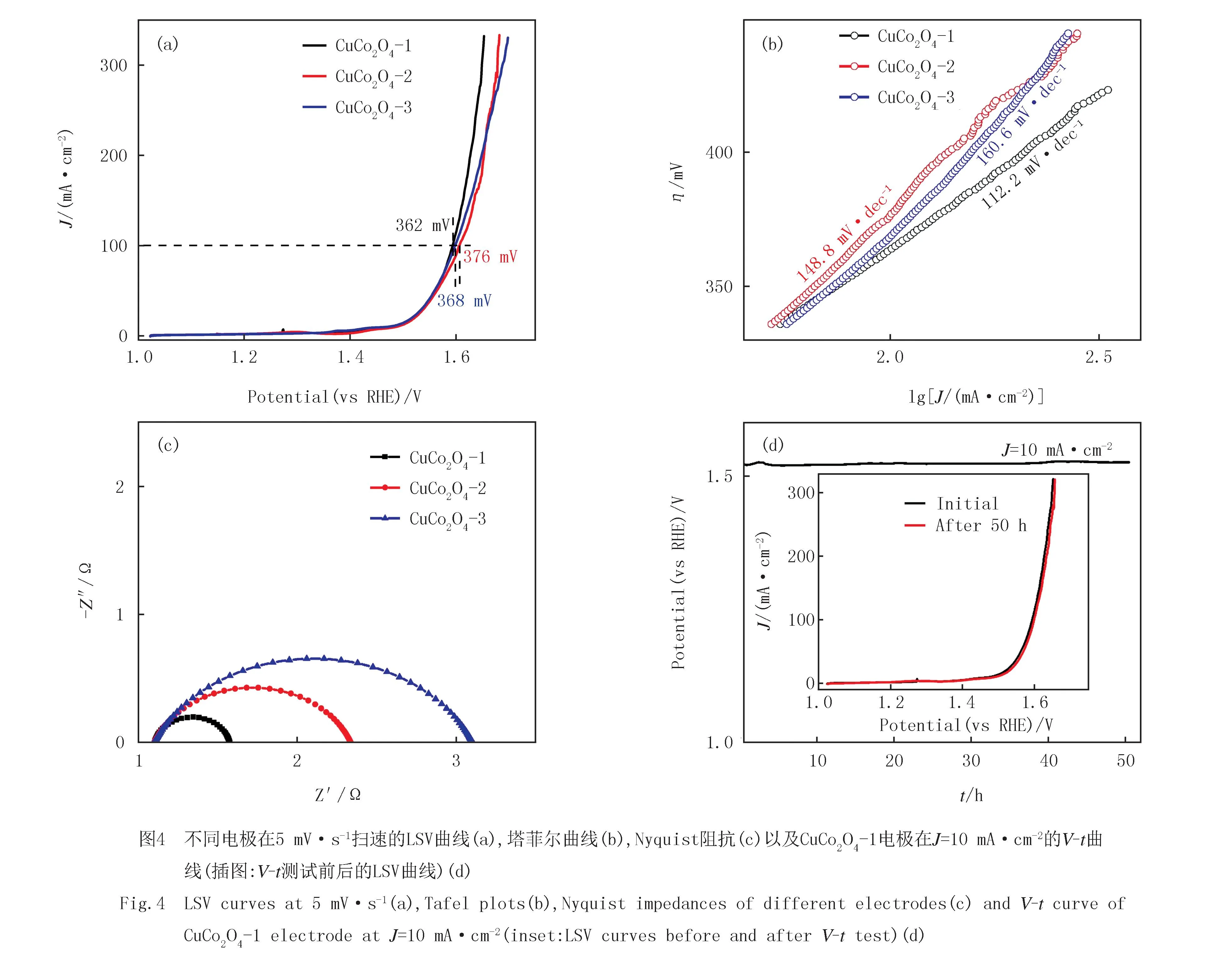

表1 不同Co、Cu基催化电极的过电位和塔菲尔斜率参数比较Tab. 1 The comparisons on overpotentials and Tafel plots of Co,Cu based catalytic electrodes
图4(c)为3个电极的Nyquist阻抗图,3个电极均展示出几乎相等的高频端实轴截距及明确的高频圆弧.Nyquist阻抗高频端实轴截距代表电极的串联阻抗,包括电极材料自身电阻,电极材料与集流体接触电阻及电解质离子电阻,3个电极的相同串联电阻主要归因于催化剂的相同物相及相同电极制作工艺[31].高频圆弧直径代表电极-电解质界面电荷转移电阻(Rct),反映OER的难易程度,Rct越小说明更充分快速界面反应[31].3个电极的阻抗主要差别在于Rct,根据圆弧直径,CuCo2O4-1、CuCo2O4-2和CuCo2O4-3电极的Rct分别为0.5、1.2及2.0 Ω,CuCo2O4-1的最低Rct表明其界面的最充分快速OER,因此该电极具有最佳催化性能.
为了进一步确定电极可接触表面积对OER的贡献,测试了各个电极在非法拉第电位区间不同扫速下的CV曲线,并借此衡量电极的双电层电容(Cdl)[24],如图5(a-c)所示,所有CV曲线均显示出良好的矩形,都表现出双电层电容特性;根据ΔJ/2与电位扫速的曲线斜率(图5(d)),CuCo2O4-1,CuCo2O4-2及CuCo2O4-3电极的Cdl值分别为73.0,67.3和50.0 mF·cm-2,显然,CuCo2O4-1电极能提供更大可接触表面积,在OER反应过程中能够提供更多的活性位点,很大程度上提高催化效率.OER稳定性也是评价电极催化性能的一个重要指标,因此采用J=10 mA·cm-2的计时电位(V-t)曲线评估了CuCo2O4-1电极的催化稳定性(图4(d)),经过50 h测试,电极的电位几乎没有增加,表明该电极具有良好OER稳定性.V-t测试前后该电极的LSV高度重合,也进一步表明该电极的良好OER稳定性.根据上述电化学性质,CuCo2O4-1可用作高活性及高稳定性OER催化电极.

3 结 论
通过水热反应及高温热解合成了CuCo2O4,该材料呈现出由粗糙表面片层交叉连接形成的多孔结构,可提供快速电解质传质通道及较高可接触表面积.同时该材料表面含有丰富O缺陷,能有效调节周围金属位点价态,优化价层电子填充,并能保证较高导电性,这些结构和表面特性有助于提升相应电极的电催化性能.电化学测试表明,所制作CuCo2O4-1电极表现出良好的OER性能,在J=100 mA· cm-2时的η为362 mV,并拥有良好的OER稳定性.本研究为高性能OER催化电极设计,以及进一步提升电解水制备绿氢的能量效率提供了可行途径.

