CCD无损测量生物组织光学参数的实验研究
杨 丽,孙建华,张连顺
(中国民航大学理学院,天津 300300)
激光与生物组织间的相互作用规律是激光生物医学的应用基础和前提,激光在生物组织中的衰减主要包括光子的被吸收和被散射,通常以吸收系数和有效散射系数来表示。确定组织体尤其是人体组织的光学特性参数,即吸收系数μa、有效散射系数μs′和散射相位函数或散射各项因子g以及折射率n等是生物医学光子学中的关键性工作[1]。漫反射光在组织表面的分布是由组织的光学特性确定的,可以通过测量生物组织表面漫反射光的分布来研究生物组织本身的光学特性[2]。测量组织表面的漫反射光分布的方法主要有:光纤逐点扫描法和CCD视频摄像测量法。传统的光纤逐点扫描存在如下问题:测量时间较长,测量过程中光纤与组织表面的距离可能发生变化;近光源区的光分布无法测量;集成光纤阵列接触组织表面测量,组织表面会因受压而对组织的实际生理状态产生一定的影响。用CCD测量生物组织表面的漫反射光、透射光分布是20世纪90年代出现的新技术[3]。从原理上,CCD视频摄像技术具有易于控制、效率较高的优点,并且可以测量近光源区的光强空间分布。R.A.Bolt[4]运用CCD测定了一些生物组织模型的反射率随位置的分布,Alwin Kienle[5]测定了牛肌肉、牛肝、牛脂肪和鸡胸肉的反射率,在处理方法上,R.A.Bolt和Alwin Kienle按照漫射理论和随机游走理论推算出了样本的光学特性参数[4-5],但所采用的光路和处理方法比较复杂。
在本研究中,简化了上述两人的测量光路,用二维CCD测量装置以及配套的图像处理软件测量了生物组织模拟液(Intralipid-20%稀释液)表面的漫射光分布,实验所得的结果与Monte Carlo模拟所得的结果做了比较,对比的结果显示两者在10mm范围内的符合程度较高,证明了所设计装置的合理性。通过漫射近似理论所获得的表面漫射光分布的解析表达式对实验结果进行了Matlab非线性拟合,反演获得了生物组织模拟液的光学参数,实现了光学参数的无损测量。
1 CCD实验装置及测量方法
用CCD测量生物组织空间分辨的漫射光分布的装置如图1所示。He-Ne激光器发出的激光光束(波长632.8 nm,功率为11.13 mW)经衰减器、光栏(φ=1.0 mm)、反光镜和聚焦透镜以较小的入射角(5°~10°)入射到组织样品的表面上,小的入射角可避免垂直入射时样品表面的镜面反射对CCD成像的影响。由于CCD摄像所需的入射光功率较小,一般在1~100 μW范围内,因此用光衰减器对入射光束功率进行衰减以防止CCD饱和;凸透镜用于改变入射光的光束直径,实验选用的光束直径φ=1 mm。测量所用CCD为150CLM型数码显微镜用冷却型,分辨率为1 392×1 040像素,灵敏度设置为200,曝光时间设置为1/10s。光束入射到组织样品表面其漫反射光形成以入射光束入射点为中心光强逐渐向外衰减的圆形分布,由二维CCD探测器对其成像,CCD输出图像数据馈送到CCD控制器进行存储和简单计算,再送计算机作进一步的图像分析和处理。
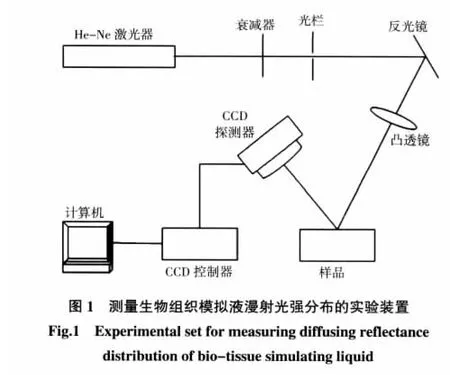
实验采用了与CCD配套的图像分析系统Simple-PCI(Hamamatsu公司开发)对CCD摄取的漫反射光图像进行处理和分析,以更简便、更迅速及更准确的方法再现、收集、分析图像的细节。
标定的方法是在被拍摄的组织样品表面的位置安装毫米刻度的标尺,用拍摄组织样品的方法拍摄标尺的图像,由图像可以确定标尺的某一长度与像素的比例关系。
实验所用样品为生物组织模拟液(Intralipid-20%稀释液)。实验样品的制备方法是:取10 mL脂肪乳母液,加入蒸馏水稀释成100 mL。样品标记为I10。实验中样品的厚度保持30 mm。
2 测量结果与分析
2.1 样品表面漫射光分布的测量结果与分析
用CCD拍摄的样品I10表面的漫反射光分布如图2所示。图3是样品I10表面漫反射相对光强随像素点位置变化的分布图像。
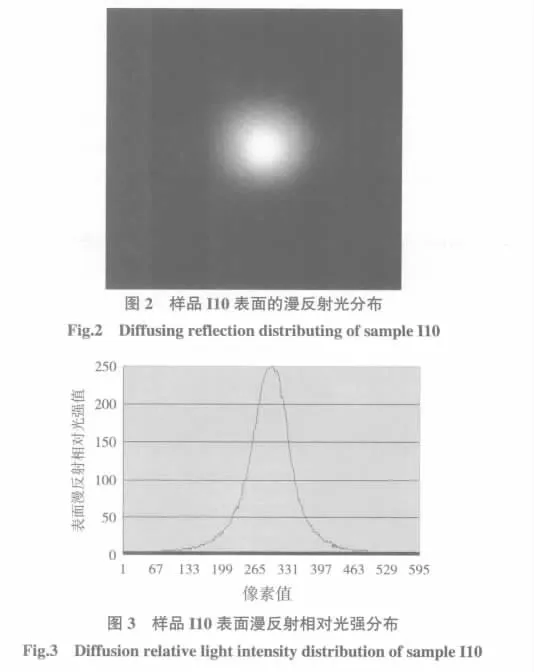
在保持样品测量条件不变的情况下用CCD拍摄了刻度尺的图像,如图4所示,由图4可以确定1 mm距离对应31个像素点,按此比例常数可以将相对光强与像素的关系换成相对光强与空间坐标的关系。

Monte Carlo模拟法首次被使用是在1983年,Wilson[6]通过该方法分析了光在生物组织中的传播。Monte Carlo方法是在假定生物组织光学特性参数的前提下,用计算机跟踪每一个入射光子的散射、吸收、以及传输过程。对大量光子进行统计、平均,最终给出光在组织内部以及表面的分布规律[7-8]。实践证明,Monte Carlo方法精度高,且其结果与生物组织的离体切片实验结果相一致[9]。Monte Carlo模拟法已成为研究光与强散射介质相互作用的非实验性标准。在本文的实验中,样品的厚度为30 mm,远大于光子在样品中散射的平均自由程,可以近似地作为半无限大介质处理,满足Monte Carlo模拟所要求的条件。
本文亦将Monte Carlo模拟结果作为标准,来检验漫反射光图像测量结果的精度。采用文献[8]中的模拟程序对高斯光束入射到样品I10的表面漫射光分布情况进行模拟,样品的光学参数选择如下[4]:μa=0.049 mm-1,μs=11.3 mm-1,g=0.75,n=1.40,光束直径 φ =1 mm。
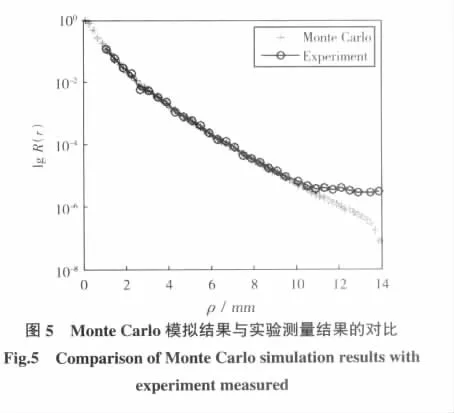
Monte Carlo模拟结果与经过软件分析,做归一化及取对数处理后的样品I10实验测量结果的对比如图5所示。
从图5的对比可以看出:在距离光束中心10 mm的范围内两者具有较高的一致性,但在距离光束中心10 mm以外两者出现偏差,实验测量值趋于不变,而Monte Carlo模拟值仍在继续减小。这是由于理论计算是以半无限大介质模型为基础,在无限远处漫反射光强必然为0;而CCD设备无可避免地存在细微的暗电流,使图像暗区的测量有一定误差,因此当测量距离光束中心超过10 mm时实验与理论偏差逐渐增大,在远离反射光强光斑中心的区域,漫射光强极其微弱,暗电流的影响也趋于明显,导致测量光强减少缓慢。
2.2 吸收系数μa和有效散射系数μs′的确定与分析
由于实验样品的尺寸远大于光子的实际传输路程,可以看作半无限大介质。根据漫射近似理论,当无限细光束垂直入射到组织表面时,在外延边界条件下,且漫射系数D取为

对于样品I10测量结果,分别利用Matlab程序做基于方程(2)的R(ρ)与ρ的非线性拟合,如图6所示,同时可以得到所测样品I10的吸收系数μa和有效散射系数 μs′。
表1是本文实验获得的吸收系数μa和有效散射系数μs′与文献[4]的比较。可见本文获得的光学参数与R.A.Bolt等报道的数据非常接近,有效散射系数μs′的误差为4.73%,吸收系数μa的误差为9.79%,显然都是在允许的系统误差范围内[13]。分析造成上述差别的原因可能有以下几方面的因素:所选用Intralipid-20%原液的生产厂商不同,液体内部颗粒的大小及均匀性会存在差异;CCD自身的暗电流以及环境中存在微小的噪声光源;由测量数据拟合反演光学特性参数所用算法带来的误差等因素的影响。
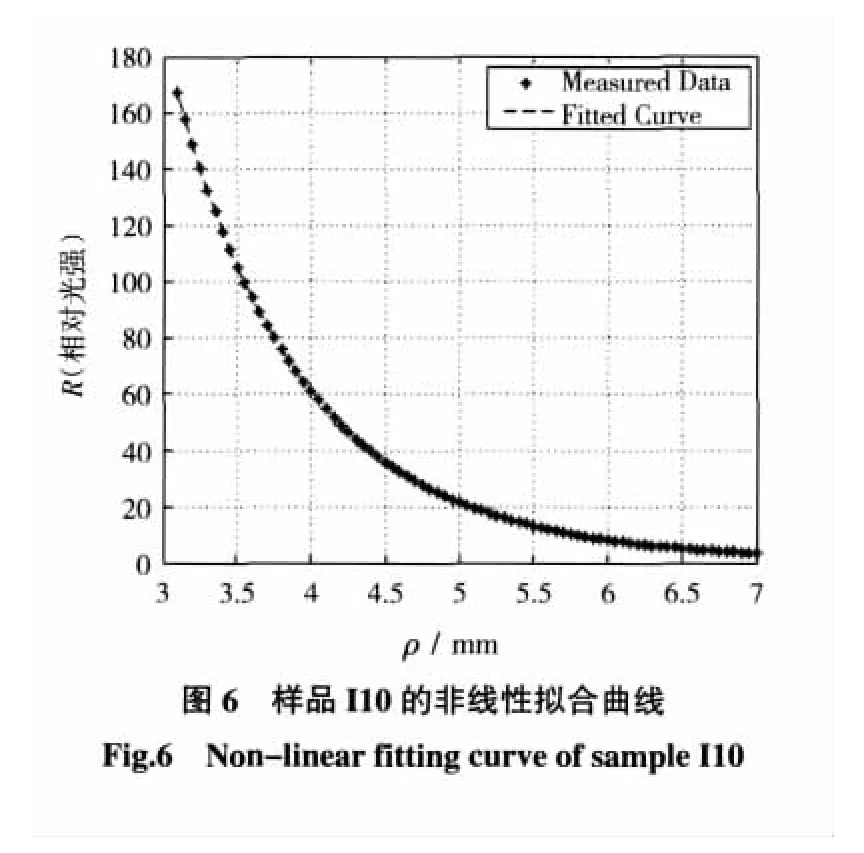

表1 测量结果与R.A.Bolt等报道的数据比较Tab.1 Comparison of experimental measurement results with that reported by R.A.Bolt,et al.
3 结语
采用CCD无损测量技术,获得了生物组织模拟液(Intralipid-20%稀释液)在连续的He-Ne激光光束照射下的表面漫射光分布图像;并以Monte Carlo模拟结果作为标准,检验漫反射光图像测量结果的精度。结果显示理论计算与实验测量结果在10 mm范围内相吻合。根据漫射近似理论对实验测量的数据进行非线性拟合,获得了生物组织模拟液的光学参数,与报道的结果进行了比较,结果表明设计的实验装置可用于生物组织光学特性参数的无损测量。CCD无损和快速取像的特点与图像分析系统Simple-PCI的配合更好地发挥了CCD在生物组织无损测量中的优势。通过实验系统和实验技术的进一步改进与完善,有望实现活体生物组织的光学特性参数的测量。
[1]KASHIMA SUSUMU.Spectroscopic measurement of blood volume and its oxygenation in a small volume of tissue using red laser lights and differential calculation between two point detections[J].Optics and Laser Technology,2003,35(6):485-489.
[2]LI ZHONG-MING,LIU XIAO-HUA.The theoretical analysis of thermal interaction between laser and bio-tissue[J].Journal of Optoelectronics·Laser,2002,13(8):860-863.
[3]SPLINTER R,NANNY G A,LITTMAN L.Monitoring tissue optical characteristics in situ using a CCD camera[J].Laser Life Sci,1994,6:15-25.
[4]BOLT R A,BOSCH J T.Method for measuring position-dependent volume reflection[J].Applied Optics,1993,32(24):4641-4645.
[5]ALWIN KIENLE,LOTHAR LILGE,PATTERSON M S.Spatially resolved absolute diffuse reflectance measurements for non-invasive determination of scattering and absorption coefficients of biological tissues[J].Appl Opt,1996,35(13):2304-2314.
[6]WILSON B C,PARK Y D,HEFETZ Y,et al.Potential of Time-Resolved Reflectance Measurements for Noninvasive Determination of Tissue Optical Properties[C]//SPIE Proceedings of Thermal and Optical Interactions with Biological and Related Composite Materials.Harpole,1989:97.
[7]WANG L H,JACQUES S L,ZHENG L Q.MCML-Monte Carlo modeling of light transport in multi-layered tissues[J].Computer Methods and Programs in Biomedicine,1995,47(2):131-146.
[8]FLOCK S T,WILSON B C,PATTERSON M S.Monte Carlo modeling of light propagation in highly scattering tissues-Ⅱ:Comparison with measurements in phantoms[J].IEEE Transaction of Biomedicine Engineering,1989,36(12):1169-1173.
[9]REBECCA SIMPSON C,MATTHIAS KOHL.Near-infrared optical properties of ex vivo human skin and subcutaneous tissues measured using the Monte Carlo inversion technique[J].Phys Med Biol,1998,43:2465-2478.
[10]ALWIN KIENLE,PATTERSON M S.Improved solutions of the steady-state and the time-resolved diffusion equations for reflectance from a semi-infinite turbid media[J].Journal of the Optical Society of America A,1997,14(1):246-254.
[11]AKIRA ISHIMARU.Wave Propagation and Scattering in Random Media[M].New York:Academic Press,1978:147-167.
[12]HASKELL R C,SVAASAND L O,TSAY T T.Boundary conditions for the diffusion equation in radioactive transfer[J].Opt Soc Am,1994,AⅡ(10):2727-2741.
[13]XU HE-PING,MICHAEL S PATTERSON.Determination of the optical properties of tissue-simulating phantoms from interstitial frequency domain measurements of relative fluence and phase difference[J].Optics Express,2006,14(14):6485-6501.

