肉桂酸制备实验的改进*
曹燕明 夏加亮 罗燕花 冼银桃 曾梓诚 林三清 徐春曼
(湛江师范学院化学科学与技术学院 广东湛江524048)
肉桂酸是一种重要的精细化工合成中间体,被广泛应用于医药、香料、塑料、感光树脂、食品添加剂等精细化学品的制备。肉桂酸的合成方法较多,主要有Perkin法、苯乙烯-四氯化碳法、苯甲醛-丙二酸法、苯甲醛-乙烯酮法、肉桂醛氧化法、氯代芳烃-丙烯酸及其衍生物法等[1]。
在很多大学有机化学实验教材中,将Perkin反应制备肉桂酸作为有机化学实验教学的重要内容[2]。实验过程为:苯甲醛和乙酸酐在无水碳酸钾存在下加热反应一定时间制备肉桂酸。由于苯甲醛易被氧化为苯甲酸,而苯甲酸很难与肉桂酸分离,故实验中对苯甲醛的清除直接影响肉桂酸的纯度。教材中多用水蒸气蒸馏的方法清除未反应的苯甲醛,再用碱溶解残留液,最后酸化析出肉桂酸粗产物,经重结晶得到产品。为简化实验过程,很多教材采用简单的水蒸气蒸馏,即向反应体系中加入足够的水后直接将回流装置改为蒸馏装置。但在实际学生实验过程中,常出现以下问题:(1)由于苯甲醛在直型冷凝管中的滞留,难以实现对蒸馏终点的准确判断,过早结束会有苯甲醛残留,结束晚了又会浪费时间和能源;(2)水蒸气蒸馏后残留物会结成硬块,碱化时很难将其捣碎,常有学生在这个过程中损坏玻璃棒、圆底烧瓶等仪器,甚至受伤;(3)粗产品颜色偏黄,需进行脱色和重结晶处理;(4)碱化溶解时,由于加入的氢氧化钠溶液体积较大,接下来进行活性炭脱色时易暴沸;(5)若改水蒸气蒸馏,搭建仪器和蒸馏都需要较长时间。
通过化学反应进行除杂和纯化产物,是化学合成中的重要方法,但在大学有机化学实验的教材和教学中,这种方法很少得到体现。本文介绍的方法利用了氨水与苯甲醛的反应性[3]及其碱性,可以同时清除苯甲醛和溶解肉桂酸,简化了实验步骤,提高了实验的可操作性。在实验中引入了化学除杂的方法,丰富了有机化学实验教学的内容,有利于培养学生分析和解决问题的能力。
1 实验目的
掌握高温反应和空气冷凝管的使用方法及安装、操作;掌握Perkin反应的原理;学习并掌握化学除杂方法的设计与应用;学习并掌握回流、重结晶、过滤等实验技术。
2 实验原理
芳香醛和酸酐在碱性催化剂作用下,发生缩合,生成α,β不饱和芳香酸的反应称为Perkin反应。催化剂通常是相应酸酐的羧酸钾或钠盐,有时也可以用碳酸钾或叔胺等碱性试剂代替。用碳酸钾代替乙酸钠来合成肉桂酸,操作方便,缩短了反应时间,收率也能有所提高。
该反应的化学方程式见图1。

图1 Perkin反应制备肉桂酸的反应方程式
碳酸钾的催化机理尚不清楚,可能是体系中的少量水使乙酸酐水解,继而与碳酸钾反应生成乙酸钾,乙酸钾催化反应的机理如图2所示。

图2 乙酸钾催化Perkin反应的反应机理
Perkin反应得到的主要是反式肉桂酸(熔点:133℃);顺式异构体(熔点:68℃)不稳定,在加热条件下很容易转变为热力学更稳定的反式异构体。
在反应后,对未反应的苯甲醛的清除会直接影响肉桂酸的纯度。本实验采用化学反应清除苯甲醛。氨水与苯甲醛反应生成水不溶性席夫碱沉淀,同时氨水与肉桂酸发生中和,生成水溶性盐;故通过过滤可实现对苯甲醛的清除。反应方程式见图3。

图3 氨水与苯甲醛及肉桂酸的反应方程式
3 仪器与试剂
仪器:三口烧瓶、烧杯、空气冷凝管、干燥管、锥形瓶、布氏漏斗、抽滤瓶、玻璃棒、量筒、滤纸、恒压滴液漏斗、滴管、表面皿、温度计、电热套、磁力搅拌器。
试剂:无水碳酸钾、新蒸苯甲醛、新蒸乙酸酐、浓盐酸、10%氨水、无水氯化钙、pH试纸。
4 实验步骤
(1)制备:在100mL三口瓶中加入3.0mL(0.030mol)新蒸馏的苯甲醛、8.0mL(0.084mol)新蒸馏的乙酸酐以及研细的4.4g无水碳酸钾,振荡使其混合均匀。装上带有氯化钙干燥管的空气冷凝管,加热回流45min。
(2)提纯:待反应物稍冷,在磁力搅拌下,用恒压滴液漏斗滴加约25mL 10%氨水溶液至pH=9~10,再持续搅拌30min。随着氨水的加入,先出现大量沉淀,随后沉淀逐渐溶解,最后得淡黄色液体和少量黏稠状固体。待液体冷至室温后,用三角漏斗过滤。在搅拌下慢慢用浓盐酸将滤液调至酸性(pH<3),有晶体析出。待晶体析出完全后抽滤,用少量冷水洗涤晶体。粗产品在100℃下干燥,称重并计算收率。粗产品可用热水或乙醇与水(V(C2H5OH):V(H2O)=1:5)为溶剂进行重结晶。
5 讨论与小结
通过对改进后方法制备得到的肉桂酸与标准肉桂酸样品进行熔点对比,证明改进方法制备得到的是肉桂酸纯品。具体数据如表1所示。熔点测试使用的仪器为WRS-2A微机熔点仪(上海精科)。

表1 不同方法制备的肉桂酸的熔点测试
由熔点对比可知,通过教材所述方法和改进方法所制备的肉桂酸都是纯品。由此可说明,改进后的纯化方法能够获得质量合格的肉桂酸产品。同时也说明,在实验给出的条件下,氨水与苯甲醛完全进行了反应,清除了体系中未反应的苯甲醛。在加入氨水后,体系先出现大量沉淀,随着氨水的加入,沉淀逐渐减少,最后又出现黏稠状固体。加入少量氨水时产生的大量沉淀为肉桂酸;此时氨水先和体系中的乙酸酐以及乙酸反应,随着乙酸酐和乙酸的消耗,肉桂酸溶解度下降,产生沉淀;当氨水加入到一定量,体系变为碱性后,肉桂酸溶解。最后生成的固体为席夫碱,可通过过滤清除。
不同方法获得的肉桂酸的红外光谱对比见图4。由图4可看出,教材所述方法和改进后方法获得的肉桂酸具有与标准肉桂酸相同的红外光谱。
与教材中的传统方法相比,该改进路线有以下优势:
(1)改进后的实验路线减少了水蒸气蒸馏部分的实验操作,学生节省了搭建复杂的水蒸气蒸馏仪器和进行水蒸气蒸馏的时间,取而代之的是滴加氨水和室温下磁力搅拌30min,更易于操作。
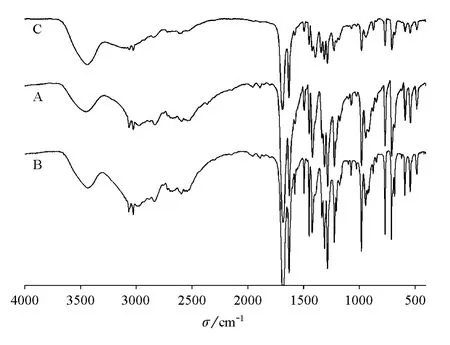
图4 不同方法制备的肉桂酸的红外光谱
(2)按照传统教科书的方法,该实验的收率约为54.0%(2011年11月在广东湛江进行的广东省高校第3届化学化工实验技能大赛决赛阶段63名选手的平均收率,此收率为活性炭脱色并重结晶后的收率)。通过改进后,粗产品收率可达到74.5%(因产品色泽较好,未经活性炭脱色和重结晶操作)。改进后产品的收率如此之高,除了没有活性炭吸附和重结晶操作的影响外,改进后路线在纯化过程中引入的水比传统方法少很多,可减少在酸化沉淀肉桂酸时产品的损失。
(3)实现了对有机化学实验教学内容的补充。传统实验方法强调学生对水蒸气蒸馏相关技术理论及操作的掌握,而这部分内容在苯胺的制备实验中已有全面涉及。改进后的实验路线减少了相应操作,增加了传统教材很少涉及的化学除杂方法。实际上,化学除杂也是有机合成中最常见的纯化方法之一,很有必要让学生学习和掌握。
最后需要说明的是,此改进实验尚有一些不足之处,有待进一步优化。如:
(1)与教材实验方法相比,减少了从回流装置改蒸馏装置的操作,使学生缺少了相关操作的锻炼。
(2)氨水碱性强、气味浓且难闻。实验中大量使用氨水给实验室的通风条件提出了很高的要求。
[1]徐兆瑜.化工科技市场,2005,9:1
[2]沈戮,石晓波.化学合成实验.北京:化学工业出版社,2010
[3]吴霞.由苯甲醛合成间氟苯甲醛的研究.南京理工大学硕士论文,2009

