纳米ZnO-La2O3固体碱的制备及其催化废弃煎炸油制备生物柴油*
侯谦奋,张前前,李 铁,李 苓
(中国海洋大学化学化工学院,山东 青岛266100)
生物柴油作为石化燃料的替代品[1],具有无毒、可被生物降解、十六烷值高以及硫含量低等优点[2-3]。生物柴油的主要成分是脂肪酸烷基酯的混合物[4],通常是在催化剂催化下,由动植物油脂中的甘油三酸酯与甲醇或乙醇发生酯交换反应来制备的[5]。在工业生产中,制备生物柴油的传统方法是使用强酸或强碱作为均相催化剂的酯交换法[6]。均相碱催化剂的催化活性高,对设备腐蚀小,因而应用更加广泛[7-9]。然而,均相碱催化剂对原料油的品质要求高,原料油的酸值和含水量必须很低;同时后处理过程会产生大量的废水造成环境污染,并且有可能使产品发生一定程度的皂化或乳化,降低生物柴油的产率[10]。为此,固体碱催化剂的研究应运而生。文献报道的固体碱催化剂主要有负载型碱金 属 氧 化 物[11-12]、碱 土 金 属 氧 化 物[13-14]以 及 掺杂型碱土金属氧化物[15-16]等,但这些催化剂都存在活性组分易于流失及催化剂失活等问题。而且,值得注意的是,研究发现在固体碱催化剂制备过程中若使用了含有碱金属离子的盐或碱,即使洗涤至中性,残留的碱金属离子仍会使固体碱具有优异的催化活性却无法重复使用[17],这意味着在固体碱制备过程中应避免使用碱金属离子的盐或碱。为此,研究者随将目光转向了具有与碱土金属氧化物类似碱度[18]且难溶于水的稀土金属氧化物。2001年Bancquart等[19]报道了首个稀土金属氧化物CeO2作为固体碱催化剂催化甘油和硬脂酸甲酯的酯交换反应。2007年Li等[20]制备了Eu2O3/Al2O3固体超强碱,催化大豆油和甲醇的酯交换反应,反应8h后转化率达到63.2%。2010年Sun等[21]采用等体积浸渍法制备了La2O3/ZrO2固体碱,200℃催化葵花籽油和甲醇的酯交换反应制备生物柴油,产率达到84.9%。近年来,锌镧体系的固体碱催化剂因其优异的催化活性以及良好的抗酸抗水性能[22-24],受到人 们 的 极 大 关 注。 在 2009 年,Yan等[22]采用均匀沉淀法,以尿素为沉淀剂,在尿素水解4h后,经逐级升温煅烧8h,制备了ZnO/La2CO5/LaOOH固体碱,200℃催化制备生物柴油,反应3h产率达到96%;但使用之初锌镧流失严重[23]。2011年Jin等[24]采用原位沉淀法,以KOH和K2CO3的混合溶液为沉淀剂,在550℃煅烧制备了ZnO/La2O2CO3固体碱,利用微波快速制备生物柴油产率达到95%;但这种方法难免会引入钾离子。因此,本文旨在对锌镧体系的固体碱催化剂做进一步的研究。选择草酸铵为沉淀剂制备ZnO-La2O3固体碱,不仅可以避免引入碱金属离子,同时缩短了制备催化剂的时间。着重考察锌镧摩尔比和煅烧温度这两个因素,在不同条件下制备ZnOLa2O3固体碱,将其用于催化废弃煎炸油和甲醇的酯交换反应制备生物柴油,通过比较其催化活性优化催化剂的制备条件。我国餐饮业每年都会产生大量的废弃煎炸油,如何避免其重新流入百姓餐桌已迫在眉睫。本研究结果为有效利用餐饮行业的废弃煎炸油提供技术支持。
1 实验部分
1.1 材料与仪器
材料 十九烷酸甲酯标准品(Aladdin Industrial Corporation);脂肪酸甲酯混标(Sigma);正己烷(HPLC,Amethyst Chemicals);硝酸镧(AR,国药集团化学试剂有限公司);硝酸锌(AR,天津市巴斯夫化工有限公司);所用其余试剂均为分析纯。废弃煎炸油购于海大康惠达超市,经实验室纯化后[25]酸值低于1mg KOH/g油,平均摩尔质量为859g/mol。
仪器 7890A-5975C气相色谱-质谱联用仪(Agilent Technologies);S-4800冷场发射扫描电子显微镜(Hitachi High-Technologies);D/max 2500/PC X 射线衍射仪(Rigaku Corporation);iCAP 6000系列电感耦合等离子体原子发射光谱仪(Thermo Fisher Scientific);SRJX-4-13高温电阻炉(上海申光仪器仪表有限公司);3K30高速冷冻离心机(Sigma Laborzentrifugen GmbH)。
1.2 催化剂的制备
采用共沉淀法,以草酸铵为沉淀剂制备ZnOLa2O3固体碱催化剂。用蒸馏水分别配制2mol/L的硝酸锌水溶液和1mol/L的硝酸镧水溶液,将其二者按一定量混合均匀,得到不同锌镧摩尔比(1∶1、2∶1、3∶1和4∶1)的混合溶液。在电磁搅拌条件下,滴加到一定量的0.4mol/L草酸铵水溶液中,得到白色沉淀。过滤并洗涤沉淀,先在烘箱中120℃干燥8h,再置于马弗炉中于不同温度(400、500、600、700和850℃)煅烧3h,即得到相应的催化剂。不同锌镧摩尔比的催化剂分别记为Zn1La1、Zn2La1、Zn3La1和Zn4La1。根据其催化制备生物柴油的效果,确定优化的制备条件。此外,在同样的条件下,分别制备了单一组分的ZnO和La2O3,并用于催化制备生物柴油,以做比较。
1.3 催化剂的表征
1.3.1 X射线衍射(XRD)分析 通过XRD分别对催化剂及其使用1次后(经甲醇洗涤4次,正己烷洗涤1次并在120℃干燥)的物相进行表征。辐射源为Cu Kα(40kV,100mA),扫描角度10°~80°,扫描步长0.02°,扫描速度8(°)/min。通过Jade 5.0软件和PDF2-2004标准卡片对所得XRD图进行分析。
1.3.2 电感耦合等离子体原子发射光谱(ICP-AES)分析 通过ICP-AES对700℃煅烧制备的Zn3La1催化剂中的锌镧摩尔比进行分析。射频功率1 150W,垂直观测高度12mm,蠕动泵泵速25r/min,冷却气流量12L/min,辅助器流量1.0L/min,载气压强0.2MPa。
在213.8nm的波长下测量不同浓度的硝酸锌标准溶液,得到Zn2+标准曲线。在419.6nm的波长下测量不同浓度的硝酸镧标准溶液,得到La3+标准曲线。称取700℃煅烧制备的Zn3La1催化剂0.073 3g,用1mol/L的硝酸溶解并定容至250mL,逐级稀释200倍,得到待测催化剂溶液;同时将1mol/L的硝酸溶液稀释相同倍数作为空白实验。
1.3.3 扫描电子显微镜(SEM)分析 通过SEM分别对催化剂及其使用1次后(经甲醇洗涤4次,正己烷洗涤1次并在120℃干燥)的形貌进行观察,加速电压为5kV。
1.4 生物柴油的制备
催化制备生物柴油的反应在100mL高压反应釜中进行。反应釜中装有8.000g纯化后的废弃煎炸油[26],13.6mL甲醇(醇油摩尔比为36∶1),0.400g催化剂(占油质量的5%),在200℃温度下反应3h。冷至室温,高速(8 000r/min)离心20min去除催化剂,减压蒸馏去除甲醇,然后于分液漏斗中静置,除去下层的甘油,即得到黄色的生物柴油产品。
在考察催化剂重复使用的效果时,将与产物分离的催化剂用甲醇洗涤4次,再用正己烷洗涤1次,120℃干燥后,即用于下一轮的生物柴油制备反应,反应条件不变。
1.5 生物柴油的成分分析及产率计算
通过GC-MS分析生物柴油的成分。实验条件为:19091N-133HP-INNOWAX 色谱柱(30m×0.250mm×0.25μm),进样口温度250℃。柱温采用程序升温,初温100℃保持1min,以5℃/min速度升至150℃,再以10℃/min升至240℃,保持10min。采用分流进样,分流比为100∶1,进样量1μL,载气为高纯氦气,流速1.0mL/min。溶剂延迟3.75min,接口温度180℃,EI离子源,电子能量70eV,离子源温度230℃,四级杆温度150℃,质量扫描范围30~500u。
通过脂肪酸甲酯的混标测量脂肪酸甲酯相对于十九烷酸甲酯的相对校正因子,以十九烷酸甲酯为内标物对生物柴油的产率进行定量计算。根据公式(1)计算生物柴油的产率(ωFAME)[27]。
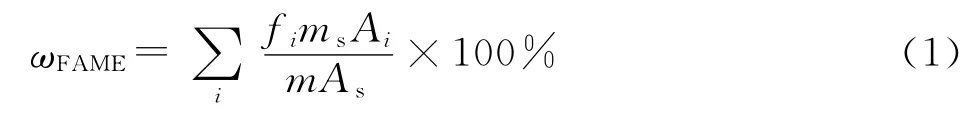
其中:Ai为第i种脂肪酸甲酯的峰面积;As为内标物的峰面积;ms为待测样品中内标物的质量;m为待测样品中生物柴油的质量;fi为第i种脂肪酸甲酯相对于十九烷酸甲酯的相对校正因子。
1.6 生物柴油的理化性质
根据国标GB/T 20828-2007柴油机燃料调和用生物柴油(BD100)[28]规定的方法,对所制得的生物柴油的理化性质进行检测。
1.7 生物柴油中金属离子含量的测定
称取1.000 0g生物柴油于坩埚中,加热坩埚至生物柴油燃烧。待生物柴油完全烧尽后,将坩埚放入马弗炉中600℃煅烧3h。冷至室温,取出坩埚,向其中加入1mol/L的硝酸。充分溶解残留物后,转入10mL容量瓶中。用1mol/L硝酸定容后,再稀释20倍,得到待测样品;将干净的空坩埚进行相同的操作来作为空白试验。采用ICP-AES,通过已做好的Zn2+和La3+的标准曲线测得生物柴油中Zn2+和La3+的含量。
2 结果与讨论
2.1 ZnO-La2O3催化剂制备条件的优化
为了优化ZnO-La2O3固体碱催化剂的制备条件,本文在不同煅烧温度(400、500、600、700和850℃)条件下制备了不同锌镧摩尔比的催化剂(Zn1La1、Zn2La1、Zn3La1和Zn4La1),并分别将所制得的催化剂用于催化废弃煎炸油与甲醇的酯交换反应制备生物柴油,通过反应后产物甘油的收率来判断催化剂活性的高低,从而确定催化剂较优的锌镧摩尔比和煅烧温度,结果见图1。从图1所示的结果可以看出,不同锌镧摩尔比和煅烧温度下制备的催化剂的活性不同,使用700℃煅烧制得的Zn3La1催化剂催化酯交换反应,副产物甘油的收率最大,表明其具有较好的催化活性。此外,700℃煅烧制得的Zn3La1催化剂与700℃煅烧制得的单一组分的氧化锌和氧化镧相比,具有更高的催化活性(见图2),这表明在700℃煅烧制得的Zn3La1复合催化剂中,组分之间有一定的作用,产生了协同催化的效果。因此,本文对700℃煅烧制备的Zn3La1催化剂的组成和形貌进行表征,对其催化制备的生物柴油的成分和产率进行分析和计算,考察其重复使用性能及流失情况,并讨论了其可能的反应机理。
2.2 Zn3La1催化剂的组成与形貌
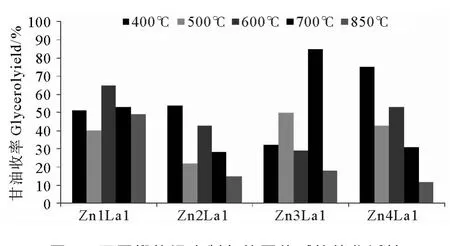
图1 不同煅烧温度制备的固体碱的催化活性Fig.1 Catalytic activity of solid bases calcined at different temperatures

图2 在700℃煅烧制备的Zn3La1,ZnO和La2O3的催化活性Fig.2 Catalytic activity of Zn3La1,ZnO and La2O3calcined at 700℃
通过XRD表征700℃煅烧制备的Zn3La1催化剂在使用前后的物相组成,结果见图3。新制的Zn3La1催化剂由氧化锌和氧化镧组成(见图3a),在31.742°、34.419°、36.221°、47.540°、56.562°、62.860°、67.938°和69.118°处为氧化锌的衍射峰;在26.061°、29.101°、29.940°、39.463°、46.039°、52.140°、55.460°、55.878°、72.040°和 75.159°处为氧化镧的衍射峰,这说明在700℃的温度下煅烧3h,催化剂的前驱体完全分解。使用过1次后,经洗涤并干燥的Zn3La1催化剂的XRD图(见图3b)显示,催化剂中氧化锌的衍射峰未发生改变,而氧化镧衍射峰消失,在15.617°、27.319°、27.959°、39.441°、48.638°和55.199°处为氢氧化镧的衍射峰,这可能是由于反应体系中含有的微量水造成的。
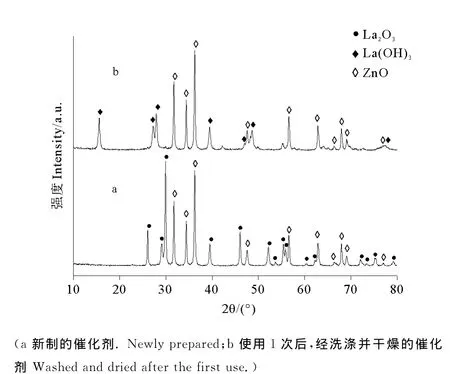
图3 Zn3La1催化剂的XRD图Fig.3 XRD patterns of Zn3La1
通过ICP-AES对700℃煅烧制备的Zn3La1催化剂中锌镧的摩尔比进行了检测,检测结果见表1。由表1的检测结果可知,制得的催化剂中锌镧摩尔比为2.98∶1,与理论摩尔比3∶1吻合,同时也表明采用共沉淀法制得的催化剂中Zn2+和La3+2种离子的分布是比较均匀的。
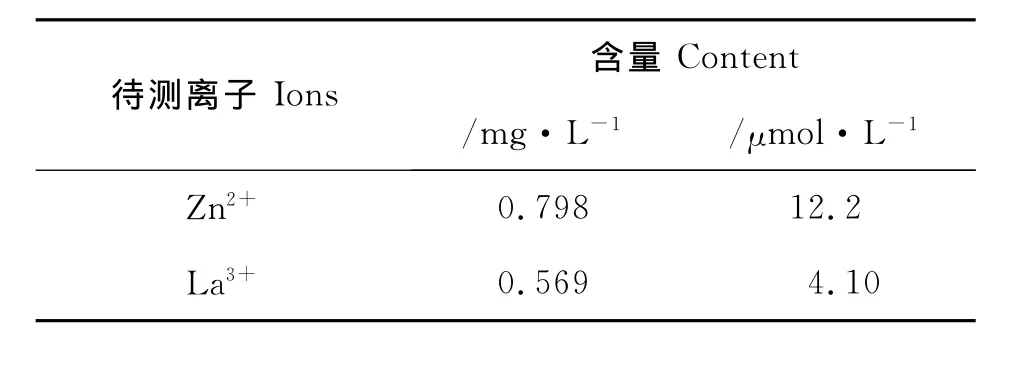
表1 Zn3La1催化剂的ICP-AES分析结果Table 1 ICP-AES analytical results of the Zn3La1catalyst
通过SEM观察700℃煅烧制备的Zn3La1催化剂在反应前后的表面形貌,结果见图4。新制的Zn3La1催化剂的SEM图(见图4a和4b)显示Zn3La1催化剂比较均匀,粒径在100nm左右,这有助于该固体碱的催化活性。Zn3La1催化剂在使用1次并洗涤干燥后其表面形貌发生了变化(见图4c和4d),催化剂的表面变的更加光滑,呈现珊瑚状多孔结构,这可能是由于催化剂在反应过程中长时间与液相发生接触引起的,原有的微粒彼此联结的更加紧密,形成更大的颗粒。

图4 Zn3La1催化剂SEM图Fig.4 SEM images of the Zn3La1catalysts
2.3 生物柴油成分及产率
通过GC-MS对所制得的生物柴油进行分析。图5是对700℃煅烧制备的Zn3La1催化剂制得的生物柴油的GC-MS分析。从图中可见7个明显的峰,通过Nist08质谱库分析可知,这7个峰分别是制得的生物柴油中6种主要的脂肪酸甲酯峰和1个十九烷酸甲酯内标物峰。计算结果显示油酸甲酯的含量最多,为34.4%,其 次为亚油酸甲酯 27.7%,棕 榈 酸 甲 酯17.3%,硬脂酸甲酯5.68%,亚麻酸甲酯2.87%,棕榈油酸甲酯2.34%。除此之外,还有花生一烯酸甲酯、肉豆蔻酸甲酯以及花生酸甲酯的峰,但这些峰的面积相对较小,在图中不明显,经计算其总含量为1.29%。所制备的生物柴油中脂肪酸甲酯的脂肪酸碳链长度主要为16碳和18碳,不饱和脂肪酸甲酯的相对含量为74.0%,不饱和脂肪酸甲酯的含量大于饱和脂肪酸甲酯的含量。通过GC-MS对催化剂重复使用制得的生物柴油进行分析,结果显示生物柴油中脂肪酸甲酯的种类没有变化。

图5 生物柴油的GC-MS分析Fig.5 GC-MS analysis of the biodiesel
2.4 生物柴油理化性质分析结果
表2是700℃煅烧制备的Zn3La1固体碱催化制得的生物柴油理化性质的检测结果。从表中可以看出,通过废弃煎炸油制备的生物柴油的运动黏度较大,十六烷值却较低,这主要是原料废弃煎炸油的成分造成的。由生物柴油的成分分析已知,废弃煎炸油所制得的生物柴油中含量最高的2种脂肪酸甲酯为油酸甲酯和亚油酸甲酯,二者相对含量之和为67.8%,而这2种脂肪酸甲酯都含有较长的碳链,由于运动粘度随脂肪酸甲酯碳链长度的增加而增大[29-30],所以制得的生物柴油运动粘度较大,因此实际使用时需要与石化柴油混合使用。废弃煎炸油制备得到的生物柴油中不饱和脂肪酸甲酯的相对含量为74.0%,十六烷值随着脂肪酸甲酯不饱和程度的增大而减小[31],含有如此多不饱和脂肪酸甲酯使得生物柴油的十六烷值略低于我国国标的要求[28],但这并不影响其热效应及使用,事实上,美国的大多数制造商的发动机要求十六烷值在40~50[32]。

表2 生物柴油的理化性质分析结果Table2 Results of physical and chemical properties of the biodiesel
2.5 生物柴油中金属离子的含量
通过ICP-AES对700℃煅烧制备的Zn3La1固体碱催化制得的生物柴油中Zn2+和La3+的含量进行分析,ICP-AES的分析结果见表3。从表中可以看出,所制备的生物柴油中La3+的含量为0.878mmol/L,Zn2+的含量为0.421mmol/L,Zn2+与La3+的物质的量之比近似等于0.479;鉴于催化剂自身Zn2+与La3+的物质的量之比为3,说明生物柴油中检测出的Zn2+和La3+主要是由催化剂的流失导致的;并且La3+比Zn2+容易流失,这可能与700℃煅烧制备的Zn3La1中组分La2O3易受水分影响而变为La(OH)3有关。从目前研究结果看,锌镧体系的催化剂仍存在一定程度的流失[23],介孔材料的引入有望抑制其流失[33]。

表3 生物柴油中金属离子含量的ICP-AES分析结果Table 3 ICP-AES analytical results of the metallic ions in the biodiesel
2.6 催化剂的重复使用性能及催化机理讨论
固体碱催化剂的重复使用性能是评价催化剂的一个非常重要的指标。Sun等[21]制备的La2O3/ZrO2催化剂第一次使用时,生物柴油产率为84.9%,催化剂经洗涤并煅烧活化后重复使用,第五次使用时,产率下降为28.8%。Jin等[24]制备的ZnO/La2O2CO3催化剂,第四次使用时生物柴油产率下降为75%。Yan等[34]制备的CaO/La2O3催化剂,第四次使用时所制生物柴油的产率低于80%。本文考察了700℃煅烧制备的Zn3La1催化剂在使用4次过程中的催化活性,结果见图6。从图中可以看出,使用新制的Zn3La1催化剂,生物柴油的产率达到91.6%。在每次反应结束之后,分离催化剂,并用甲醇洗涤4次,正己烷洗涤1次,在120℃干燥后,继续用于下一次的反应。催化剂第二次使用时,产率下降为83.8%,这说明催化剂成分由氧化镧变为氢氧化镧对其催化活性有所影响。第三次和第四次使用时,产率分别为80.7%和80.5%,表明催化剂的催化性能逐渐趋于稳定。与同类文献[21,24,34]相比,本催化剂的重复使用性能有所提高。

图6 催化剂使用次数对于脂肪酸甲酯产率的影响Fig.6 Effect of reutilization of catalyst on the FAME yield
固体碱催化酯交换反应制备生物柴油的过程,可以用亲核取代反应机理进行解释[35]。反应历程如图7所示:首先,反应物甲醇1与Zn3La1催化剂2表面的晶格氧碱性中心发生作用,甲醇1失去氢离子而产生甲氧基负离子3,Zn3La1催化剂2得到氢离子转化为4;然后,甲氧基负离子3作为亲核试剂,进攻甘油三酸酯5中带有部分正电荷的羰基碳原子,形成活性中间体6;活性中间体6旋即进行电子转移,发生消除反应而生成中间产物7和产物脂肪酸甲酯8;最后,中间产物7与4表面的氢离子重新结合生成副产物甘油二酸酯9,而4则被还原为Zn3La1催化剂2。甘油二酸酯9中剩余的2个羰基碳原子与甲醇继续发生上述过程,最终得到副产物甘油。显然,在催化反应之初,甲氧基负离子生成的难易决定于固体碱催化剂表面晶格氧碱性中心的电子云密度。Zn3La1催化剂在第二次使用时,催化性能下降较大,之后,催化性能逐渐趋于稳定,这与Zn3La1使用后组分由氧化镧变成氢氧化镧有关。相比于氧化镧中氧的电子云密度,氢氧化镧的氧由于键合氢而导致电子云密度降低,表现为夺取甲醇中氢离子的能力减弱,因而催化性能有所降低。
3 结语

图7 催化机理示意图Fig.7 Schematic representation of possible catalytic mechanism
本文以草酸铵为沉淀剂制备了ZnO-La2O3复合固体碱催化剂,锌镧摩尔比为3∶1,粒径为100nm。将其应用于催化废弃煎炸油和甲醇的酯交换反应制备生物柴油,在醇油摩尔比36∶1,催化剂用量5%,200℃反应3h后,生物柴油产率达到91.6%;催化剂一经使用后,组分La2O3变为La(OH)3而使催化活性有所降低,连续使用4次,产率仍保持在80%以上。该催化剂的制备方法简单快捷,具有良好的重复使用性能。将该催化剂与介孔材料结合,以抑制其少量流失,是今后需要进行的工作。
[1] Crabbe E,Nolasco-Hipolito C,Kobayashi G,et al.Biodiesel production from crude palm oil and evaluation of butanol extraction and fuel properties[J].Process Biochemistry,2001,37(1):65-71.
[2] Clark S J,Wagner L,Schrock M D,et al.Methyl and ethyl soybean esters as renewable fuels for diesel engines[J].Journal of the American Oil Chemists Society,1984,61:1632-1638.
[3] Muniyappa P R,Brammer S C,Noureddini H.Improved conversion of plant oils and animal fats into biodiesel and co-product[J].Bioresource Technology,1996,56:19-24.
[4] Srivastava A,Prasad R.Triglycerides-based diesel fuels[J].Renewable and Sustainable Energy Reviews,2000,4:111-133.
[5] Ma F R,Hanna M A.Biodiesel production:a review[J].Bioresource Technology,1999,70(1):1-15.
[6] López D E,Goodwin J G,Bruce D A,et al.Transesterification of triacetin with methanol on solid acid and base catalysts[J].Applied Catalysis A:General,2005,295:97-105.
[7] Freedman B,Pryde E H,Mounts T L.Variables affecting the yields of fatty esters from transesterified vegetable oils[J].Journal of the American Oil Chemists Society,1984,61(10):1638-1643.
[8] Freedman B,Butterfield R O,Pryde E H.Transesterification kinetics of soybean oils[J].Journal of the American Oil Chemists Society,1986,63(10):1375-1380.
[9] Kawashima A,Matsubara K,Honda K.Acceleration of catalytic activity of calcium oxide for biodiesel production[J].Bioresource Technology,2009,100(2):696-700.
[10] Zhang Y,DubéM A,McLean D D,et al.Biodiesel production from waste cooking oil:1.Process design and technological assessment[J].Bioresource Technology,2003,89(1):1-16.
[11] Noiroy K,Intarapong P,Luengnaruemitchai A,et al.A comparative study of KOH/Al2O3and KOH/NaY catalysts for biodiesel production via transesterification from palm oil[J].Renewable Energy,2009,34(4):1145-1150.
[12] D’Cruz A,Kulkarni M G,Meher L C,et al.Synthesis of biodiesel from canola oil using heterogeneous base catalyst[J].Journal of the American Oil Chemists Society,2007,84:937-943.
[13] Kouzu M,Kasuno T,Tajika M,et al.Calcium oxide as a solid base catalyst for transesterification of soybean oil and its application to biodiesel production[J].Fuel,2008,87:2798-2806.
[14] Venkat C R,Oshel R,Verkade J G.Room-temperature conversion of soybean-oil and poultry fat to biodiesel catalyzed by nanocrystalline calcium oxides[J].Energy Fuels,2006,20:1310-1314.
[15] MacLeod C S,Harvey A P,Lee A F,et al.Evaluation of the activity and stability of alkali-doped metal oxide catalysts for application to an intensified method of biodiesel production[J].Chemical Engineering Journal,2008,135:63-70.
[16] Liang X,Gao S,Yang J,et al.Highly efficient procedure for the transesterification of vegetable oil[J].Renewable Energy,2009,34:2215-2217.
[17] Kim M,Yan S,Salley S O,et al.The effect of sodium on the catalytic activity of ZnO-Al2O3/ZSM-5and SnO-Al2O3/ZSM-5for the transesterification of vegetable oil with methanol[J].Catalysis Communications,2009,10:1913-1919.
[18] Sato S,Takahashi R,Kobune M,et al.Basic properties of rare earth oxides[J].Applied Catalysis A:General,2009,356:57-63.
[19] Bancquart S,Vanhove C,Pouilloux Y,et al.Glycerol transesterification with methyl stearate over solid basic catalysts:I.Rela-tionship between activity and basicity[J].Applied Catalysis A:General,2001,218:1-11.
[20] Li X,Lu G Z,Guo Y L,et al.A novel solid superbase of Eu2O3/Al2O3and its catalytic performance for the transesterification of soybean oil to biodiesel[J].Catalysis Communications,2007,8(12):1969-1972.
[21] Sun H,Ding Y Q,Duan J Z,et al.Transesterification of sunflower oil to biodiesel on ZrO2supported La2O3catalyst[J].Bioresource Technology,2010,101:953-958.
[22] Yan S L,Salley S O,Simon Ng K Y.Simultaneous transesterification and esterification of unrefined or waste oils over ZnOLa2O3catalysts[J].Applied Catalysis A:General,2009,353,203-212.
[23] Yan S L,Mohan S,DiMaggio C,et al.Long term activity of modified ZnO nanoparticles for transesterification[J].Fuel,2010,89:2844-2852.
[24] Jin L,Zhang Y S,Dombrowski J P,et al.ZnO/La2O2CO3layered composite:A new heterogeneous catalyst for the efficient ultra-fast microwave biofuel production[J].Applied Catalysis B:Environmental,2011,103:200-205.
[25] Meng X M,Chen G Y,Wang Y H.Biodiesel production from waste cooking oil via alkali catalyst and its engine test[J].Fuel Processing Technology,2008,89:851-857.
[26] 何东平.油脂精炼与加工工艺学[M].北京:化学工业出版社,2005:22-86.
[27] 中华人民共和国国家质量监督检验检疫总局.GB/T 17377-2008动植物油脂脂肪酸甲酯的气相色谱分析[S].北京:中国标准出版社,2009.
[28] 中华人民共和国国家质量监督检验检疫总局.GB/T 20828-2007柴油机燃料调合用生物柴油(BD100)[S].北京:中国标准出版社,2007.
[29] Antolín G,Tinaut F V,Brice珘no Y,et al.Optimisation of biodiesel production by sunflower oil transesterification[J].Bioresource Technology,2002,83:111-114.
[30] Allen C A W,Watts K C,Ac km an R G,et al.Predicting the viscosity of biodiesel fuels from their fatty acid ester composition[J].Fuel,1999,78:1319-1326.
[31] Dorado M P,Ballesteros E,Arnal J M,et al.Testing waste olive methyl ester as a fuel in a diesel engine[J].Energy and Fuels,2003,17:1560-1565.
[32] Knothe G,Gerpen J V,Krahl J.The Biodiesel Handbook[M].Champaign:AOCS Press,2005.
[33] Quintella S A,Saboya R M A,Salmin D C,et al.Transesterificarion of soybean oil using ethanol and mesoporous silica catalyst[J].Renewable Energy,2012,38:136-140.
[34] Yan S L,Kim M,Mohan S,et al.Effects of preparative parameters on the structure and performance of Ca-La metal oxide catalysts for oil transesterification[J].Applied Catalysis A:General,2010,373:104-111.
[35] Kouzu M,Kasuno T,Tajika M,et al.Calcium oxide as a solid base catalyst for transesterification of soybean oil and its application to biodiesel production[J].Fuel,2008,87:2798-2806.

