Cu对K-LaZrO2异丁醇合成催化剂的影响
武应全 王思晨 解红娟 高俊文 田少鹏 韩怡卓 谭猗生,*(中国科学院山西煤炭化学研究所煤转化国家重点实验室,太原0000;中国科学院大学,北京00049;陕西延长石油(集团)有限责任公司,西安70075)
Cu对K-LaZrO2异丁醇合成催化剂的影响
武应全1,2王思晨3解红娟1高俊文3田少鹏1,2韩怡卓1谭猗生1,*
(1中国科学院山西煤炭化学研究所煤转化国家重点实验室,太原030001;2中国科学院大学,北京100049;3陕西延长石油(集团)有限责任公司,西安710075)
采用X射线衍射(XRD)、程序升温脱附(TPD)、X射线光电子能谱(XPS)、傅里叶变换红外(FTIR)光谱技术及富集法考察了K-LaZrO2和K-CuLaZrO2催化剂结构、CO和H2在锆基催化剂上的吸附行为及异丁醇合成活性的影响.结果表明,催化剂添加Cu后,与Zr形成较好的固溶体,促进了CuO的分散,且抑制了ZrO2结晶,增强Cu-Zr相互作用,提高了催化活性.CO-TPD结果显示,引入Cu后,催化剂表面CO吸附量明显增加,有利于碳链增长;H2-TPD结果显示,与活性相关的低温脱附氢量也明显增加.另外,FTIR及富集法结果发现,Cu的引入促进了表面C1物种的形成,增加了表面C1物种含量,促进了碳链增长,明显改善了异丁醇的选择性.在p= 10.0 MPa,空速(GHSV)=3000 h-1,T=360°C,V(H2)/V(CO)=1:1条件下,异丁醇选择性达到48.5%.
氧化铜;锆基催化剂;合成气;异丁醇
©Editorial office of Acta Physico-Chimica Sinica
1 引言
异丁醇是一种基本有机化工原料,用于制造抗氧剂、乙酸异丁酯(涂料溶剂)、异丁酸异丁酯(食用香料)、乳酸异丁酯、异丁腈(精细化工中间体)、邻苯二甲酸二异丁酯增塑剂、合成橡胶、人造麝香、果子精油和合成药物等.1我国是稀土资源大国,异丁醇作为溶剂广泛用于稀土生产中锶、钡和锂等盐类的提纯,市场需求巨大.2010年,异丁醇被列入美国环保署燃料添加剂目录,进一步扩展了异丁醇的应用前景.目前,工业异丁醇主要来自丙烯羰基合成法制丁醇时的副产品,是石油基产品,产量少,不能满足对异丁醇日益增长需求的要求.
煤基合成气合成异丁醇的催化剂体系主要有碱改性甲醇催化剂2-5和锆基催化剂.6-10在碱金属改性的甲醇催化剂作用下,合成反应的产物中富含支链醇,但产物组分较复杂,除了甲醇和异丁醇外,其他直链醇所占的比例也较大,不利于分离.而在锆基催化剂上,合成产物中主要是甲醇和异丁醇,其它醇类的含量较小,产品纯度高,但异丁醇的选择性仍然偏低,最高为24.5%.9
Cu-Zr基催化剂在甲醇合成、11-13甲醇重整、14,15水煤气变换反应16以及其他加氢反应17等方面具有较好的催化活性,但是在合成气制备异丁醇方面未见报道.
理论上讲催化剂的活性、选择性与吸附物种数量、强度直接相关.研究反应物种在还原态催化剂上的吸附行为对于认识催化剂活性中心,了解反应机理均有重要意义.因此本文采用共沉淀法,分别制备了K-LaZrO2和K-CuLaZrO2催化剂,用于催化合成气制备异丁醇,同时采用XRD、程序升温脱附、XPS及FTIR技术考察了CO在锆基催化剂上的吸附行为,并着重探讨铜对催化剂结构、CO和H2在锆基催化剂上的吸附行为及异丁醇合成活性的影响.
2 实验部分
2.1 催化剂制备
采用共沉淀法制备催化剂.以Cu(NO3)2·3H2O、ZrO(NO3)2·2H2O(分析纯,国药集团化学试剂有限公司),La(NO3)3·6H2O(分析纯,天津市光复精细化工研究所)为原料,按摩尔比n(Cu):n(La):n(Zr)=1:0.2:4配制成1 mol·L-1的溶液,然后与1 mol·L-1的KOH (分析纯,国药集团化学试剂有限公司)溶液并流进料进行共沉淀,沉淀条件:60°C,pH为11.沉淀物在室温下老化3 h,然后用去离子水洗涤至中性.120°C干燥12 h后在450°C下进行焙烧.
将以上所得催化剂研磨后分别浸渍2%(w)的K (KOH(分析纯,国药集团化学试剂有限公司)为前驱物),在120°C下干燥12 h,然后在450°C下进行焙烧,压片后破碎至30-40目备用.
2.2 表征及反应条件
催化剂的XRD图谱在德国Bruker公司D8型X射线衍射仪上测定,以Cu Kα特征谱线照射,Ni滤波,电压40 kV,电流100 mA.
CO程序升温脱附(CO-TPD)在自制装置上进行.称取100 mg催化剂,在H2/Ar(H2,10%,体积分数)气氛中程序升温至350°C并恒温2 h后,切换为Ar,吹扫20 min后降温至50°C,采用脉冲法通入CO气体,吸附饱和后Ar气吹扫,基线走平后,进行升温脱附到600°C,升温速率5°C·min-1,热导检测器(TCD)检测.
H2-TPD在如上的装置上进行.称取100 mg催化剂,在H2/Ar(H2,10%)气氛中程序升温至350°C并恒温2 h后,在该气氛下降温至50°C,然后切换Ar走平基线后进行程序升温脱附到600°C,升温速率5°C·min-1,热导检测器检测.
X射线光电子能谱是在英国Kratos公司AXIS ULTRA DLD型X射线光电子能谱仪上测定的,使用的是Al Kα射线,污染碳C 1s的结合能为284.6 eV.
吸附态CO红外光谱在德国Bruker公司生产的Tensor 27型红外光谱仪上进行的.磨细的催化剂装入样品池,于350°C纯氢还原2 h,通Ar气吹扫20 min,降温后扫背景,然后通入CO吸附30 min,最后切换成Ar吹扫,间隔5 min测谱.
H2/CO共吸附在以上红外光谱仪上采用相同的还原程序还原并吹扫之后降温到50°C后扫背景,然后通入V(H2)/V(CO)吸附30 min后测谱,之后程序升温(5°C·min-1)到400°C,分别在100、150、200、250、300、350、400°C条件下测谱.
量取5 mL催化剂装入不锈钢制固定床反应器,在10%H2/N2稀释气下进行程序升温还原至360°C,并保持2 h.而后引入合成气(H2/CO体积比为2.7或1)至反应压力,在所需温度下进行合成反应.反应尾气进入冷却器冷凝分相,气相产物在线分析后,经湿式流量计计量排空;6 h后收集液相产物进行计量、分析.
气相产物在两台气相色谱仪上进行在线分析:色谱仪1,GC4000A(碳分子筛柱,TCD检测)分析尾气中的H2、CO、CH4及CO2;色谱仪2,GC4000A (GDX-403柱,FID检测器)分析尾气中的C1、C2、C3、C4、C4+烷烃以及甲醇、二甲醚等的组成.液相产物在两台气相色谱仪上进行,色谱仪3,GC4000A(GDX-401柱,TCD检测)分析水和甲醇;色谱仪4,GC-7AG (Chromsorb l01柱,氢火焰离子化检测器(FID))检测分析液相中的醇组成.最后将分析数据进行归一化处理.
3 结果和讨论
3.1 XRD测定
图1为添加Cu前后K-LaZrO2催化剂的XRD谱图.从图中可以看出,催化剂不添加Cu时,在30.2、35.0、50.5和60.0°处出现了明显衍射峰,归属为t-ZrO2的特征衍射峰,18同时,在30°-40°出现了宽化的包峰,对应于无定形ZrO2,19说明催化剂由t-ZrO2和无定形ZrO2混合相组成.当添加Cu以后.30°-40°之间的包峰进一步宽化,并且t-ZrO2的特征衍射峰消失,同时未发现CuO的特征衍射峰,说明铜在催化剂中分散较好,且铜的引入抑制了四方相ZrO2的生成,与锆形成较好的Cu-Zr固溶体.由于La含量较少,因此在添加Cu前后都未观察到其特征衍射峰.
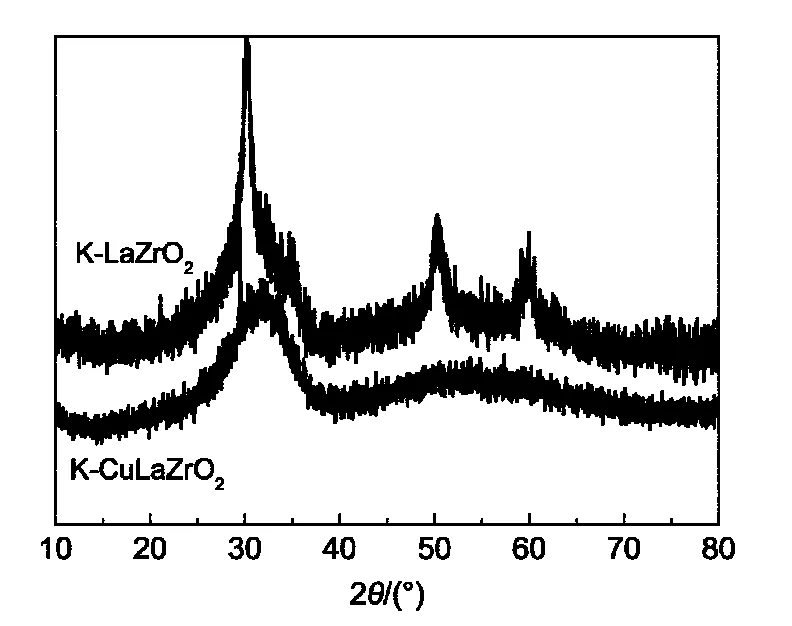
图1 添加Cu前后K-LaZrO2催化剂的XRD谱图Fig.1 XRD patterns of K-LaZrO2catalysts before and after Cu addition
3.2 H2-TPD测定
图2为不同催化剂的H2-TPD谱图.从图中可以看出,催化剂不含Cu时,主要呈现两个脱氢峰,在174°C附近出现一宽化的H2脱附峰,对应于H2的弱脱附峰;在422°C附近也可以观察到微弱的H2脱附峰,对应于H2的强脱附峰.当引入Cu以后,弱H2脱附峰明显向低温方向移动(129°C),而高温区H2脱附峰温未发生偏移.另外,从H2脱附峰面积可以看出,Cu引入后,催化剂表面H2吸附量发生了明显增加,尤其是弱H2吸附量.Ishihara等20认为,脱氢峰的位置与活性金属的电子云密度有关,金属的电子云密度越高,相应氢脱附温度越低.陈建刚等21在考察钴基催化剂上H2吸附性能时同样发现,锆引入后引起金属钴的电子云密度略有下降而带上微正电性,从而导致H2脱附温度向低温方向移动.说明Cu促进了H2在催化剂表面脱附性能,明显增加了催化剂表面弱H2的吸附量.
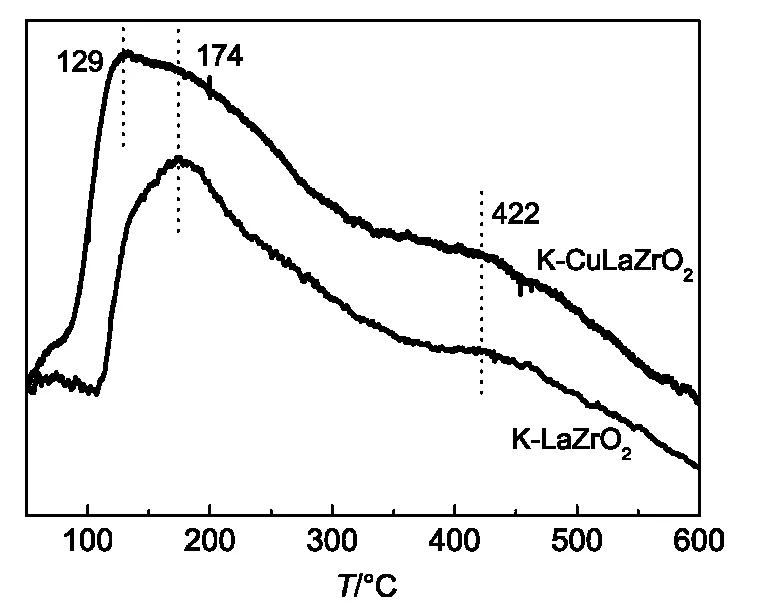
图2 添加Cu前后K-LaZrO2催化剂的H2-TPD谱图Fig.2 H2-TPD profiles of K-LaZrO2catalysts before and after Cu addition
3.3 XPS测定
图3给出了添加Cu前后催化剂的XPS图谱.从图中可以看出,未添加Cu时,Zr 3d5/2结合能为182.0 eV,当引入Cu后,Zr 3d5/2结合能降为181.7 eV,说明Cu的添加引起了Zr周围电子云密度增加,导致Zr 3d结合能降低,进一步验证了H2-TPD结果,H2脱附温度向低温方向移动,确实由于Cu的添加增加了Zr周围电子云密度引起.同时,Zr 3d5/2结合能发生变化,说明Cu与Zr之间发生了相互作用.

图3 添加Cu前后K-LaZrO2催化剂的Zr 3d的XPS图谱Fig.3 XPS spectra of Zr 3dof K-LaZrO2catalysts before and after Cu addition
3.4 CO-TPD
图4为不同催化剂的CO-TPD谱图.从图中可以看出,催化剂不含Cu时,CO脱附峰主要在188°C附近,通过仔细观察可以发现,在127°C处有一微弱的CO脱附峰,对应于弱CO吸附.当引入Cu以后,CO脱附峰发生了明显的变化,在低温处(127°C)的CO脱附峰强度明显增加,同时在451°C处出现了CO强吸附峰.由CO-TPD计算得到添加Cu前后的CO吸附量分别为2.4和8.1 μmol·g-1,这意味着Cu增加了催化剂表面CO吸附量.

图4 添加Cu前后K-LaZrO2催化剂的CO-TPD谱图Fig.4 CO-TPD profiles of K-LaZrO2catalysts before and after Cu addition
3.5 吸附态CO的红外光谱
图5(a)给出K-LaZrO2催化剂CO吸附饱和后表面吸附物种随着Ar吹扫时间变化的FTIR谱图.从图中可以看出,2361、2337 cm-1的吸收峰为气相CO2特征峰,2172、2113 cm-1为气相CO特征峰,1675 cm-1为不同配位的羧酸盐(),1241 cm-1为催化剂表面双配位羧酸盐特征峰(),1377 cm-1为表面碳酸盐吸附物种(),22谱图中这些特征峰的出现,说明部分CO与催化剂表面羟基和活性氧物种发生了反应.随着Ar气不断吹扫,气相CO2特征峰逐渐减弱,气相CO特征峰也逐渐减弱,最后消失;催化剂表面观察不到任何形式的CO吸附,说明K-LaZrO2催化剂表面分子态CO吸附量很少,CO在催化剂表面吸附较弱.
图5(b)给出K-CuLaZrO2催化剂CO吸附饱和后表面吸附物种随着Ar气吹扫时间变化的FTIR谱图.从图中可以看出,2172、2095 cm-1为气相CO特征峰,1671 cm-1为不同配位的羧酸盐(), 1254 cm-1为催化剂表面羧酸盐特征峰(), 1374 cm-1为表面碳酸盐吸附物种).随着Ar气不断吹扫,2172 cm-1处的谱峰逐渐消失,但是当气相CO特征峰2172 cm-1消失以后,2095 cm-1仍存在,说明2095 cm-1处吸收峰为表面CO吸附峰,与气相CO吸附峰相互重叠.根据文献23可知,2095 cm-1为Cu0表面线性吸附CO.相比较图5中(a)和(b)可见,当催化剂添加Cu以后,催化剂表面CO吸附量明显增加,与CO-TPD结果一致.
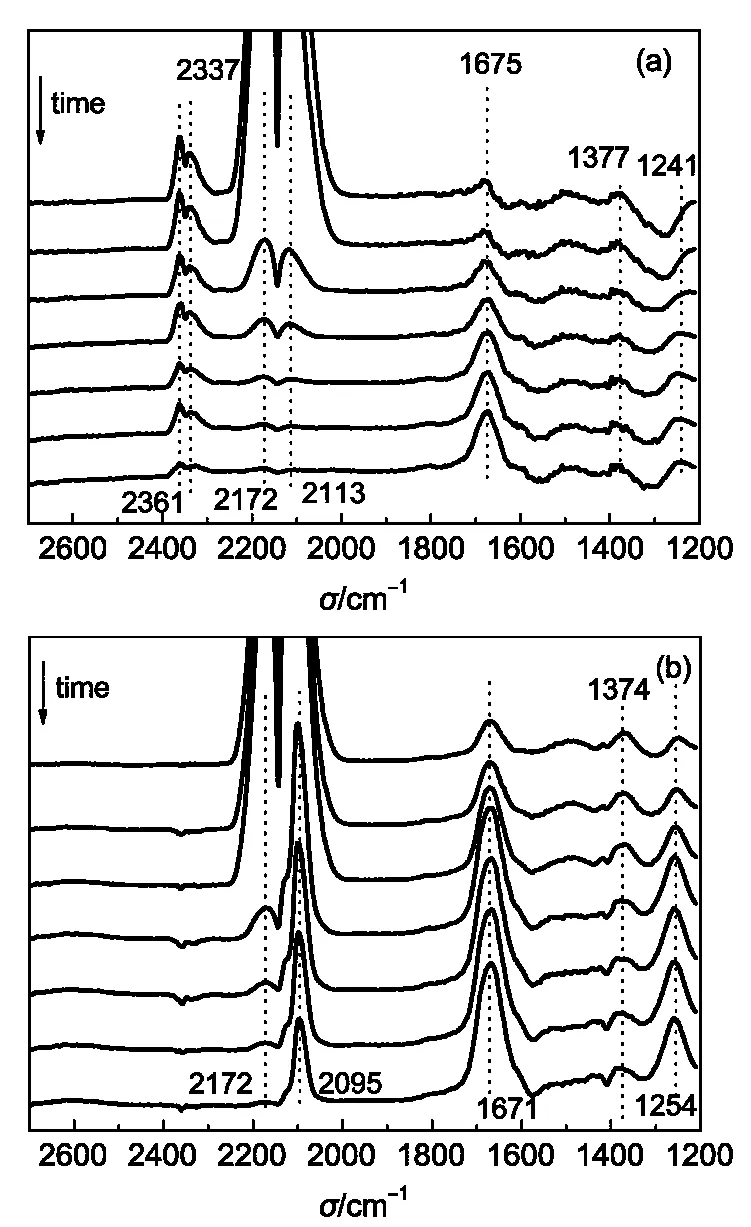
图5 锆基催化剂在Ar吹扫下随时间变化的CO吸附FTIR图谱(30°C)Fig.5 FTIR spectra of adsorbed species on Zr-based catalysts as a function of purging time inAr purging(30°C)
3.6 H2/CO共吸附红外光谱
图6(a)给出K-LaZrO2催化剂在V(H2)/V(CO)=2: 1气流中程序升温(5°C·min-1)过程中的红外谱图.从图a中可以看出,在低温下(50°C),催化剂表面只能观察到气相CO特征峰;当温度达到100°C时,在3500-3700 cm-1之间出现了倒峰,说明表面羟基发生了脱附,同时,在1606、1252 cm-1处出现了明显的吸收峰,为表面双配位羧酸盐物种(b-HCO-3)物种,说明表面羟基与CO发生了反应,消耗了表面羟基,形成了表面羧酸盐物种,1707、1444 cm-1处吸收峰为i-HCO-3物种,1560 cm-1处吸收峰为表面双配位碳酸盐物种().22随着温度不断提高,3500-3700cm-1之间倒峰强度增大,说明催化剂表面羟基在高温下更容易参加反应,同时表面C1物种吸收峰强度逐渐增强,当温度达到300°C时,在2932、2824 cm-1附近出现了CH2基的不对称、对称伸缩振动,说明H2与表面吸附CO发生了反应,生成了表面烃物种,为CH3O-Zr特征峰.24
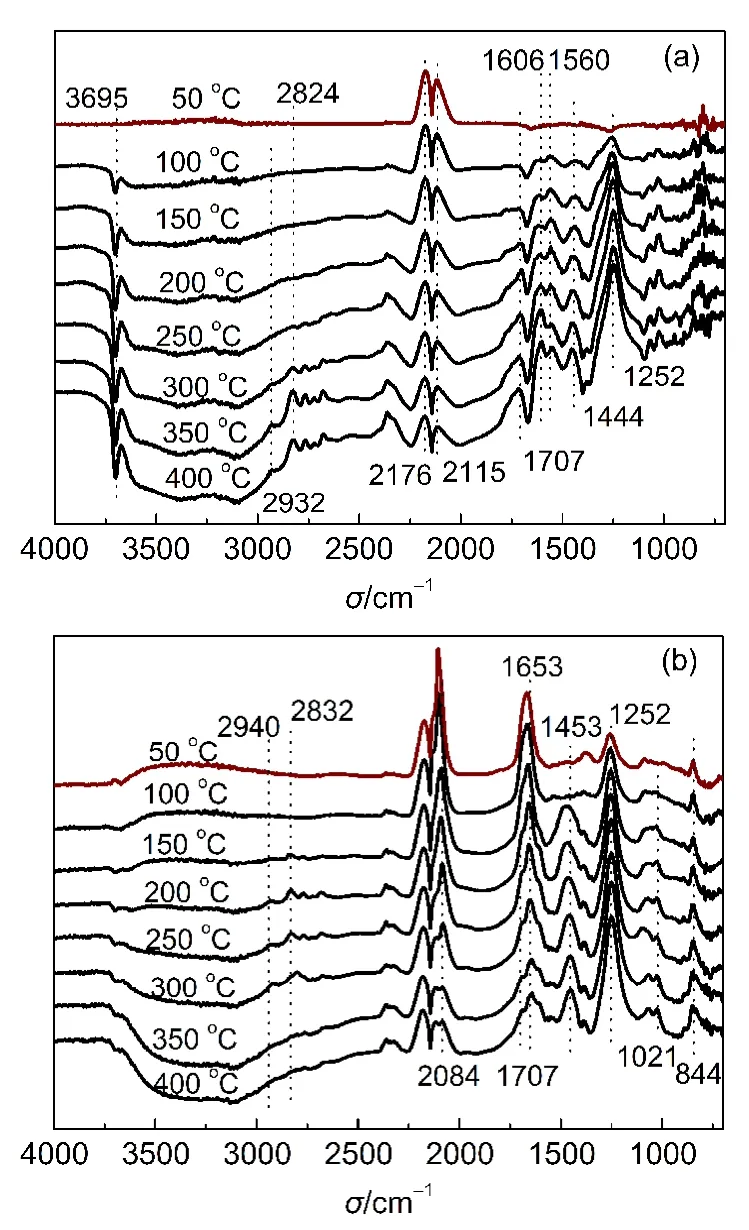
图6 锆基催化剂上的吸附物种在H2/CO气氛下随温度变化的FTIR图谱Fig.6 FTIR spectra of adsorbed species on Zr-based catalysts as a function of purging temperature at H2/CO atmosphere
图6(b)给出K-CuLaZrO2催化剂在V(H2)/V(CO)= 2:1气流中程序升温(5°C·min-1)过程中的红外谱图.从图中可以看出,在低温下(50°C),3500-3700 cm-1之间就出现了吸收峰,除了2176 cm-1附近气相CO特征峰外,1653、1252 cm-1分别出现了不同配位表面羧酸盐物种(p-HCO3-)和双配位羧酸盐物种(b-HCO3-).提高反应温度后,表面羧酸盐物种吸收峰强度增强.当温度为150°C时,2940、2832 cm-1就出现了CH2基的不对称、对称伸缩振动(CH3O-Zr),同时,在1453 cm-1出现了碳酸盐物种.随着温度进一步升高,表面羟基逐渐被消耗,3500-3700 cm-1之间出现倒峰,2940、2832 cm-1处吸收峰强度增强,1653 cm-1处羧酸盐物种吸收峰强度不断降低且宽化,逐渐在1707和1607 cm1处形成了两个肩峰,说明羧酸盐物种在升温过程中发生了转化,分别形成了i-HCO3-和b-HCO3-物种.而1252 cm-1处羧酸盐吸收峰强度不断增强.相比较图6中(a)和(b)可见,添加Cu以后,催化剂在较低的温度下,H2即可发生解离吸附,经溢流效应,在ZrO2上形成表面羟基,之后与催化剂表面吸附CO发生反应,形成丰富的C1物种.
3.7 异丁醇合成反应性能
催化剂异丁醇合成反应性能见表1.K-LaZrO2催化剂在V(H2)/V(CO)为2.5:1时,CO转化率仅14.0%,总醇时空收率为22 g·L-1·h-1,醇产物中甲醇和异丁醇为主要产物,占总醇的86.7%,其中异丁醇选择性为14.1%.V(H2)/V(CO)为1:1时,CO转化率略有下降,总醇时空收率增加到31 g·L-1·h-1.醇产物中,甲醇选择性降为63.7%,而异丁醇选择性增加到20.4%,其他醇选择性变化较小.当催化剂添加Cu时,CO转化率由14.0%提高到60.5%,且醇时空收率也由22 g·L-1·h-1增加到140 g·L-1·h-1,醇产物中,异丁醇选择性在V(H2)/V(CO)为2.5:1时达到了32.9%,当V(H2)/V(CO)为1:1时,CO转化率下降为52.8%,总醇时空收率进一步增加到187 g·L-1·h-1,异丁醇此时选择性为48.5%.
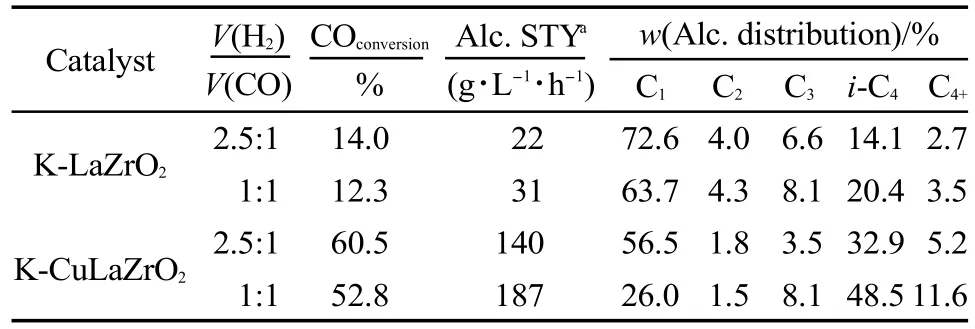
表1 锆基催化剂的异丁醇合成反应性能Table 1 Performance of Zr-based catalysts in isobutanol synthesis
不同H2/CO比对低碳醇选择性有非常重要的影响.前人已对不同V(H2)/V(CO)(0.45-3)对反应的影响作了详细研究,25-27由于在低碳醇合成反应过程中存在水煤气变换反应(WGS),因此,在实际反应中V(H2)/V(CO)会随着反应条件变化而变化.28一般来说,降低V(H2)/V(CO)比会使催化剂活性降低,29但是,由于CO含量增加,使得催化剂表面CO吸附量增加,能够明显促进C―C键增长,有利于C2+醇选择性提高.30相反,高V(H2)/V(CO)比更有利于甲醇的形成,31,32同时对甲烷选择也可能产生明显的影响.29,30在K-LaZrO2中引入Cu后,增加了催化剂表面CO吸附量,提高了催化剂表面CO浓度,因而有利于碳链增长及C2+醇的生成.
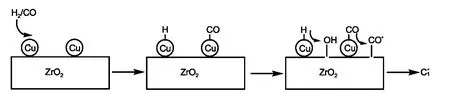
图7 Cu的添加对C1物种形成的影响Fig.7 Effect of Cu addition on the formation of C1species
3.8 甲醇富集
表2为K-LaZrO2和K-CuLaZrO2催化剂上富集甲醇实验结果.由表可知,催化剂不添加Cu时,甲醇和异丁醇为主要产物,其时空收率分别为15.8和3.1 g·L-1·h-1,其它醇时空收率较低,相比较KCuLaZrO2催化剂,虽然醇分布相似,以甲醇和异丁醇为主,但是各醇时空收率明显偏低.当在K-LaZrO2催化剂上富集甲醇时,从表中可以看出,C2及C2+醇的时空收率都明显增加,其中异丁醇时空收率增加3倍以上,说明甲醇在引入以后所形成的C1中间体参与了链增长反应,进而提高了C2及C2+醇的时空收率.当在K-CuLaZrO2催化剂上富集甲醇时,从表2中可以看出,C2及C2+醇的时空收率变化较小,说明在含Cu催化剂上,即使引入C1中间体,对碳链增长反应影响不明显.

表2 甲醇富集对不同催化剂上醇时空收率的影响Table 2 Effect of methanol addition on the STY of alcohols on different catalysts
在之前研究33中也发现,CuO-ZrO2之间相互作用对异丁醇选择性影响较大,CuO-ZrO2之间相互作用越强,合成异丁醇的活性就越好.结合XRD结果, Cu引入后与Zr形成了较好的固溶体,不仅Cu分散较好,而且也抑制了ZrO2结晶,促进了两者协同作用,提高了异丁醇的选择性.
一般而言,较低温度脱附的氢才与催化剂的活性相关,20,21结合H2-TPD结果,Cu添加后,引起Zr周围电子云密度增加,导致催化剂表面H2脱附温度向低温方向移动,即增加了催化剂表面低温脱附氢,提高了催化剂的催化活性.
Fisher和Bell34认为,铜主要功能是解离吸附H2和提供非解离吸附CO,而ZrO2提供合成醇的场所;同时,由于铜在甲醇合成中被认为是甲醇形成活性中心,12因此,铜可能在异丁醇合成中提供了丰富的C1中间体,进而促进了异丁醇选择性提高.从图6中也可以看出,添加Cu以后,在低温(50°C)下,H2就发生了解离吸附,形成了表面羟基,进而与CO形成表面羧酸盐物种,同时在150°C条件下形成了醇类生成必需的甲氧基物种,相比较K-ZrLaO2催化剂,反应温度提高到300°C时才出现甲氧基物种.前人研究发现,35-37甲氧基和羧酸盐都与甲醇的形成有关,且在富集甲醇实验结果中可以看出,当催化剂不添加Cu时,由于在反应过程中形成的表面C1中间体较少,因此,富集甲醇后能够明显提高C2及C2+醇的时空收率;但是当催化剂含有Cu时,催化剂表面能够形成丰富的C1中间体,此时即使再富集甲醇,也不会对C2及C2+醇的时空收率产生明显的影响.因此,Cu引入以后,不仅使得催化剂在低温下就可解离吸附H2,同时提高了催化剂表面CO吸附量,增加了表面C1物种含量(见图7),进而促进了碳链增长,明显改善了异丁醇的选择性,与前人结果一致.
4 结论
在K-LaZrO2催化剂中引入Cu后显著改变了催化剂的性能及反应物种在其上的吸附行为,使得异丁醇合成的反应性能、选择性得到很大提高.在p= 10.0 MPa,GHSV=3000 h-1,T=360°C,V(H2)/V(CO)= 1:1条件下,异丁醇选择性达到48.5%.结论如下.
(1)Cu添加后与Zr形成较好的固溶体,Cu-Zr相互作用增强,促进了Cu的分散,抑制了ZrO2结晶,最终提高了合成异丁醇的活性.
(2)Cu的添加使吸附氢性质改变,降低了H2脱附强度,提高了催化剂的活性.同时也增加了催化剂表面CO的吸附量,提高了催化剂表面CO浓度,有利于碳链增长及C2+醇的生成.
(3)Cu的引入促进了表面C1物种的形成,增加了表面C1物种含量,促进了碳链增长,明显改善了异丁醇的选择性.
(1) Cheng,J.;Jiang,C.B.Chem.Ind.2007,25,28. [程 佳,姜春波.化学工业,2007,25,28.]
(2) Epling,W.S.;Hoflund,G.B.;Minahan,D.M.J.Catal.1997,169,438.doi:10.1006/jcat.1997.1725
(3) Beretta,A.;Sun,Q.;Herman,R.G.;Klier,K.Ind.Eng.Chem. Res.1996,35,1534.doi:10.1021/ie9505219
(4) Burcham,M.M.;Herman,R.G.;Klier,K.Ind.Eng.Chem.Res.1998,37,4657.doi:10.1021/ie9705620
(5) Jiang,T.;Niu,Y.Q.;Zhong,B.Chin.J.Catal.2000,21,319. [姜 涛,牛玉琴,钟 炳.催化学报,2000,21,319.]
(6) Tan,Y.S.;Niu,Y.Q.;Zhong,B.;Peng,S.Y.J.Fuel.Chem. Technol.1996,24,368. [谭猗生,牛玉琴,钟 炳,彭少逸.燃料化学学报,1996,24,368.]
(7) Cai,Y.N.;Niu,Y.Q.;Chen,Z.H.;Zhong,B.;Peng,S.Y.J.Fuel Chem.Technol.1996,24,11.[蔡亚宁,牛玉琴,陈正华,钟 炳,彭少逸.燃料化学学报,1996,24,11.]
(8) Cai,Y.N.;Niu,Y.Q.;Chen,Z.H.Fuel Processing Technology1997,50,163.doi:10.1016/S0378-3820(96)01060-0
(9) He,D.P.;Ding,Y.J.Chin.J.Catal.2005,26,961.[何代平,丁云杰.催化学报,2005,26,961.]
(10) Wang,J.W.;Tan,Y.S.;Niu,Y.Q.;Zhong,B.;Peng,S.Y.J.Fuel.Chem.Technol.1998,26,390.[王军威,谭猗生,牛玉琴,钟 炳,彭少逸.燃料化学学报,1998,26,390.]
(11) Gao,P.;Li,F.;Zhao,N.;Wang,H.;Wei,W.;Sun,Y.H.Acta Phys.-Chim.Sin.2014,30,1155.[高 鹏,李 枫,赵 宁,王 慧,魏 伟,孙予罕.物理化学学报,2014,30,1155.]doi: 10.3866/PKU.WHXB201401252
(12) Ma,Z.Y.;Yang,C.;Wei,W.;Li,W.H.;Sun,Y.H.J.Mol. Catal.A:Chem.2005,231,75.doi:10.1016/j.molcata. 2004.12.026
(13) Fornero,E.L.;Sanguineti,P.B.;Chiavassa,D.L.;Bonivardi, A.L.;Baltanás,M.A.Catal.Today2013,213,163.doi: 10.1016/j.cattod.2013.03.012
(14) Esposito,S.;Turco,M.;Bagnasco,G.;Cammarano,C.;Pernice, P.;Aronne,A.Appl.Catal.A2010,372,48.
(15) Chen,H.W.;Yin,A.Y.;Guo,X.Y.;Dai,W.L.;Fan,K.N.Catal.Lett.2009,131,632.doi:10.1007/s10562-009-0008-x
(16) Aguila,G.;Valenzuela,A.;Guerrero,S.;Araya,P.Catal. Commun.2013,39,82.doi:10.1016/j.catcom.2013.05.007
(17) Wang,L.X.;Zhu,W.C.;Zheng,D.F.;Yu,X.;Cui,J.;Jia,M. J.;Zhang,W.X.;Wang,Z.L.Reac.Kinet.Mech.Catal.2010,101,365.doi:10.1007/s11144-010-0216-9
(18) Li,W.;Yin,Y.Q.;Gao,R.X.;Hou,R.L.J.Mol.Catal.1999,13,186.[李 文,殷元骐,高润雄,侯瑞玲.分子催化,1999,13,186.]
(19) Zhao,N.;Yang,C.;Wei,W.;Wang,T.Y.;Sun,Y.H.;Zhang,J.; Xie,Y.N.;Hu,T.D.Chin.J.Catal.2002,23,571.[赵 宁,杨 成,魏 伟,王太英,孙予罕,张 静,谢亚宁,胡天斗.催化学报,2002,23,571.]
(20) Ishihara,T.;Harada,K.;Eguchi,K.;Arai,H.J.Catal.1992,136,161.doi:10.1016/0021-9517(92)90115-X
(21) Chen,J.G.;Xiang,H.W.;Dong,Q.N.;Wang,X.Z.;Sun,Y.H.Acta Phys.-Chim.Sin.2001,17,161.[陈建刚,相宏伟,董庆年,王秀芝,孙予罕.物理化学学报,2001,17,161.]doi: 10.3866/PKU.WHXB20010214
(22) Pokrovski,K.;Jung,K.T.;Bell,A.T.Langmuir2001,17, 4297.doi:10.1021/la001723z
(23) Mudiyanselage,K.;Kim,H.Y.;Senanayake,S.D.;Baber,A. E.;Liu,P.;Stacchiola,D.Phys.Chem.Chem.Phys.2013,15, 15856.doi:10.1039/c3cp52295d
(24) Jung,K.D.;Bell,A.T.J.Catal.2000,193,207.doi:10.1006/ jcat.2000.2881
(25) Smith,K.J.;Anderson,R.B.Can.J.Chem.Eng.1983,61, 40.doi:10.1002/cjce.v61:1
(26) Xu,R.;Wei,W.;Li,W.H.;Hu,T.D.;Sun,Y.H.J.Mol.Catal. A:Chem.2005,234,75.doi:10.1016/j.molcata.2005.01.048
(27) Zhao,N.;Xu,R.;Wei,W.;Sun,Y.H.React.Kinet.Catal.Lett.2002,75,297.doi:10.1023/A:1015203113811
(28) Xu,X.;Doesburg,E.B.M.;Scholten,J.J.F.Catal.Today1987,2,125.doi:10.1016/0920-5861(87)80002-0
(29) Mahdavi,V.;Peyrovi,M.H.;Islami,M.;Mehr,J.Y.Appl. Catal.A2005,281,259.doi:10.1016/j.apcata.2004.11.047
(30) Zhang,H.;Chu,W.;Xu,H.;Zhou,J.Fuel2010,89,3127.doi: 10.1016/j.fuel.2010.04.014
(31) Majocchi,L.;Lietti,L.;Beretta,A.;Forzatti,P.;Micheli,E.; Tagliabue,L.Appl.Catal.A1998,166,393.doi:10.1016/ S0926-860X(97)00281-0
(32) Smith,K.J.;Anderson,R.B.J.Catal.1984,85,428.doi: 10.1016/0021-9517(84)90232-X
(33) Wu,Y.Q.;Xie,H.J.;Kou,Y.L.;Tan,L.;Han,Y.Z.;Tan,Y.S.J.Fuel Chem.Technol.2013,41,868.[武应全,解红娟,寇永利,谭 理,韩怡卓,谭猗生.燃料化学学报,2013,41,868.] doi:10.1016/S1872-5813(13)60036-5
(34) Fisher,I.A.;Bell,A.T.J.Catal.1997,172,222.doi:10.1006/ jcat.1997.1870
(35) Wu,G.S.;Zhao,N.;Chen,X.P.;Ren,J.;Sun,Y.H.J.Fuel Chem.Technol.2001,29,490.[吴贵升,赵 宁,陈小平,任杰,孙予罕.燃料化学学报,2001,29,490.]
(36) Sanchez-Escribano,V.;Larrubia,V.M.A.;Finocchio,E.Appl. Catal.2007,136,68.
(37) Kiennemann,A.;Idriss,H.;Kieffer,R.;Chaumette,P.;Durand, D.Ind.Eng.Chem.Res.1991,30,1130.doi:10.1021/ ie00054a009
Influence of Cu on the K-LaZrO2Catalyst for Isobutanol Synthesis
WU Ying-Quan1,2WANG Si-Chen3XIE Hong-Juan1GAO Jun-Wen3TIAN Shao-Peng1,2HAN Yi-Zhuo1TAN Yi-Sheng1,*
(1State Key Laboratory of Coal Conversion,Institute of Coal Chemistry,Chinese Academy of Sciences, Taiyuan 030001,P.R.China;2University of the Chinese Academy of Sciences,Beijing 100049,P.R.China;3Shaanxi Yanchang Petroleum(Group)Corp.Ltd.,Xi'an 710075,P.R.China)
The K-LaZrO2and K-CuLaZrO2catalysts used for the synthesis of isobutanol from syngas have been characterized by X-ray diffraction(XRD),temperature programmed desorption(TPD),X-ray photoelectron spectrometry(XPS),Fourier transform infrared(FTIR)spectroscopy,and chemical enrichment methods.The results of these analyses indicated that a solid solution of Cu-Zr was formed after the addition of Cu,and that the CuO was well dispersed.Furthermore,the addition of Cu inhibited the formation of t-ZrO2.CO-TPD showed that the addition of Cu led to an increase in the amount of CO adsorbed by the catalyst.Furthermore,H2-TPD showed that the addition of Cu led to an increase in the amount of H2adsorbed at low temperatures,which was related to the activity of catalyst.The results of FTIR and chemical enrichment analyses also revealed that the level of CO adsorption increased following the addition of Cu,as well as amount of C1intermediates.Taken together,these results indicated that the activity of catalyst was significantly enhanced by the addition of Cu and that the selectivity towards isobutanol increased up to 48.5%when the reaction was conducted at p=10.0 MPa,gas hourly space velocity(GHSV)=3000 h-1,T=360°C,and V(H2)/V(CO)=1:1.
CuO;ZrO2-based catalyst;Syngas;Isobutanol
O643
10.3866/PKU.WHXB201411241www.whxb.pku.edu.cn
Received:October 1,2014;Revised:November 21,2014;Published on Web:November 24,2014.
∗Corresponding author.Email:tan@sxicc.ac.cn;Tel:+86-351-4044287.
The project was supported by the Prospective Project of Institute of Coal Chemistry,Chinese Academy of Sciences(2011SQZBJ13)and Cooperative Project of Shaanxi Yanchang Petroleum(Group)Corp.Ltd.,China(JT1014SKF0003).
中国科学院山西煤炭化学研究所前瞻性布局项目(2011SQZBJ13)和陕西延长石油(集团)有限责任公司合作项目(JT1014SKF0003)资助

