富血小板纤维蛋白盖髓的动物实验研究
富血小板纤维蛋白盖髓的动物实验研究
李响1,孙淑芬1*,姜南1,武兴2
(1.吉林大学口腔医学院,吉林 长春130021;2.吉林大学第一医院)
直接盖髓术是用药物覆盖在牙髓暴露处,以保护牙髓、保存牙髓活力的方法。而直接盖髓术能否成功与盖髓剂有着密切的关系,寻找一种性能优越的盖髓材料一直是学者们所关注的问题。富血小板纤维蛋白(platelet-rich fibrin,PRF)是一种富含自体细胞因子和生长因子的新型生物材料。目前PRF已经被应用于口腔颌面外科、牙周科和口腔种植等领域,并均取得了较好的临床疗效,但关于将PRF作为盖髓剂应用于牙体的报道却很少。据报道,PRF具有很好的促进牙髓细胞增殖和分化的能力,且在组织愈合、炎症调节和抗感染方面也具有良好的效果[1,2]。本实验以PRFDycal、Dycal及PRF分别作为盖髓剂对家兔门齿进行直接盖髓术,观察术后牙髓的炎症情况和修复性牙本质的形成程度。
1材料与方法
1.1实验动物及分组选取3.0-3.5 kg的健康家兔21只及对照兔1只(购于吉林大学口腔医院动物实验室),左右上颌前牙共42颗实验牙,分为3组:PRFDycal组、Dycal组和PRF组,5 d和10 d两个实验周期。
1.2主要材料和试剂Dycal(登士柏,美国)、玻璃离子水门汀(上海医疗器械股份有限公司齿科材料厂)、台式低温高速离心机(贝克曼仪器公司 美国)、电子天平(上海越平科学仪器有限公司)、显微镜及照相系统(日本)、自动脱水处理机(徕卡显微系统上海有限公司)、常规手术器械(吉林大学口腔医院病理科提供)
1.3实验方法
1.3.1实验步骤自家兔耳中动脉采血制备PRF膜[1]。按0.1 ml/kg注射氯眠宁麻醉动物,仰卧固定;用3%的H2O2液清洁口腔,洗必泰消毒实验牙齿;用006球钻在唇侧颈部制洞,见洞底透红后,用自制直径0.5 mm的探针轻轻穿髓,生理盐水冲洗,无菌棉球轻压止血,将盖髓剂分别放于漏髓处,然后以玻璃离子水门汀充填窝洞。
1.3.2组织学标本制作分别在术后5 d和10 d灌流处死实验动物,分离上下颌骨,4%多聚甲醛固定72 h,15%EDTA(pH=7.2-7.4)脱钙6周,自动脱水机脱水,包埋,以平行于牙长轴方向做颊舌向连续切片,HE染色,树胶封片,光镜下进行组织学观察。
1.4统计学方法
采用 SPSS 17.0 软件包进行统计学分析。卡方检验分析数据。P<0.05 表示差异有统计学意义。
2结果
PRFDycal、Dycal及PRF分别作为盖髓剂对家兔门齿进行直接盖髓术,术后5d组织学观察结果见图1。PRFDycal组(图1a):均未见修复性牙本质桥形成。4例露髓口下方可见散在的钙化团块,大量炎症细胞聚集。2例无钙化物形成,露髓口下方大量中性粒细胞、浆细胞聚集,血管数量增加,扩张充血明显。1例牙髓细胞坏死或崩解,髓腔空虚。Dycal组(图1b):均未见修复性牙本质桥形成。4例露髓口下方可见散在的钙化团块,大量炎症细胞聚集。3例牙髓细胞坏死或崩解,髓腔空虚。PRF组(图1c):均未见修复性牙本质桥形成。4例无钙化物形成,露髓口下方大量中性粒细胞、浆细胞聚集,血管数量增加,扩张充血明显。3例牙髓细胞坏死或崩解,髓腔空虚。术后10d组织学观察结果见图1。PRFDycal组(图1d):3例可见修复性牙本质桥形成,髓腔内可见散在的钙化团块,露髓口下方可见少量炎细胞或无炎细胞。4例无完整修复性牙本质桥形成,但髓腔内可见大量钙化团块形成,隔绝损伤处与健康牙髓,露髓口下方可见中等程度炎细胞聚集及血管增生、扩张充血。Dycal组(图1e):1例可见修复性牙本质桥形成,髓腔内可见散在的钙化团块,中等程度炎细胞聚集。2例无完整修复性牙本质桥形成,但髓腔内可见大量钙化团块,呈弥漫性钙化。4例牙髓细胞坏死或崩解,髓腔空虚。PRF组(图1f):1例髓腔内可见少量钙化团块形成,2例未见钙化团块形成,此3例牙髓内均有大量炎症细胞聚集,血管数量增加,扩张充血明显。4例牙髓细胞坏死或崩解,髓腔空虚。
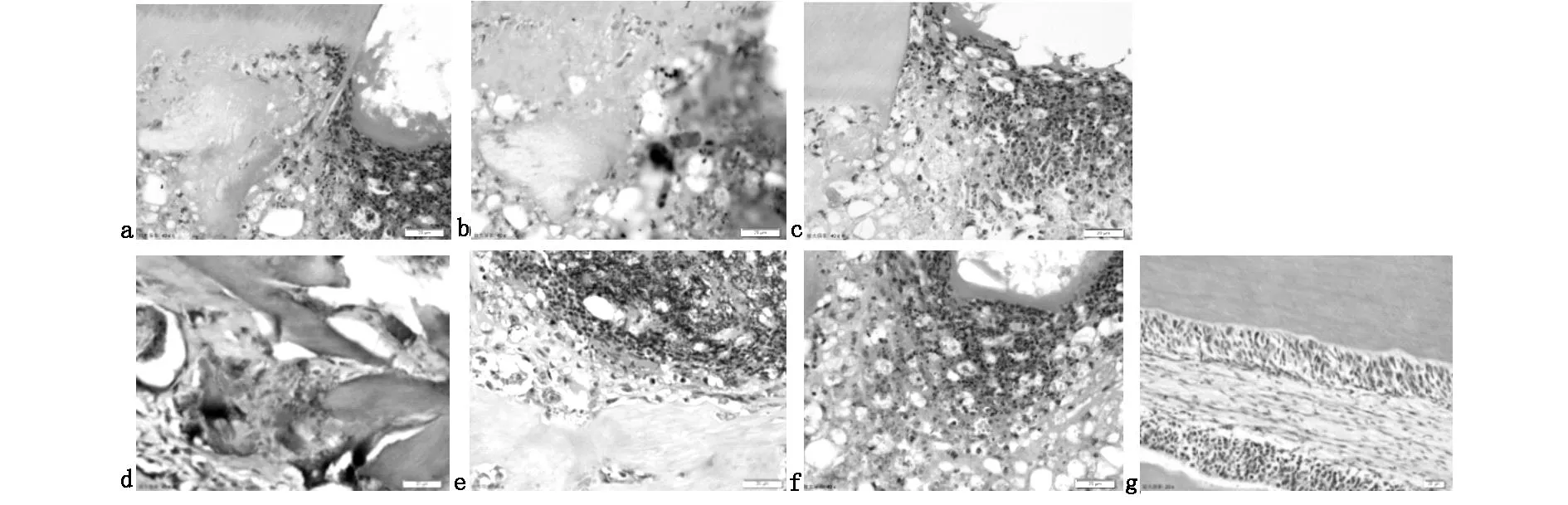
a PRFDycal直接盖髓后5 d(HE×40);b Dycal直接盖髓后5 d(HE×40);c PRF直接盖髓后5 d(HE×40);d PRFDycal直接盖髓后10 d(HE×40);e Dycal直接盖髓后10 d(HE×40);f PRF直接盖髓后10 d(HE×40);g 正常牙髓组织(HE×40)
图1HE染色图片
3讨论
目前临床常用的盖髓材料中,以氢氧化钙制剂的应用最为广泛,且疗效也相对肯定,是常规盖髓材料的金标准[3],故选作本实验的对照材料。有机生物材料对修复性牙本质形成具有很强的促进作用,但异体生物材料存在潜在的排异反应,获取成本也较高,不适合临床推广应用[4]。富血小板纤维蛋白(PRF)是新一代自体有机生物材料,取材简便,成本低廉,且不存在免疫排斥反应。PRF中含有大量的血小板和白细胞,其纤维蛋白将血小板与生物因子以化学键的方式相结合,并可缓慢释放其中的生物因子,包括血小板衍生生长因子AB(PDGF-AB) 、转化生长因子-β1(TGF-β1)、血管内皮生长因子(VEGF )、胰岛素样生长因子(IGF-1)、表皮生长因子 (EGF) 等[5]。
本实验选取家兔作为实验动物,由于家兔属大型啮齿类动物,身体抵抗力好,便于取血,牙齿生长速度快,牙髓自身修复能力较强,虽然与人类牙齿存在较大差异,但其快速修复能力可使我们能够在PRF有效释放主要生物因子期间观察到PRF在牙髓损伤修复中的作用。有研究指出,PRF能够缓慢释放生物因子持续7-10天[6],最长可达28 d[7]。故本实验设计5 d和10 d两个周期,本实验周期的设计与家兔牙齿的生长速度和PRF的生物因子释放速度相吻合。
体外研究指出,PRF促进牙髓细胞增殖和分化,显著上调碱性磷酸酶(ALP)和骨保护素(OPG)的表达,促进修复性牙本质的形成[2]。另有大量研究证明,PRF主要通过缓慢释放生物因子实现其生物学作用,PRF释放的生物因子在牙髓损伤修复中具有重要的作用,其中,PDGF-AB对多种细胞均具有强效的趋化作用,促进牙髓细胞增殖和分化,同时它又是成纤维细胞的有丝分裂剂,促使成纤维细胞增殖[8,9]。TGF-β1和EGF均可促进牙髓细胞增殖、迁移和分化,且TGF-β1 在损伤的牙髓中还参与基质的分泌和免疫反应过程[10,11]。
以上研究均是PRF在体外的诸多促进表现,根据其表现我们推测,PRF可能会在牙髓损伤修复中发挥其积极的生物学作用,故我们进行了此项实验研究,但PRF组却得到了与预期相反的结果。PRF组结果显示:术后5 d时和10 d时,几乎无修复性牙本质形成,且牙髓内呈现不同程度的炎症表现。为什么性能优越的PRF在本实验中却没有优越的结果出现,我们分析原因可能是:试验中我们在PRF外以玻璃离子水门汀封洞,而玻璃离子对牙髓具有一定的刺激性,会引起牙髓坏死;另外,PRF膜直接覆盖在露髓口上,其封闭性能较差,加之PRF膜表面湿度较大,而玻璃离子遇水不易固化,影响其封闭性,易形成边缘微渗漏[12]。术后难以避免细菌侵入牙髓,使牙髓受到了外界的污染刺激,而刺激程度超过了PRF的修复能力,导致PRF的优越性能不能体现出来,至牙髓崩解坏死,这可能是引起本实验PRF组出现阴性结果的主要原因。
虽然PRF组的结果不尽如人意,但本实验还出现了另外一种非常值得我们思考的结果:术后5 d,PRFDycal组与Dycal组均无牙本质桥形成,但牙髓内均有修复性牙本质钙化团块形成,无统计学差异;而术后10 d,PRFDycal组除了有多例牙本质桥形成外,牙髓内还有大量的修复性牙本质的钙化团块形成,且形成量及例数均明显较Dycal组多,具有统计学差异。我们还观察到,在PRFDycal组所形成的大量修复性牙本质钙化团块中多处可见被包裹的成牙本质细胞(如图d)。这可能由于PRFDycal激活牙髓内的未分化的间充质细胞分化为成牙本质细胞或为损伤的成牙本质细胞,在损伤部位快速分泌牙本质基质,由于形成速度过快,导致部分成牙本质细胞被包裹在钙化团块中,形成一种骨样牙本质状的钙化物。PRFDycal组之所以出现如此显著的疗效,我们分析原因可能由于两种材料互相促进,取长补短,各自发挥优势导致的。因为Dycal的颗粒小,流动性好,可以覆盖PRF及其边缘,并很快凝固,故边缘封闭性良好,且硬度及强度较大[3],弥补了PRF封闭性差、湿度大的缺点,并保持了PRF缓慢释放生物因子和促进细胞增殖、分化及修复性牙本质形成的优点;同时PRF也缓冲了Dycal的强碱性,减轻了Dycal的细胞毒性,弥补了Dycal生物相容性差的缺点[14],并保持了其抗菌性及促进修复性牙本质形成的优点[3,13]。两个周期内,PRFDycal组均无变性和坏死现象出现,而Dycal组出现多例牙髓弥漫性钙化、变性和坏死,可能由于Dycal具有强碱性,易造成与之相接触的牙髓组织出现局部变性和坏死导致的[14]。
更值得关注的是,PRFDycal组有钙化桥形成的样本中炎症明显减轻甚至无炎症,而Dycal组和PRF组均存在不同程度的炎症。可能由于PRF中富含大量与免疫调节相关的细胞因子, Dohan DM 等分析PRF中存在的主要白细胞,包括3种促炎细胞因子IL-1β,IL-6,TNF-α,一个抑炎细胞因子IL-4和一个血管生成促进因子VEGF,它们通过分泌细胞因子作用于止血和炎症反应过程,研究结果显示PRF具有促进组织愈合,在炎症调节和抵抗感染方面可能发挥一定的积极作用[1]。说明PRF在有Dycal存在时的抗炎调节作用更加显著。
本实验以PRF作为盖髓剂应用于牙髓损伤的修复治疗中,对其可行性和应用方式进行初步探索,从本次试验的结果中可以得出结论:PRFDycal可以更好的发挥促进修复性牙本质形成和抗炎调节的作用。但单独以PRF膜作为盖髓材料在封闭性能上存在着一定的缺陷,有望在后续实验中将此材料的应用方式改良,使其更有效的发挥优势。
参考文献:
[1]Dohan DM,Choukroun J,Diss A,et al.Platelet-rich fibrin(PRF):a second-generation platelet concentrate[J].Oral Surg Oral Med Oral Pathol Oral Radiol Endod,2006,101:e37.
[2]Huang FM,Yang SF,Zhao JH,et al.Platelet-rich fibrin increases proliferation and differentiation of human dental pulp cells[J].J Endod,2010,36(10):1628.
[3]Parolia A,Kundabala M,Rao NN,et al.A comparative histological analysis of human pulp following direct pulp capping with Propolis,mineral trioxide aggregate and Dycal[J].Aust Dent J,2010,55(1):59.
[4]Ko H,Yang W,Park K,et al.Cytotoxicity of mineral trioxide aggregate ( MTA) and bone morphogenetic protein 2(BMP-2) andresponse of rat pulp to MTA and BMP-2[J].Oral Surg Oral Med Oral Pathol Oral Radiol Endod,2010,109(6):e103.
[5]Kang YH,Jeon SH,Park JY,et al.Platelet-rich fibrin is a bio-scaffold and reservoir of growth factors for tissue regeneration[J].Tissue Eng Part A,2011,17(3-4):349.
[6]Dohan Ehrenfest DM,de Peppo G M,Doglioli P,et al.Slow release of growth factors and thrombospondin-1 in Choukroun's platelet-rich fibrin (PRF):a gold standard to achieve for all surgical platelet concentrates technologies[J].Growth Factors,2009,27(1):63.
[7]He L,Lin Y,Hu X,et al.A comparative study of platelet-rich fibrin ( PRF) and platelet-rich plasma ( PRP) on the effect of proliferation and differentiation of rat osteoblasts in vitro[J].Oral Surg Oral Med Oral Pathol Oral Radiol Endod,2009,108:707.
[8]Yokose S,Kadokura H,Tajima N .Platelet-derived growth factor exerts disparat e effect s on odontoblast differentiation depending on the dimers in rat dental pulp cells[ J] .Cell Tissue Res,2004 ,315(3):375.
[10]FargesJ C,Romeas A,Melin M,et al.TGF-beta1 induces accumulation of dendritic cells in the odontoblast layer[J].J Dent Res,2003,82(8):652.
[11]Melin M,Joffre-Romeas A,FargesJ C,et al.Effects of TGF-beta 1 on dental pulp cells in cultured human tooth slices[J].J Dent Res,2000,79(9):1689.
[12]崔恺,陈吉华,赵三军.玻璃离子水门汀的研究进展[J].牙体牙髓牙周病学杂志,2008,11:644.
[13]Leye Benoist F,Gaye Ndiaye F,Wakhade Kane A,et al.Evaluation of mineral trioxide aggregate ( MTA) versus calcium hydroxide cement(Dycal) in the formation of a dentine bridge:a randomized controlled trial[J].Int Dent J,2012,62(1):33.
[14]Guven EP,Yalvac ME,Sahin F,et al. Effect of dental materials calcium hydroxide-containing cement,mineral trioxide aggregate,and enamel matrix derivative on proliferation and differentiation of human tooth germ stem cells[J]. J Endod,2011,37(5):650.
收稿日期:(2013-09-27)
文章编号:1007-4287(2015)03-0363-03
通讯作者*

