离子液体基磁性固相萃取技术的研究进展
刘 勤,何丽君,杨 君,范 璐,江秀明
(河南工业大学 化学化工学院,河南 郑州 450001)
前处理是整个样品分析过程中的重要环节,随着样品基质越来越复杂,目标分析物含量越来越低,建立快速、简单、可靠、绿色的样品前处理技术一直是分析化学工作者关注的热点。磁性固相萃取(Magnetic solid-phase extraction,MSPE)是一种利用磁性材料作为吸附剂的新型样品前处理技术。在MSPE中,磁性吸附剂与样品基质通过外部磁场分离,目标分析物被洗脱剂从磁性吸附剂上洗脱下来,进入光谱或者色谱仪进行分析[1]。MSPE技术具有操作简单、萃取时间短、有机溶剂用量少的优点,且避免了传统的固相萃取小柱易堵塞以及不能重复利用的缺陷,已被成功地应用于环境、食品和生物样品的萃取富集[2-6]。磁性吸附剂的种类是决定萃取效率高低的关键因素,因此设计和制备新型磁性吸附剂已成为MSPE的发展趋势。
离子液体(Ionic liquid,IL)是由有机阳离子和无机/有机阴离子构成,在室温或者其附近呈液态的有机盐类。IL具有的独特物化性质使其广泛应用于有机合成、催化和分离分析领域。IL对目标分析物的良好萃取能力,其结构的可设计性和易功能化使其在液相微萃取[7-8]、分散液液微萃取(Dispersive liquid - liquid microextraction,DLLME)[9-12]、固相萃取[13-14]和固相微萃取[15-16]中已作为一种优良的液相萃取剂或者固载式吸附剂被广泛关注。
将IL固载在磁性颗粒表面,作为MSPE的吸附剂,能够充分发挥两者的优势。2010年,Yao研究小组[17]首次将1-癸基/十六烷基-3-甲基咪唑溴负载在Fe3O4的表面制备磁性吸附剂,萃取油样及水样中的多环芳烃(Polycyclic aromatic hydrocarbon,PAH)。近年来,关于IL-MSPE的应用研究增多,本文介绍了IL修饰磁性吸附剂的制备方法,IL-MSPE的萃取方式,以及近5年来其在有机物污染物、金属离子和生物活性物质的分离富集中的应用。
1 IL修饰磁性吸附剂的制备方法
在MSPE中,磁性颗粒(Magnetic particles,MPs)主要有Fe3O4,γ-Fe2O3和S-BaFe,但其单分散性差、易团聚和被氧化。对磁性颗粒表面进行改性,可以抑制磁性微球被氧化,改善分散性,使其易于进一步改性[6]。Fe3O4以及经SiO2改性的Fe3O4(Fe3O4@SiO2)是目前IL修饰磁性吸附剂中应用最广泛的磁性载体。
1.1 物理涂覆法
物理涂覆法是利用疏水作用等将IL直接涂覆在MPs表面以制备IL负载的磁性吸附剂(如图1所示)。在此方法中,MPs被分散在溶解有IL的溶剂中,IL被MPs充分吸附后,利用外部磁场收集IL-MPs,蒸发溶剂以干燥IL-MPs。Hu研究小组[18]将甲基三辛基氯化铵盐涂覆在Fe3O4@SiO2的表面制备磁性吸附剂,并以其萃取尿液及头发中的Cu2+,Zn2+和Cd2+。Wang研究小组[19-20]利用此方法将IL直接涂覆在Fe3O4@碳纳米管或Fe3O4@壳聚糖@氧化石墨烯磁性颗粒表面,并将制备的磁性吸附剂用于生物样品中蛋白质的萃取。为了增加IL在MPs上的涂覆量,提高萃取效率,文献 [21-22]对上述方法进行改进,不通过磁场,直接蒸发溶剂干燥IL-MPs,延长了涂覆时间,增加了涂覆量。物理涂覆法虽能成功地制备IL-MPs,但MPs上的IL不稳定,易脱落,且涂覆量少。
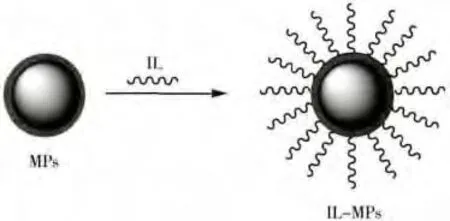
图1 物理涂覆法制备IL-MPs示意图Fig.1 Schematic diagram of the preparation of IL-MPs by physical coating method
1.2 化学键合法
化学键合法是通过化学反应将IL键合至磁性微球(Fe3O4@SiO2)表面制备IL修饰的磁性吸附剂。采用此法制备的IL-MPs,IL键合量大,稳定,可重复使用多次。键合方式包括直接法和间接法两种。
直接法是将IL单体直接键合在硅烷化的Fe3O4@SiO2表面(如图2Ⅰ)。2013年,Jia研究小组[23]首次用此方法制备N-甲基咪唑负载的磁性吸附剂,并用于转基因大豆中DNA的萃取。本实验室用此方法将1-乙烯基-3-己基咪唑溴盐共价聚合至Fe3O4@SiO2的表面,首次制备出聚合IL负载的磁性吸附剂,聚合IL相对于普通IL有更多的作用位点,负载量更大,能用于茶饮料中有机磷农药的高效萃取[24]。
间接法则是先将IL硅烷化,然后将硅烷化的IL键合在Fe3O4@SiO2表面(如图2Ⅱ)。Zougagh等[25]首次用此方法制备N-甲基咪唑负载的磁性吸附剂,并用于河水中磺酰脲类除草剂的萃取。采用直接法时,MPs要经过若干高温过程,易被氧化,吸附剂的磁性强度会有所降低,从而影响磁性材料的分离效果。而间接法制备IL-MPs可减轻以上问题,但键合时空间位阻大,IL的键合量受影响。
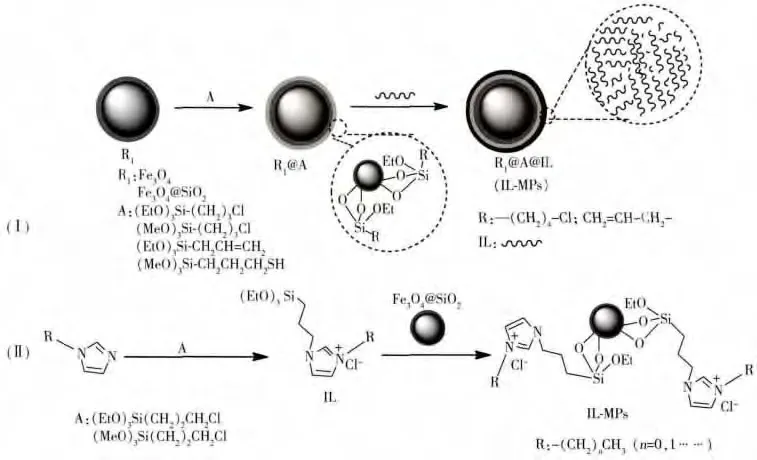
图2 直接(Ⅰ)和间接(Ⅱ)化学键合法制备IL-MPs的示意图Fig.2 Schematic diagrams of the preparation of IL-MPs by direct(Ⅰ)and indirect(Ⅱ)chemical bonding methods
1.3 包埋法
包埋法是将MPs表面用油酸等修饰,然后将含有双键的聚合物通过自由基反应直接聚合在磁性材料的表面,溶液中的IL在聚合的同时被包埋在聚合物和磁性材料之间的空隙中。此方法比化学键合法制备过程简单,且比物理涂覆法制备的IL-MPs热稳定性高。2014年,Yan研究小组[26]用此方法将1-甲基-3-丁基咪唑六氟磷酸盐包埋在聚甲基丙烯酸乙二醇酯和十八油酸之间的孔穴中,并应用于尿液中磺胺甲基嘧啶和磺胺氯吡嗪的萃取富集。
2 IL-MSPE萃取方式
IL-MSPE包括传统MSPE、混合半胶束-MSPE(MH-MSPE)和分散液液微萃取-MSPE(DLLMEMSPE)3种萃取方式。根据IL和目标分析物的种类选择合适的萃取方式可以获得更好的萃取效果。
2.1 传统MSPE萃取
传统的MSPE方式如图3A所示,将制备好的IL-MPs分散在含有目标分析物的样品中,通过辅助手段(超声、旋涡或振荡)使吸附剂充分吸附目标分析物,利用外界磁场将磁性吸附剂和样品基质分离。加入洗脱剂解吸目标分析物后,取适量体积的洗脱剂进行检测分析。Zougagh研究小组[25]首次用此萃取方式对河水中的磺酰脲类除草剂进行了萃取分离。此萃取方式操作简单,但IL-MPs需要提前制备,且若IL-MPs放置时间过长,未被完全包覆的磁性核易被氧化,导致其磁性减弱。
2.2 MH-MSPE萃取
MH-MSPE是指将带有较长碳链的IL和磁性颗粒分散在溶液中,IL在超声、旋涡或振荡条件下负载在MPs表面形成混合半胶束,通过疏水、静电和π-π作用吸附萃取目标分析物,其吸附和解吸过程与传统的MSPE方式类似(如图3B所示)。Luo研究小组[27]将1-十六烷基-3-甲基咪唑溴盐负载在Fe3O4表面形成混合半胶束,并用其萃取环境水样中的氯酚类物质。He等[28-29]将相同的IL分别负载在磁性碳纳米管和Fe3O4@SiO2表面形成半胶束,用于萃取分离尿样中的黄酮类物质。此萃取方式无需提前制备磁性吸附剂,总耗时短,但磁性微球负载的IL量少,萃取效率低;另外,IL-MPs表面脱落的IL会对目标分析物的分离检测产生干扰。
2.3 DLLME-MSPE萃取
DLLME-MSPE在DLLME的基础上发展而来(如图3C所示)。其操作方式是将IL及MPs同时快速加入到样品溶液中,IL呈细小液滴状均匀分散在样品中吸附目标分析物,而MPs进一步吸附IL;后续分离和解吸过程与传统的MSPE类似。Yao研究小组[17]首次用此方式将1-癸基-3-甲基咪唑溴盐与Fe3O4结合后用于水样及油样中PAH的萃取。2013年,Gao研究小组[30]采用相同的方式将1-烷基(丁基、己基和辛基)-3-甲基咪唑双三氟甲磺酰亚胺和磁性微球结合后富集萃取果汁中的杀螨剂。DLLME-MSPE结合了DLLME和MSPE的优点,整个萃取过程耗时短,IL能与目标分析物充分接触,萃取效率高,且无需提前制备IL修饰磁性吸附剂,但洗脱剂中若含有IL,将会影响目标分析物的分离检测。
对于上述3种MSPE方式,影响其萃取效率的因素基本相同,主要有:负载IL的种类(包括阴阳离子的种类)、IL-MPs的用量、吸附时间、解吸剂的种类及体积、解吸时间、pH值、盐浓度等。
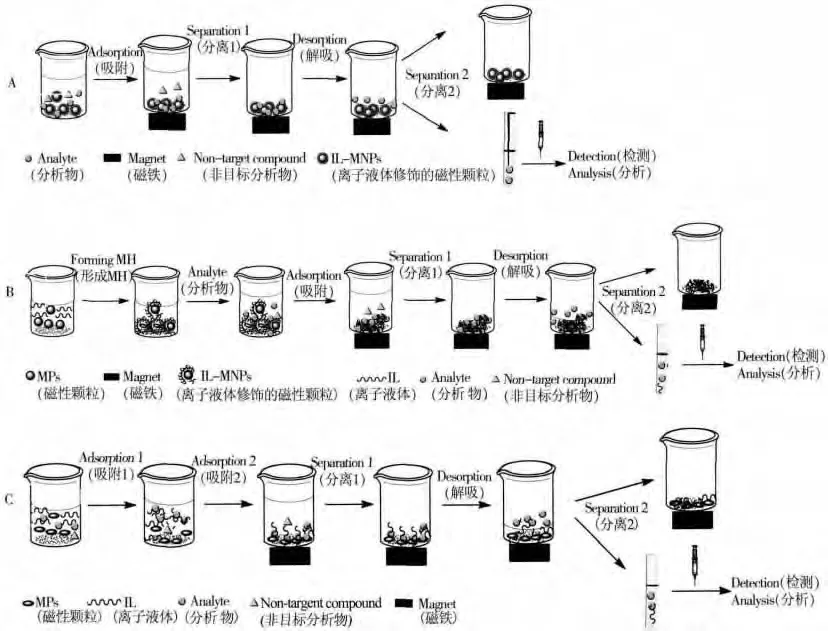
图3 传统MSPE(A)、MH-MSPE(B)及DLLME-MSPE(C)萃取方式示意图Fig.3 Schematic diagrams of traditional MSPE(A),MH-MSPE(B)and DLLME-MSPE(C)
3 IL-MSPE技术的应用
3.1 在有机污染物分析中的应用
IL-MSPE所具有的独特优点使其在有机污染物的样品前处理过程中得到了广泛应用。自从Yao等[17]报道IL修饰磁性材料萃取水样及油样中的PAH以来,IL-MSPE在萃取分离PAH中有较多应用,如:Valcárcel等[31]制备的IL修饰磁性吸附剂,磁性微球仅有12 nm,比表面积较大,对环境水样中PAH的富集倍数高达158倍。Lu研究小组[32]将1-十八烷基-3-甲基咪唑溴盐和甲基橙组装在Fe3O4@SiO2表面制备磁性吸附剂,结合HPLC-荧光检测,能分析环境水样中0.1~1.0 ng·L-1的PAH。IL - MSPE技术也广泛应用于农药残留的样品的前处理[21,24-26,30,33-36]。Gao 等[30,34]采用 DLLME - MSPE方式,用[C6MIM][NTf2]萃取蜂蜜及果汁中的杀螨剂及拟除虫菊酯。Zhou研究小组[35]将1-(3-氨丙基)-3-丁基咪唑溴键合在γ-Fe2O3表面,用于萃取水样中的除草剂。Zhu研究小组[22]将[C8MIM][PF6]负载在Fe3O4表面,并用于湖水、生菜及苹果中利谷隆农药的萃取。除了PAH及农药残留外,ILMSPE技术还被应用于酚类[27,37-38]及硝基苯类[39]等污染物的富集萃取,表1列出了IL-MSPE在有机污染物分析中的应用情况。

表1 IL-MSPE在萃取富集有机污染物中的应用Table 1 Application of IL-MSPE in extraction and enrichment of organic pollutants
3.2 在萃取富集金属离子中的应用
IL-MSPE利用外界磁场可将样品基质与吸附有目标分析物的IL-MPs分离,对复杂基质中微量金属离子的萃取富集有较好的效果[18,41-47]。Soylak研究小组[41]以 DLLME -MSPE 方式,用[C4MIM][PF6]萃取水样、植物和头发中的吡咯二硫代甲酸氨盐-Pb2+络合物,对Pb2+的富集倍数高达160倍。Shemirani研究小组[42]采用相同的萃取方式,将[C6MIM][PF6]和磁性微球结合,利用Pb2+和1-(2-吡啶偶氮)-2-萘酚形成配合物,分离富集土样及大米中的Pb2+。Hu等[18]将甲基三辛基氯化铵涂覆在MPs表面,与ICP-OES联用,测定尿样及头发中的 Cu2+,Zn2+和 Cd2+。马晓国等[46]将[C6MIM][PF6]涂覆在Fe3O4@SiO2表面,对湖水及河水中微量Cd2+进行了萃取富集。表2列出了IL-MSPE技术在萃取富集金属离子的应用。

表2 IL-MSPE技术在萃取富集重金属离子中的应用Table 2 Application of IL-MSPE in extraction and enrichment of heavy metal ions

(续表2)
3.3 在萃取分离生物活性物质中的应用
生物样品基质复杂,其含有的无机盐、蛋白质、脂肪等对样品中目标物的分离分析有影响。MSPE技术因具有易于将目标分析物与基质分离,操作简单等特点,在生物样品中也得到应用。Jia等将N-甲基咪唑键合在Fe3O4@SiO2表面制备磁性吸附剂,并用于转基因大豆中DNA[23]及水中细菌[48]的萃取,结果令人满意。Wang等[19]用羟基功能化的IL修饰的磁性微球作为吸附剂萃取分离蛋白质。另外,IL-MSPE技术还被用于尿样中的黄酮类[28-29]及营养品中蒽醌类[49]物质的萃取富集。表3列出了ILMSPE在萃取分离生物活性物质中的应用。
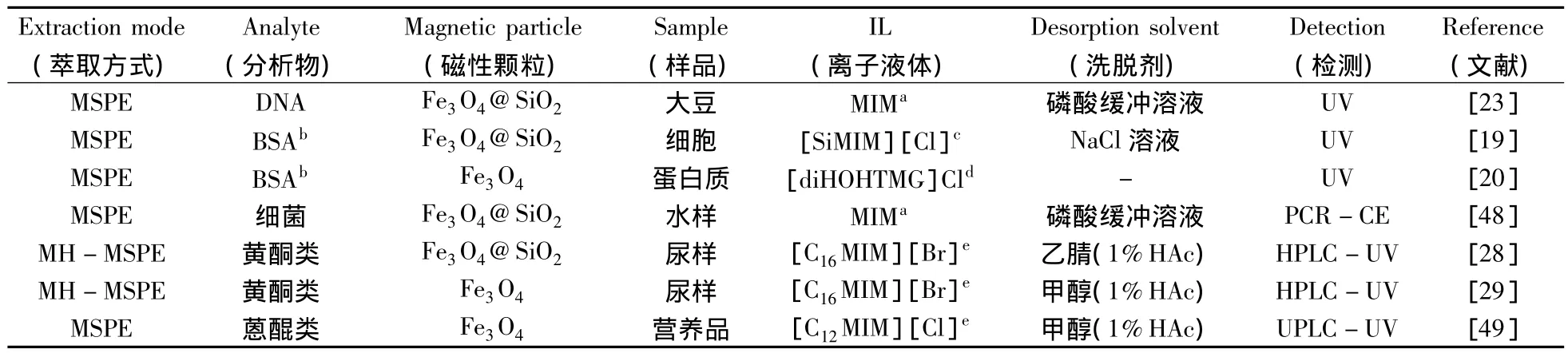
表3 IL-MSPE技术在萃取分离生物活性物质中的应用Table 3 Application of IL-MSPE in extraction and separation of biological active substances
4 展望
本文综述了IL修饰磁性吸附剂的制备方法、IL-MSPE的萃取方式,以及IL-MSPE结合色谱和光谱技术在有机污染物、金属离子和生物活性物质萃取分离中的应用。目前,IL-MSPE技术虽在样品前处理中得到了广泛关注,但如何根据特定目标物的种类设计IL的种类以实现对目标物的高效萃取仍是难题;颗粒细小的IL-MPs有利于萃取,但不易被收集,导致重复利用次数减少。因此,既能保证萃取效率又能使IL-MNPs可被多次重复使用,以及简化IL-MPs的制备过程,并制备出颗粒均匀的磁性颗粒以提高萃取重复性将成为IL-MSPE技术的发展方向。此外,目前发展的IL修饰磁性吸附剂主要为核壳结构,萃取效率依赖于磁性核表面的IL与分析物之间的作用,因此研发新型具有孔结构及网状结构的磁性吸附剂,并利用网孔结构的筛分作用提高萃取选择性也是IL-MSPE技术的发展趋势。
[1]Gao Q,Luo D,Ding J,Feng Y Q.J.Chromatogr.A,2010,1217:5602-5609.
[2]Wang Z,Wang C.Chin.J.Chromatogr.(王志,王春.色谱),2012,30(10):977-979.
[3]Wu K S,Xu H Y,Guo L,Liang Y Y,Xiong Y H.Food Sci.(吴科盛,许恒毅,郭亮,梁语嫣,熊勇华.食品科学),2011,32(23):317-320.
[4]Zhang S X,Niu H Y,Hu Z J,Cai Y Q,Shi Y L.J.Chromatogr.A,2010,1217:4757-4764.
[5]Huang C Z,Hu B.Spectrochim.Acta B,2008,63:437-444.
[6]Li X S,Zhu G T,Luo Y B,Yuan B F,Feng Y Q.Trend Anal.Chem.,2013,45:233-247.
[7]Chen X C,You X W,Liu F M,Hou F,Zhang X.J.Sep.Sci.,2015,38:93-99.
[8]Naeemullah,Kazi T G,Tuzen M.Food Chem.,2015,172:161-165.
[9]Liu L H,He L J,Jiang X M,Zhao W J,Xiang G Q,Anderson J L.J.Sep.Sci.,2014,37:1004 -1011.
[10]Clark K D,Nacham O,Yu H L,Li T H,Yamsek M M,Ronning D R,Anderson J L.Anal.Chem.,2015,87(3):1552-1559.
[11]Zheng X Y,He L J,Zhang K G,Jiang X M,Xiang G Q,Liu J P.J.Instrum.Anal.(郑小焱,何丽君,张凯歌,江秀明,向国强,刘建平.分析测试学报),2014,33(5):566-571.
[12]Chen X H,Wei X Q,Cai M Q,Zhao Y G,Pan S D,Jin M C.J.Instrum.Anal.(陈晓红,魏晓琴,蔡美强,赵永纲,潘胜东,金米聪.分析测试学报),2014,33(6):648-652.
[13]Ramandi N F,Shemirani F.Talanta,2015,131:404-411.
[14]Wang C L,Hu X L,Guan P,Wu D F,Qian L W,Song R Y.J.Pharm.Biomed.,2015,102:137-143.
[15]Cui M Y,Qiu J X,Li Z H,He M,Jin M S,Kim J,Quintoc M,Li D H.Talanta,2015,132:564-571.
[16]Zhang C,Anderson J L.J.Chromatogr.A,2014,1344:15-22.
[17]Zhang Q L,Yang F,Tang F,Zeng K,Wu K K,Cai Q Y,Yao S Z.Analyst,2010,135(9):2426 -2433.
[18]Cui C,Hu B,Chen B B,He M.J.Anal.At.Spectrom.,2013,28(7):1110-1117.
[19]Chen J,Wang Y Z,Ding X Q,Huang Y H,Xu K.Anal.Methods,2014,6:8358-8367.
[20]Ding X Q,Wang Y Z,Wang Y,Pan Q,Chen J,Huang Y H,Xu K J.Anal.Chim.Acta,2015,861:36-46.
[21]Peng B,Zhang J H,Lu R H,Zhang S B,Zhou W F,Gao H X.Analyst,2013,138:6834-6843.
[22]Chen J P,Zhu X S.Spectrochim.Acta A,2015,137:456-462.
[23]Deng M C,Jiang C,Jia L.Anal.Chim.Acta,2013,771:31 -36.
[24]Zheng X Y,He L J,Duan Y J,Jiang X M,Xiang G Q,Zhao W J,Zhang S S.J.Chromatogr.A,2014,1358:39-45.
[25]Bouri M,Gurau M,Salghi R,Cretescu I,Zougagh M,Rios A.Anal.Bioanal.Chem.,2012,404:1529-1538.
[26]Yan H Y,Gao M M,Yang C,Qiu M D.Anal.Bioanal.Chem.,2014,406:2669-2677.
[27]Cheng Q,Qu F,Li N B,Luo H Q.Anal.Chim.Acta,2012,715:113-119.
[28]He H,Yuan D H,Gao Z Q,Xiao D L,He H,Dai H,Peng J,Li N.J.Chromatogr.A,2014,1324:78-85.
[29]Xiao D L,Yuan D H,He H,Pham-Huy C,Dai H,Wang C X,Zhang C.Carbon,2014,72:274-286.
[30]Zhang J H,Li M,Li Y B,Li Z Y,Wang F F,Li Q,Zhou W F,Lu R H,Gao H X.J.Sep.Sci.,2013,36:3249-3255.
[31]Galán -Cano F,Alcudia-León M D C,Lucena R,Cárdenas S,Valcárcel M.J.Chromatogr.A,2013,1300:134 -140.
[32]Liu X F,Lu X,Huang Y,Liu C W,Zhao S L.Talanta,2014,119:341-347.
[33]Zhang J H,Li M,Yang M Y,Peng B,Li Y B,Zhou W F,Gao H X,Lu H H.J.Chromatogr.A,2012,1254:23-29.
[34]Li M,Zhang J H,Li Y B,Peng B,Zhou W F,Gao H X.Talanta,2013,107:81-87.
[35]Luo M,Liu D H,Zhao L,Han J J,Liang Y R,Wang P,Zhou Z Q.Anal.Chim.Acta,2014,852:88-96.
[36]Zhang R Z,Su P,Yang L,Yang Y.J.Sep.Sci.,2014,37:1503 -1510.
[37]Dong S Y,Huang G Q,Wang X H,Hu Q,Huang T L.Anal.Methods,2014,6:6783-6788.
[38]Bi W T,Wang M,Yang X D,Row K H.J.Sep.Sci.,2014,37:1632-1639.
[39]Cao X J,Shen L X,Ye X M,Zhang F F,Chen J Y,Mo W M.Analyst,2014,139:1938-1944.
[40]Yang M Y,Xi X F,Wu X L,Lu R H,Zhou W F,Zhang S B,Gao H X.J.Chromatogr.A,2015,1381:37-47.
[41]Yilmaz E,Soylak M.Talanta,2013,116:882-886.
[42]Ramandi N F,Shemirani F,Farahani M D.Microchim.Acta,2014,181(15/16):1833-1841.
[43]Ramandi N F,Shemirani F.Talanta,2015,131:404-411.
[44]Khan S,Kazi T G,Soylak M.Spectrochim.Acta A,2014,123:194-199.
[45]Gharehbaghi M,Farahani M D,Shemirani F.Anal.Methods,2014,23(6):9258-9266.
[46]Dang Y F,Ma X G,Zou J P.J.Instrum.Anal.(党永锋,马晓国,邹建平.分析测试学报),2012,31(7):823-827.
[47]Soylak M,Yilmaz E.Anal.Lett.,2015,48:464 -476.
[48]Wang Y,Deng M C,Jia L.Microchim.Acta,2014,181:1275-1283.
[49]Hu S S,Cao W,Dai H B,Da J H,Ye L H,Cao J,Li X Y.J.Agric.Food Chem.,2014,62(35):8822-8829.

