甲酸-盐酸还原浸出低品位软锰矿
明宪权,卢友志,陈南雄,李维健,郭雨桐,袁爱群,黄增尉,韦冬萍,唐雅芳
(1.中信大锰矿业有限责任公司,广西 南宁 530022;2.广西民族大学 化学化工学院 化学与生物转化过程新技术重点试验室,广西 南宁 530006)
目前,我国对低品位软锰矿的回收利用存在生产成本高、经济效益差等问题[1]。解决这些问题主要从还原工艺和锰盐电解两方面考虑。传统的两矿法[2]能耗大、渣量大且难处理、污染环境;近几年,以废糖蜜为还原剂的湿法还原工艺[3]因具有资源再利用率高、锰浸出率高等优点而被工业化,但电解所得的硫酸锰溶液中阳极板严重腐蚀,大大增加生产成本[4];停留在试验室规模的SO2、硫酸亚铁、木屑等湿法还原工艺存在副反应多或酸耗量大等问题[5-8]:因此,探求一种反应机制清晰、氧化产物明确、经济效益好的还原工艺十分重要。目前,锰盐的电解主要是以硫酸锰溶液作为电解液,由于锰和氢竞争析出,通常需加入二氧化硒添加剂来提高锰浸出率,但二氧化硒有剧毒,会对生产带来安全隐患。以氯化锰溶液为电解液电解锰,电解温度低,电流效率高,产品晶型更适合于电池用电解二氧化锰[9]。
试验以价格便宜、结构最简单的有机酸——甲酸作为还原剂,考察其在盐酸介质中还原浸出低品位软锰矿的工艺条件,旨在为锰资源的合理利用及高品质锰产品的研究开发提供新思路。
1 试验部分
1.1 试验原料与仪器
试验所用低品位软锰矿矿石粉取自广西大新锰矿,矿石粉中全锰、全铁及三氧化二铝的质量分数分别为20%、9.82%和8.23%。
试验用试剂包括:甲酸、硫酸、盐酸,均为分析纯;铁、铝标准溶液,国家钢铁材料测试中心;甲酸标准产品,阿拉丁公司。
分析仪器包括美国热电公司的ICAP-6300等离子体发射光谱仪(ICP-AES),美国Agilent Technology公司的Agilent1260高效液相色谱仪(HPLC)。
1.2 试验方法
取10.0g未过筛矿石粉和一定浓度的盐酸溶液置于250mL三口烧瓶中,机械搅拌,水浴加热至所需温度后加入甲酸,反应一段时间后过滤。滤液取样定容分析。滤液中锰质量浓度按硫酸亚铁铵滴定法检测,铁和铝质量浓度采用等离子体发射光谱法检测。金属浸出率计算公式为

式中:m0—浸出液中元素的质量,g;m1—矿石粉中元素的质量,g。
溶液中有机物含量采用高效液相色谱法测定。
2 试验结果与讨论
2.1 单因素试验
2.1.1 盐酸浓度对锰、铁、铝浸出率的影响
在反应温度为90℃、液固体积质量比为10∶1、甲酸用量为3mL,反应时间为1h条件下,盐酸浓度对锰、铁、铝浸出率的影响试验结果如图1所示。可以看出,随盐酸浓度增大,铁浸出率显著升高,由24.06%升高到62.82%;盐酸浓度由0.1mol/L增大到0.15mol/L时,锰浸出率由70.54%迅速升高到84.75%,之后,变化不大;铝浸出率随盐酸浓度增大缓慢升高,由17.79%升高到25.82%。综合考虑,确定适宜的盐酸浓度为0.3mol/L。

图1 盐酸浓度对锰、铁、铝浸出率的影响
2.1.2 甲酸用量对锰、铁、铝浸出率的影响
在盐酸浓度为0.3mol/L、液固体积质量比为10∶1、反应温度为90℃、反应时间为1h条件下,甲酸用量对锰、铁、铝浸出率的影响试验结果如图2所示。
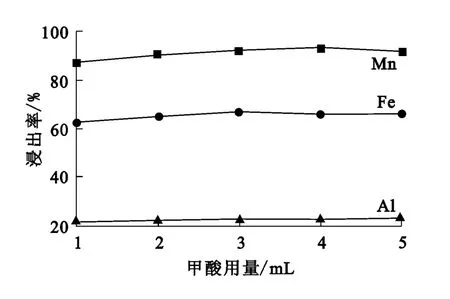
图2 甲酸用量对锰、铁、铝浸出率的影响
从图2看出,随甲酸用量增大,锰、铁、铝浸出率均变化不大。综合考虑,甲酸用量确定为3mL。
2.1.3 液固体积质量比对锰、铁、铝浸出率的影响
在盐酸浓度为0.3mol/L、甲酸用量为3 mL、温度为90℃、反应时间为1h条件下,液固体积质量比对锰、铁、铝浸出率的影响试验结果如图3所示。可以看出:随液固体积质量比由4∶1增大到8∶1,锰、铁浸出率提高明显,铝浸出率变化不大。这可能是因为在合适的搅拌条件下,液固体积质量比增大有利于物料之间的混合,但液固体积质量比过大,会导致还原剂浓度降低,不利于反应进行。综合考虑,确定适宜的液固体积质量比为10∶1。

图3 液固体积质量比对锰、铁、铝浸出率的影响
2.1.4 反应温度对锰、铁、铝浸出率的影响
在盐酸浓度为0.3mol/L、甲酸用量为3 mL、液固体积质量比为10∶1、反应时间为1h条件下,反应温度对锰、铁、铝浸出率的影响试验结果如图4所示。

图4 反应温度对锰、铁、铝浸出率的影响
从图4看出:随反应温度升高,锰、铁、铝浸出率均显著提高;60℃后,锰浸出率增速放缓;铁浸出率在反应温度高于50℃后保持稳定升高;铝浸出率增幅相对较小,但总体上也有所升高;反应温度达90℃时,铁浸出率达62.82%,锰浸出率增大幅度相对变小。考虑到后续工作中的处理负荷,反应温度不宜再升高,实际应用中,以90℃较为适宜。
2.1.5 反应时间对锰、铁、铝浸出率的影响
在盐酸浓度为0.3mol/L、甲酸用量为3 mL、液固体积质量比为10∶1、反应温度为90℃条件下,反应时间对锰、铁、铝浸出率的影响试验结果如图5所示。

图5 反应时间对锰、铁、铝浸出率的影响
从图5看出,反应时间对锰、铁、铝浸出率影响均不大。这可能是由于还原剂甲酸为液体,在搅拌条件下,能迅速与锰矿石粉混合并发生反应。综合考虑,确定反应时间以2.5h为宜。
2.2 正交试验
为探讨各因素对锰、铁、铝浸出率的影响主次顺序和最优反应条件,根据单因素试验结果,拟定5因素4水平正交试验方案。试验条件及结果见表1。可以看出:5因素对锰浸出率的影响顺序依次为盐酸浓度、液固体积质量比、甲酸用量、反应温度、反应时间;最优反应条件为:甲酸用量4 mL,盐酸浓度0.3mol/L,反应时间2.5h,反应温度90℃,液固体积质量比10∶1。结合各因素对锰、铁、铝浸出率的影响及生产成本的控制,将最优反应条件调整为:甲酸用量3mL,反应时间2h,液固体积质量比8∶1,盐酸浓度和反应温度保持不变。按照该条件进行平行验证试验,结果锰浸出率为93.4%,铁、铝浸出率分别为65.86%和27.54%。铁浸出率虽然相对较高,但电解液中铁的除杂工艺已比较成熟,不会对后续的氯化锰溶液电解产生太大干扰。

表1 试验条件及结果
2.3 反应机制推测
锰矿石粉中,锰的存在形式可能为 Mn2+、Mn2O3和 MnO2,铁主要以Fe2O3形式存在,铝以Al2O3形式存在,在以盐酸为介质、甲酸为还原剂条件下,可能发生的反应为:

有还原剂存在时,Mn2O3转化路径可能为Mn2O3→Mn3O4→MnO。显然,锰元素在盐酸溶液中最终以 Mn2+形式存在[10]。
为验证反应(1)能否完全反应,即甲酸是否被彻底氧化为CO2和H2O,分别对甲酸为理论量1 mL和过量3mL时,还原软锰矿的过滤液取样,采用HPLC测定其中有机物,同时参考白酒中甲醇的检测方法[11],对浸出液中甲醇和甲醛进行定性检测。甲醛测定时不加高锰酸钾和磷酸。结果表明:甲酸为理论量时,浸出液中甲酸残余量很少;即使过量条件下,浸出液中残留的甲酸量也不大,且未见其他有机物;而定性试验中,溶液亦不含甲醛和甲醇。由此可知,甲酸还原氧化锰的反应进行的比较完全,氧化产物只有CO2和H2O,未产生副产物。

表2 HPLC检测结果
3 结论
甲酸在盐酸溶液中还原浸出低品位氧化锰是可行的,反应进行的较完全,无副产物产生。正交试验结果表明:各因素对锰浸出率的影响顺序为盐酸浓度>液固体积质量比>甲酸用量>反应温度>反应时间;最优反应条件为:盐酸浓度0.3 mol/L,甲酸用量3mL,液固体积质量比8∶1,反应温度90℃,反应时间2h。最优条件下,锰、铁、铝浸出率分别为93.4%、65.86%和27.54%。
[1]徐昱,王建平,吴景荣,等.我国锰资源存在的问题及可持续开发对策[J].矿业研究与开发,2013,33(3):111-115.
[2]贺周初,彭爱国,郑贤福,等.两矿法浸出低品位软锰矿的工艺研究[J].中国锰业,2004,22(2):35-37.
[3]Lasheen T A,El-Hazek M N,Helal A S,et al.Recovery of Manganese Using Molasses as Reductant in Nitric Acid Solution[J].Int J Miner.Process,2009,92(3):109-114.
[4]孟丹.去除还原软锰矿的废糖蜜中氯离子的研究[D].上海:华东理工大学,2013.
[5]粟海锋,黎克纯,文衍宣,等.硫酸-糖蜜酒精废液浸出锰矿的工艺研究[J].高校化学工程学报,2008,22(5):779-784.
[6]Sun W Y,Su S J,Wang Q Y,et al.Lab-scale Circulation Process of Electrolytic Manganese Production With Lowgrade Pyrolusite Leaching by SO2[J].Hydrometallurgy,2013,133:118-125.
[7]Das S C,Sahoo P K,Rao P K.Extraction of Manganese From Low Grade Manganese Ores by FeSO4Leaching[J].Hydrometallurgy,1982,8(1):35-47.
[8] Hariprasad D,Dash B,Ghosh M K et al.Leaching of Manganese Ores Using Sawdust as A Reductant[J].Minerals Engineering,2007,20(14):1293-1295.
[9]尹文新,韩跃新,刘瑶,等.用钛钌阳极从氯化锰溶液电解二氧化锰的研究[J].东北大学学报(自然科学版),2007,28(6):855-858.
[10]赵鹏飞.低品位氧化锰矿制备电解锰过程研究[D].长沙:中南大学,2012.
[11]陈坚.浅谈对《GB10345.1-89白酒试验方法总则》中甲醇试验方法的认识[J].计量与测试技术,2005,32(12):44-45.

