唑来膦酸对骨质疏松症患者P波离散度的影响
陆冰,刘晔,孔繁荣,禇静,胡健,傅坤发
(江苏省老年医院干部保健科,江苏 南京 210024)
唑来膦酸对骨质疏松症患者P波离散度的影响
陆冰,刘晔,孔繁荣,禇静,胡健,傅坤发
(江苏省老年医院干部保健科,江苏 南京 210024)
目的 探讨唑来磷酸对骨质疏松症患者P波离散度(Pd)的影响。方法选取2013年1月至2015年1月本院住院的骨质疏松症患者44例,所有患者予一次性静脉滴注唑来磷酸5 mg,并适当水化,观察骨质疏松患者用药前及用药后24 h、1个月、6个月患者的P波最大时限(Pmax)、P波最小时限(Pmin)及Pd的变化,采用多元线性回归分析影响Pd的因素。结果与用药前相比,患者静滴唑来膦酸24 h后Pd增大[(45.25±8.46)ms vs(49.20±8.07)ms],差异有统计学意义(P<0.05);用药后1个月、6个月的Pd分别为(46.41±7.35)ms、(46.25±7.28)ms,分别与用药前比较,差异均无统计学意义(P>0.05);随访6个月未发现新增房颤;多元线性回归分析显示,使用唑来磷酸前患者左房直径(LAD)、Pmin和年龄是影响Pd的因素(P<0.05)。结论静脉滴注唑来膦酸仅增加骨质疏松患者早期P波离散度,但对远期P波离散度及新发房颤率没有影响。
唑来膦酸;骨质疏松;P波离散度;心房颤动;影响
双膦酸盐主要是通过抑制破骨细胞功能,从而抑制骨吸收,已成为治疗骨质疏松症的常用药物之一。双膦酸盐药物常见的不良反应有胃肠道反应、发热、肌肉酸痛等,近年来,Black等[1]观察到双膦酸盐可能增加心房颤动的发生风险,但是亦有研究并未显示双膦酸盐的应用会增加房颤发生的风险[2]。心房颤动(房颤)是临床上最常见的心律失常之一,心房内非均质性电活动与房颤的触发和维持关系密切。1998年Dilaveris等[3]首先提出了以P波离散度(Pd)评估心房内非均质性电活动,并认为它是预测心房颤动的敏感指标。因此,本研究旨在通过观察骨质疏松症患者静脉使用唑来膦酸前后P波时限和Pd的变化,采用多元线性回归分析影响Pd的因素,以探讨唑来膦酸是否会增加骨质疏松症患者的房颤发生风险。
1 资料与方法
1.1 一般资料 选取2013年1月至2015年1月在我院住院的绝经后女性或年龄大于60岁男性,并予以唑来膦酸(密固达)治疗的骨质疏松症患者44例,其中女性32例,男性12例。纳入标准:根据骨密度检测结果T值<-2.5 SD,或T<-1.0 SD既往有脆性骨折病史,并签署知情同意书;排除标准:(1)肝、肾功能异常者;(2)患有甲状腺疾病、甲状旁腺疾病、肾上腺或性腺疾病、使用糖皮质激素以及结核、炎症、肿瘤者;(3)明确有心房颤动等心律失常或使用抗心律失常药物者;(4)存在使用唑来膦酸禁忌证者。正常对照组为16例健康志愿者,其中女性10例,男性6例,无骨质疏松症病史,骨密度检查正常,除外冠心病、心律失常、甲亢等疾病。
1.2 治疗方法 44例骨质疏松症患者予以一次性静滴唑来膦酸(商品名:密固达,诺华制药公司)5 mg,并予以适当水化(静滴0.9%生理盐水250~500 ml,并适当饮水),继续服用钙剂及活性维生素D,观察用药后不良反应。
1.3 观察指标 用药前测定血生化、甲状腺功能、甲状旁腺激素、血钙、磷、血清抗酒石酸酸性磷酸酶5b(TRACP5b)、血清25羟基维生素D,测定骨密度(BMD),心脏彩超测定左房直径(LAD)、左室射血分数(LVEF),并收集骨质疏松组及对照组一般资料及检查结果,用药24 h内行持续心电监护;观察用药前及用药后24 h、1个月、6个月患者的P波最大时限(Pmax)、P波最小时限(Pmin)及P波离散度(Pd)。
1.4 骨密度测定方法 采用美国HOLOGIC-Discovery A(S/N 85538)双能X线骨密度仪,测量腰椎(L1~4)、股骨颈和大转子的骨密度,CV<1.0%。
1.5 P波时限测定 患者取平卧位,平静呼吸,行十二导联体表心电图检查,走纸速度50 mm/s,增益10 mm/mV。选择基线平稳、图形清晰的心动周期进行测量,由同一位有经验心电图医师完成。P波起点与等电位线交点为P波测量起点,P波终点与等电位线交点为P波测量终点,每个导联测量3个P波,取平均值为该导联P波持续时间,计算P波最大时限(Pmax)、P波最小时限(Pmin)和Pd(=Pmax-Pmin)。
1.6 统计学方法 应用SPSS20.0统计软件进行数据分析,计量资料以均数±标准差(±s)表示,两组均数比较采用配对t检验,影响Pd的因素采用多元线性回归分析。以P<0.05表示差异有统计学意义。
2 结 果
2.1 两组一般资料及主要检查结果比较 共入选骨质疏松症患者44例,与对照组比较,除腰椎BMD、腰椎T值、髋部BMD、髋部T值比较差异有统计学意义(P<0.05)外,性别、年龄、体重指数、血钙、血磷、血钾、高敏C-反应蛋白、血甲状旁腺激素、血TRACP5b、血25羟基维生素D、LAD、LVEF、Pmax、Pmin、Pd比较差异均无统计学意义(P>0.05),见表1。
表1 两组一般资料及主要检查结果比较(±s)
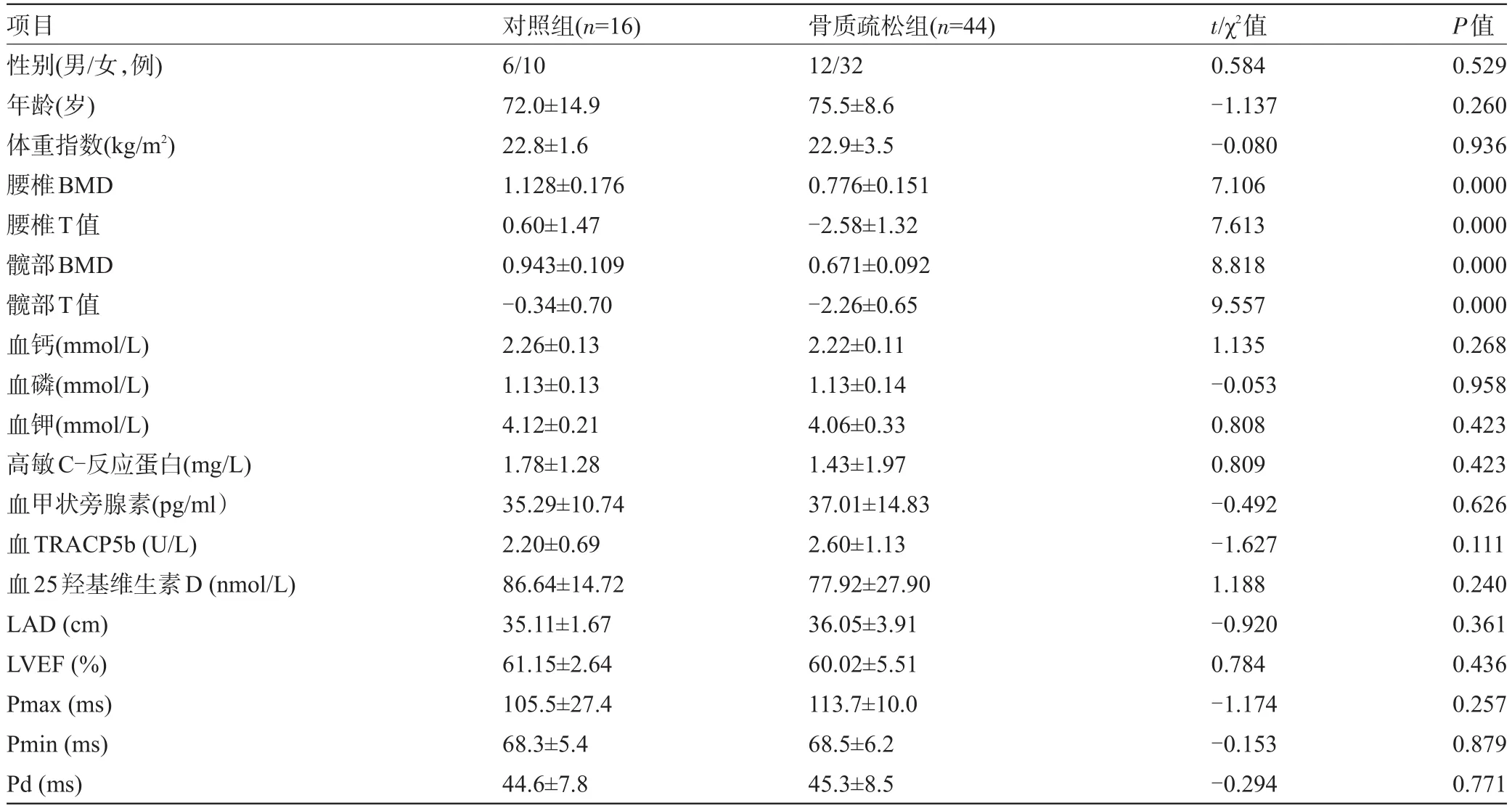
表1 两组一般资料及主要检查结果比较(±s)
项目性别(男/女,例)年龄(岁)体重指数(kg/m2)腰椎BMD腰椎T值髋部BMD髋部T值血钙(mmol/L)血磷(mmol/L)血钾(mmol/L)高敏C-反应蛋白(mg/L)血甲状旁腺素(pg/ml)血TRACP5b(U/L)血25羟基维生素D(nmol/L) LAD(cm) LVEF(%) Pmax(ms) Pmin(ms) Pd(ms)对照组(n=16) 6/10 72.0±14.9 22.8±1.6 1.128±0.176 0.60±1.47 0.943±0.109 -0.34±0.70 2.26±0.13 1.13±0.13 4.12±0.21 1.78±1.28 35.29±10.74 2.20±0.69 86.64±14.72 35.11±1.67 61.15±2.64 105.5±27.4 68.3±5.4 44.6±7.8骨质疏松组(n=44) 12/32 75.5±8.6 22.9±3.5 0.776±0.151 -2.58±1.32 0.671±0.092 -2.26±0.65 2.22±0.11 1.13±0.14 4.06±0.33 1.43±1.97 37.01±14.83 2.60±1.13 77.92±27.90 36.05±3.91 60.02±5.51 113.7±10.0 68.5±6.2 45.3±8.5 t/χ2值0.584 -1.137 -0.080 7.106 7.613 8.818 9.557 1.135 -0.053 0.808 0.809 -0.492 -1.627 1.188 -0.920 0.784 -1.174 -0.153 -0.294 P值0.529 0.260 0.936 0.000 0.000 0.000 0.000 0.268 0.958 0.423 0.423 0.626 0.111 0.240 0.361 0.436 0.257 0.879 0.771
2.2 骨质疏松组患者静滴唑来膦酸24 h、1个月、6个月前后的Pd变化 与用药前比较,患者静滴唑来膦酸24 h后Pd增大[(45.25±8.46)ms vs(49.20±8.07)ms],差异有统计学意义(P<0.05),见表2。用药后1个月、6个月的Pd分别为(46.41±7.35)ms、(46.25±7.28)ms,分别与用药前比较,差异均无统计学意义(P>0.05),见表3。
表2 患者静滴唑来膦酸24 h前后P波时限的变化结果(±s)
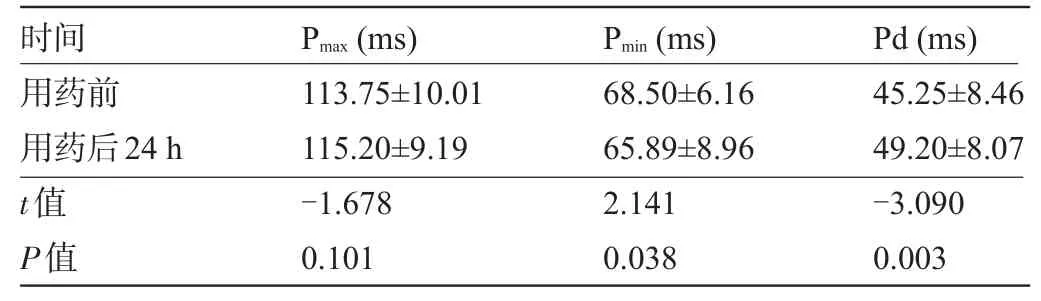
表2 患者静滴唑来膦酸24 h前后P波时限的变化结果(±s)
时间Pmax(ms)Pmin(ms)Pd(ms)用药前用药后24 h t值P值113.75±10.01 115.20±9.19 -1.678 0.101 68.50±6.16 65.89±8.96 2.141 0.038 45.25±8.46 49.20±8.07 -3.090 0.003
表3 患者静滴唑来膦酸1个月、6个月前后P波时限的变化结果(±s,ms)
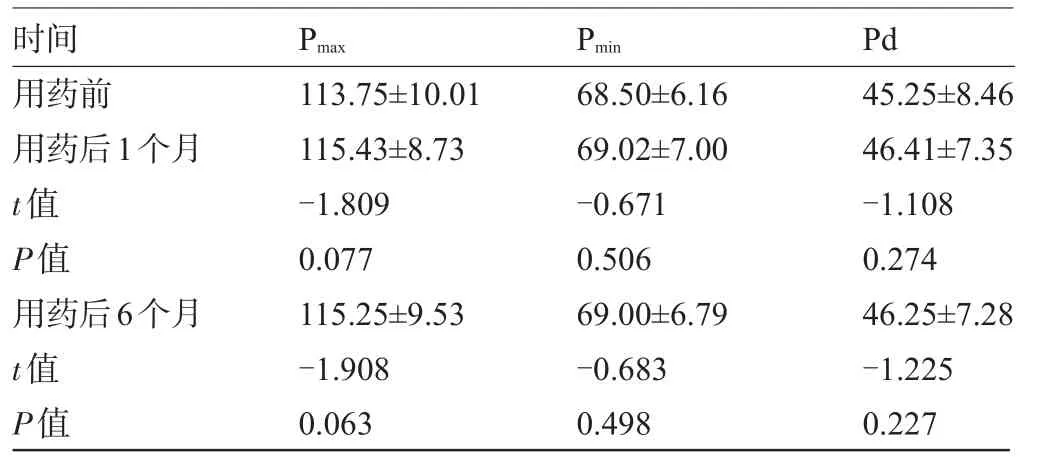
表3 患者静滴唑来膦酸1个月、6个月前后P波时限的变化结果(±s,ms)
时间PmaxPminPd用药前用药后1个月t值P值用药后6个月t值P值113.75±10.01 115.43±8.73 -1.809 0.077 115.25±9.53 -1.908 0.063 68.50±6.16 69.02±7.00 -0.671 0.506 69.00±6.79 -0.683 0.498 45.25±8.46 46.41±7.35 -1.108 0.274 46.25±7.28 -1.225 0.227
2.3 影响Pd的因素 以Pd为因变量,以患者的年龄、BMI、血钙、血磷、hsCRP、PTH、血25羟基维生素D以及使用唑来膦酸前患者Pmin、LAD和LVEF为自变量。多元线性回归分析结果显示使用唑来膦酸前患者LAD、Pmin和年龄是影响Pd的因素(P<0.05),见表4。
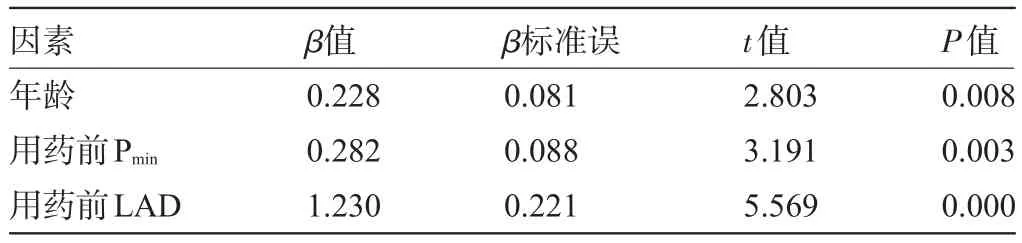
表4 多元线性回归分析影响P波离散度的因素
3 讨 论
P波离散度(Pd)是体表心电图同一心动周期不同导联中最长P波时限与最短P波时限的差值,反映了心房内部和心房间不同部位非均质的电传导及活动[4]。心房颤动有房内传导延迟与房内不应期缩短并离散的特征,近年研究表明Pd能在不同人群预测房颤发生的特异性敏感指标[5]。正因如此,我们选择Pd为研究指标可以间接反映使用双膦酸盐与房颤发生风险之间的联系。
双膦酸盐治疗增加心房颤动发生的风险最初是因Black等[1]在HORIZON-PFT研究观察到,与安慰剂组相比,使用唑来膦酸组患者有更多的房颤事件(1.3%vs 0.5%),进而引发了人们对于使用双膦酸盐导致房颤发生风险的关注。Abrahamsen等[6]报道了一组来自丹麦人口数据库资料的研究结果,使用双膦酸盐骨折患者较未使用双膦酸盐骨折患者房颤的发生率分别为20.6/1 000人(年)和16.5/1 000人(年),HR为1.29(95%CI 1.17~1.41),提示服用双膦酸盐后房颤风险有所增加,但是风险因素主要集中在老龄化及原有心血管疾病的骨折患者。但是随后进行的大部分Meta分析和回顾性分析结果并未显示双膦酸盐的应用会增加房颤发生的风险[2,7]。当前对于使用双膦酸盐药物相关性房颤的研究还处于初级阶段,有待更多的国内外多中心研究予以佐证。我们的研究结果显示,骨质疏松症患者静脉滴注5 mg唑来膦酸24 h后Pd与用药前比较差异有统计学意义(P<0.05),用药后24 h对44例患者持续心电监护未观察到房颤的发生,但8例患者观察到频发房性早搏或房性心动过速,推测使用唑来磷酸可能会在短期内增大患者心房间或心房内非均质性电传导,使其出现房性异位心律。İlgezdi等[8]报道的在33例骨质疏松患者接受唑来磷酸治疗时行24 h动态心电图观察,有5例患者出现房性异位心律,但未观察到新发房颤,我们的观察与其相符。与Black等[1]报道的在用药30 d后发生心房颤动不同,在随后的1个月及6个月随访12导心电图,8例前面观察到频发房性早搏或房性心动过速的患者在后面的随访中未再观察到房性心律失常的发生,Pd与用药前相比差异无统计学意义(P>0.05),提示唑来磷酸并不增加骨质疏松患者房颤发生风险。此外,我们观察到骨质疏松组与对照组P波离散度差异无统计学意义,提示骨质疏松症本身不会导致房颤发病率的增加。
有学者认为双膦酸盐药物通过降低血钙磷浓度[9],导致机体对心律失常的敏感性增加,会增加房颤的发生,其机制与继发性甲状旁腺亢进引起低钙血症的病理过程类似[10],此外心房肌细胞已被证实对血钙浓度降低具有高敏感性[11]。但HORIZON-PFT研究中发生房颤与未发生房颤的患者血钙磷差异无统计学意义[1],同样我们通过多元回归分析结果也显示Pd与患者用药前血钙磷水平无明显相关性,而与Pd有关的因素包括患者的左房内径、用药前最小P波时限和年龄等。因此对于双磷酸盐导致钙磷酸盐减少导致房颤这一观点还需更多研究数据支持。由于心房扩大后心房肌细胞肥大甚至引起超微结构发生改变,造成心房内各向异性传导增大,造成P波离散度增大[12],会增加房性心律失常的发病风险。人群中房颤的患病率是随年龄增加而升高,年龄因素是目前已知最基本的心房颤动发生的独立危险因素,随着年龄增长,心房肌纤维化逐渐明显,心房肌内非均质性程度加重,进而导致Pd增大,房颤及其他房性心律失常的发生风险大幅增加。我们纳入的44例患者平均年龄75岁,属于心律失常高发人群,虽然在用药后24 h未发现心房颤动,但是观察到有8例患者房性心律失常的发生增加,因此对于使用双磷酸盐的老年骨质疏松患者最好给予心电监护或24 h动态心电图,密切观察心电情况。
目前对于双磷酸盐药物引起的房颤,其诊断和鉴别诊断标准还不明确,需要进一步全面研究。尽管一些数据揭示长期使用双磷酸盐药物与房颤不良事件的增加有潜在相关性,但是所有可利用的数据及证据并不支持一个持续的相关性或存在因果关系,而且目前没有一个明确的分子机制来解释这种效应[13]。我们的研究发现老年骨质疏松患者应用唑来磷酸24 h后有短暂的P波离散度增大,但是用药后24 h及随后的1个月和6个月随访心电图均未发现心房颤动,同时患者的骨密度及疼痛症状均改善,因此在未存在或未发现有房颤或其他心律失常事件的老年骨质疏松患者,使用双磷酸盐治疗骨质疏松带来的好处可能远高于潜在的房颤事件发生风险。
本研究不足之处包括样本量较小,随访缺乏连续动态心电图的数据,同时缺乏更长时间的观察资料,有待今后进一步研究。
[1]Black DM,Delmas PD,Eastell R,et al.Once-yearly zoledronic acid for treatment of postmenopausal osteoporosis[J].N Engl J Med, 2007,356(18):1809-1822.
[2]Loke YK,Jeevanantham V,Singh S.Bisphosphonates and atrial fibrillation:systematic review and meta-analysis[J].Drug Saf,2009,32 (3):219-228.
[3]Dilaveris PE,Gialafos EJ,Andrikopoulos GK,et al.Clinical and electrocardiographic predictors of recurrent atrial fibrillation[J].PACE, 2000,23(3):352-358.
[4]Yazici M,Oidemir K,Altunkeser BB,et al.The effect of diabetes on the P-wave dispersion[J].Circ J,2007,71(6):880-883.
[5]Dilaveris PE.P-wave dispersion:a novel predictor of paroxysmal atrial fibrillation[J].Ann Noninvasive Electrocardiol,2001,6(2):59-65.
[6]Abrahamsen B,Eiken P,Brixen K.Atrial fibrillation in fracture patients treated with oral bisphosphonates[J].J Intern Med,2009,265 (5):581-592.
[7]Pazianas M,Compston J,Huang CL.Atrial fibrillation and bisphosphonate therapy[J].J Bone Miner Res,2010,25(1):2-10.
[8]İlgezdi ZD,Aktaş İ,Doğan Metin F,et al.Acute effect of zoledronicacid infusionon atrial fibrillation development in patients with osteoporosis[J].Anatol J Cardiol,2015,15(4):320-324.
[9]Poole KE,Reeve J,Warburton EA.Falls,fractures,and osteoporosis after stroke:time to think about protection?[J].Stroke,2002,33(5): 1432-1436.
[10]Kim HW,Park CW,Shin YS,et al.Calcitriol regresses cardiac hypertrophy and QT dispersion in secondary hyperparathyroidism on hemodialysis[J].Nephron Clin Pract,2006,102(1):21-29.
[11]Van Wagoner DR,Nerbonne JM.Molecular basic of electrical remodeling in atrial fibrillation[J].J Mol Cell Cardiol,2000,32(6): 1101-1117.
[12]张淑花,陈明龙,杨兵,等.P波离散度及心钠素与房性心律失常的关系研究[J].南京医科大学学报,2009,29(12):1713-1715.
[13]张刚,蒋电明.双磷酸盐药物及心房颤动的相关性研究进展[J].重庆医学,2014,43(16):2074-2076.
Influence of zoledronic acid on P-wave dispersion in osteoporotic patients.
LU Bing,LIU Ye,KONG Fan-rong,CHU Jing,HU Jian,FU Kun-fa.VIP Health Care Department,Jiangsu Province Geriatric Hospital,Nanjing 210024,Jiangsu, CHINA
ObjectiveTo explore the influence of zoledronic acid on P-wave dispersion(Pd)in patients with osteoporosis.MethodsForty-four osteoporotic patients in our hospital were recruited from January 2013 to January 2015,which all received intravenous injection of 5 mg zoledronic acid(Aclasta)once,and with proper hydration.The maximum P-wave duration(Pmax),minimum P-wave duration(Pmin),and changes of Pd were measured at baseline and 24 h,1 month,and 6 months after treatment.ResultsNone of the patients developed atrial fibrillation six months after zoledronic acid injection.Pd was increased significantly at 24 h after zoledronic acid injection[(45.25±8.46)ms vs (49.20±8.07)ms,P<0.05],but Pd at 1 month[(46.41±7.35)ms]and 6 months[(46.25±7.28 ms)]after treatment showed no significant difference with the baseline(both P>0.05).Multivariate linear regression showed that left atrial dimension (LAD),Pmin and age were associated with Pd(all P<0.05).ConclusionZoledronic acid increases P-wave dispersion on short-term(within 24 hours after treatment),but no influence is found on long-term P-wave dispersion and new onset atrial fibrillation rate in osteoporotic patients.
Zoledronic acid;Osteoporosis;P-wave dispersion;Atrial fibrillation;Influence
R681
A
1003—6350(2016)04—0571—04
10.3969/j.issn.1003-6350.2016.04.019
2015-09-17)
江苏省卫计委保健局资助项目(编号:BJ14015)
傅坤发。E-mail:fukunfa@126.com

